2023年是生机焕发、希望绵延的一年。后疫情时代,国内外神经介入领域在全球复苏的活力迸发中保持着全速前进的步伐。学术大会上的聚首与切磋、临床试验的续力与推进,为神经介入领域的发展添足动力。这一年,中国神经介入学者步履不停、勇攀高峰,在国际脑血管病学术舞台上不断发出响亮的中国声音,展现中国医学的卓越。刘建民教授带领大家梳理回顾2023年度公布的国内外神经介入领域的重大研究成果,让我们在回顾中见证全球尤其中国学者的智慧凝聚,共同探寻未来的潜力与可能。
动脉取栓已经成为前循环大血管闭塞性急性缺血性卒中最为有效的标准治疗方法。该方法可以显著改善患者的临床结局、降低残死率,但是对于动脉取栓前是否可以跳过静脉溶栓这一问题,国际上一直存在较大争议。2020年,由海军军医大学第一附属医院(上海长海医院)刘建民教授牵头组织的DIRECT-MT研究率先完成;随后的两年多时间里,全球其他五项针对这一问题的高质量临床研究也陆续发表于国际顶刊。但由于各项研究的设计方法、入组数量、覆盖人群、基线资料等诸多方面存在较大差异,六项临床研究的最终结果并不一致,因此亟需开展基于高质量RCT研究单个受试者数据的荟萃分析以及更加深入的亚组研究。
基于此,刘建民教授与Yvo Roos教授(荷兰)、Urs Fischer教授(瑞士)等多国脑卒中领域专家联合牵头发起基于单个受试者数据的荟萃分析:“改善急性缺血性卒中再灌注策略研究”(IRIS研究),相关结果于2023年8月26日登顶《柳叶刀》杂志。该研究纳入来自8个国家207个研究中心的2314例患者。基于5%的非劣效界值,IRIS研究未证实直接取栓不劣于桥接取栓(校正后OR值,0.89;95% CI,0.76~1.04);同时也未能证实桥接治疗优于直接取栓。两种治疗方法之间差异极小,仅有1.7%的结局差异。这意味着对于符合IVT+EVT治疗条件的患者,每桥接治疗57例患者,才可能使1例患者较单纯EVT额外获益,提示应从成本效益、患者特点、预期延误等方面予以个体化精准决策,为动脉取栓前的静脉溶栓相关问题提供了最高级别的循证医学证据。IRIS研究汇聚了全球卒中学者的集体智慧,为这一问题提供了最高级别的循证医学证据,彰显了我国脑血管病介入治疗领域的国际影响力。
血管内治疗已成为急性颅内大血管闭塞的标准治疗方法,但血管内治疗是否有益于大核心梗死患者,目前仍不确定。由首都医科大学附属北京天坛医院缪中荣教授以及首都医科大学附属北京天坛医院、国家神经系统疾病临床医学研究中心王拥军教授牵头发起的前瞻性、多中心、开放标签、终点盲法(PROB设计)的随机对照临床研究——“急性前循环大血管闭塞合并大梗死核心患者血管内治疗研究”(ANGEL-ASPECT研究)验证了发病24h内的急性前循环大血管闭塞且CT-ASPECTS评分3~5分或梗死体积70~100ml的患者中,血管内治疗在改善患者功能预后方面优于单纯的药物治疗这一假设;相关结果于2023年2月10日在国际卒中大会(ISC2023)上发布,并在线发表在《新英格兰医学杂志》上。
研究结果显示,在最终入组的456例患者(血管内治疗组231例,药物治疗组225例)中,取栓组的患者90天mRS显著优于单纯最佳药物治疗组(Generalized odds ratio,1.37;95% CI,1.11~1.69;P=0.004);90天mRS 0~2的在血管内治疗组为30.0%,在药物治疗组为11.6%(relative risk [RR],2.62;95% CI,1.69~4.06);90天mRS 0~3的比率在血管内治疗组为47.0%,在药物治疗组为33.3%(RR,1.50;95% CI,1.17~1.91);安全性终点显示,血管内治疗组的症状性颅内出血14例(6.1%),药物治疗组症状性颅内出血为6例(2.7%)(RR,2.07;95% CI,0.79~5.41;P=0.12)。血管内治疗组任何颅内出血113例(49.1%),药物治疗组任何颅内出血39例(17.3%)(RR,2.71;95% CI,1.91~3.84;P<0.001);血管内治疗组患者的去骨瓣减压数量上更高,但无统计差异(7.4% vs 3.6%,RR,1.92;95% CI,0.78~4.73;P=0.15);血管内治疗组死亡率为21.7%,药物治疗组为20.0%。ANGEL-ASPECT研究证实,血管内治疗对于伴有大核心梗死的急性前循环大血管闭塞患者优于单纯药物治疗,为大核心梗死患者的取栓治疗贡献了高质量的循证证据,结合同期发表的几项结果一致的大核心梗死研究,将为进一步国际指南的改写奠定重要基础。
延伸阅读:登顶NEJM!缪中荣教授团队ANGEL-ASPECT研究结果在国际卒中大会现场发布,同时《新英格兰医学杂志》在线发表!
在颅内侧支循环良好的患者中,病变血管区域内的脑组织在转变为核心梗死之前可能存活较长时间。一项“急性缺血性卒中血管内治疗多中心随机临床试验”(MR CLEAN研究)的事后分析显示,对于CTA发现侧支循环较好的患者进行血管内治疗有更好的治疗获益。因此,来自荷兰马斯特里赫特大学医学中心神经内科的Robert J van Oostenbrugge教授等人认为与目前使用的标准相比,侧支循环的存在可能为晚时间窗患者选择血管内治疗提供一个更具包容性和实用性的工具,并进行了一项多中心、开放标签、盲法终点、随机对照的3期临床研究——急性缺血性卒中晚期时间窗血管内治疗多中心随机临床试验(MR CLEAN-LATE研究)。相关结果于2023年3月29日在线发表在《Lancet》上。
MR CLEAN-LATE研究旨在评估晚期时间窗(6-24小时)血管内治疗对于伴有侧支循环AIS患者的疗效和安全性。主要结局是随机分组90天后的改良Rankin量表(mRS)评分;安全性指标包括随机分组90天后的全因死亡率和症状性颅内出血。最终有535名患者被随机分组,502名(94%)患者提供了延期同意或在获得同意前死亡(血管内治疗组255名,对照组247名;其中261[52%]女性)。血管内治疗组90天mRS评分中位数低于对照组(3 [IQR 2-5]和4[2-6]),观察到血管内治疗组mRS评分改善(校正OR为1.67 [95% CI,1.20-2.32])。两组间全因死亡率无显著差异(255例患者中62例[24%]和247例患者中74例[30%];校正后OR为0.72 [95% CI,0.44-1.18])。血管内治疗组症状性颅内出血发生率高于对照组(17例[7%]和4例[2%]);校正后OR为4.59[95% CI,1.49-14.10])。
MR CLEAN-LATE研究结果表明,基于CTA上是否存在侧支血流,血管内治疗对于发病后6-24小时内就诊或最后一次正常的前循环大血管闭塞引起的缺血性卒中患者有效且安全。
目前,静脉溶栓治疗是急性缺血性卒中唯一标准药物治疗方法。然而,由于静脉溶栓狭窄的治疗时间窗(发病4.5小时以内)及严格的禁忌症,我国静脉溶栓率仅约5.64%,未能接受静脉溶栓治疗的大量患者,尤其是非大、中血管闭塞性致残性卒中患者,缺乏高级别循证医学证据推荐的有效治疗方法。因此,针对这一治疗困境,陆军军医大学第二附属医院(重庆新桥医院)杨清武教授和资文杰教授团队牵头发起了前瞻性、多中心、双盲、双模拟、随机对照临床研究——“急性非大、中血管闭塞性卒中早期替罗非班治疗临床试验”(RESCUE BT2试验)探索了静脉替罗非班治疗急性非大、中血管闭塞性致残性卒中患者的安全性及有效性,相关结果于2023年6月1日发表在《新英格兰医学杂志》上。
研究最终入组1177例患者,其中606例为替罗非班组,571例为阿司匹林组。研究结果显示,替罗非班组和阿司匹林组分别有29.1%和22.2%的患者达到主要疗效终点(90天mRS评分0~1分),两组之间具有统计学差异(校正相对风险比,1.26;95% CI,1.04~1.53,P=0.02);安全性结局方面,根据海德堡出血分类标准定义的症状性颅内出血率在替罗非班组略高于阿司匹林组(0.99% vs 0.0%,P=0.03);90天的死亡率在替罗非班组与阿司匹林组无显著统计学差异(3.8% vs 2.6%,P=0.12)。RESCUE BT2研究最终证实,静脉替罗非班治疗相较于传统治疗方式能显著降低急性非大、中血管闭塞性致残性卒中患者的致残率,为急性非大、中血管闭塞性致残性卒中患者治疗提供了新疗法,并打开了替罗非班类药物在缺血性卒中临床治疗的大门。
AIS患者EVT成功再灌注后的最佳血压控制标准尚不清楚。对确定接受EVT并成功再灌注后24小时内强化血压管理是否比常规血压管理能带来更好的临床结局,韩国延世大学医学院神经内科Ji Hoe Heo教授牵头开展了进行了一项多中心、随机、开放标签、盲法终点的评估研究——“动脉内取栓患者的预后:最佳血压控制”(OPTIMAL-BP研究)。相关结果于2023年9月5日发表在《JAMA》上。
OPTIMAL-BP研究的主要安全性结局是36小时内出现症状性脑出血、3个月内与卒中相关的死亡。数据和安全监测委员会注意到了安全问题,建议该试验被提前终止。302名患者(99.0%)完成了试验(平均年龄73.0岁;122名女性[40.4%]),强化组症状性脑出血的发生率为9.0%,常规组为8.1%。卒中后3月内相关死亡发生率强化组为7.7%,常规组为5.4%。强化降压组83%时间SBP值在靶目标值(SBP<140mmHg),常规降压组42.1%时间的SBP值在靶目标值(SBP 140-180mmHg);强化降压组99.6%时间的SBP值<180mmHg,常规降压组99.1%时间的SBP<180mmHg;强化降压组发生血压下降(SBP<100mmHg)的频率明显多于常规降压组(29.7% vs 17.3%,P=0.02),2组间血压超标事件(SBP>180mmHg)无明显差别(3.9% vs 9.3%,P=0.09)。强化降压组常规使用静脉降压药更多(74.2% vs 18.7%,P<0.001),26例常规降压组患者经历了低血压事件(SBP<100mmHg),其中2例使用静脉降压药,强化降压组46人中有35人(76.1%)使用了静脉降压药。
OPTIMAL-BP研究结果显示,在EVT成功再灌注治疗大血管闭塞的急性缺血性卒中的患者中,与传统的血压管理相比,24小时的强化血压管理导致3个月时功能独立性的可能性较低。这些结果表明,在急性缺血性卒中的EVT成功后,应避免强化BP管理。
急性缺血性卒中血管内治疗成功再通后适度降低收缩压(SBP)的效果尚不确定,研究目的是确定血管内治疗后较低SBP目标(<140mmHg或160mmHg)与较高目标(180mmHg)相比的无效性。大血管闭塞性(LVO)急性脑梗死(AIS)血管内治疗(EVT)术后的血压管理,目前仍不清楚。对此,美国辛辛纳提大学Pooja Khatri博士牵头开展了一项前瞻性、多中心、随机、开放标签、盲法终点、无效性设计的2期临床试验——“血管内卒中治疗后的血压管理II期研究”(BEST-II研究)。相关结果发表在2023年9月5日的《JAMA》杂志上。
BEST-II研究旨在探究对急性缺血性卒中(AIS)患者接受血管内治疗(EVT)并成功再灌注后,前24小时内中等血压(BP)水平管理是否比较高BP水平管理能带来更好的临床结局,主要观察36h的脑梗死体积和90d神经功能预后结果(效用加权mRS评分),次要终点包括任何颅内出血和症状性出血。113名患者(94.2%)随访了影像学梗死体积,<140mmHg降压组的平均随访梗死体积为32.4mL,<160mmHg降压组为50.7mL,≤180mmHg降压组为46.4mL。<140mmHg降压组的效用加权mRS评分为0.51,<160mmHg降压组为0.47,≤180mmHg降压组为0.58。3组的症状性颅内出血比例分别为5%、2.5%和5%。
BEST-II研究结果表明,急性前循环大血管闭塞型缺血性卒中患者接受血管内治疗再通后,较低的SBP管理目标(<140mmHg或160mmHg)与较高的SBP管理目标(≤180mmHg)相比,未达到研究预先设定的无效性标准,因此尚不能证明较低的术后血压管理目标值是有害的。然而,该研究结果提示,如果在未来更大规模的试验中进行测试,从较低SBP目标中获益的可能性很低。
07
脑机接口(BCI)可以利用皮层运动信号绕过受损肢体,直接控制外部设备来恢复运动能力。已有病例报告描述了脑机接口设备对外骨骼、假肢和通信技术的控制,并显示出解码皮质活动成为语言和书写的能力。但这项技术在更广泛的患者群体中应用是有限的,部分原因是由于在大脑中植入电极需要进行开颅手术或部分颅骨切除术,这具有侵入性。2023年3月1日,来自澳大利亚墨尔本大学皇家墨尔本医院放射科的Peter Mitchell等对血管内脑机接口是否可以安全植入并用于瘫痪患者的功能提高做了首次人体研究评估,结果发表于《JAMA Neurology》(Q1)上。该研究是一项单中心、前瞻性、首次将Stentrode设备应用于人体内的研究,目的是评估血管内植入脑机接口设备后实现控制电脑的安全性及可行性。研究对象均为双侧上肢严重瘫痪的患者,研究随访12个月。主要安全终点为设备相关严重不良事件导致死亡或永久性的残疾加重,次要终点事件是设备所植入的血管闭塞及器械移位,探索性终点包括12个月持续性的信号稳定、指令的形成及电子设备的成功使用。研究结果提示,4位纳入分析的研究对象在完成随访12个月内无严重不良反应,没有血管闭塞或设备移位,所有信号带宽稳定,每一位患者均能够通过脑机接口成功控制电脑。该研究具有划时代的意义,不单证实了通过血管内介入这种微创的方法可以安全的植入脑机接口,同时也证明了脑机接口设备可以在血管内顺利接受神经元信号。随着SWITCH研究的发布,神经介入领域也进入全新的功能神经介入时代,相信未来会有越来越多的高科技设备可以通过神经介入的方式进行植入,从而改变我们的生活。

eShunt系统包括血管内可植入式脑脊液分流管和相关递送组件,旨在避免侵入式手术、全身麻醉、住院时间延长和术后疼痛管理。2023年6月,利用Pedro Lylyk教授来华参会间隙,受海军军医大学第一附属医院刘建民教授委托,脑医汇-神介资讯对Pedro Lylyk教授进行了一次深度采访。在采访中,Pedro Lylyk教授畅谈了eShunt系统所带来的改变和创新,谈及eShunt自身的改进与发展时,他表示:“第一代eShunt上带有肝素,以防止血栓的形成,而且也很薄。但开发者在考虑进行第二代改进,我相信eShunt会有改进。”2023年9月18日,eShunt的开发公司CereVasc宣布,该公司已获批美国食品药品监督管理局(FDA)“试验装置豁免”(IDE),可以扩大eShunt系统治疗正常压力脑积水(NPH)的研究,并增加更多研究参与者和临床试点。与此同时,IDE补充批准也允许第二代eShunt系统用于NPH研究,新一代系统设计旨在简化装置准备流程,提高整体易用性,并维持eShunt植入的性能表现。

PEDV是用于颅内动脉瘤治疗的第四代血流导向装置,3.5mm及以下规格可以使用021微导管释放,4mm及以上规格使用027微导管释放。PEDV在植入式Shield技术的表面共价键合磷酰胆碱,经科学证实可降低植入材料的血栓形成性,减少体外血液接触激活。同时对孔隙率、侧壁厚度和贴壁效果进行优化,进一步提高分流效果。然而,目前没有关于第二代PEDV的结局研究。为了评估PEDV的安全性和有效性,英国威尔士大学医院神经放射科Anand Sastry博士等人开展了一项多中心回顾性和前瞻性研究(PEDVU(R)研究),其主要和次要目标是分别确定第二代PEDV在未破裂和破裂动脉瘤的治疗结局。研究纳入了121名患者的131个动脉瘤,在短期和中期随访中,未破裂动脉瘤队列的闭塞率以及短期随访中破裂动脉瘤队列的闭塞率>90%,2例动脉瘤(1.5%)接受再治疗。当排除未破裂队列中姑息性病例或破裂队列中蛛网膜下腔出血导致的死亡率时,各队列的总体主要不良事件发生率分别为7.5%和23.5%,每个队列的死亡率为0%。当所有事件原因都纳入意向性治疗时,各队列的主要不良事件发生率分别为8.3%和40.9%,死亡率分别为0.9%和22.7%。PEDVU(R)研究结果表明,对于未破裂动脉瘤治疗,第二代PEDV具有优于上一代PED的疗效和相似的安全性。动脉瘤破裂结局的分析受队列规模的限制,则需要进一步针对破裂的动脉瘤的前瞻性研究。

瘤内扰流(WEB)是一种血管内治疗的方法,用于治疗宽颈动脉瘤,WEB以往系列的安全性已在许多多中心前瞻性研究和全球范围内对破裂和未破裂动脉瘤进行的回顾性系列研究进行了评估。其最新型号,即WEB17系列,使得通过0.017英寸的微导管输送植入成为可能。由NEURI脑血管中心Laurent Spelle教授牵头发起的一项观察性、多中心、前瞻性研究——WEB17瘤内扰流装置在颅内动脉瘤中的安全性(CLEVER研究)验证了使用WEB 17对破裂和未破裂的宽颈分叉动脉瘤进行血管内治疗是安全的。相关结果于2023年11月1日在线发表在《Journal of Neurointerventional Surgery》上。CLEVER研究的目的是提供有关WEB17治疗宽颈分叉动脉瘤的安全性和有效性数据。研究共纳入欧洲17个中心的163例患者(平均年龄58.1岁;68.1%为女性),其中103例未破裂动脉瘤和60例动脉瘤破裂。大多数动脉瘤位于前交通动脉(ACom)(37.4%)或大脑中动脉(MCA)分叉处(30.1%)。动脉瘤宽度范围为2.0-9.2mm,平均囊宽度为5.0mm。WEB植入手术在163例患者(100%)中成功完成。在12个月的随访中,163例患者中有3例(1.8%)发生重大卒中事件,未观察到与设备相关的死亡率。CLEVER研究证实,WEB17装置并发症发生率低,无器械相关死亡率,在长达1年的随访中,没有破裂的动脉瘤再次出血事件发生,是未破裂和破裂的宽颈分叉动脉瘤的安全治疗选择。此外,WEB17还可以治疗更远端和/或复杂分叉部位的小动脉瘤,但其临床疗效必须通过评估1年时的血管造影疗效来确认。

Neuroguard IEP是Contego Medical研发的一种创新颈动脉支架置入“三合一”系统,集颈动脉支架(采用闭环设计)、后扩张球囊以及40 μm集成式栓子保护(IEP)过滤器于一体,可减少颈动脉支架置入(CAS)的治疗步骤,保持对较大栓子和微栓子的保护。在2023年10月30日至11月2日于美国拉斯维加斯举办的血管介入进展(VIVA)基金会-VIVA年度血管教育研讨会(VIVA 2023)中,使用Neuroguard IEP系统进行颈动脉支架置入时对栓子的保护(PERFORMANCE II期)的30天和1年结果正式公布。PERFORMANCE II期研究的主要终点是严重不良事件的30天发生率(定义为首次手术30天内的死亡、卒中和心肌梗死[MI]率),以及术后第31天至1年的同侧卒中率。研究共纳入了来自美国和欧洲40家中心的305例患有颈动脉狭窄的颈动脉内膜剥脱术(CEA)高危患者,230例(75%)符合生理高危标准,75例(25%)符合解剖学高危标准;平均基线血管造影狭窄率为85%,病变严重钙化率为34%。结果显示,30天的死亡/卒中/MI率在意向性分析和符合方案分析队列中分别为2.3%和1.97%;符合方案分析队列中排除了1例需接受慢性抗凝治疗的血液高凝状态患者。1年时,主要终点(30天死亡/卒中/MI+第31天至1年的同侧卒中)事件发生率在意向性分析和符合方案分析队列中分别为2.67%和2.33%。术后第31天至1年间,1例患者发生轻度同侧卒中(0.37%)。术后1年内,没有患者发生严重卒中或神经系统相关死亡,靶区病变血运重建率为1.47%(4例)。Neuroguard系统具有耐久性、安全性和治疗有效性。
延伸阅读:Neuroguard IEP颈动脉支架系统具有耐久性、安全性和治疗有效性:PERFORMANCE II期研究30天和1年结果公布

目前大口径微导管的使用在神经介入手术中越来越多见,其内径可达0.033英寸,以适应囊内扰流装置或瘤颈辅助装置,包括血流导向装置。使用大直径微导丝可以减轻导丝和导管之间的壁架间隙,利于导管到位,并为远端迂曲解剖结构提供支持。在神经血管介入中使用新型Aristotle18和24微导丝的一项单中心早期经验中,对患者的临床结果进行了分析,包括成功的靶血管、动脉瘤导管插入术和围手术期并发症(血栓栓塞、出血、血管夹层或穿孔)。研究期间,共有84项神经介入手术记录了Aristotle18和24微导丝的使用,包括血管内动脉瘤治疗(n=30)、血管内血栓切除术(n=46)、硬脑膜静脉窦测压/支架置入(n=7)和颅外颈动脉支架置入(n=1)。Aristotle18微导丝与0.021微导管结合使用,Aristotle 24微导丝与0.027或0.033微导管结合使用。在所有病例(100%)中,微导丝均到达目标血管或动脉瘤,从而允许所选微导管无缝推进且没有记录到与手术相关的并发症。在神经介入手术中使用Aristotle 18和24微导丝是可行且安全的,且与标准的0.014微导丝相比,减少了壁架间隙,提高了扭矩、支撑性和安全性。
由于血凝块在当前设备中的结合不良,通过机械取栓术治疗卒中的首过完全再通仍然受到限制。抽吸可以帮助取出主要血凝块,但不能预防远端动脉区域的继发性栓塞。最近在卒中相关凝块中描述的细胞外DNA的密集网状物可能作为取栓设备的锚定点。为了评估DNA反应表面涂层的潜力,以帮助保留血栓切除装置内的主要凝块和小片段,提高MT手术疗效,开展了相关研究。结果表明,与体外裸合金样品相比,涂有所有化合物的样品的DNA结合特性增加(≈3倍),血液元素结合特性降低(≈5倍)。功能测试表明,在三维模型中,在大血管闭塞的实验性MT期间,用DNA结合化合物进行表面修饰可改善凝块修复并显着减少远端栓子。因此,涂有DNA结合化合物的取栓装置可以显著改善中风患者MT手术的结果。

iNedit球囊远端通路导管是一种结合BGC和DAC功能的新型装置。它的内径为0.058英寸,近端外径为2.13毫米,远端外径为1.67毫米。它与0.088英寸引导导管兼容,包括一个距离导管尖端5厘米的球囊,可实现近端血流限制和支架取栓器的联合治疗。其首次人体研究收集了22例在24小时内对因大血管闭塞引起的急性缺血性卒中接受Nedit导管进行取栓术治疗的患者的前瞻性数据。结果评估以5分制评分,范围从1(差)到5(优秀),包括对安全性结果的评估,例如动脉穿孔和动脉闭塞、疗效结果、首过效应(脑梗死溶栓[TICI] 2c/3)和最终再通(TICI 2b/3),和临床疗效结果,例如3个月的0-2 改良Rankin量表(mRS)。结果显示,在这种初步的临床经验中,iNedit设备实现了较高的首过率和最终再通率,没有安全问题。
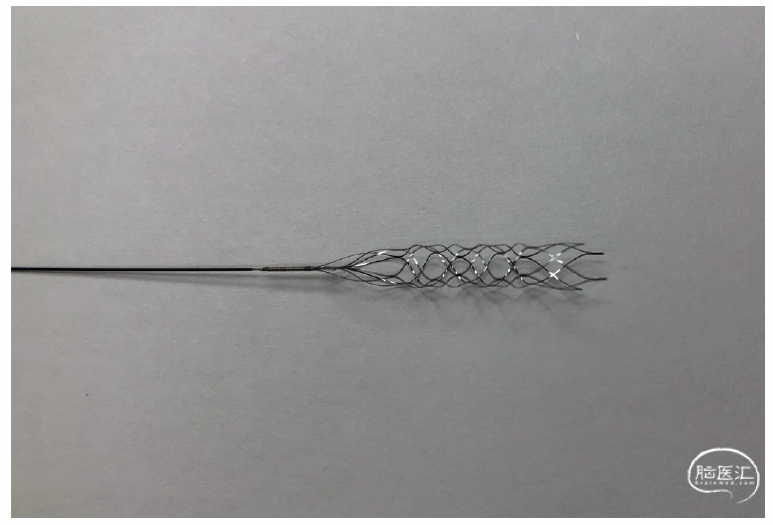
颅内动脉粥样硬化疾病(ICAD)是缺血性卒中的重要原因,尤其是在亚洲人群中。在需要血管内治疗的急性缺血性卒中病例中,潜在ICAD导致的大血管闭塞(LVO)占15-35%。然而,ICAD相关LVO的成功再通率仍然较低。TG扩张器是一种自扩张装置,可暂时扩张ICAD相关的阻塞血管。为了证明TG扩张器对ICAD相关急性缺血性卒中的安全性和有效性开展了一项单臂、开放标签、非随机、前瞻性、多中心的试验,涉及因ICAD相关LVO或严重狭窄引起的急性缺血性卒中而接受TG扩张器治疗的患者。研究在2022年11月至2023年4月期间招募了10名患者。在使用扩张器之前,7名患者接受了取栓治疗。所有10名患者均服用了负荷剂量的阿司匹林和普拉格雷。中位施用时间为10(10–12)min。在手术结束时,立即在所有患者中实现了显著再通。狭窄/闭塞从100%(100-100)下降到68%(56.3-75.3)。没有患者在90天内出现复发性缺血性卒中或再闭塞。到第90天,8名患者改良Rankin量表评分0-2,无需要干预的颅内出血、设备故障、远端栓塞、血管痉挛、夹层或穿孔的病例。TG自膨胀临时扩张系统在ICAD相关急性缺血性卒中的首次人体试验证实,对ICAD相关LVO或严重狭窄患者使用TG扩张器进行急性血管重建未引起任何重大不良事件,并且在90天时血流量持续改善。

瘤内扰流装置是治疗颅内动脉瘤安全有效的策略。近期研究人员利用高频光学相干断层扫描(HF-OCT)和数字减影血管造影术(DSA)在动物模型中评估一种新的瘤内扰流装置SEAL Arc,将其结果与公认的Woven EndoBridge(WEB)装置进行比较。在兔模型中,用SEAL Arc(n=11)装置治疗弹性蛋白酶诱导的动脉瘤。植入后进行HF-OCT和DSA检查,12周后重复检查。在植入时对器械突出和贴壁不良进行评估,并在二元系统上进行评分。在12周时用WEB闭塞量表评估动脉瘤闭塞,并将其分为完全闭塞(A和B)或不完全闭塞(C和D)。使用HF-OCT对12周后新生内膜覆盖率量化,并将这些数据与WEB(n=24)进行比对。结果显示动脉瘤大小和装置位置两组之间没有显著差异。80%的Seal Arc装置显示动脉瘤完全闭塞(P=0.002)。SEAL Arc装置的内膜覆盖率为86±15%(P=0.001)。突出装置的新生内膜明显更少的覆盖率(P<0.001)和更少的不完全闭塞率(P<0.001)。组织学上,所有使用SEAL Arc装置治疗的动脉瘤均完全愈合。该研究提示,使用SEAL Arc治疗实现早期动脉瘤完全愈合,12周后具有显著的内膜覆盖。

颅内宽颈和分叉部动脉瘤(WNBA)的介入治疗在技术上具有挑战性。Nautilus™瘤内系统旨在为动脉瘤颈部提供机械屏障,以支持弹簧圈栓塞。使用Nautilus™瘤内系统治疗颅内动脉瘤的单中心研究结果提示,在41例平均年龄56.7岁(范围37-83岁)的接受了Nautilus™瘤内系统治疗的患者中,41例都是囊状动脉瘤(18例(43.9%)未破裂,23例(56.1%)破裂),大多数动脉瘤(39/41(95.1%))位于前循环,术中没有遇到任何技术上的复杂情况。一名患者无症状的术后轻微卒中与手术相关。30例(73.1%)患者实现了即刻I类闭塞。全因死亡率为7.3%(3/41)。1例患者失访。随访时,94.5%(35/37)的患者达到I级闭塞,94.5%(35/37)的mRS评分为0。出院或随访时没有与程序相关的死亡或永久性发病。Nautilus™瘤内系统治疗破裂和未破裂的颅内动脉瘤表现出良好安全性和有效性,但仍需更大规模的研究来证实这些发现。
回顾2023,全球临床研究与技术创新继续为神经介入发展持续注入动力。展望未来,我们期待2024年能见证更多神经介入领域的探索与发现,在你我共同的努力下,通过高质量临床研究和技术革新为患者带来更美好的明天。
执笔:复旦大学附属中山医院 张颖影
参考文献
(上下滑动查看更多文献内容)
专家简介
刘建民 教授
海军军医大学第一附属医院
主任医师,博导
海军军医大学第一附属医院脑血管病中心主任,战创伤中心主任
全军脑血管病研究所所长
加拿大多伦多大学客座教授
国家卒中中心管理专家委员会副主任;中国卒中专科联盟副主席;中国医师协会介入医师分会副会长;中国医师协会神经外科医师分会常务委员;中华医学会神经外科分会常务委员;全军神经外科专业委员会副主任委员;上海市医师协会神经介入专业委员会会长
世界神经介入大会(WLNC)执委;2011世界颅内支架大会(ICS)主席;2016/2021 WLNC主席;东亚神经介入大会(EACoN)主席
脑医汇-神介资讯主编
往/期/回/顾
声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。
投稿邮箱:NAOYIHUI@163.com
未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。
投稿/会议发布,请联系400-888-2526转3。






