
胶质瘤是成人最常见的恶性原发性脑肿瘤,具有进展迅速、复发率和致死率高的特点[1]。近年来,随着医学技术的不断进步,胶质瘤的诊断和治疗有了新的进展,异柠檬酸脱氢酶(IDH)检测的重要性也日益凸显。
一、胶质瘤的分子诊断进展
过去,胶质瘤确诊主要依赖组织病理学检查,但这种方法对后续治疗的指导意义相对有限[2]。近年来,分子标志物的发现及应用使胶质瘤的诊疗模式发生变革,不仅促进胶质瘤精准诊断,还在一定程度上为患者提供有价值的预后信息。
目前,胶质瘤的诊断模式已从单一的组织病理诊断转变为结合组织病理和分子病理整合诊断,越来越多的分子标志物被发现并应用于胶质瘤诊断中。例如IDH突变、染色体1p/19q联合缺失、ATRX突变、H3突变、TERT启动子突变、染色体7/10拷贝数改变、EGFR扩增或突变等。最新指南中,常规推荐用于胶质瘤分子病理诊断的标志物已达27项,可提供更多的肿瘤分子遗传学变异特征[3]。
二、IDH突变作为诊断标志物的意义
IDH突变状态是弥漫性胶质瘤的关键诊断指标,可用于弥漫性胶质瘤与胶质神经元肿瘤、胶质增生等的鉴别;也是成人型弥漫性胶质瘤分类的关键分子标志物。根据IDH突变状态,可将成人型弥漫性胶质瘤分为IDH突变伴1p/19q联合缺失的少突胶质细胞瘤、IDH突变型星形细胞瘤和IDH野生型胶质母细胞瘤(图1)[3]。此外,IDH突变状态也可为肿瘤患者预后的评估和治疗方案的选择提供重要参考。
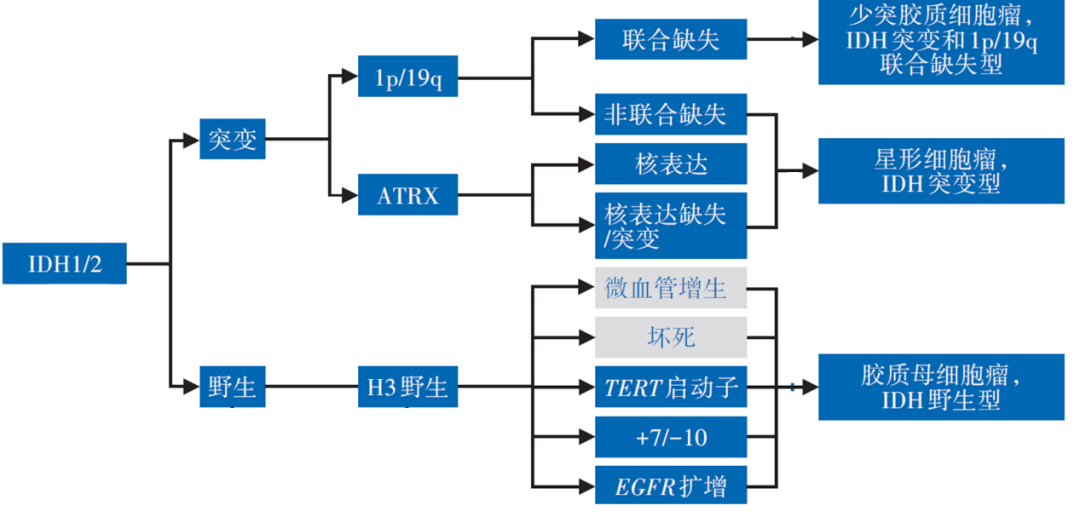
图1. 成人弥漫性胶质瘤基于IDH突变状态的分类
三、IDH突变的检测方法
所有弥漫性胶质瘤都应进行IDH突变检测,以达到标准诊断要求。IDH突变检测主要有以下几种方法:
● 免疫组化:最常用的分子病理学检测方法。通过检测突变的IDH蛋白表达来反映基因的变化,能检出的突变位点包括IDH1 R132H、IDH1 R132G、IDH2 R172K、IDH2 R172G和IDH2 R172M。该方法便于实行且费用较低,但可能存在一定的假阳性或假阴性结果,建议作为首选检测手段,用于初步筛查[4,5]。
● 基因测序:检测IDH突变的金标准。直接在基因层面准确检测少量肿瘤细胞内是否存在IDH突变。该方法敏感性更高,但耗时较长且费用昂贵,适用于免疫组化检测突变阴性的病例作为验证或检出少见突变[4]。
● 液体活检:新兴的检测方法,通过检测脑脊液或血液中的肿瘤脱落细胞和代谢产物来判断IDH突变。该方法的准确性和可靠性仍需进一步验证,可为传统活检困难或风险较高的患者提供一种选择[6]。
● 质谱检测:术中获取IDH突变信息的重要手段。通过质谱技术测定代谢产物的浓度来反映胶质瘤IDH突变状态。近年来的技术发展能够在保证准确性的同时大大缩减检测时长,可满足术中实时检测的需求,有助于更好地指导外科手术切除范围[7]。
四、IDH突变检测结果如何指导治疗选择
对于IDH突变的胶质瘤患者,是否需要接受术后辅助治疗,需临床医生根据患者的年龄、是否新诊断、手术切除程度、病理类型、肿瘤级别等因素充分评估确定。基于INDIGO研究的显著成果,2024年8月FDA批准IDH1/IDH2抑制剂vorasidenib应用于存在IDH1或IDH2突变的2级星形细胞瘤或少突胶质细胞瘤成人和儿童患者(≥12岁)的术后治疗,手术可包括活检、大部切除术或完全切除术,这是FDA首次批准此类患者的全身治疗方案[8]。
中国抗癌协会发布的《中国抗癌协会脑胶质瘤整合诊治指南》(2024版)指出[3]:
● 对存在残留或复发病灶的IDH突变型低级别胶质瘤,IDH抑制剂vorasidenib或ivosidenib分子靶向治疗可能是一种延迟化疗和放疗的方法;
● 低级别脑胶质瘤复发后,如有IDH1/IDH2突变可考虑IDH抑制剂vorasidenib或ivosidenib治疗。
五、小结
IDH检测在胶质瘤的诊断、预后评估和治疗选择中具有重要价值。相信随着分子诊断技术的不断发展,IDH检测将为胶质瘤患者的精准治疗提供更有力的支持。
六、参考文献
[1]苏东元,等.光明与挑战:胶质瘤靶向治疗前沿进展[J].中国神经精神疾病杂志,2025,51(01):1-7.
[2]Ghosh HS, et al. Contemporary prognostic signatures and refined risk stratification of gliomas: An analysis of 4400 tumors. Neuro Oncol. 2025 Jan 12;27(1):195-208.
[3]中国抗癌协会脑胶质瘤专业委员会. 脑胶质瘤整合诊治指南V2.0_2025. https://cacaguidelines.cacakp.com/
[4]林俐,等.全自动免疫组化法与一代测序技术在检测人脑胶质瘤异柠檬酸脱氢酶1突变中的应用价值比较[J].现代肿瘤医学,2022,30(04):599-602.
[5]Dogan S, et al. Molecular epidemiology of IDH2 hotspot mutations in cancer and immunohistochemical detection of R172K, R172G, and R172M variants. Hum Pathol. 2020 Dec;106:45-53.
[6]依日扎提·艾力,等.液体活检在胶质瘤中的应用及展望[J].临床神经外科杂志,2024,21(01):91-94.
[7]Hua W, et al. Rapid detection of IDH mutations in gliomas by intraoperative mass spectrometry. Proc Natl Acad Sci U S A. 2024 Jun 4;121(23):e2318843121.
[8]Mellinghoff IK, et al. Vorasidenib in IDH1- or IDH2-Mutant Low-Grade Glioma. N Engl J Med. 2023 Aug 17;389(7):589-601.
脑胶质瘤前沿创新治疗(CURE)联合门诊
每周二上午,北京天坛医院B区国际部会诊中心。
● 北京天坛医院神经外科江涛院士团队领衔成立国内首个脑胶质瘤前沿创新治疗门诊(CURE)——以精准医学突破脑胶质瘤治疗困境
专家简介
江涛 院士
● 中国工程院院士
● 首都医科大学附属北京天坛医院神经外科中心主任,北京市神经外科研究所所长
● 曾担任中国医师协会脑胶质瘤专业委员会主任委员,中国抗癌协会脑胶质瘤专委会主任委员,中国脑胶质瘤协作组首任组长等
● 作为首席专家主持国家科技部“十一五”支撑计划重点项目、国家科技部“863”重大科技专项项目、国家重大研发计划精准医学专项、国家自然科学基金委重点项目等
● 中国脑胶质瘤基因组图谱计划(CGGA)与亚洲脑胶质瘤基因组图谱计划(AGGA)的发起人和创建者
● 以通讯作者在Cell、Cancer Discovery、Genome Research、PNAS、Clinical Cancer Research、Neuro-Oncology等SCI期刊发表论文400余篇;连续多次入选Elsevier高被引学者榜
● 以第一完成人获得国家科技进步二等奖1项、省部级一等奖2项;获评北京学者,中国工程院光华工程科技奖等;研究成果获评2018年“中国生命科学十大进展”、2021年“中国生物信息学十大进展”
● 主持制定国家卫健委《脑胶质瘤诊疗规范(2018年版)》、《脑胶质瘤诊疗指南(2022年版)》等多部临床诊疗指南
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。






