
胶质母细胞瘤(GBM)是一种具有高度侵袭性的肿瘤,患者确诊后的平均生存期仅为12至15个月,且5年生存率不足5%。该肿瘤的复杂性在一定程度上源于其对血管内皮细胞的高度依赖。这些细胞不仅负责为肿瘤提供氧气和营养,还通过与肿瘤细胞的相互作用,促进肿瘤的生长与存活。然而,目前人们对于这种相互作用的具体机制尚不完全明了,这也限制了新型疗法的开发。
在此背景下,来自美国加州大学洛杉矶分校(UCLA)和日本Harada医院的研究团队近日揭示,血管内皮分泌的蛋白多糖Endocan(ESM1)能够激活GBM细胞表面的血小板衍生的生长因子受体-α(PDGFRA),进而促进肿瘤生长,并导致其对放射治疗等标准疗法产生耐药性。这一发现为开发相关特异性疗法提供了全新的治疗思路。最新研究成果以“内皮分泌的Endocan激活PDGFRA并调控胶质母细胞瘤中的血管生成和空间表型”为题,于2025年1月7日发表在《Nature Communications》(IF:14.7/Q1)(doi:10.1038/s41467-024-55487-1)上。

为了探究胶质母细胞瘤如何与附近的血管细胞相互作用以促进其生长,研究人员首先分析了先前建立的数据库,识别出Endocan作为推动肿瘤生长的关键候选分子。
随后,研究人员运用了多种实验模型进行深入研究,包括患者来源的GBM细胞和血管内皮细胞、经过基因工程改造敲除Endocan的小鼠模型,以及实验室中的肿瘤行为测试模型。研究结果显示,Endocan能够显著促进GBM细胞的增殖、迁移以及血管生成能力。
进一步地,研究团队发现肿瘤的不同区域具有不同的功能特性。Endocan不仅支持肿瘤生长,还定义了肿瘤的分子特征,尤其是手术后常残留的侵袭性边缘区域的特征。
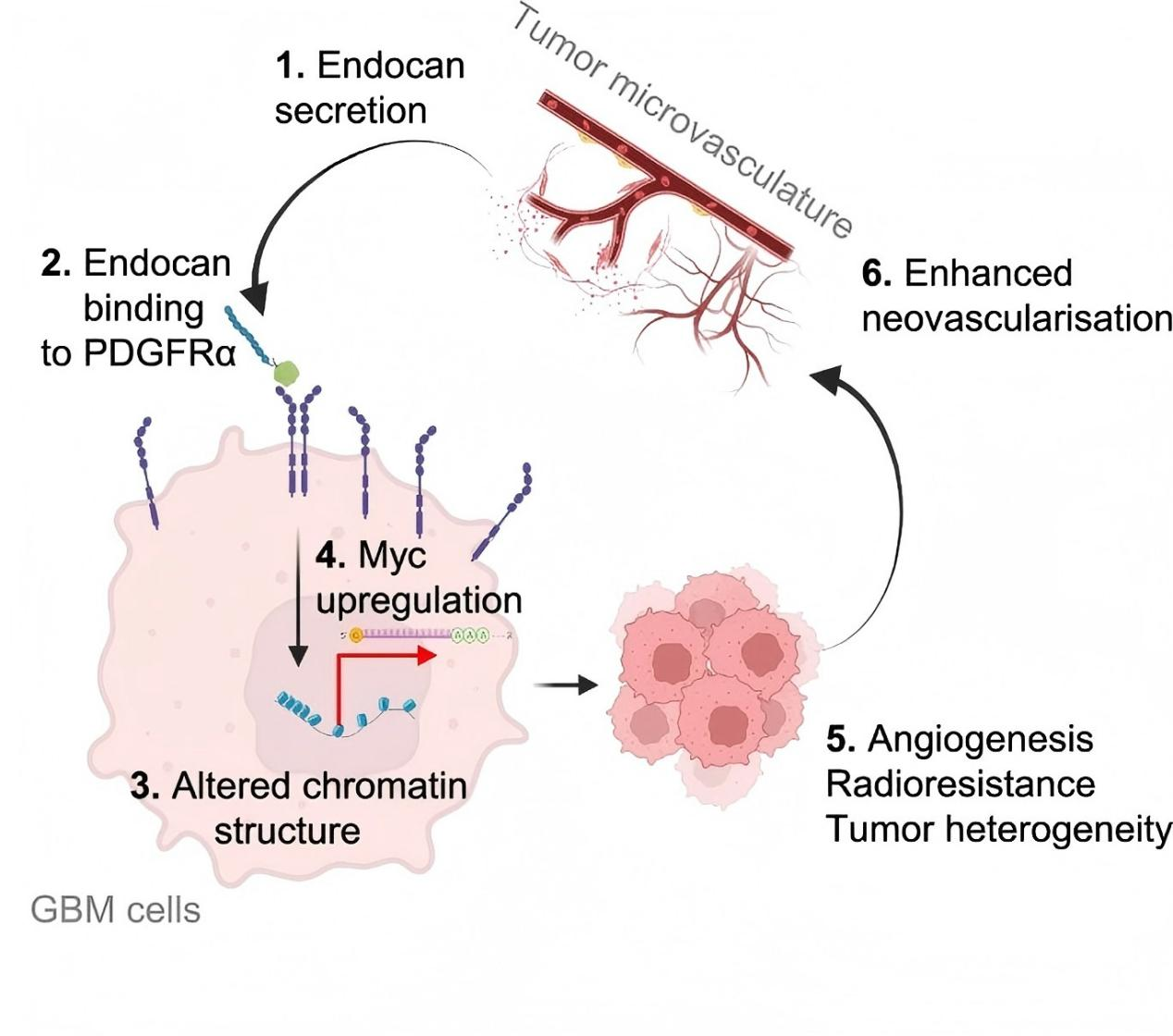
接下来,研究人员通过质谱分析、表面等离子共振(SPR)和邻近连接分析(PLA)等技术,深入剖析了Endocan的作用机制。结果表明,Endocan与PDGFRA受体相互作用,进而影响下游信号通路,增强关键癌基因Myc的表达。此外,高水平的Endocan表达使肿瘤对放射治疗产生更强的抵抗力,且其与肿瘤的侵袭性和患者的生存期呈负相关,这使得Endocan成为潜在的治疗靶点。
基于上述发现,研究人员进一步探讨了Endocan作为治疗靶点的潜力。通过使用PDGFRA抑制剂Ponatinib,他们发现抑制Endocan-PDGFRA信号通路能够显著提高野生型(WT)小鼠的生存率,但在Esm1 KO小鼠中效果不明显。这一结果表明,Endocan及其下游信号通路可能是治疗GBM的潜在靶点,尤其是在那些Endocan表达水平较高的肿瘤中。
随着研究成果的不断深入,未来的研究将聚焦于在人类肿瘤中验证这些发现,特别是胶质母细胞瘤浸润性边缘区域的细胞。此外,研究团队还计划探究靶向Endocan是否能够改善肿瘤对放射治疗的反应。
研究共同资深作者、UCLA智力和发育研究中心主任、UCLA大卫·格芬医学院Harley Kornblum教授表示,“通过靶向胶质母细胞瘤和血管内皮细胞之间的相互作用机制,我们有望开发出阻止肿瘤适应和存活的治疗方法。这将显著提升治疗的效果,特别是放射治疗方面。”
![]()
声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。
投稿邮箱:NAOYIHUI@163.com
未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。
投稿/会议发布,请联系400-888-2526转3。




