REVIEWS
1. 脑肿瘤患者PET和高级MRI的挑战、局限性和陷阱:PET/RANO小组的报告Challenges, limitations, and pitfalls of PET and advanced MRI in patients with brain tumors: A report of the PET/RANO group
Norbert Galldiks and others
Neuro Oncol. 2024 Jul 5;26(7): 1181–1194, doi.org/10.1093/neuonc/noae049
随着正电子发射断层扫描(PET)和高级磁共振成像(MRI)技术的应用,脑肿瘤的诊断有了显著进展。除了解剖核磁共振成像外,这些成像方式还可为多种临床应用提供有价值的信息,如鉴别诊断、肿瘤范围的划分、预后判断、肿瘤复发与治疗相关变化的区分,以及抗癌治疗反应的评估。特别是,神经肿瘤学反应评估(RANO)小组、欧洲神经肿瘤学协会以及欧洲和美国主要核医学会的联合建议强调,放射性标记氨基酸与单纯的解剖磁共振成像相比具有突出的临床价值,应支持其在临床广泛应用。对于先进的磁共振成像及其在临床实践中日益增长的应用,脑肿瘤药物研发联盟标准化小组委员会最近为广泛应用的动态感性对比灌注磁共振成像提供了最新的采集协议。除氨基酸PET和灌注MRI外,其他PET示踪剂和先进的MRI技术(如MR光谱)也颇受临床关注,并日益融入日常临床实践中。然而,这些模式也有不足之处,在临床实践中应加以考虑。本综述概述了胶质瘤或脑转移瘤患者使用PET成像和先进磁共振成像技术可能面临的挑战、局限性和陷阱。尽管存在这些问题,PET成像和高级磁共振成像技术仍将在脑肿瘤治疗中发挥不可或缺的作用。通过跨学科合作、标准化方案和持续创新来认识和应对这些挑战,将进一步提高这些模式在指导最佳患者护理方面的效用。2. 美国镭学会关于表皮生长因子受体突变和ALK融合型非小细胞肺癌脑转移适当使用标准执行摘要Executive summary of the American Radium Society appropriate use criteria for brain metastases in epidermal growth factor receptor mutated-mutated and ALK-fusion non-small cell lung cancer Neuro Oncol. 2024 Jul 5;26(7): 1195–1212, doi.org/10.1093/neuonc/noae041美国镭学会(ARS)中枢神经系统(CNS)委员会审查了有关表皮生长因子受体突变(EGFRm)和ALK融合(ALK+)酪氨酸激酶抑制剂(TKIs)治疗非小细胞肺癌(NSCLC)脑转移(BrMs)的文献,以制定TKIs与放疗(RT)联合使用或替代放疗的适当使用指南。专家组提出了三个关键问题来指导系统性审查:接受表皮生长因子受体或ALK TKIs的患者在(1)诊断或(2)复发时能否推迟放疗;(3)TKI是否应与RT同时进行。进行了两次文献检索(2019年5月和2023年12月)。根据UCLA/RAND适当性方法,专家小组制定了8个模型病例,并采用9分制对治疗方案进行投票,1-3、4-6和7-9分别对应通常不适当、可能适当和通常适当。只有4种治疗方案达成了共识,均符合ARS-AUC现有的多发性BrM指南。对于接受中枢神经系统穿透性ALK或表皮生长因子受体TKIs治疗的BrM患者是否可以适当推迟RT治疗,专家小组未达成共识,但中位数评分表明在大多数情况下推迟RT治疗可能是合适的。除了2-4例BrM病例外,全脑RT并用TKI引起了广泛的分歧,在这些病例中,全脑RT通常被认为是不合适的。我们没有发现任何明确的研究可以确定全脑RT与同期TKI的最佳排序。
BASIC AND TRANSLATIONAL INVESTIGATIONS
1. 性别偏倚坏死性炎症可预测贝伐单抗对胶质母细胞瘤的治疗效果
Sexual-biased necroinflammation is revealed as a predictor of bevacizumab benefit in glioblastoma Sara Hiller-Vallina and othersNeuro Oncol. 2024 Jul 5;26(7): 1213–1227, doi.org/10.1093/neuonc/noae033胶质母细胞瘤(GBM)是一种高度恶性的脑肿瘤,男性发病率高于女性。此外,前者的生存预后较差。迄今为止,这种性别特异性侵袭性的原因仍不清楚。因此,本研究的目的是调查解释这些性别差异的肿瘤过程。这是一项针对GBM患者的回顾性研究,根据性别进行了分层。通过免疫组化、RNA-seq和RT-qPCR分析了73例肿瘤,以确定血管和免疫特征的差异。通过转录组学分析、基因组富集分析和通路富集分析,我们发现了各组中占主导地位的分子通路。我们根据性别差异进一步研究了贝伐单抗(血管内皮生长因子 A(VEGFA)阻断抗体)在回顾性GBM队列(36例肿瘤)中的治疗效果。结果我们发现,在肿瘤缺氧条件下,会形成两种不同的肿瘤免疫血管生成生态系统,这与性别差异和ESR1表达有关。其中一个亚组(包括ESR1表达较低的男性患者)的特点是血管脆弱,同时出现坏死和高度炎症区域(称为坏死性炎症肿瘤)。这种男性特异性肿瘤亚型表现出与髓源性抑制细胞浸润有关的高炎症。利用这种分层方法,我们确定了一组可能对贝伐单抗(BVZ)有反应的患者,并揭示了一种基因特征,这种特征可能会应用于临床,预测哪些患者可能从这种治疗中获益最多。这项研究根据GBM的性别差异进行了分层,将预后不良与坏死区存在免疫抑制性髓细胞联系起来。使用这一新的分层方法可以筛查对BVZ治疗有反应的患者,从而改变目前GBM的预后。2. 临床前胶质母细胞瘤模型中EGFR扩增和EGFRvIII能预测并参与TAT-Cx43 266283 抗肿瘤反应EGFR amplification and EGFRvIII predict and participate in TAT-Cx43266–283 antitumor response in preclinical glioblastoma models
Andrea Álvarez-Vázquez and others
Neuro Oncol. 2024 Jul 5;26(7): 1230–1246, doi.org/10.1093/neuonc/noae060
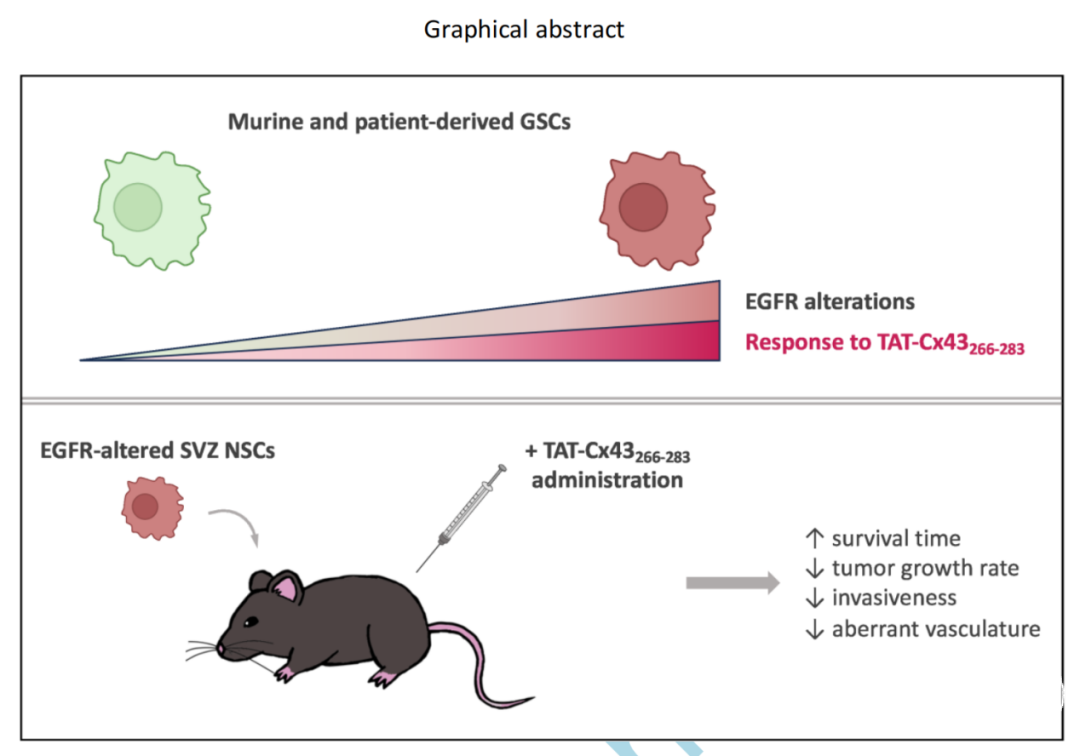
胶质母细胞瘤(GBM)尽管在基础和临床研究不断取得了进展,但仍是一种无法治愈的癌症,迫切需要新的治疗方法。GBM通常会伴有表皮生长因子(EGFR)改变(主要是扩增和EGFRVIII),EGFR、EGFRVIII触发的信号激活Src及其下游通路参与肿瘤发展,Src也可能磷酸化EGFR/EGFRVIII使之激活,形成一个正反馈循环。因此,这个正反馈循环,参与肿瘤细胞转化,被认为是一个令人关注的肿瘤治疗靶点。TAT-CX43-266283是一种Src抑制多肽,在临床前GBM模型中具有抗肿瘤特性。
本研究探讨TAT-CX43-266283、替莫唑胺(TMZ)和厄洛替尼(EGFR抑制剂)的疗效。通过Western blot(WB)和荧光原位杂交(FISH)分析这些细胞中EGFR的变化,并与TCGA GBM样本中的Src活性和存活率进行比较。1.TAT-CX43-266283对GSC活力和迁移的影响与GSC中EGFR的改变有关。我们分析了伴或不伴EGFR改变的人GSCs的侵袭和迁移。研究结果表明,TAT-CX43-266283显著降低,EGFR改变的人GSCs细胞运动率,而不伴EGFR改变的GSCs细胞运动率不受影响。
2.TAT-CX43-266283对GBM患者源性GSC活力的影响高于厄洛替尼或TMZ。我们比较了TAT-CX43-266283与厄洛替尼、TMZ对肿瘤细胞的反应差异。经TAT-CX43-266283治疗的GBM患者源性GSC细胞系,细胞活力抑制率最高。
3.TAT-CX43-266283对GSC的作用与EGFR的改变相关。我们研究了TAT-CX43-266283对不同EGFR改变的NSCs影响。首先,我们分析了TAT-CX43-266283对过表达EGFRwt(SVZ-EGFRwt)、EGFRvIII(SVZ-EGFRvIII)、 SVZ NSCs细胞活力的影响。TAT-CX43-266283仅降低过表达EGFR或EGFRvIII的NSCs细胞活力,而不影响SVZ-NSCs,证实了TAT-CX43-266283作用在肿瘤细胞中的选择性。4.IDHwt GBM患者的EGFR改变与Src活性呈正相关。在这些EGFR改变和未改变的GBM组之间的蛋白质水平比较显示,Src的活性形式(SRC_PY416)在EGFR改变的GBM中,是丰度显著增加的前十大蛋白质之一。数据分析显示,在GBM患者的TCGA样本中,EGFR改变与Src活性之间呈正相关。5.TAT-CX43-266283处理显著提高了NPE-IE细胞源性GBMs小鼠的存活率。我们选择NPE-IE细胞来测试TAT-CX43-266283对含有EGFR改变和其他GBM驱动突变的NSCs衍生肿瘤发展的影响,发现TAT-CX43-266283处理显著提高了NPE-IE细胞源性GBMs小鼠的存活率。综上所述,虽然我们的结果更支持TAT-CX43-266283治疗GBM的前景,但仍需要进一步的临床前研究。3. 联合P38MAPK和MEK抑制剂阻断间质型胶质母细胞瘤对替莫唑胺的适应性耐药Dual p38MAPK and MEK inhibition disrupts adaptive chemoresistance in mesenchymal glioblastoma to temozolomide
Hong Sheng Cheng and others
Neuro Oncol. 2024 Jul 5;26(7): 1247–1261, doi.org/10.1093/neuonc/noae028
目前对于GBM的治疗方法是最大限度的手术切除,随即使用替莫唑胺(TMZ)进行联合放疗和辅助化疗。这种治疗策略并没有考虑个体间的生物学差异,且复发率高,预后较差。间质型胶质母细胞瘤(ME)是复发性GBM的主要亚型,恢复ME对TMZ易感性可能克服其不良预后。本文是研究联合P38MAPK和MEK双重抑制对抗原发性和复发性GBM肿瘤对替莫唑胺的耐药。
通过比较SB202190(P38MAPK的抑制剂)和空白对照处理的ME胶质瘤增殖细胞(GPCs)之间的转录组学,证实了P38MAPK信号对药物外排泵的调控作用。此外,SB202190可以减弱ME GPCs中的DNA修复机制。根据彗星试验,与TMZ单独处理相比,TMZ+P38MAPK抑制剂共处理的ME GPCs中有更多的DNA断裂;而在PN GPCs中,共处理没有诱导额外的DNA损伤。
为了探索P38MAPK信号传导与DNA修复之间的关系,在ME GPCs中发现过度表达一种活性形式的MKK3(CAMKK3),它是P38MAPK激酶的上游调节因子,可增强P38MAPK的磷酸化。CAMKK3消除了P38MAPK抑制剂对DNA修复的抑制作用。用DNA- PK抑制剂AZD7648靶向DNA修复信号,加重了对照ME GPCs的DNA损伤,但在CAMKK3样本中效果较差。因此,DNA修复能力明显受到P38MAPK级联反应的影响。ME GPCs保留了较高的P38MAPK基础活性,提高了药物外排和DNA修复活性,这两者都有助于ME亚型的内在化学耐药。利用P38MAPK抑制剂作为辅助治疗可以使ME GPCs对TMZ重新敏感。
通过RNA-SEQ数据,发现酸分泌活性和钙信号明显受到P38MAPK抑制的干扰。根据基因组学筛选,MEK/ERK通路也是ME特异性激酶靶点,通过检测耐药ME GPCs中MEK/ERK的磷酸化,建立细胞内钙与MEK/ERK信号传导之间的调节关系。发现,在耐药的ME GPCs中,PH稳态受到P38MAPK的影响。P38MAPK抑制引起的酸中毒增加了胞质钙,激活了MEK/ERK信号作为延长生存期的适应性反应。P38MAPK和MEK/ERK信号通路的同步衰减有效对抗了ME GPCs中的TMZ化学耐药。
一种通过血脑屏障的P38MAPK抑制剂Ralimetinib,在I期试验中作为新诊断的GBM患者合并TMZ放疗的辅助方案。协同SEQ分析预测,P38MAPK抑制剂如Ralimetinib和Talmapimod与TMZ+放疗表现出低转录组一致性,与ME特征高度不一致,表明标准治疗和ME型耐药逆转药物的潜在协同作用。通过细胞活力测定证实了拉利替尼与TMZ的有效特异性协同作用,增强了药物对ME而非PN GPCs的细胞毒性。当Ralimetinib和其他P38MAPK抑制剂与TMZ联合使用时,激活钙介导的MEK/ERK信号。通过对小鼠口服Ralimetinib剂量进行滴定,可以显著抑制脑组织中P38MAPK下游蛋白靶点HSP27的磷酸化。在使用BAPTA-AM(一种清除胞质钙离子的钙螯合剂)的ME GPCs中,p38MAPK抑制剂和TMZ共处理的促凋亡作用被加剧。对于P38MAPK耐药和复发性ME肿瘤的适应性化疗耐药,使用了两种不同的方法。首先,通过将亲本细胞暴露于增加TMZ和Ralimetinib浓度的多个细胞周期后,建立了抗P38MAPK的GLIO-0082细胞系GLIO-0082-R,用于颅内PDX肿瘤模型。与单独使用Ralimetinib相比,靶向P38MAPK和MEK的双重抑制策略与TMZ联合使用,提高了GLIO-0082-R脑肿瘤小鼠的存活率,并降低了肿瘤的增殖。另外,通过将皮下GLIO-0087异种移植物的活细胞重新植入小鼠,建立了复发性GBM模型;先前暴露于TMZ+SB202190+Binimetinib(MEK抑制剂)联合治疗的肿瘤细胞,与单独接受TMZ+SB202190治疗的肿瘤细胞相比,表现出延迟复发和较慢的生长速度。P38MAPK抑制对于恢复ME GPCs体内TMZ化学敏感性至关重要。但这种效应很快被MEK/ERK信号的激活所抵消,从而导致适应性化学耐药。通过来自不同GBM PDX肿瘤模型的数据强调了双重P38MAPK-MEK抑制的有效性,通过同时靶向内在和适应性耐药机制可实现持久的TMZ再致敏。
联合抑制p38MAPK和MEK双重抑制的辅助治疗不仅延长了TMZ敏感性,而且有效地对抗了原发性和复发性GBM肿瘤异种移植体,特别是ME亚型的适应性化疗耐药。这种方法作为一种精确的治疗策略具有很大的前景,可以专门针对并克服ME亚型肿瘤带来的挑战。
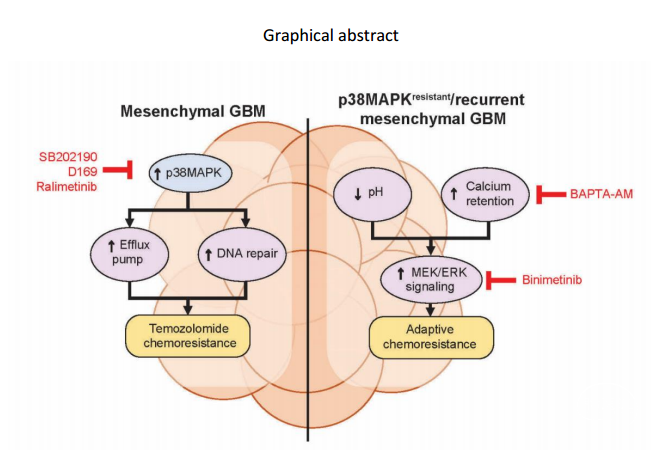
图:Mesenchymal GBM:间充质胶质母膜细胞瘤;Temozolomide chemoresistance:替莫唑胺药物抗性;Efflux pump:外排泵;DNA repair:DNA修复;Calcium retention:钙保留;MEK/ERK signaling:MEK/ERK信号转导;Adaptive chemoresistance:自适应化学抗性;BAPTA-AM:一种清除胞质钙离子的钙螯合剂
4.脑膜瘤中分泌型簇集素调节肿瘤细胞和巨噬细胞以抑制肿瘤发生Secreted clusterin inhibits tumorigenesis by modulating tumor cells and macrophages in human meningioma
Chao Ke and others
Neuro Oncol. 2024 Jul 5;26(7): 1262–1279, doi.org/10.1093/neuonc/noae034
脑膜瘤是成人中枢神经系统常见的原发性肿瘤之一。约20%的高级别脑膜瘤尽管采用了综合治疗,仍然表现出侵袭性。因此,需要在深入探索肿瘤恶性进展与微环境演变相关的分子变化,开发新的治疗方法。首先该研究通过对单细胞测序数据进行分析标记主要细胞种类,随后筛选出与肿瘤恶性相关的细胞簇;然后对该细胞簇进行多轮细胞命运轨迹分析,筛选出始终与恶性程度呈负相关的基因——CLU,最后在细胞系和动物实验中进行相关功能验证,如通路富集分析、生存分析、免疫评分等。(1)利用单细胞RNA测序研究了13例患者的18个脑膜瘤样本,包括正常脑膜、良性与高级别脑膜瘤、复发性及转移性脑膜瘤,较好地代表了脑膜瘤的恶性进展过程。通过细胞命运轨迹分析与免疫组化表明,CLU表达与脑膜瘤恶性程度呈负相关,CLU表达降低可能与肿瘤增殖和进展有关。
(2)通过分别建立CLU过表达与敲除细胞系与相关动物实验进一步表明:CLU可降低脑膜瘤细胞的致瘤潜能、抑制细胞的肿瘤干性和侵袭性,同时发现CLU 蛋白的抑制作用依赖于其细胞外分泌异构体而不是细胞内异构体。(3)CLU抑制脑膜瘤的分子机制包括:CLU过表达导致线粒体数量减少;CLU 可能通过P65和促炎细胞因子发挥抑制作用;CLU通过触发I型干扰素通路来发挥抑制作用;CLU可能通过CLU-TLR2-INFs轴抑制脑膜瘤的发生和生长,TNFα可增强这一作用。
(4)通过对脑膜瘤的微环境表征发现:CLU通过刺激TNFα表达来诱导巨噬细胞向M1表型极化,从而促进巨噬细胞的抗肿瘤功能。
最终本研究得出结论:CLU可能通过调节肿瘤细胞及其微环境成为恶性脑膜瘤的关键抑制剂,为恶性脑膜瘤的治疗提供新的思路。
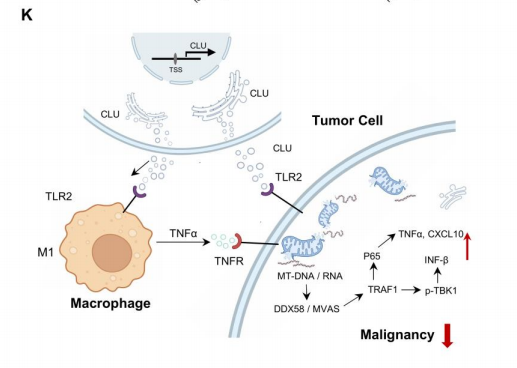
图:CLU抑制脑膜瘤的模型。组蛋白去乙酰化酶抑制可促进脑膜瘤肿瘤细胞中CLU的表达。分泌的CLU蛋白与肿瘤细胞表面的TLR2结合,导致线粒体损伤,促进I型干扰素途径和P65的表达。分泌的CLU蛋白还能刺激M1巨噬细胞产生TNFα和吞噬功能。TNFα还能促进脑膜瘤中的I型干扰素途径。总的来说,CLU通过抑制肿瘤细胞和极化M1巨噬细胞来预防脑膜瘤恶性肿瘤。
5. 循环细胞外囊泡作为胶质母细胞瘤患者诊断、预后和监测的生物标志物Circulating extracellular vesicles as biomarker for diagnosis, prognosis, and monitoring in glioblastoma patients
Franz L Ricklefs and others
Neuro Oncol. 2024 Jul 5;26(7): 1280–1291, doi.org/10.1093/neuonc/noae068
胶质母细胞瘤患者通过重复磁共振成像(MRI)扫描进行常规诊断和术后监测。然而,因MRI检查昂贵且耗时,并且可能表现为假性进展,为了更好的诊断和评估胶质母细胞瘤患者预后,本文作者提出了通过非侵入性液体活检从患者血液中获得的细胞外囊泡(EV)可以作为1种有效的生物标志物。
方法:分别在术前、术后1天和术后4-6天。从病情稳定或进展的患者亚组中采集血液。通过纳米颗粒示踪分析和成像流式细胞术测量EV浓度。通过3D重建对肿瘤负荷和水肿进行定量。在胶质瘤小鼠中进一步监测EV和肿瘤。
本文研究发现:胶质母细胞瘤患者中少于10%的循环EV来源于肿瘤细胞。目前已知大多数循环EV来源于血细胞,特别是血小板。胶质母细胞瘤患者经常显示血小板增多,本文发现血小板计数和循环EV之间没有相关性,表明EV升高并不主要来源于血小板。CD 63+ EV在患者血浆中升高最强烈(10倍),并且双阳性CD 63+/CD 81+ EV甚至升高14倍,表明这些循环EV的肿瘤细胞来源。CD 63+和CD 81+ EV进一步与FLAIR高信号相关,表明血脑屏障(BBB)的泄漏参与了它们进入血流。值得注意的是,CD 63+以及CD 9+/CD 63+ EV进一步与中性粒细胞和嗜中性粒细胞与淋巴细胞比率相关。中性粒细胞和单核细胞反过来与FLAIR相关,表明BBB通透性增加可能影响外周髓样细胞数量,并且肿瘤源性EV升高可能参与骨髓髓样细胞募集,这是胶质母细胞瘤患者肿瘤诱导免疫抑制的重要机制。为了进一步评估EV用于监测治疗反应和疾病控制的潜力,本文在长期随访检查期间重复测量血浆EV浓度,并将其与MRI确定的肿瘤状态进行比较。在病情稳定的患者中,EV浓度保持在健康供体水平的范围内,而在肿瘤复发的患者中,EV水平再次显著升高。
结论:1.循环EV是胶质母细胞瘤患者生存的独立预后参数;2.血浆EV水平与FLAIR高信号相关,但与肿瘤大小或血液参数无关;3.EV计数在术后迅速下降,术后下降的幅度与肿瘤切除的程度相关;4.EV浓度在肿瘤复发时再次增加,并且可以在MRI明显可检测之前指示肿瘤的存在。本文首次证明了术前循环EV浓度是总生存率的独立预后参数。这表明EV浓度的评估在临床上可用于支持治疗决策,并且高水平的囊血症可能主张更激进的治疗方案。术前定量EV分析可以提供有价值的预后信息,以帮助治疗决策。通过非侵入性液体活检进行术后EV连续监测可能有助于早期复发检测和适当的治疗适应。从未来的角度来看,循环肿瘤EV的定量和分子分析可能能够额外告知临床医生肿瘤细胞随时间推移获得的遗传和表观遗传改变。【刘仲涛】
NEUROIMAGING
1. 中期FDG-PET改善原发性中枢神经系统淋巴瘤治疗失败的预测:一项前瞻性多中心研究
Interim FDG-PET improves treatment failure prediction in primary central nervous system lymphoma: An LOC network prospective multicentric studyLaura Rozenblum and othersNeuro Oncol. 2024 Jul 5;26(7): 1292–1301, doi.org/10.1093/neuonc/noae029本研究的目的是评估60岁及以上原发性中枢神经系统淋巴瘤(PCNSL)患者接受大剂量甲氨蝶呤化疗(HD-MBC)期间2-18氟-2-脱氧葡萄糖(FDG)正电子发射断层扫描(PET)/MRI的预测和预后作用。
老年人原发性中枢神经系统淋巴瘤(PCNSL)的治疗是神经肿瘤学的一个关键挑战。目前用于早期风险分层的工具不够准确,导致次优治疗策略。这项研究强调了中期2-18F-氟-2-脱氧-D-葡萄糖(FDG)正电子发射断层扫描(PET)区分治疗反应良好和不良的PCNSL患者的潜力。在部分缓解的情况下,中期FDG-PET可能优于中期形态学MRI,可更有效地预测诱导治疗结束时的无进展生存期和缓解。在我们的研究中,多变量分析也证实了中期FDG-PET成像的预测能力。这些结果加强了FDG-PET在PCNSL管理中的作用,并可作为未来FDG-PET指导的临床试验的基础。将FDGPET成像整合到常规实践中有望改善PCNSL的风险适应性治疗策略和改善结局。
原发性中枢神经系统淋巴瘤(PCNSL)是一种罕见的非霍奇金淋巴瘤,局限于脑、眼和脑脊液(CSF),无任何全身扩散。1 PCNSL的治疗基于老年患者的高剂量甲氨蝶呤化疗(HD-MBC),以及与干细胞自体移植相关或不相关的HD-MBC,作为年轻和健康患者的巩固治疗。2-PCNSL的预后是高度可变的,特别是在老年人中,和临床标志物,如年龄或体能状态,不足以预测化疗后的耐药性或复发风险。国际原发性中枢神经系统淋巴瘤协作组(IPCG)目前建议使用主要基于脑部MRI的标准进行反应评估。Tabouret等人10已经描述了T1造影剂的客观反应之间的相关性,治疗结束时的增强MRI和总生存期(OS)。然而,几项研究报告了在治疗结束时MRI显示完全缓解(CR)的患者中早期检测到复发,从而质疑其评估残留疾病的有效性。在一项涉及199名PCNSL患者的随机对照试验中,发现一线治疗结束时MRI显示CR或部分缓解(PR)的患者之间的无进展生存期(PFS)或OS无显著差异。因此,尽管MRI是PCNSL评估中的一种有价值的工具,但仍需要改进评估方法,特别是中期评估。
我们在增强MRI序列上使用相同的靶病变来评估增强靶病变体积的变化,表示为TVOL 1-2。在随访评估中,患者被分为2类:“反应良好”和“反应不良”。对于MRI,良好应答者组包括CR和CRu,而不良应答者组包括SD、PR或进展患者。对于PET,良好应答者组具有阴性扫描,表明任何先前病理性摄取完全正常化。低反应者的FDG-PET扫描呈阳性,表明PR、疾病稳定或进展。PR的标志是病变代谢减少,但残留活性超过对侧镜像皮质。病情稳定显示靶病变无变化,而进展定义为新病灶、扩展或病变代谢增加。应该强调的是,在诱导治疗完成后,治疗决定完全由IPCG标准指导,不受中期或最终FDGPET评估结果的影响。
我们研究的局限性包括由于这种疾病的罕见性,患者样本量相对较小。然而,我们的队列,预先确定的评估时间点和统一的诱导化疗,是最大的PET研究报告。该研究的优势包括其前瞻性设计和创新的混合PET/MRI系统的使用。这种先进的技术通过允许同时研究代谢摄取以及扩散和灌注模式,促进了对潜在病理生理机制的并行分析。另一个限制是诱导后PET-MRI管理策略的变化,一些患者接受维持治疗,另一些患者仅接受监测。在BLOCAGE 01试验结束之前,亚组分析待定(主要分析计划于2024年进行)。尽管有这些局限性,我们的研究的关键发现是,中期FDG-PET成像可以作为PCNSL进展的简单,早期和独立的生物标志物。然而,这些发现需要在更大的患者队列中进一步验证。其他成像方式,如11C-蛋氨酸和18F-氟达拉滨,正在研究其在管理PCNSL的有用性。然而,关于其效用的数据仍然有限,需要进一步的研究来确定其在这种疾病中的作用。循环肿瘤DNA也被发现是侵袭性淋巴瘤的独立预测因子,并可能在未来的治疗评估中发挥作用。
据我们所知,我们的研究是第一个提供前瞻性证据,支持早期FDG-PET评估在预测化疗反应中的作用和老年PCNSL患者的结局。这种方法,可以很容易地纳入临床实践中,有望成为一个关键的工具,在PCNSL的管理。我们的研究结果表明,密切的MRI随访应及时考虑患者的中期FDGPET结果呈阳性。虽然我们的研究强调了PET在PCNSL个性化医疗策略中的潜力,但还需要进一步的研究来充分证实其预测作用。
【刘仲涛】
2. EORTCBTG-1320临床试验中WHO 2级和3级复发性脑膜瘤的3D体积生长率评价
3D volume growth rate evaluation in the EORTC-BTG-1320 clinical trial for recurrent WHO grade 2 and 3 meningiomasEmeline Tabouret and othersNeuro Oncol. 2024 Jul 5;26(7): 1302–1309, doi.org/10.1093/neuonc/noae037我们之前报道了肿瘤三维体积生长速率(3DVGR)分类可以帮助评估脑膜瘤患者的药物活性,采用3个主要分类,共5个亚分类:1类:减少;2类:稳定或严重减缓;3:进展。EORTC-BTG-1320临床试验是一项随机II期试验,评估trabectedin治疗复发性WHO 2或3型脑膜瘤的疗效。我们的目的是评估EORTC-BTG-1320中3DVGR分类的判别价值。
脑膜瘤是成人最常见的颅内肿瘤。大多数脑膜瘤是良性的,符合CNS WHO 1级。然而,大约20%-25%的病例表现为脑侵袭性、细胞异型性或有丝分裂活性增加,导致复发风险增加。因此,这些肿瘤被划分为CNS WHO 2级或3级脑膜瘤这些侵袭性脑膜瘤经常在局部治疗(如手术和放疗)后进展,构成治疗挑战和神经肿瘤学未满足的医疗需求。尽管在过去几年中对各种药物进行了多次临床试验,但大多数药物对脑膜瘤患者的活性和临床益处的证据有限。在过去的几年里,对脑膜瘤的突变景观、细胞内信号通路激活和微环境的了解有所增加。
最近,我们报道了基于CEVOREM脑膜瘤临床试验数据的3D体积增长率(3DVGR)可用于评估药物活性。3DVGR似乎比经典PFS6在活动信号方面更具判别性。根据治疗前和治疗后的3DVGR,该分类将脑膜瘤反应分为3个主要类别,共5个亚类别。EORTC-1320-BTG随机II期试验评估了trabectedin在复发性侵袭性脑膜瘤中的活性。Trabectedin是一种从加勒比海鞘中提取的四氢异喹啉碱。Trabectedin形成DNA加合物,影响多种转录因子和DNA修复机制,具有免疫调节和抗血管生成proper-ties。
Trabectedin在晚期软组织肉瘤和卵巢癌中已显示出临床意义的疗效和良好的耐受性,目前已被批准用于这些适应症。然而,使用trabectedin并没有显著改善复发性WHO 2级或3级脑膜瘤患者的无进展生存期(PFS)和总生存期(OS)。
我们的研究有助于验证3DVGR评估在脑膜瘤临床试验中的临床价值。我们发现,与经典的修正麦克唐纳标准相比,这种分类允许更准确的患者分层,并且是6个月时PFS的相关替代标记。此外,这种分类与患者的临床获益相关,突出了其在早期药物评估中的潜在作用。脑膜瘤临床试验中药物活性的评估仍然具有挑战性,但在有效的全身治疗有限的疾病中至关重要。治疗获益评估面临着不同的挑战:低患病率使3期临床试验具有挑战性,高度可变的生长速率,低反应率(小于5%)和长期的总生存期。SD患者通常表现出高度可变的进化,包括非常快的进展和更长期的稳定,强调了该亚组的异质性医学上迫切需要完善脑膜瘤临床试验的反应标准,以便早期发现药物活性。PFS6是目前临床试验中评估复发性高级别脑膜瘤的最一致的标准,历史临床试验之间的比较较少。然而,PFS6也有许多局限性,特别是在生长缓慢的肿瘤中。其他经典的神经影像学主要疗效终点是麦克唐纳、RECIST、RANO标准或体积估计的缓解率症状评估也被用作次要终点。最后,质子治疗脑膜瘤的表观扩散系数的变化也被认为是治疗反应的预测指标。
我们最近提出将体积评估和更具体的3DVGR计算纳入脑膜瘤临床试验。我们的3DVGR分类的双重利益是引入脑膜瘤生长放缓(2级)的积极影响的概念,并带来真正的患者利益,以及使用患者自己的比较,从而实现个性化的反应评估。在CEVOREM研究中,评估依维莫司和奥曲肽联合使用,只有10%的治疗肿瘤出现体积缩小,也没有达到定义PR的25%的缩小。尽管如此,患者经历了这种治疗的临床益处,神经系统改善,PFS和OS延长。这些结果表明,尽管没有观察到肿瘤大小缩小,但治疗后3DVGR的减缓可能会使患者受益。3DVGR似乎与生长缓慢的中枢神经系统WHO 1级脑膜瘤特别相关,而PFS6率不适用。在本研究中,类似地,我们观察到一些有临床获益的患者根据修改的麦克唐纳标准没有反应;然而,它们被归类为3DVGR 1级或2级。因此,3DVGR分类在区分患者获益方面似乎比经典反应标准更敏感。基线前MRI可用的患者数量较少是我们研究的一个局限性。然而,该结果与CEVOREM试验的观察结果一致,并加强了对脑膜瘤临床试验中纵向3DVGR评估的兴趣。
综上所述,脑膜瘤3DVGR分级可以更准确地进行患者反应分层,并与PFS6和临床获益相关。这种分类可能对未来脑膜瘤临床试验早期识别积极和有前景的全身治疗有兴趣。
【刘仲涛】
PEDIATRIC NEURO-ONCOLOGY
1. 视神经通路胶质瘤患儿的长期疗效:一项纵向队列研究
Very long-term outcomes of pediatric patients treated for optic pathway gliomas: A longitudinal cohort studyNeuro Oncol. 2024 Jul 5;26(7): 1310–1324, doi.org/10.1093/neuonc/noae045
背景:视路胶质瘤(OPG)占儿童脑肿瘤的5%。反复复发导致治疗次数增多最终导致晚期并发症增多。
方法:本研究纳入1980年1月至2015年12月在古斯塔夫鲁西(GR)中心接受治疗的,年龄<18岁,诊断后生存期大于5年的OPG患者。死亡和健康状况数据从医疗数据文件提取。
结果:研究纳入182例存活5年以上的OPG-儿童患者(男女性比0.8,患有1型神经纤维瘤病[NF1] 的35%)。中位随访时间为17.2年(范围为5-41年)。5年后有82例复发、9例继发性恶性变和15例死亡,将这些患者作为的主要观察的终点事件,患者20年的总生存期(C-OS)和晚期无事件生存期分别为79.9%(95% CI=71-86)和43.5%(95% CI=36-51)。在多变量分析中, NF1患者的放疗暴露(危险比[HR]=6,95% CI=1.7-21.2)和下丘脑受累(HR=3.2,95% CI=14-7.3)与C-OS显著相关。95%的存活5年OPG患者存在一些健康问题,特别是视力方面“<1/10”(n=109),垂体功能缺陷(n=106)和神经认知障碍(n=89)。NF1(HR2.1)与性早熟有关。在21例患者中观察到33次脑血管事件,诊断后平均生存期为4.2年。
结论:晚期复发,继发性恶变和脑血管疾病是导致过早死亡的严重事件。虽然该病发病率高,但加强癌后的护理,可以提高生活质量。在后续的研究中,可以根据风险因素,更好地进行分层研究。
【郭少春】
2. MYB/MYBL1改变的儿童型弥漫性低级别胶质瘤的综合分析
Comprehensive analysis of MYB/MYBL1-altered pediatric-type diffuse low-grade glioma Daniel C Moreira and othersNeuro Oncol. 2024 Jul 5;26(7): 1327–1334, doi.org/10.1093/neuonc/noae048背景:儿童型弥漫性低级别胶质瘤(pLGG)含有涉及MYB或MYBL1的复发性基因改变,是跟肿瘤密切相关。目前缺乏大型队列的详细治疗和结果数据研究。本研究旨在全面评估具有这些改变的pLGG,以确定其最佳治疗策略。
方法:研究回顾了在圣裘德儿童研究医院接受治疗或转诊进行病理审查的患者中具有MYB或MYBL1改变的pLGG的详细信息。对肿瘤样本进行集中审查,并整理临床数据。
结果:共纳入33例患者(18例男性;年龄中位数为5岁)。2例肿瘤MYBL1发生改变;31例MYB发生改变,MYB:QKI融合是最常见的改变(10例,30%)。大多数肿瘤位于大脑半球(22例,67%)。2例患者(6%)在诊断时出现转移。中位随访时间为6.1年。5年无事件生存(EFS)率为81.3%±8.3%;5年总生存(OS)率为96.4%±4.1%。接受近全切除或全切除的患者5年EFS率为100%;接受活检或次全切除的患者5年的EFS率为56.6%±15.2%(P<0.01)。根据位置、组织学或分子改变,EFS率没有差异。然而,进展或转移的肿瘤可能具有独特的甲基化特征,有证据表明MAPK和PI3K/AKT/mTOR通路被激活。
结论:具有MYB/MYBL1改变的pLGG有良好的预后。我们的发现表明,手术可切除性是EFS的关键决定因素。需要进一步表征以确定进展性肿瘤的最佳治疗策略。
【郭少春】
3. 颅内生殖细胞肿瘤的新型分子亚型扩大了治疗机会
Novel molecular subtypes of intracranial germ cell tumors expand therapeutic opportunitiesNeuro Oncol. 2024 Jul 5;26(7): 1335–1351, doi.org/10.1093/neuonc/noae038背景:颅内生殖细胞肿瘤(IGCTs)是一组罕见的恶性肿瘤,临床上分为生殖母细胞瘤和非生殖母细胞瘤(NGGCTs)。既往研究发现,涉及丝裂原活化蛋白激酶/mTOR信号通路的体细胞突变是常见的早期事件。然而,目前仍缺乏对IGCTs的全面基因组学认识。
方法:我们建立了一个包括100多个IGCT的队列,并进行基因组和转录组测序。
结果:我们发现了新的复发驱动基因组突变,包括USP28截短突变和由外染色体DNA复制引起的KRAS和CRKL的高水平拷贝数扩增。转录组分析确定了与独特的基因组和临床表型相关的三种不同亚型:免疫热、MYC/E2F和 SHH。免疫热和MYC/E2F主要在成釉细胞瘤中鉴定到,并具有涉及 RAS/MAPK信号通路的相似突变。然而,免疫热组显示出较晚的疾病发作年龄和显着的免疫反应。MYC/E2F的特征是较年轻的疾病发作年龄和增加的基因组不稳定,有较高比例的肿瘤显示全基因组加倍。此外,SHH亚型主要在NGGCTs中鉴定到。
结论:在IGCTs中发现了新的基因组异常和分子亚型,这些发现为在这一背景下引入新的治疗策略提供了分子基础。
【郭少春】
















