
【大家说】栏目,关注脑疾病转化医学前沿,综合研究成果概述、研究作者自述和国内权威专家解读。本期栏目,我们特别邀请到中山大学肿瘤防治中心的陈忠平教授和杨群英主任医师,为我们解读并分享最新发表在《The NEW ENGLAND JOURNAL of MEDICINE》(NEJM)上关于脑室内输注CARv3-TEAM-E T细胞治疗复发性胶质母细胞瘤的研究成果。
一、研究概述
胶质母细胞瘤(GBM)是最具侵袭性的原发性脑肿瘤,复发后预后极差且无有效疗法。嵌合抗原受体T细胞(CAR-T细胞)在治疗癌症方面颇具潜力,已被证明对难治性淋巴系统恶性肿瘤有效并成为标准疗法。然而,CAR-T细胞在GBM等实体瘤中的应用一直受限,主要是因为在异质性疾病中靶向单一抗原存在挑战,且存在与肿瘤微环境相关的免疫抑制机制。


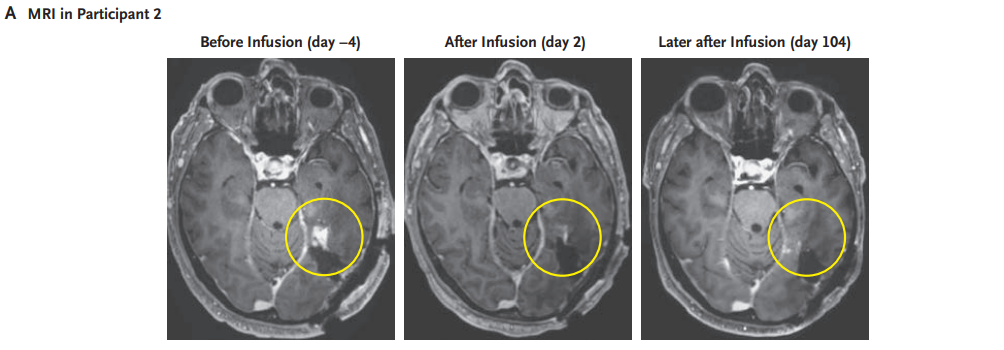
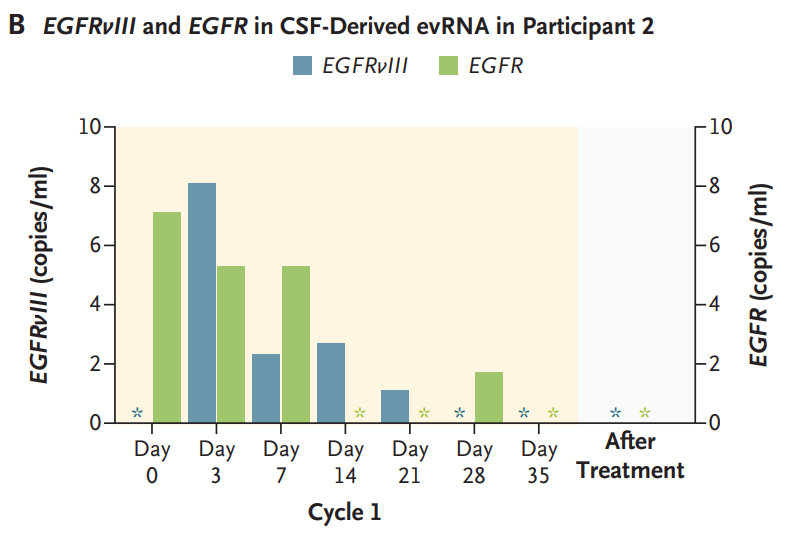
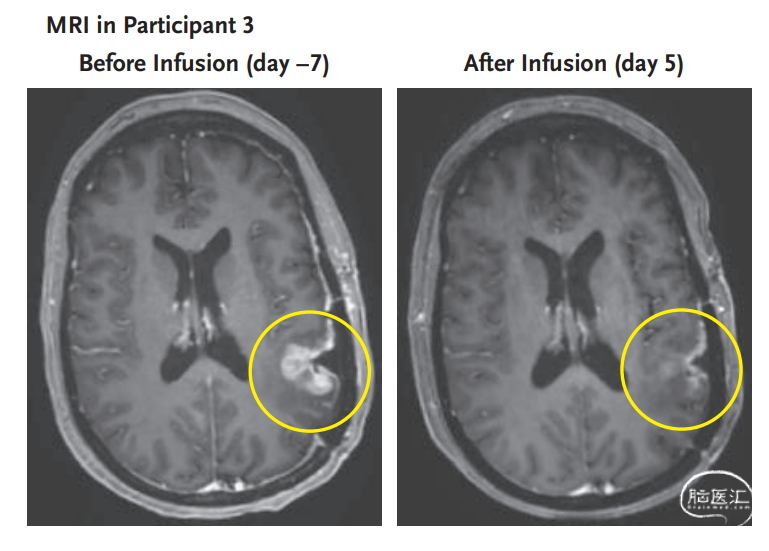
患者3


+ + + + + + + + + + +
文章来源
Choi BD, Gerstner ER, Frigault MJ, et al. Intraventricular CARv3-TEAM-E T Cells in Recurrent Glioblastoma. N Engl J Med. Published online March 13, 2024. doi:10.1056/NEJMoa2314390
二、作者自述
三、陈忠平教授和杨群英主任医师的权威解读
专家介绍
陈忠平 教授
中山大学肿瘤防治中心
主任医师、教授、博士生导师
中山大学肿瘤防治中心神经外科创科主任,胶质瘤单病种首席专家
中国名医百强榜“脑胶质瘤手术Top 10医生”
王忠诚神经外科医师奖(2006年学术奖)
中国抗癌协会神经肿瘤专业委员会(第一、二、五届)主任委员
中华医学会神经外科分会神经肿瘤专业委员会第一届委员
中国医师协会神经外科医师分会神经肿瘤专业委员会第一届委员
广东省/广州抗癌协会神经肿瘤专业委员会第一届主任委员
广东省神经外科学会第七、届八副主任委员
《Glioma》主编
杨群英 主任医师
中山大学肿瘤防治中心
医学博士,主任医师,硕士生导师
中山大学附属肿瘤医院神经外科/神经肿瘤主诊教授,胶质瘤单病种专家组核心成员
新疆医科大学附属肿瘤医院神经外科名誉科室主任
广东省基层医药学会脑胶质瘤专委会主任委员
中国抗癌协会神经肿瘤专业委员会委员
中国医师协会脑胶质瘤专业委员会委员
中国医学同行评议神经肿瘤学委员会委员
中国神经科学学会神经肿瘤分会委员
广东省抗癌协会神经肿瘤专委会常委/儿童脑瘤学组副组长
广东省医疗行业协会神经外科管理分会常委
《医学参考报》神经肿瘤专刊常务编委
泛中南神经肿瘤联盟远程会诊负责人
M.D. Anderson癌症中心、香港中文大学访问学者
第十批中央和国家机关、中央企业优秀援疆干部人才
第九届“羊城好医师”
![]()
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。
投稿邮箱:NAOYIHUI@163.com
未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。








