作者单位:1江苏省人民医院神经外科,2南京脑科医院
REF: Zhang J, Zhao L, Xuan S, et al. Global analysis of iron metabolism-related genes identifies potential mechanisms of gliomagenesis and reveals novel targets [published online ahead of print, 2023 Aug 7]. CNS Neurosci Ther. 2023;10.1111/cns.14386. doi:10.1111/cns.14386
铁是人类细胞各种基本功能所必需的元素,涉及DNA复制、修复和转运的众多酶依赖于细胞内铁。然而过多的铁负荷与增加的活性氧有强烈关联,从而促使癌症发生。Zhou等人发现铁螯合剂Dp44mT通过IL6/JAK2/STAT3信号通路抑制了胶质瘤细胞的增殖并促进凋亡。Masui等人证明mTORC2通过调节铁相关基因的启动子区域的组蛋白H3乙酰化来调控胶质瘤细胞的铁代谢,从而维持其恶性特征。然而既往研究多着眼于某单个基因,尚未广泛地研究铁代谢在胶质瘤中的分子机制。
利用来自多个跨平台的胶质瘤队列的大规模转录组数据,基于一系列生物信息学和机器学习方法,鉴定了与铁代谢相关的关键基因(IMRGs),并分析了IMRGs与患者预后、间质表型和基因组变化之间的关联。本研究还评估了基于IMRGs的模型在预测替莫唑胺治疗敏感性方面的性能。此外,通过一系列体内、外实验探究了这些关键基因的在胶质瘤中的细胞生物学功能。TCGA GTEx队列转录组数据提示IMRGs在正常脑组织和胶质瘤样本之间存在不同的表达模式。同时,REMBRANDT、GSE147352、GSE59612和GSE116520的四个独立的外部数据集进一步确认了IMRGs在胶质瘤中的异常调控。通过加权基因共表达网络分析、差异基因筛选以及单因素Cox回归分析,初步筛选出7个潜在的关键IMRGs。进一步结合随机生存森林算法根据相对重要性鉴定出STEAP3、LTF、HMOX1作为胶质瘤进展中的关键铁代谢调控基因。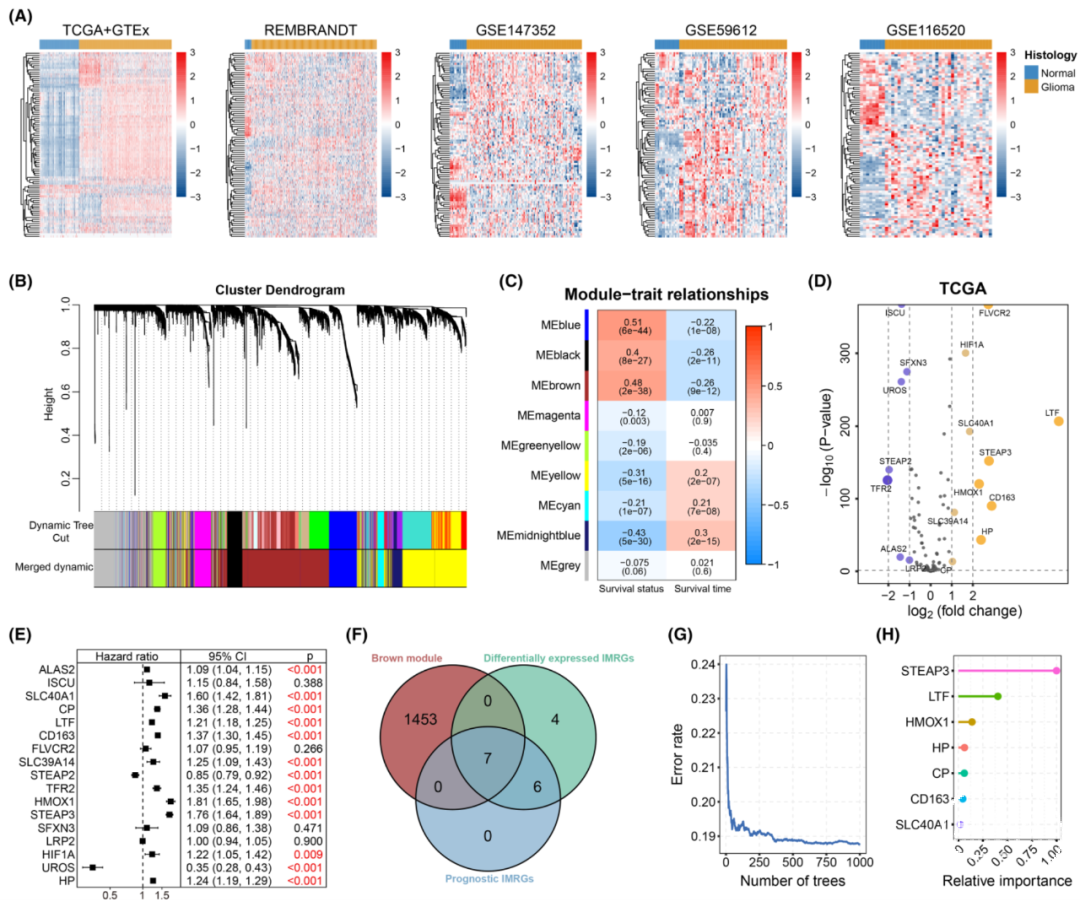
图1. 铁代谢相关基因在胶质瘤中的表达模式及关键基因的鉴定。
在TCGA、CGGA和Gravendeel队列中,STEAP3、LTF、HMOX1的表达随着组织病理等级的升高而增加。同时,关键IMRGs在胶质母细胞瘤(GBM)中的表达水平显著高于配对正常脑组织。免疫组织化学染色进一步验证了IMRGs的蛋白表达与病理等级密切相关。
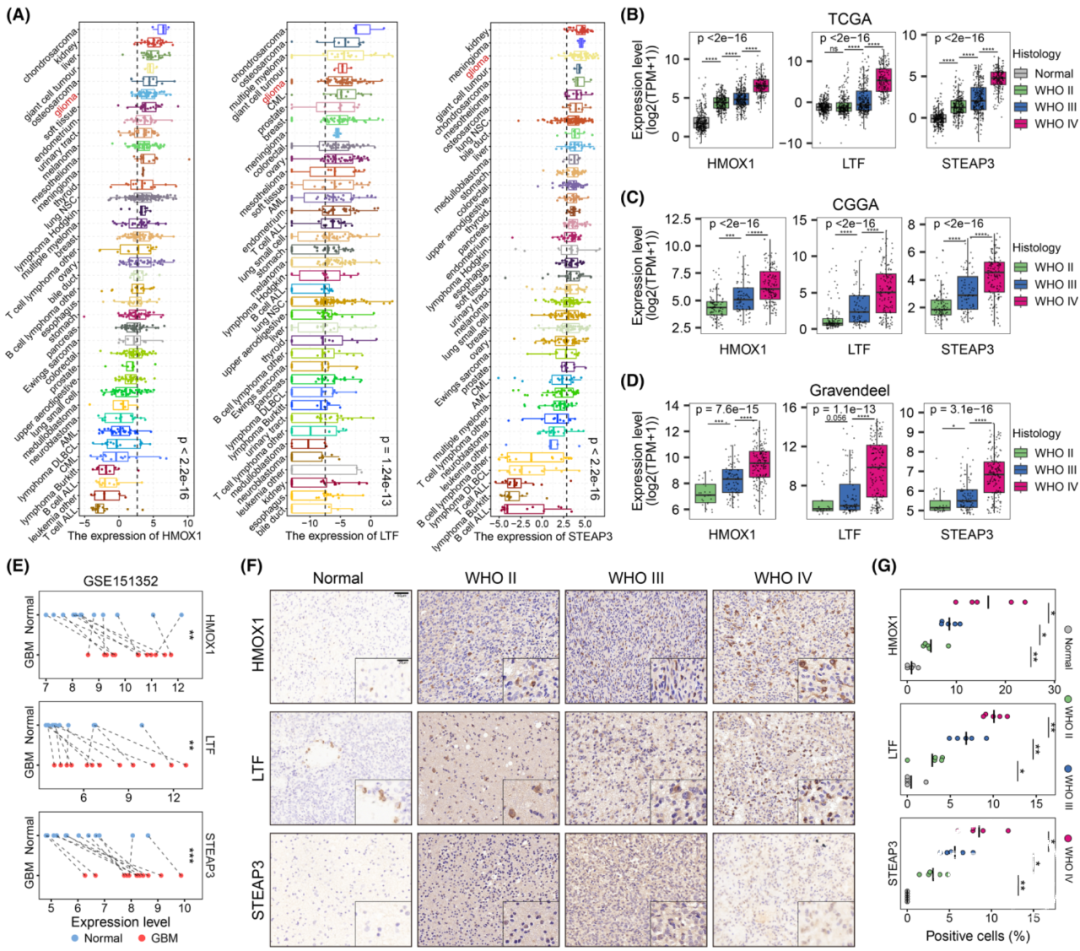
图2. 关键IMRGs的表达与胶质瘤病理等级密切相关。
TCGA和CGGA队列表明STEAP3、LTF、HMOX1的表达水平和IDH突变、1p/19q共缺失状态显著相关。此外,它们的表达与胶质瘤的分子亚型和肿瘤组织内的空间结构区域有关。间质型胶质瘤中表达这三个基因相较于其他亚型更多。这些基因在肿瘤内的坏死区域和影像学对比增强区域的表达水平更高。
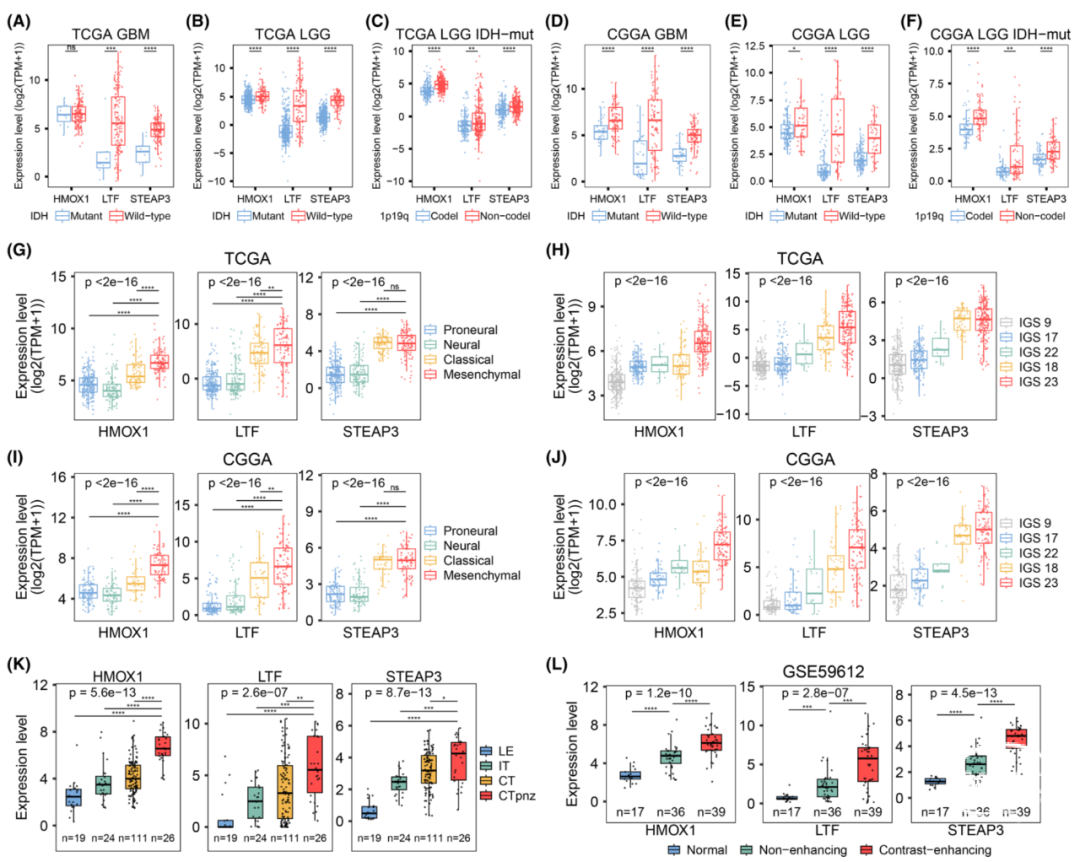
图3. 不同分子特征和细胞组成的胶质瘤中IMRGs的表达模式。
利用TCGA队列构建了一个基于IMRGs的风险模型,从而进一步将患者分为高风险和低风险组。Kaplan– Meier生存分析提示高风险组的患者预后明显差于低风险组。这一结果在多个独立数据集中均得到验证。Meta分析也证实了这三个关键铁代谢相关基因与患者的预后密切相关。单因素和多因素Cox回归分析证明IMRGs组成的基因signature可以作为胶质瘤的独立预后因子。本研究还开发了一个基于列线图的预测模型,可以辅助量化每个患者个体的风险得分以预测第1、2、3和5年的预后情况,且该模型展现出令人满意的预测效果。
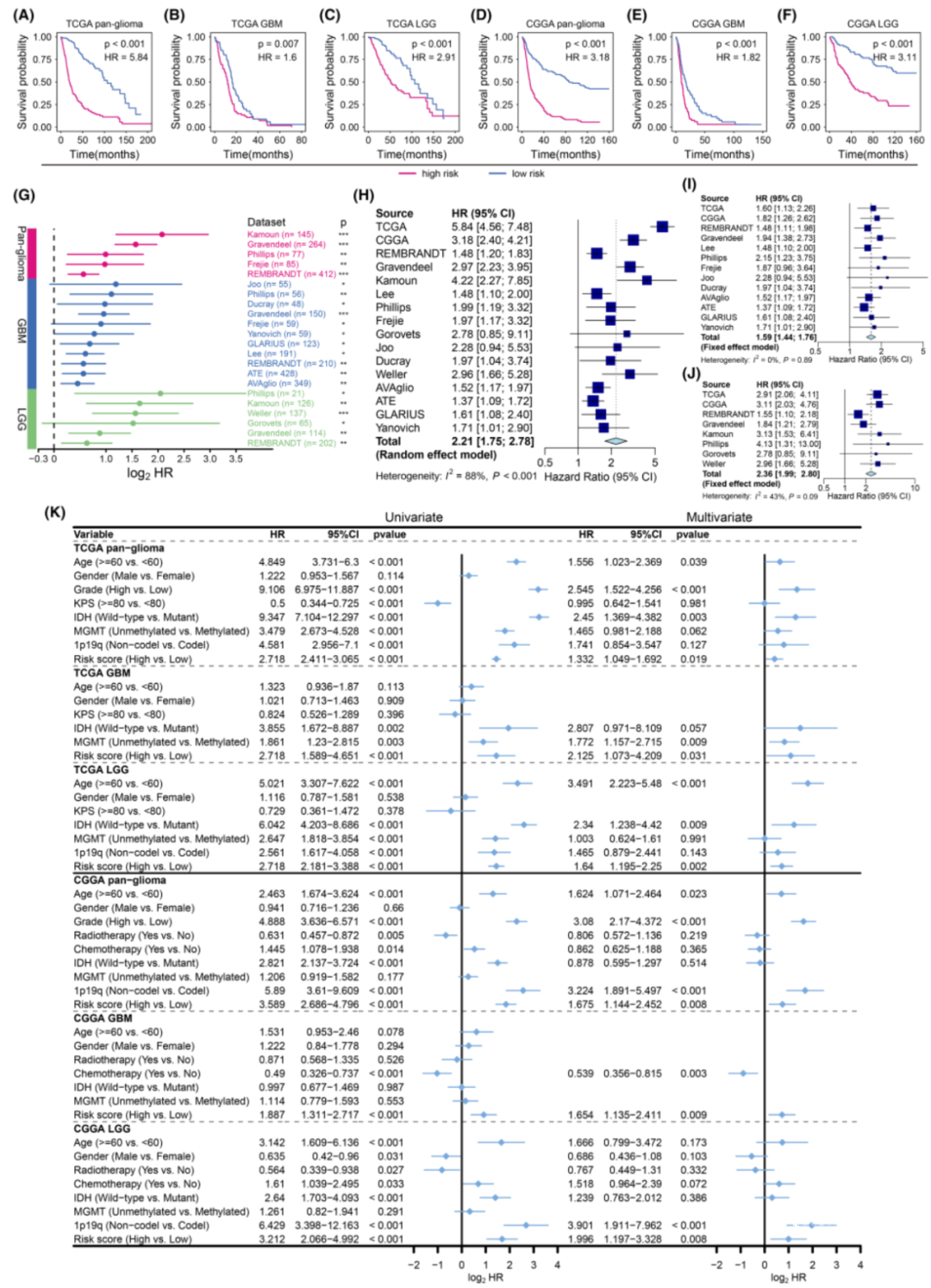
图4. 构建基于的胶质瘤预后风险模型。
高、低风险组胶质瘤患者的总体生存存在显著差异,表明IMRGs组成的基因signature与肿瘤异质性存在关联。风险评分与多种算法计算得到的肿瘤纯度呈显著负相关,而与肿瘤异质性显著正相关。GSEA分析显示高风险组显著富集了间质型胶质瘤基因集,而低风险组富集了前神经型基因集。此外,基于细胞系的表达谱数据和免疫荧光实验表明这三个基因与CD44强正相关,是可能作为间质性胶质瘤的潜在标志物。单细胞RNA-seq数据证实STEAP3、LTF、HMOX1在间质性亚型胶质瘤细胞中显著高表达,并在肿瘤细胞间质型转化中发挥作用。
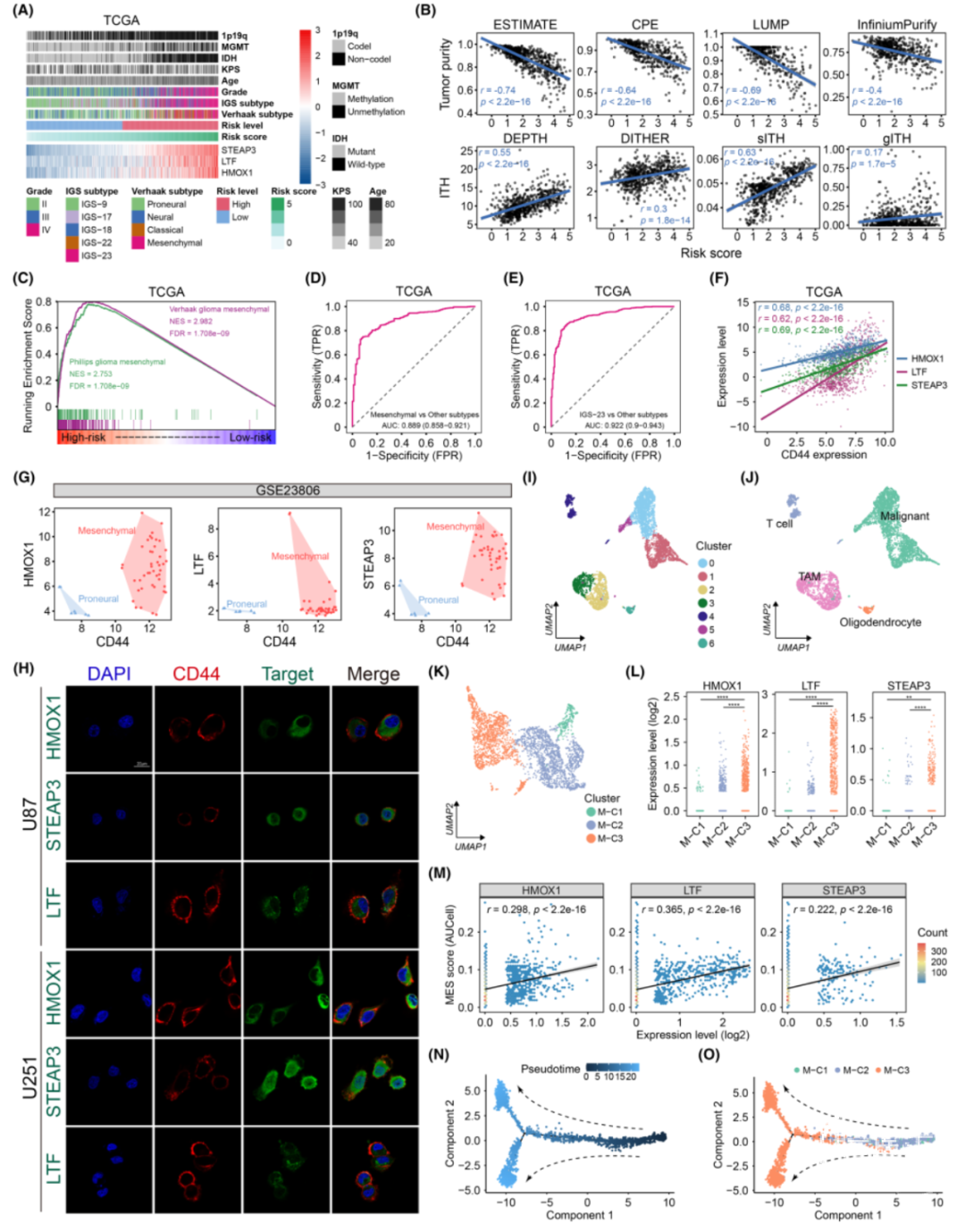
图5. IMRGs与胶质瘤的肿瘤异质性和间质型表型密切相关。
在TCGA队列中,基于IMRGs的风险评分与所有突变、非同义突变和同义突变计数呈显著正相关。高风险患者中有30个基因的突变率超过5%,低风险组只有15个。Fisher精确检验检测了两个风险组之间差异性突变的基因。例如,IDH1、CIC、FUBP1和NOTCH1的突变倾向于出现在低风险组,而EGFR、PTEN和NF1的突变在高风险组更为常见。使用MutSigCV模块确定了不同风险组的显著突变基因,这些基因在不同风险组中互斥突变多于共存突变。此外,风险评分与拷贝数变异数量呈正相关。高风险评分患者中有更多携带chr13/14缺失和chr19/20扩增的样本。高风险评分患者中代表性的扩增包括EGFR、CDK4、PDGFRA、PIK3C2B和CPM,缺失包括CDKN2A、PTEN、CDKN2C和QKI。而在低风险组中,扩增的基因包括ZHX2、PDGFRA和CCND2,缺失包括CDKN2A、ACTN1和NEK1。
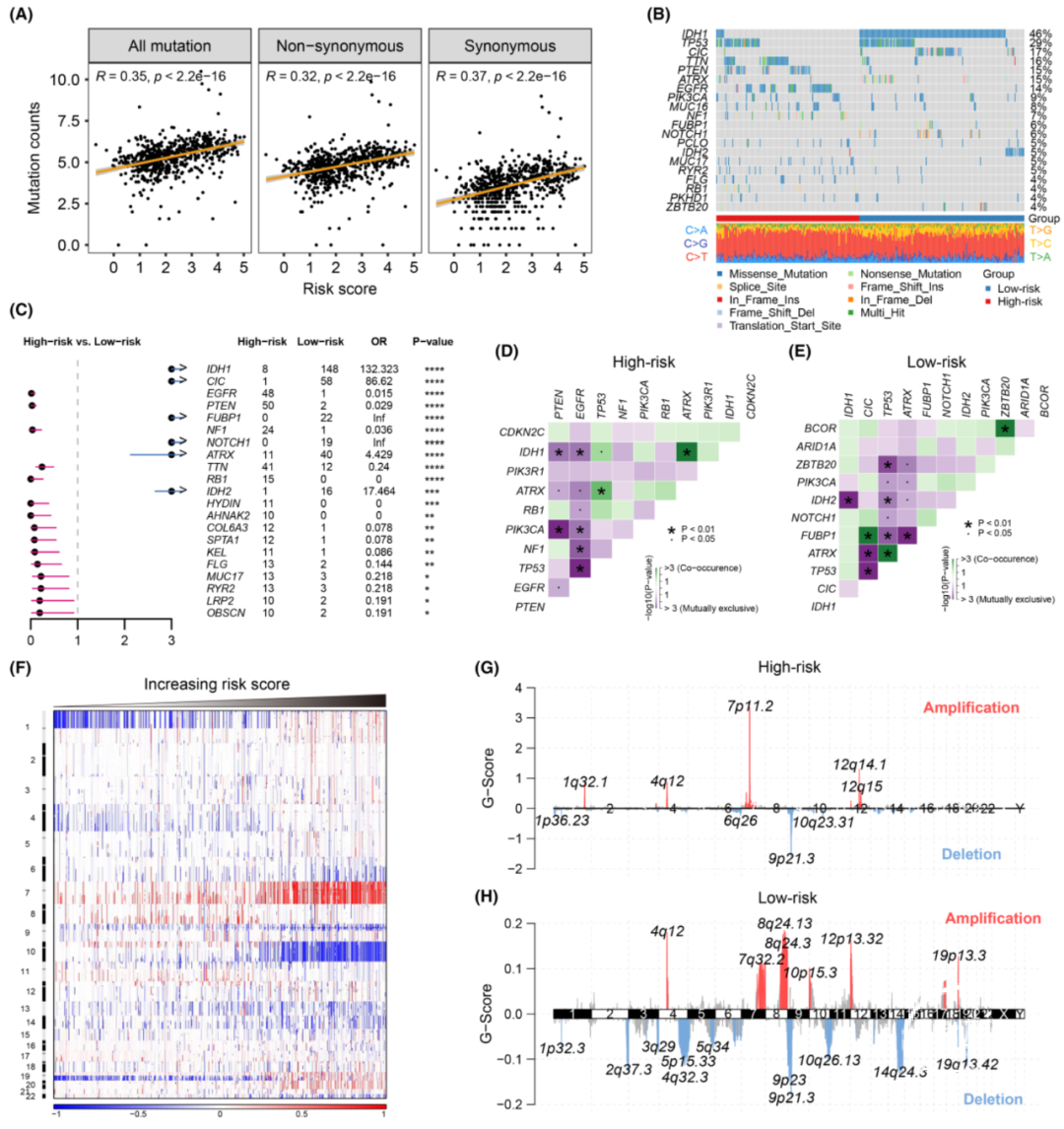
图6. 不同风险组胶质瘤中显著差异的突变和拷贝数变异特征。
GSEA分析显示替莫唑胺治疗的耐药性基因集在TCGA中高风险GBM组显著富集。使用pRRophetic R包的岭回归模型基于转录组数据估算GBM患者对替莫唑胺治疗的潜在响应性。利用CTRP和PRISM数据集,进一步探讨了TMZ敏感性与这三个基因标志之间的关系,结果表明高风险组GBM患者相较于低风险组患者可能从替莫唑胺治疗中获益更少。通过Ivy-GAP队列的表达谱和MRI数据相结合,研究发现高风险组GBM患者更可能对替莫唑胺治疗产生化疗耐药性。相比于传统的MGMT甲基化状态,IMRGs模型能够更好地预测患者对替莫唑胺治疗的响应。此外,体内外实验也证实了STEAP3、LTF和HMOX1对替莫唑胺敏感性的影响。这些结果表明,IMRGs与GBM中的替莫唑胺耐药性密切相关,并且有潜力作为新的预测替莫唑胺疗效的生物标志物。
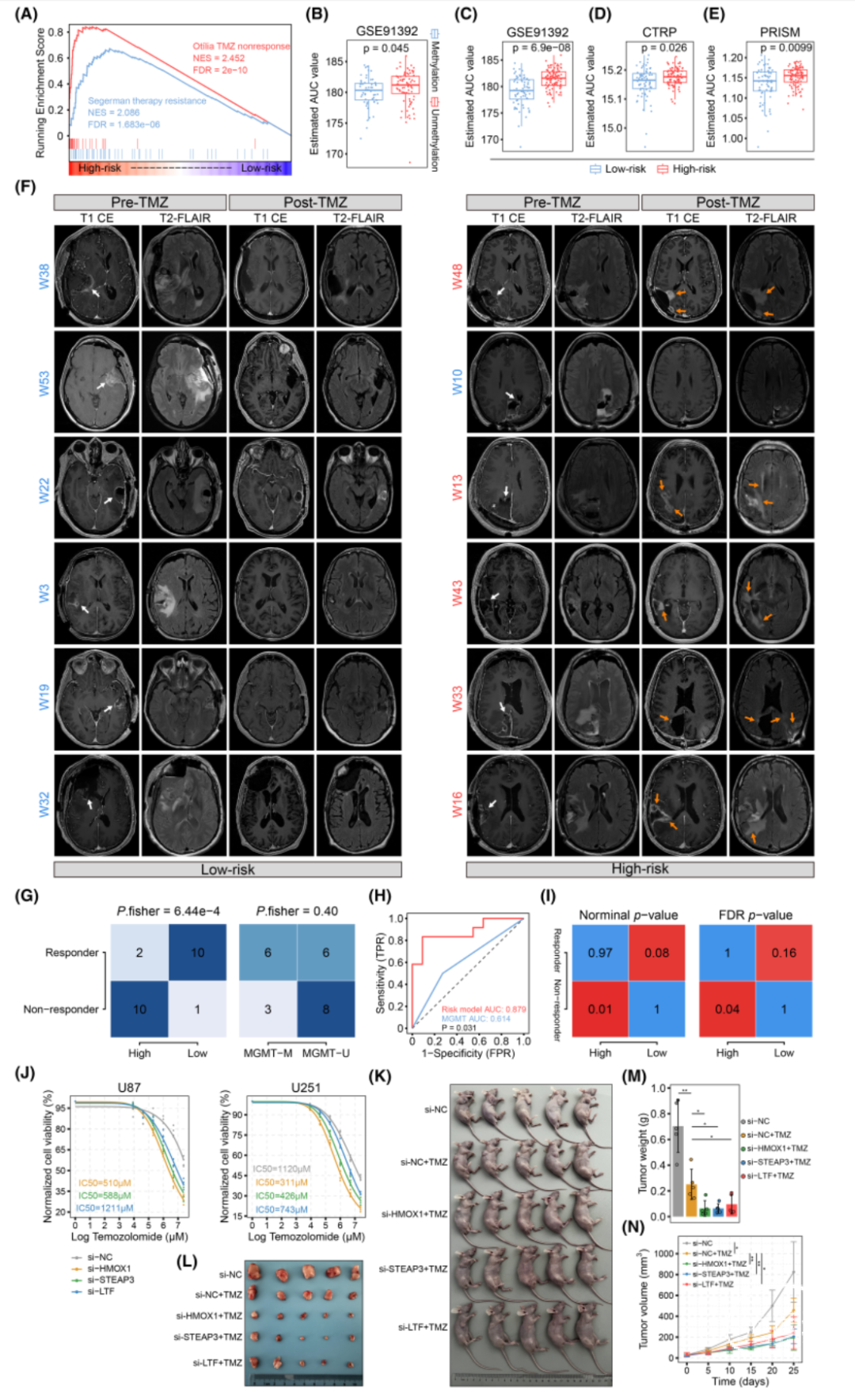
图7. IMRGs与替莫唑胺治疗的耐药性密切相关。
在不同剂量的DFO和erastin处理后,U87和U251胶质瘤细胞中的HMOX1、LTF和STEAP3的转录活性显著降低,表明这些基因在铁代谢调控中起作用。使用DepMap CRISPR-Cas9基因敲除效应评分探讨了这三个基因是否影响胶质瘤细胞的增殖。在敲除HMOX1、LTF和STEAP3后,大多数胶质瘤细胞显示负值评分,表明这些基因的敲除抑制了细胞生长。CCK-8、平板克隆、流式细胞术、划痕实验以及traswell实验表明,在敲低HMOX1、LTF和STEAP3后,U87和U251细胞的增殖、克隆形成、细胞迁移侵袭受到明显抑制。这些实验结果表明,HMOX1、LTF和STEAP3可以促进胶质瘤细胞的恶性发展。
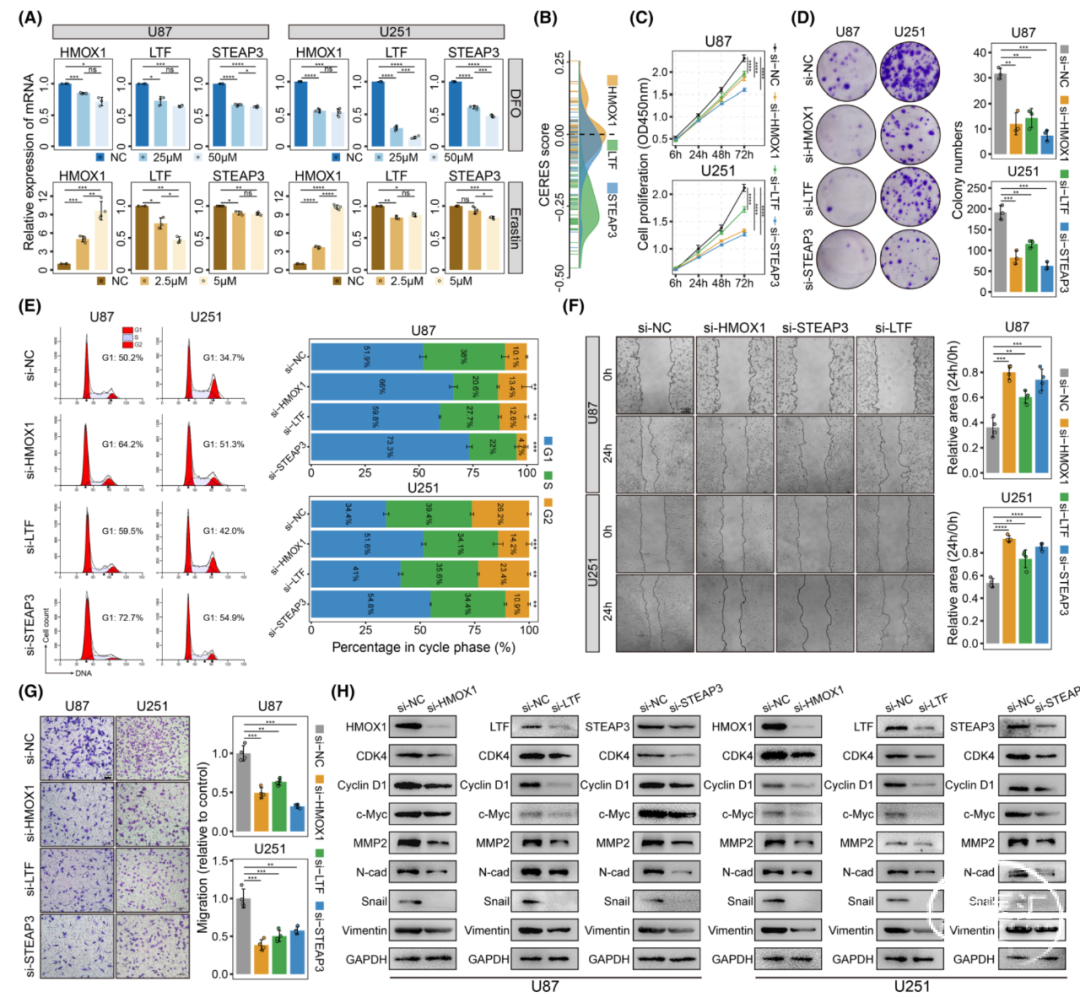
图8. 体外实验证实HMOX1、LTF和STEAP3在胶质瘤细胞中的细胞生物学功能。
本研究通过对铁代谢相关基因的全面分析,揭示了胶质瘤恶性进展的驱动机制,并确定了其中潜在的关键基因。利用这些关键基因建立的新型基因集可以用于预测胶质瘤患者的预后。此外,该基因集与间质型表型和替莫唑胺耐药性密切相关,为药物的开发提供了新的潜在靶点。
主任医师,教授,博士生导师
现任中国垂体腺瘤协作组委员,中国医师协会胶质瘤专委会委员,江苏省医学会颅内肿瘤学组副组长,江苏省医师协会神经肿瘤学组副组长
从事神经外科临床、教学及科研工作20余年,现全年手术量近500台,擅长微创手术治疗垂体腺瘤、胶质瘤、脑膜瘤、听神经瘤等颅内肿瘤,尤其在神经内镜下微创切除垂体腺瘤、松果体区肿瘤、颅底肿瘤以及三叉神经痛及面肌痉挛微血管减压手术方面有较高造诣。曾多次在美国Thomas Jefferson大学、Saint Louis大学、St Anthony`s Medical Center访学、培训
荣获江苏省科学技术奖三等奖,国家发明专利一项,先后主持国家、部、省级以上课题8项,在国内外发表高水平专业学术论文40余篇(其中SCI收录30余篇),培养研究生10余名
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、AiBrain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。
投稿邮箱:NAOYIHUI@163.com
未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。















