
【摘要】
目的:研究顺铂联合替莫唑胺放化疗治疗MGMT启动子未甲基化胶质母细胞瘤临床随机对照试验的设计方案,及其治疗效果。
方法:对2016年6月~2017年8月新诊断的50例MGMT启动子未甲基化胶质母细胞瘤患者,进行临床随机对照试验。患者随机分为替莫唑胺标准放化疗组(对照组,24例)及顺铂联合替莫唑胺放化疗组(联合治疗组,26例)。观察并比较两组患者在同期放化疗和放疗后辅助化疗期间的不良反应;分析两组患者的生存情况。
结果:患者主要的不良反应为骨髓抑制、恶心呕吐、食欲减退、便秘和疲乏。对照组中2例患者发生骨髓抑制,联合治疗组中共有12例患者发生骨髓抑制;两组骨髓抑制发生率比较,差异有统计学意义(P=0.002)。经对症处理后,患者的骨髓抑制均得到改善。联合治疗组中有42%~50%的患者出现恶心呕吐、食欲减退、便秘,对照组中有25%~33%的患者出现以上症状;对照组中出现疲乏者5例,联合治疗组为8例;两组比较,差异均无统计学意义(均P>0.05)。两组患者中均未有肝肾功能损害及耳毒性发生者。联合治疗组有23%的患者、对照组有8%的患者出现生活质量评分下降,两组的差异无统计学意义(P>0.05)。两组患者中均无因严重不良反应退出研究者。截至2018年3月,共有29例患者出现复发,其中联合治疗组14例、对照组15例;13例患者死亡,其中联合治疗组6例、对照组7例。Kaplan-Meier生存函数分析显示,两组OS和PFS的差异无统计学意义(均P>0.05)。
结论:顺铂联合替莫唑胺组治疗后的骨髓抑制较为严重,但经对症处理后均能恢复;没有患者因不良反应退出治疗。患者的1年生存率与单用替莫唑胺放化疗的患者相仿。
胶质母细胞瘤(glioblastoma,GBM)是最常见的颅内原发性恶性肿瘤[1],预后很差,生存时间短[2,3];并且近年来的发病率逐年升高[4]。2015年版《中国中枢神经系统胶质瘤诊断和治疗指南》[5]推荐的治疗方案是,手术联合术后替莫唑胺(temozolomide,TMZ)同步放化疗及TMZ辅助化疗[6]。2018年NCCN指南[7]明确提出,O6-甲基鸟嘌呤-DNA甲基转移酶(O6-methylguanine DNA methyl-transferase,MGMT)是GBM重要的预后因子和疗效预测因子;并将GBM按照MGMT启动子是否存在甲基化分成两组,MGMT启动子未甲基化患者对TMZ耐药,疗效更差[8-9];并鼓励开展临床试验。顺铂(cisplatin,DDP)是传统的神经肿瘤化疗药物,有学者发现,DDP可以降低MGMT活性,DDP与TMZ联合使用能更好地达到长期耗竭MGMT的作用[10]。本课题组前期曾开展小样本的临床研究,发现DDP联合TMZ同期放化疗治疗MGMT启动子未甲基化的高级别胶质瘤患者的不良反应少,近期疗效较好[11]。因此本研究进行前瞻性随机对照试验(中国临床试验注册中心注册号:ChiCTR-IIR-17010327),比较DDP联合TMZ同期放化疗组与单纯TMZ同期放化疗治疗新诊断的MGMT启动子未甲基化GBM患者的疗效;探讨该治疗方法的设计方案,并分析比较两种治疗的不良反应及疗效。
资料与方法
1.1
入组标准
1.2
方法
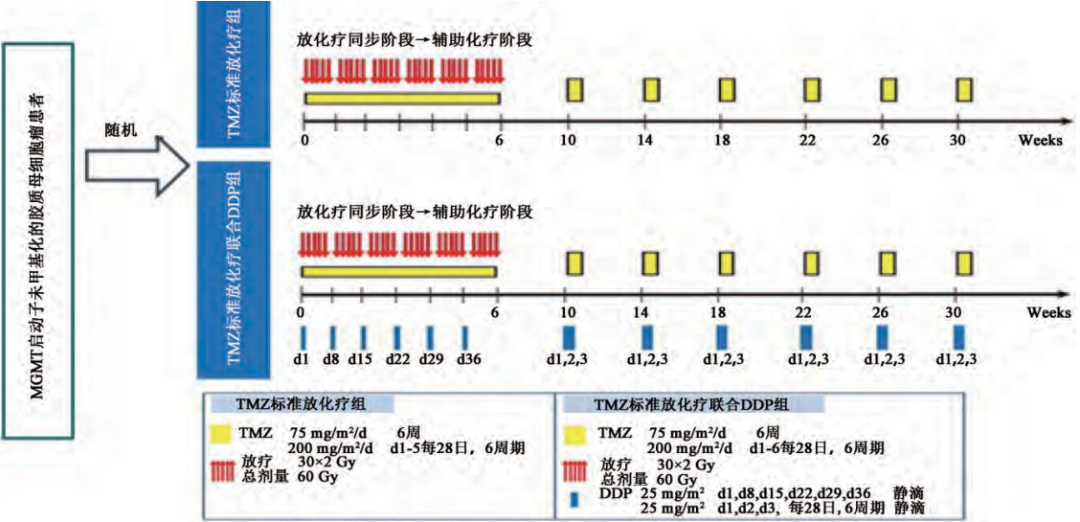
图1. TMZ标准放化疗与联合DDP的治疗方案
1.3
统计学方法
采用SPSS16.0软件进行统计分析处理。
结果
2.1
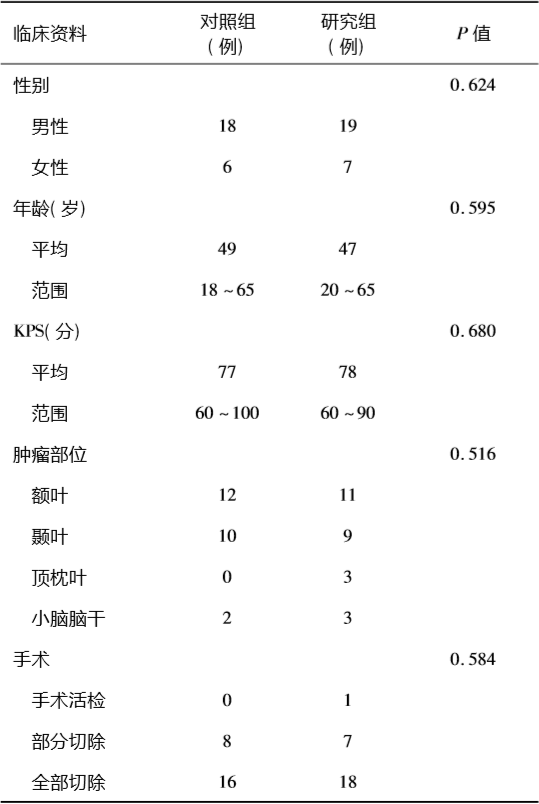
两组患者的临床资料 见表1。
自2016年6月-2017年8月收治的新诊断MGMT启动子未甲基化的50例GBM患者,随机分为对照组(24例)和联合治疗组(26例)。两组患者的一般资料及临床特征比较,差异均无统计学意义(均P>0.05)。
表1 两组患者的临床资料比较
2.2
放化疗完成及随访
2.3
两组不良反应比较
表2 两组骨髓抑制的比较
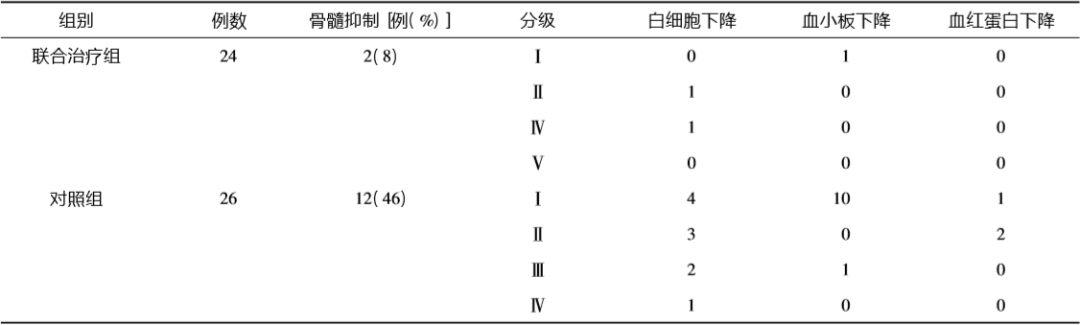
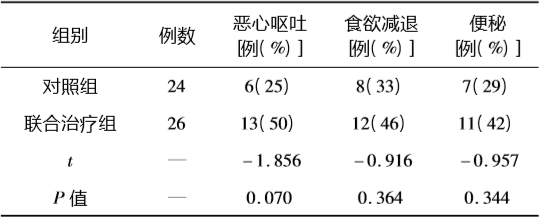
表3 两组消化道反应的症状比较
2.4
QOL 评分
2.5
治疗效果
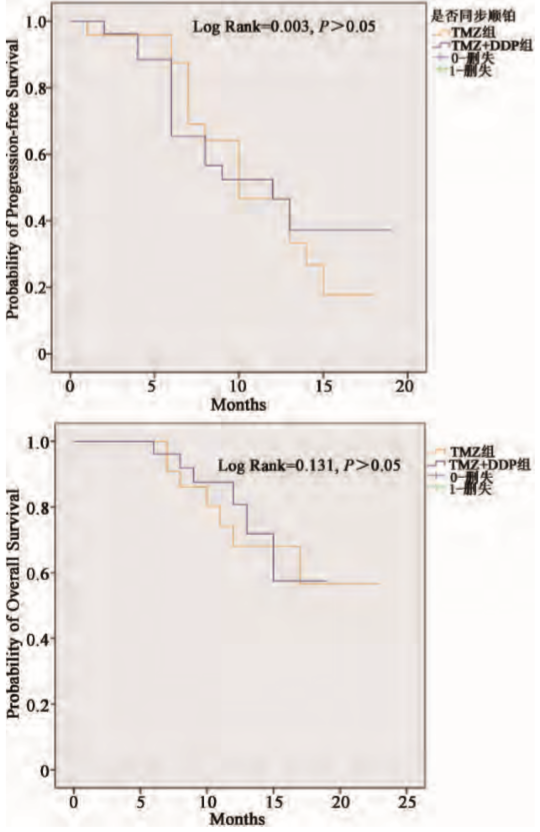
图2. 两组患者的生存情况分析
(蓝线为联合治疗组,黄线为对照组)
讨论
2017年版的CNS-NCCN指南[12]对GBM包括MGMT启动子未甲基化患者术后,均推荐行TMZ同步放化疗及辅助化疗。2018年的CNS-NCCN指南对治疗策略做了重大的改变,除了推荐常规方案外,更鼓励治疗创新;鼓励患者参与临床试验。MGMT是由MGMT基因编码的DNA修复蛋白,避免烷化基团对细胞的损害,从而造成MGMT启动子未甲基化的GBM患者对TMZ耐药,疗效更差[13]。而GBM患者中有60%左右为MGMT启动子未甲基化状态[14]。DDP是传统神经肿瘤化疗药物[15]。实验证实,DDP可以降低MGMT活性,并且对MGMT的抑制率与浓度和作用时间呈正比,在治疗后24h可以观察到最大的MGMT抑制效应(50%)。更令人鼓舞的是,DDP与TMZ联合使用能更好地达到长期耗竭MGMT的作用;而且这种联合用药起效更快,维持时间更长。两药联合使用48h后,MGMT活性仍然恢复不到治疗前的30%。临床前实验进一步显示DDP联合TMZ方案疗效有协同效应,且两药的毒副反应没有重叠,允许两药联合运用时无需减量[16]。这为临床采用DDP联合TMZ化疗提供了理论依据。此外,DDP还是一个重要的放疗增敏剂。2014年Mahmoud报道,DDP能够激活毛细血管扩张性共济失调症突变基因(ATM),而ATM与放射高度敏感肿瘤的关系密切[17]。
Antonio[18]曾将DDP联合TMZ用于治疗33例复发的恶性胶质瘤,结果发现血液学毒性是该方案的最大毒副作用;33例患者中有40%的患者出现了3~4级的血液学毒性。同时该研究还发现,DDP联合TMZ治疗的患者可能出现恶心呕吐、肾功能异常、神经毒性。Zustovich等[19]对24例TMZ耐药的复发性恶性胶质瘤进行DDP联合TMZ方案治疗,结果显示,总反应率为29.41%,6个月的PFS是28%,中位OS是7个月,药物不良反应也以1~2级为主。本研究在国内外率先开展小样本的单臂临床研究,发现DDP联合TMZ同期放化疗治疗MGMT启动子未甲基化的高级别胶质瘤患者的不良反应少,近期疗效较好[11]。本研究采用随机对照临床试验,比较DDP联合TMZ同期放化疗与单纯TMZ同期放化疗治疗新诊断的MGMT启动子未甲基化GBM患者的疗效和安全性。
本研究的两组患者在治疗中均出现了一定程度的不良反应,其中以骨髓抑制最为突出。对照组的骨髓抑制发生率为8%,而联合治疗组的骨髓抑制发生率为46%,两组的差异有统计学意义(P=0.002)。对照组的骨髓抑制均发生在辅助化疗阶段,为1~2级,无需特殊处理,可自行缓解;但是联合治疗组有3例患者(11%),在同步放化疗阶段就出现了骨髓抑制,并且还有3例患者(11%)出现了3~4级的骨髓抑制,需予以重组人粒细胞集落刺激因子、重组人血小板生成素处理。联合治疗组患者发生骨髓抑制的时间更早,发生的几率更高;并且抑制程度更严重。但所有患者经对症处理后,均能缓解;无患者因相关毒性反应退出试验。
消化道反应也是本研究两组患者的常见毒副作用,包括恶心呕吐、食欲减退、便秘和疲乏。其中联合治疗组恶心呕吐的发生率(50%)高于对照组(25%),但差异无统计学意义(P=0.070)。联合治疗组患者中,出现食欲减退者12例(46%)、便秘者11例(42%)、明显疲乏者8例(31%);而对照组患者中出现食欲减退、便秘和疲乏症状者,分别为8例(33%)、7例(29%)和5例(21%),但均为1~2级,无需特殊处理。两组以上症状发生率比较,差异无统计学意义(均P>0.05)。两组患者QOL评定大多为稳定,但联合治疗组有23%的患者出现QOL下降,而对照组只有8%,但差异无统计学意义。Stupp等[20]曾报道,对MGMT启动子未甲基化患者采用TMZ标准方案放化疗,患者12个月的OS率不到60%。本研究中,无论是对照组,还是联合治疗组的OS率均优于Stupp等的报道。这可能与本研究入组患者的一般情况较好,以及患者相对年轻(≤65岁)等有关。本研究中联合治疗组12个月总生存率为77.8%,略优于对照组的73.3%,但差异无统计学意义。
综上所述,本研究结果显示,MGMT启动子未甲基化的GBM患者采用DDP联合TMZ放化疗,与标准TMZ放化疗方案的患者比较,骨髓抑制更严重,其他不良反应如恶心呕吐、食欲减退、便秘、疲乏的发生率也稍为增高。两组患者对治疗的耐受性均较好。虽然DDP联合TMZ组患者的骨髓抑制较为严重,但经对症处理后均能恢复,没有患者退出治疗;1年OS也略高于对照组,但差异无统计学意义。由于本研究对患者的随访时间较短,样本量较小;两种治疗方案患者的确切疗效及生存状况,还需扩大样本量和延长随访时间进行研究;并结合患者的临床特征及分子标记物作进一步深入分析。
病例分享
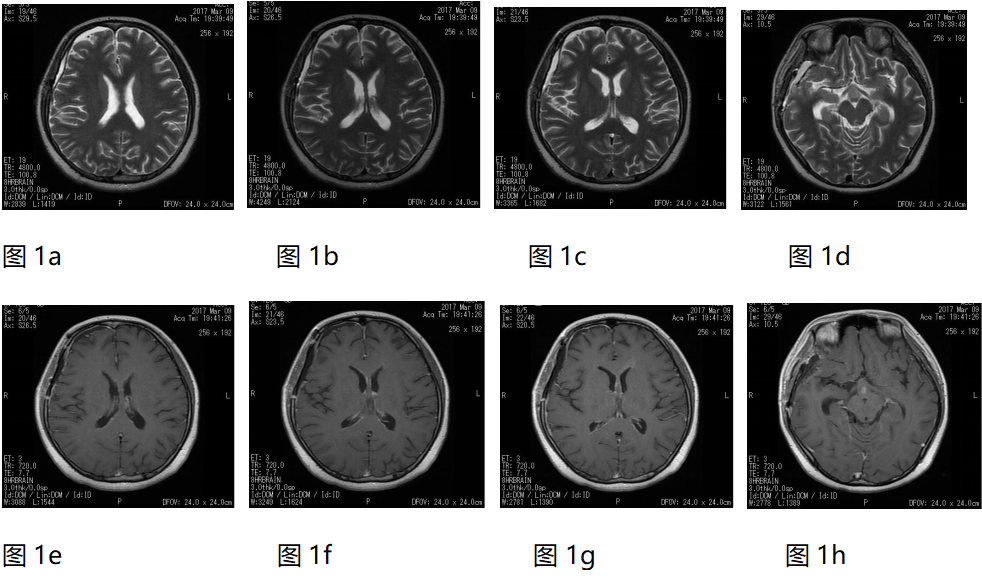
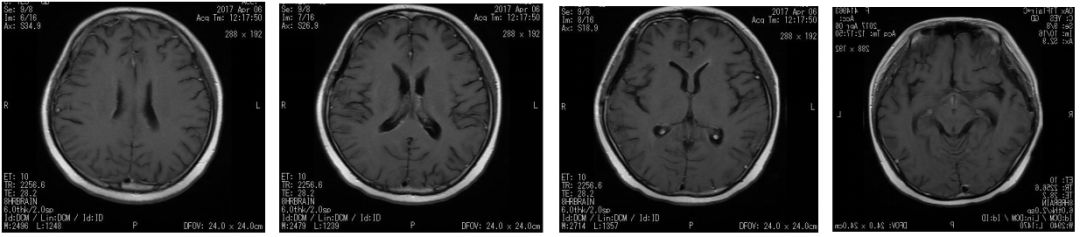
图2. 2017年4月6日放疗期间复查头颅MRI,提示强化灶有缩小
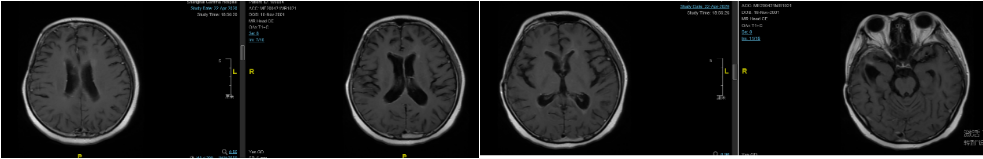
参考文献
[1]Louis DN,Ohgaki H,Wiestler OD,et al. The 2007 WHO classification of tumours of the central nervous system[J]. Acta Neuropathol,2007,114:97.
[2]丛明华,宋晨鑫,郑荣寿,等.2011年中国脑和神经系统肿瘤发病和死亡分析[J]. 中国肿瘤,2015, 24:349.
[3]Ostrom QT,Gittleman H,Fulop J,et al. CBTRUS statistical report:
primary brain and central nervous system tumors diagnosed in the United States in 2008-2012[J]. Neuro Oncol,2015,17:1.
[4]Muir CS,Storm HH,Polednak A. Brain and other nervous system tumours[J]. Cancer Surv,1994, 19:369.
[5]中国中枢神经系统胶质瘤诊断和治疗指南编写组.中国中枢神经系统胶质瘤诊断和治疗指南( 2015) [J].中华医学杂志,2016, 96:485.
[6]Schulze M,Fedorchenko O,Zink TG,et al.Chronophin is a glial
tumor modifier involved in the regulation of glioblastoma growth and invasiveness[J].Oncogene,2016, 35:3163.
[7]NCCN Guidelines Version 1.2018 Central Nervous System Cancers [OL].http: / /www. nccn.org.
[8]Hegi ME,Liu LL,Herman JG,et al. Correlation of O-6Methylguanine methyltransferase ( MGMT) promoter methylation
with clinical outcomes in glioblastoma and clinical strategies to modulate MGMT activity[J]. J Clin Oncol,2008, 26:4189.
[9]Wick W,Platten M,Meisner C,et al. Temozolomide chemotherapy
alone versus radiotherapy alone for malignant astrocytoma in the elderly: the NOA-08 randomised,phase 3 trial[J]. Lancet Oncol, 2012, 13:707.
[10] D'atri S,Graziani G,Lacal PM,et al. Attenuation of O-6
methylguanine-DNA methyltransferase activity and mRNA levels by cisplatin and temozolomide in Jurkat cells[J]. J Pharmac Exp Therap 2000,294:664.
[11]孟歌,汪洋,盛晓芳,等. 顺铂联合替莫唑胺同期放化疗方案治 疗 MGMT 启动子无甲基化高分级胶质瘤的初步研究[J]. 中国 临床神经科学,2015, 23:327.
[12]Nabors LB,Portnow J,Ammirati M,et al. NCCN guidelines insights: Central nervous system cancers,Version 1. 2017[J]. J Nati Compr Canc Netw,2017, 15:1331.
[13]Van Den Bent MJ,Brandes AA,Taphoorn MJ,et al. Adjuvant procarbazine,lomustine,and vincristine chemotherapy in newly diagnosed anaplastic oligodendroglioma: long-term follow-up of EORTC brain tumor group study 26951[J]. J Clin Oncol,2013, 31:344.
[14]中国脑胶质瘤协作组( CGCG) 和中国脑胶质瘤基因组图谱计 划( CGGA) . 中国脑胶质瘤分子诊疗指南[J].中华神经外科 杂志,2014, 30:435.
[15]Brandes AA,Basso U,Vastola E,et al. Carboplatin and teniposide as
third-line chemotherapy in patients with recurrent oligodendroglioma or oligoastrocytoma: a phase II study[J]. Ann Oncol,2003, 14:1727.
[16]Piccioni D,Datri S,Papa G,et al. Cisplatin increases sensitivity of human leukemic blasts to triazene compounds[J]. J Chemother, 1995, 7:224.
[17]Toulany M,Mihatsch J,Holler M,et al. Cisplatin-mediated
radiosensitization of non-small cell lung cancer cells is stimulated by ATM inhibition[J] . Radiother Oncol,2014,111:228.
[18]Silvani A,Eoli M,Salmaggi A,et al. Phase II trial of cisplatin plus temozolomide,in recurrent and progressive malignant glioma patients[J].J Neurooncol,2004, 66:203.
[19]Zustovich F,Lombardi G,Della Puppa A,et al.A phase II study of
cisplatin and temozolomide in heavily pre-treated patients with temozolomide-refractory high-grade malignant glioma[J].Anticancer Res,2009,29:4275.[20]Stupp R,Mason WP,Van Den Bent MJ,et al.Radiotherapy plus concomitant and adjuvant temozolomide for glioblastoma[J].N Engl J Med,2005,352:987.
作者简介

倪春霞
阔然精准诊疗脑肿瘤系列产品CaptioX-G是一款以NGS技术为基础的检测产品。CaptioX-G产品的开发主要以2016年WHO中枢神经系统肿瘤分类、胶质瘤诊疗规范(2018年版)、NCCN指南和cIMPACT-NOW update 1-7为依据,其涉及脑胶质瘤的分子分型(IDH、1p/19q、ATRX、TERTp)、化疗药物(MGMT)和潜在靶向药物相关的基因(MET、FGFR、NTRK、BRAF等)。CaptioX-G产品还利用低覆盖度全基因组测序技术检测胶质瘤患者的7、10、5p、14q和18q染色体拷贝数变异,辅助IDH野生型的较低级别星型胶质细胞瘤和IDH突变型的星形胶质细胞瘤的再分类。
“阔然生物医药科技(上海)有限公司(Shanghai KR Pharmtech, Inc. , Ltd.)”简称“阔然基因”,是一家专注于医学研究与转化的企业,专注于脑肿瘤的分子诊断与个体化治疗业务,现已有两家(上海、徐州)国家卫生健康委员会认证的医学检验实验室,在基因检测领域有自主知识产权,拥有完善的全国医疗市场的销售渠道,战略合作的神经外科医生的媒体“神外资讯”,目标成为脑肿瘤分子诊断与个体化治疗领域中国第一品牌。阔然基因重视自有技术开发,目前已建高通量测序平台、单细胞测序平台、多标荧光免疫组化平台,阔然基因在硬件与试剂盒产品端发力,布局术中、术后诊断领域,打造自有技术和行业壁垒,成为并巩固在脑肿瘤领域的领跑者地位。目前阔然基因已布局了术后分子诊断、ddPCR脑脊液检测技术和应用,以及术中实时诊断系统。





