如欲投稿请点击 神外资讯-欢迎赐稿
【Ref: Gamble AJ & Boockvar JA. Neurosur gery. 2015 Apr; 76(4): N16-8. doi: 10. 1227/ 01. neu. 0000462696. 46135. 41.】
铜绿假单胞菌外毒素(pseudomonasexotoxin ,PE)通过抑制延长因子2(elongation fac tor-2)和阻断蛋白质表达发挥细胞毒性作用。PE与配体结合而形成的肿瘤细胞特异性抗原已经应用于某些白血病和淋巴瘤的治疗并获得成功,在实体肿瘤治疗中也取得一定的疗效。最近,备受关注的是白介素13(interleukin-13,IL13)受体α2作为靶向分子治疗胶质瘤,这类受体在胶质瘤细胞过量表达,而在正常脑细胞未过度表达。有研究证实,这种靶向分子,可以选择性地将PE导入胶质瘤细胞内。美国纽约曼哈斯特Feinstein医学研究院的Alexander J.Gamble等进行有关研究,结果发表在2015年4月的《Neurosurgery》杂志上。
作者首先制作利用U87绿色荧光标记的胶质瘤小鼠动物模型(图1),观察卡莫司汀植入膜和IL13-PE结合体对胶质瘤细胞的影响,发现IL13-PE结合体直接作用胶质瘤细胞的效果较差,原因可能是给药定位问题或药物的半衰期短暂,只有四天的作用期;而卡莫司汀植入膜的优势是直接置于肿瘤边缘,卡莫司汀将在肿瘤边缘逐渐扩散进入肿瘤实质内。
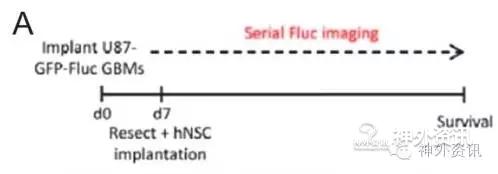
图1. 绿色荧光标记的胶质瘤鼠动物模型。
继而,通过介导编码延长因子2的基因突变培养分泌铜绿假单胞菌外毒素的神经干细胞,然后选择能持续性表达IL13-PE结合体的细胞。将多种建立的胶质瘤细胞系和5例患者的胶质瘤细胞系与PE毒素分泌的神经干细胞一起培养,这种细胞的毒性与胶质瘤细胞系中白介素13的受体α2的表达水平有关;将分泌IL13-PE的神经干细胞置于合成的细胞外基质。在小鼠胶质瘤模型中,切除肿瘤并注入分泌IL13-PE的神经干细胞一周后,胶质瘤细胞消失;在肿瘤遗留的空腔充满了分泌IL13-PE的神经干细胞(图2)。与单纯注入分泌IL13-PE的神经干细胞或单纯切除胶质瘤的大鼠相比较,发现三种方法处理的胶质瘤小鼠中位生存期分别是79、48、26天。肿瘤切除之后,只有在导入分泌IL13-PE的神经干细胞的小鼠中没有发现肿瘤细胞大量生长。
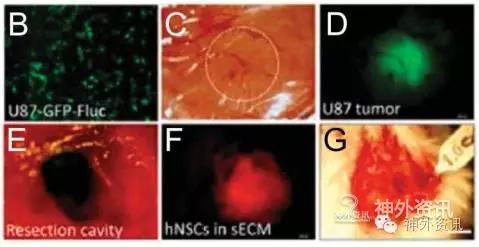
图2. 图B、C、D. 颅骨开窗法将U87绿色免疫荧光标记胶质瘤植入小鼠颅内,培育成胶质瘤;图E、F、G. 在肿瘤切除之后,红色免疫荧光蛋白标记的神经干细胞长满肿瘤残腔。
许多化疗方法治疗脑胶质瘤的效果,都会受到药物稳定性和血脑屏障的影响;应用分泌肿瘤毒素的神经干细胞或者使用其他生物技术杀灭肿瘤切除后残留的肿瘤细胞的治疗方法可能克服上述缺点。该研究显示,通过分泌IL13-PE的神经干细胞导入切除胶质瘤后的瘤腔抑制肿瘤的复发,是一种治疗胶质瘤的可取的方法。
(北京天坛医院李明耀编译,复旦大学附属华山医院陈灵朝博士审校,《神外资讯》主编、复旦大学附属华山医院陈衔城教授终审)
相关回顾
病例讨论| 华山脑胶质瘤MDT Tumor Board Case Review Ⅺ
胶质瘤干细胞通过分泌Periostin聚集巨噬细胞促进肿瘤生长
更多资讯请关注神外资讯微信公众号:neurosurgerynews



