
![]()
摘要:目的分析老年脑梗死慢性期多病共存患者跌倒的影响因素,并构建预测跌倒发生风险的列线图模型。方法回顾性连续纳入2022年8月至2024年10月合肥市第二人民医院老年医学科收治的老年(年龄≥60岁)脑梗死慢性期(末次发病至入院时间≥1个月)多病(≥2种)共存患者。收集患者出院时的一般及临床资料,包括性别、年龄、体质量指数、共病种类[高血压病、糖尿病、冠心病、慢性心力衰竭、肌少症、骨质疏松症及其他慢性疾病(甲状腺功能减退、前列腺增生等)]、共病数量(≥3种,2种)、营养状况[营养风险筛查2002(NRS-2002)量表评分]、跌倒风险[Tinetti平衡与步态评估(Tinetti POMA)量表评分]、肢体功能[改良Rankin量表(mRS)评分]、认知情况[蒙特利尔认知评估(MoCA)量表评分]、下肢偏瘫情况(Brunnstrom分期)及随访期(入院后6个月)内跌倒发生情况。入院次日晨起空腹状态下采集静脉血,检测糖化血红蛋白、空腹血糖、白蛋白、前白蛋白、三酰甘油、总胆固醇、低密度脂蛋白胆固醇、高密度脂蛋白胆固醇、肌酐、尿酸水平。根据随访6个月内是否发生跌倒将患者分为跌倒组和非跌倒组,比较两组的一般及临床资料和实验室指标,将差异有统计学意义的因素纳入多因素Logistic回归分析,探索老年脑梗死慢性期多病共存患者跌倒的影响因素并构建列线图预测模型;采用受试者工作特征(ROC)曲线、校准曲线、临床决策曲线评估该列线图模型的预测效能。结果共纳入147例老年脑梗死慢性期多病共存患者,其中男59例,女88例,年龄61~93岁,平均(77±7)岁,脑梗死末次发病至入院时间17~122个月,平均(63±17)个月,患者共病数量2~6种,中位共病数量3(2,4)种,占比前3位的共病疾病为高血压病[94.56%(139/147)]、糖尿病[57.14%(84/147)]、肌少症[42.86%(63/147)]和骨质疏松症[42.86%(63/147)];随访期间,54例(36.73%)患者发生跌倒,为跌倒组,其余93例患者为非跌倒组。(1)与非跌倒组相比,跌倒组年龄[82(76,85)岁比75(69,82)岁]、NRS-2002量表评分[4(3,4)分比3(2,3)分]及共病数量≥3种[94.44%(51/54)比44.09%(41/93)]、骨质疏松症[70.37%(38/54)比26.88%(25/93)]、肌少症[81.48%(44/54)比20.43%(19/93)]患者比例均更高,Tinetti POMA量表评分[(16.59 ± 1.09)分比(17.41±1.02)分]、白蛋白[37.65(35.60,39.73)g/L比39.90(37.55, 41.95)g/L]均更低(均P<0.01)。(2)多因素Logistic回归分析显示,骨质疏松症(OR=3.059,95% CI: 1.063~8.797)、肌少症(OR=23.698, 95% CI:5.157 ~ 108.912)、共病数量≥3种(OR=16.839,95% CI:2.227 ~ 127.348)、高NRS-2002量表评分(OR=5.346,95% CI:2.035~14.047)是老年脑梗死慢性期多病共存患者发生跌倒的独立危险因素(均P<0.05),高Tinetti POMA量表评分是老年脑梗死慢性期多病共存患者发生跌倒的独立保护因素(OR=0.434,95% CI:0.217~0.868, P=0.018)。(3)基于多因素Logistic回归分析结果绘制预测老年脑梗死慢性期多病共存患者跌倒的列线图,ROC曲线分析显示,列线图模型预测老年脑梗死慢性期多病共存患者发生跌倒的曲线下面积为0.894(95%CI:0.840~0.948),敏感度为77.80%,特异度为90.30%;Hosmer-Lemeshow拟合优度检验结果显示,该列线图模型拟合良好(χ2=9.612,P=0.293);决策曲线显示,阈值概率在0.01~0.99时模型均可产生更好的临床效益。结论老年脑梗死慢性期多病共存患者常患疾病以共病高血压病、糖尿病多见且存在较高的跌倒发生率,其跌倒与伴骨质疏松症、肌少症及共病数量多、营养风险高、Tinetti POMA量表评分低等多因素有关,基于上述因素构建的列线图模型具有良好的预测效能,可为临床预测老年脑梗死慢性期多病共存患者跌倒及制定预防策略提供量化工具。
![]()
脑梗死为我国成人致残的首要病因,2019年中国新发卒中394万例,其中脑梗死患者高达287万例[1]。脑梗死慢性期(末次发病至入院时间≥1个月)患者普遍处于多病共存的复杂健康状态,多病共存指患者同时存在≥2种且持续≥1年的慢性病,其定义最早由Feinstein[2]于1970年提出,强调共病状态的独立性与临床复杂性。多病共存状态的复杂状况导致患者临床特征多元、用药方案复杂,且常伴随身体机能老化、免疫力下降及器官系统退行性改变,慢性病及临床不良事件发生风险增加,严重影响患者的生命健康[3]。跌倒作为老年群体常见的不良事件之一,不仅降低了老年群体的活动能力,导致社会功能、生理及心理障碍,还可致老年群体伤残及死亡风险增加[4]。研究显示,老年群体跌倒发生率随着年龄增长而升高,且受自身疾病、肌肉力量、心理等多方面因素影响[5-6]。目前关于老年人群跌倒风险的研究较多,但针对具有脑梗死病史且多病共存的老年患者跌倒风险的研究鲜见报道。此外,既往研究多未将骨质疏松、肌少症等多种潜在风险纳入多病共存状态评估,且缺乏有效的预测工具。因此,探究老年脑梗死慢性期多病共存患者跌倒的影响因素,对于制定个性化的干预方案、预防跌倒事件的发生具有重要意义。Tinetti平衡与步态评估(Tinetti performance-oriented mobility assessment, Tinetti POMA)量表[7]在评估老年患者跌倒风险方面具有高敏感度和特异度,但其评分主要反映患者即时运动状态,而老年脑梗死慢性期多病共存患者跌倒还受共病状态、药物因素、营养状况及环境等多维度因素影响。鉴于此,本研究拟纳入慢性病共病状况、营养状况等多种指标,分析老年脑梗死慢性期多病共存患者跌倒的影响因素,并构建列线图预测模型,旨在为提高该类患者的生存质量,促进患者康复提供科学依据。
1 对象与方法
1.1 对象
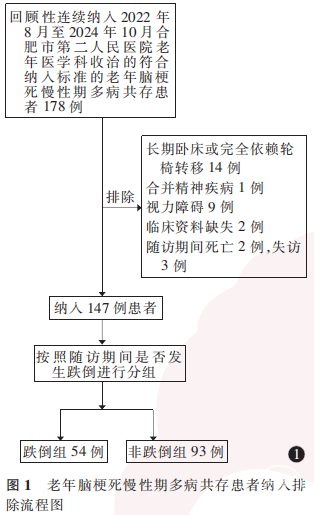
回顾性连续纳入2022年8月至2024年10月入住合肥市第二人民医院老年医学科的老年脑梗死慢性期多病共存患者。本研究方案经合肥市第二人民医院医学伦理委员会审核批准(伦理审批号:2025-科研-017)。所有患者或家属签署了诊疗知情同意书。
纳入标准:(1)年龄≥60岁;(2)脑梗死慢性期(有脑梗死[8]病史且末次发病至入院时间≥1个月)患者;(3)符合《老年共病管理中国专家共识(2023)》[9]中多病共存诊断标准,即≥2种的慢性健康问题同时发生于同一名老年个体的情况,可为脏器疾病、精神问题、老年综合征,也可为影响老年人健康状况的其他问题,且持续时间≥1年;(4)入院时改良Rankin量表(mRS)评分[10]≤2分,入院时Brunnstrom分期[11]为Ⅳ期及以上;(5)无需他人协助且不使用辅助器械可完成独立行走≥ 10m[12];(6)意识清楚,可完成问卷调查。
排除标准:(1)长期卧床或完全依赖轮椅转移;(2)多器官衰竭;(3)合并精神疾病;(4)视力障碍;(5)临床资料缺失;(6)随访期间死亡或失访。
1.2 资料收集
收集患者出院时的一般及临床资料,包括性别、年龄、体质量指数、共病种类[高血压病[13]、糖尿病[14]、冠心病[15]、慢性心力衰竭[16]、骨质疏松症[17]、肌少症[18]及其他慢性疾病(甲状腺功能减退[19]、前列腺增生[20]、脂肪肝[21]等)]、共病数量(≥3种,2种)、营养状况、跌倒风险、肢体功能、认知情况、下肢偏瘫情况及随访期(入院后6个月)内跌倒发生情况。
营养状况评估采用营养风险筛查2002(nutritional risk screening 2002, NRS-2002)量表[22]评估,总分7分,得分与营养风险成正比,评分≥3分表示存在营养风险。采用mRS评估肢体功能[10],总分0~6分,0分为无症状,1分为有症状但无明显残疾,2分为轻度残疾(可独立完成日常生活与工作但无法进行日常活动),3分为中度残疾(可独立行走但需要他人照顾),4分为重度残疾(需要他人协助行走及照顾),5分为严重残疾(卧床不起,需他人照顾),6分为死亡。采用蒙特利尔认知评估(Montreal cognitive assessment, MoCA)量表[23]评估认知情况,总分为30分,≥26分为认知功能正常。采用Brunnstrom分期[11]评估下肢偏瘫情况,根据肌张力及偏瘫侧肢体运动情况进行评价,分为Ⅰ~Ⅵ期,分期越高表示运动功能越好。采用Tinetti POMA量表[7]评估跌倒风险,量表包括平衡(9个项目,总计16分)和步态(7个项目,总计12分)两部分测试,总分28分,评分越高,表示跌倒风险越低。参考既往研究[24-25],将跌倒定义为明亮环境下行走时突发的、不自主的、非故意的体位改变,倒在地上或更低的平面上。随访期间发生跌倒次数≥1次的患者为跌倒组,未发生跌倒患者为非跌倒组。
1.3 实验室检查
患者入院次日晨起空腹状态下采集静脉血5ml,离心分离血清后,采用高效液相色谱法检测糖化血红蛋白水平,葡萄糖氧化酶法检测空腹血糖水平,免疫比浊法检测白蛋白、前白蛋白水平,胆固醇氧化酶-过氧化物酶法检测三酰甘油、总胆固醇、低密度脂蛋白胆固醇、高密度脂蛋白胆固醇水平,尿酸酶法检测肌酐、尿酸水平。
1.4 统计学分析
采用SPSS28.0软件进行统计学分析。计数资料以例(%)表示,组间比较采用χ2检验;采用Kolmogorov-Smirnov法检验计量资料是否符合正态分布,符合正态分布的计量资料以x-±s表示,组间比较采用独立样本t检验,不符合正态分布的计量资料以中位数和四分位数[M(P25,P75)]表示,组间比较采用Mann-Whitney U检验。将组间比较中差异有统计学意义的指标纳入多因素Logistic回归分析,探索老年脑梗死慢性期多病共存患者发生跌倒的影响因素。应用R3.6.3软件绘制老年脑梗死慢性期多病共存患者发生跌倒的列线图预测模型,采用受试者工作特征(receiver operating characteristic, ROC)曲线、校准曲线、决策曲线评估该列线图预测模型的效能,其中Hosmer-Lemeshow拟合优度检验用于评价模型标准度,P>0.05(实际概率与预测概率差异无统计学意义)为预测模型拟合良好。以P<0.05为差异有统计学意义。
2 结果
共纳入符合本研究纳入排除标准的老年脑梗死慢性期多病共存患者147例,男59例,女88例,年龄61~93岁,平均(77±7)岁,末次发病至入院时间17~122个月,平均(63±17)个月,其中跌倒组54例(36.73%),非跌倒组93例(63.27%)。患者共病数量2~6种,中位共病数量3(2,4)种;占比前3位的共病疾病为高血压病(94.56%)、糖尿病(57.14%)、肌少症(42.86%)、骨质疏松症(42.86%)。本研究患者纳入排除流程见图1。
2.1 跌倒组与非跌倒组一般及临床资料比较
与非跌倒组相比,跌倒组年龄、NRS-2002量表评分及共病数量≥3种、骨质疏松症、肌少症患者比例更高,Tinetti POMA量表评分更低(均P<0.01)。见表1。

2.2 跌倒组与非跌倒组实验室指标
比较
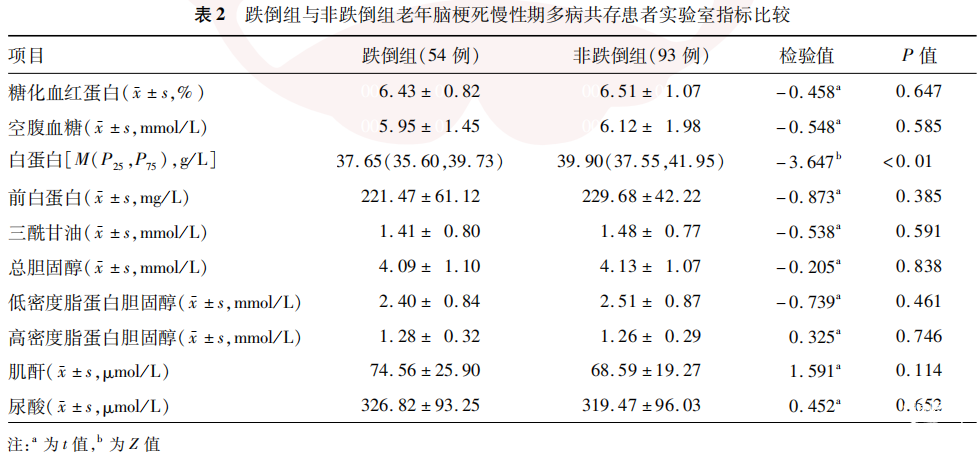
与非跌倒组相比,跌倒组白蛋白水平更低(P<0.01),余实验室指标组间比较差异均无统计学意义(均P>0.05)。见表2。
2.3 多因素Logistic回归分析
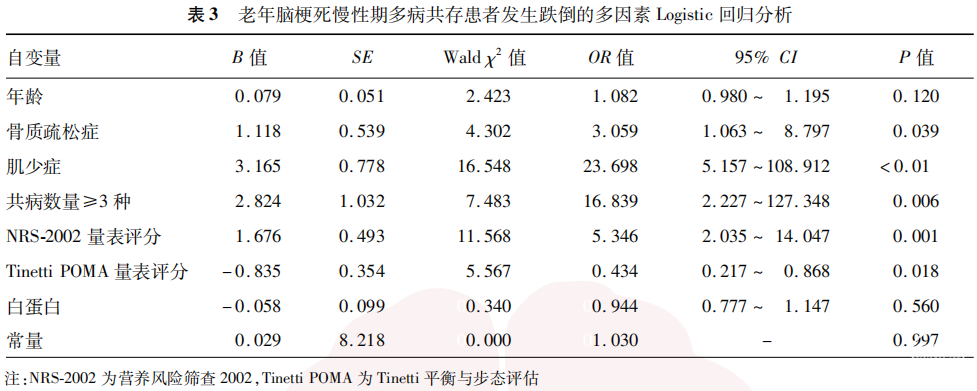
以跌倒作为因变量(跌倒=1,无跌倒=0),以骨质疏松症(是=1,否=0)、肌少症(是=1,否=0)、共病数量(≥3种=1,2种=0)、年龄、NRS-2002量表评分、Tinetti POMA量表评分、白蛋白为自变量进行多因素Logistic回归分析,结果显示,骨质疏松症、肌少症、共病数量≥3种、高NRS-2002量表评分是老年脑梗死慢性期多病共存患者发生跌倒的独立危险因素(均P<0.05),高Tinetti POMA量表评分是老年脑梗死慢性期多病共存患者发生跌倒的独立保护因素(P=0.018)。见表3。
2.4 列线图预测模型的构建、评价与
验证
基于多因素Logistic回归分析中影响老年脑梗死慢性期多病共存患者发生跌倒的因素构建列线图预测模型。见图2。
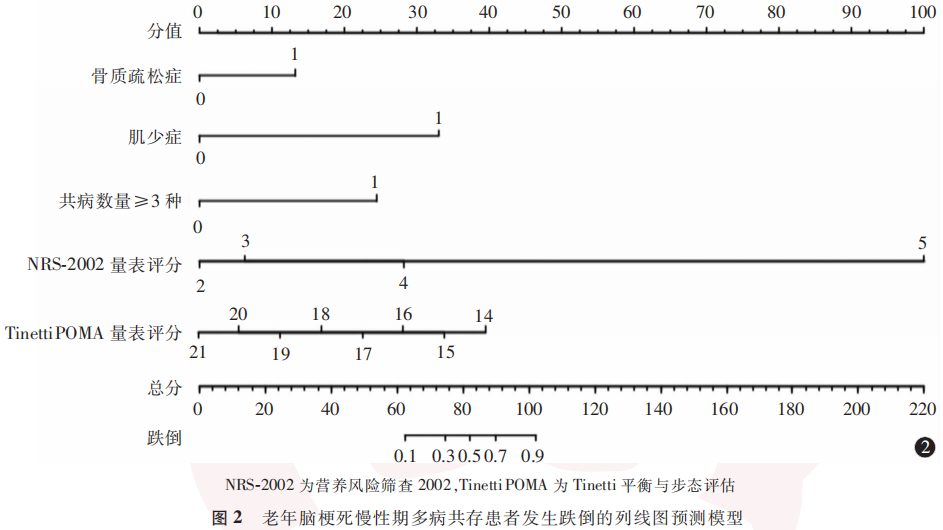
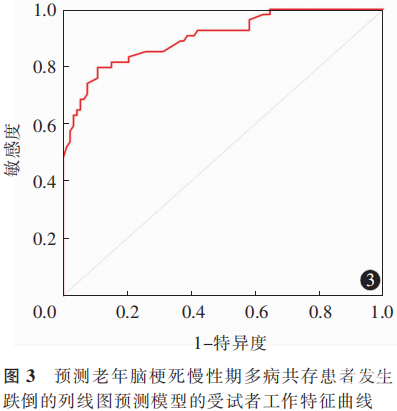
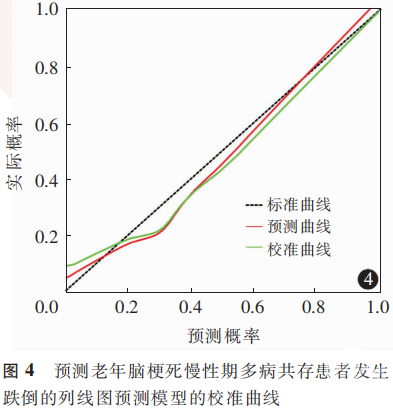
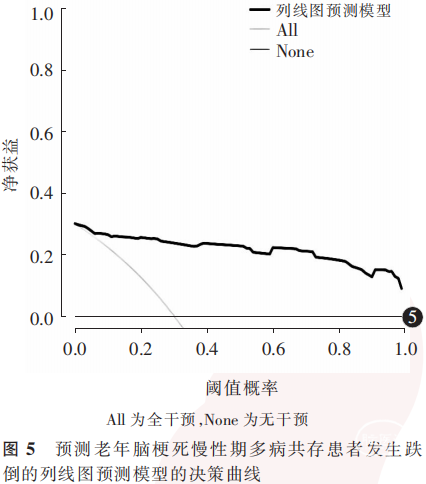
ROC曲线显示,该列线图模型预测老年脑梗死慢性期多病共存患者跌倒的曲线下面积为0.894(95%CI:0.840~0.948),敏感度为77.80%,特异度为90.30%。见图3。Hosmer-Lemeshow拟合优度检验结果显示,该列线图模型拟合良好(χ2=9.612,P=0.293)。见图4。决策曲线分析显示,阈值概率在0.01~0.99时该列线图预测模型均可产生更好的临床效益。见图5。
3 讨论
多病共存是一个复杂且日益受到关注的医疗问题,中国60岁以上人群中患有≥1种慢性病的比例超过70%[26],相比于1种慢性疾病,多病共存可导致老年患者日常生活能力下降,影响其日常活动的独立性水平[27]。既往未见针对老年脑梗死合并多种慢性疾病患者跌倒风险的研究,且目前缺乏可量化、多维度的跌倒风险评估方式。基于此,本研究对老年脑梗死多病共存患者的慢性病共存情况、营养状况、跌倒风险、临床资料及实验室指标进行分析,并构建老年脑梗死多病共存患者发生跌倒的列线图预测模型。
本研究中老年脑梗死多病共存患者共病数量为2~6种,中位共病数量3(2,4)种,以共病高血压病(94.56%)、糖尿病(57.14%)为主。潘晔等[28]研究显示,老年人(年龄≥60岁)共病以高血压病为主,占比为47.14%(5091/10800),提示高血压病在老年多病共存患者中具有一定普遍性。高血压病为心脑血管不良事件的重要危险因素之一,积极治疗与控制血压可改善高血压病合并脑梗死患者的预后[29]。高血压病可损害脑血管的弹性和通透性,导致动脉壁变硬及动脉粥样硬化斑块形成,脑部的血液供应减少,增加脑梗死的发生风险;糖尿病则可引起等血管内皮功能障碍、动脉粥样硬化、微血管病变[30]。多种疾病相互作用的病理生理过程复杂,在老年共病住院患者的临床诊治中需关注合并有高血压病、糖尿病等基础疾病的群体,为老年脑梗死患者实施个体化的综合治疗。
本研究中老年脑梗死慢性期多病共存患者入院后随访6个月内跌倒发生率为36.73%,提示老年脑梗死慢性期多病共存患者存在较高的跌倒发生率,多因素Logistic回归分析显示,年龄、白蛋白水平与跌倒无关,本研究纳入对象均为老年脑梗死慢性期患者,年龄范围可能相对集中,加之跌倒为多种因素综合作用的结果,可能导致年龄分层效应在多因素分析中被掩盖;白蛋白是反映营养状况的指标,但老年脑梗死慢性期多病共存患者白蛋白水平易受炎症、肝肾功能异常等因素影响,可能导致无法单纯依靠白蛋白反映此类患者的长期营养状态。本研究结果显示,骨质疏松症、肌少症、共病数量≥3种、高NRS-2002量表评分为老年脑梗死慢性期多病共存患者跌倒的独立危险因素,高Tinetti POMA评分为其独立保护因素。骨质疏松症是一种以骨量降低、骨组织微结构损坏导致骨脆性增加,易发生骨折为特征的全身性骨病,可出现活动障碍[31],进而干扰身体平衡控制能力,增加跌倒发生风险。脑梗死慢性期患者多存在肢体活动受限,患者日常活动受阻易导致日照时间减少,维生素D合成不足,与并存的炎症状态可共同促进骨质疏松进展。采取适当的运动锻炼并结合药物以提高肌力、改善平衡能力、增加骨密度,在日常生活中避免匆忙或剧烈动作或有利于降低跌倒发生风险[32]。肌少症是一种与年龄增长相关的肌肉量减少、肌肉力量下降和(或)躯体功能减退的综合征[33]。脑梗死后肌少症较为常见,其发病机制包括制动导致的肌肉萎缩及炎症因子持续激活、交感神经过度激活、中枢神经驱动下降等多种病理过程[34]。研究显示,肌少症在社区老年群体中普遍存在,影响患者活动能力,可导致站立平衡受损与功能下降,增加跌倒风险[35]。临床应定期对老年慢性期脑梗死患者肌肉力量、躯体体能等进行评估,及时识别并干预肌少症的发展,同时鼓励患者进行适当的肌肉锻炼,以提高肌肉质量和力量;此外,个体化用药管理、多病协同治疗有利于促进患者康复。共病数量多提示患者身体整体健康状况差,多种疾病相互作用可能进一步影响身体机能。对于脑梗死慢性期患者,合并多种疾病不仅加重了身体负担,还可能通过影响药物作用、脑灌注等方式对患者反应速度及平衡能力造成间接损害。共病数量增加可导致生理储备耗竭,多系统功能衰退形成叠加效应,既往研究显示,≥45岁群体中多病共存与跌倒密切关联,合并2、≥3种慢性疾病是≥ 45岁人群发生跌倒的危险因素,OR值分别为1.38(95%CI:1.10~1.72,P=0.005)、1.70(95%CI:1.31~2.20,P=0.001)[36]。与本研究结果具有一致性。改善脑梗死患者的营养状况,可促进患者功能康复及生活质量提高[37]。候林林等[38]研究显示,与未跌倒组(64例)卒中康复期住院患者比较,跌倒组(32例)营养不良[营养控制状态评分(淋巴细胞计数、人血白蛋白和总胆固醇水平3个指标赋值后的总分)2~12分]患者比例更高[31.3%(10/32)比12.5%(8/64),P=0.027],营养不良是卒中康复期住院患者跌倒(住院前1年内发生跌倒≥1次)的危险因素(OR=11.071, 95%CI:1.185~103.453)。NRS-2002量表为一种综合性工具,可多维度评估营养风险。本研究采用NRS-2002量表对老年脑梗死慢性期多病共存患者的营养风险进行评估,结果显示,高NRS-2002量表评分为老年脑梗死慢性期多病共存患者跌倒的危险因素,与上述研究结果相似,提示卒中患者的营养状况可能与跌倒相关。研究显示,营养不良[非自愿性体质量减轻(过去6个月内体质量下降超过10%或过去1个月内体质量下降超过5%),且体质量指数下降(<65岁患者体质量指数< 18.5kg/m2,≥65岁患者体质量指数< 20kg/m2)为高龄(≥80岁)住院患者住院期间跌倒的危险因素(OR=2.1, 95%CI:1.2~3.6)[39]。营养状态不佳可对肌肉造成影响,导致患者活动减少、合成代谢抵抗,发生炎症、酸中毒和维生素D缺乏,进而造成肌力下降或衰弱[40]。因此对于存在营养风险的脑梗死慢性期患者可补充蛋白质并结合阻力训练,以维持身体的平衡能力和稳定性,降低跌倒风险。临床应关注老年多病共存脑梗死慢性期患者的饮食习惯和摄入量,避免过度限制饮食或暴饮暴食,指导患者保持均衡饮食,确保摄入足够的营养物质以改善患者的营养状况,降低跌倒风险。Tinetti POMA量表在脑梗死慢性期患者的平衡状态评估中具有良好的应用价值[41]。Tinetti POMA量表评分≤24分提示患者的平衡与步态功能受损[42]。卒中患者因上肢功能障碍出现平衡问题时,可能无法完成高质量的保护性反射,从而发生跌倒[43]。临床可以个体化康复训练改善运动功能为核心,改善患者的运动功能,进而减少跌倒发生[44]。综合评估上述影响因素有利于多维度评估脑梗死慢性期老年患者跌倒风险。
在预测模型构建方面,与既往研究相比,本研究在模型性能、预测因素整合及人群特异性方面均具有一定价值。Kim等[45]研究显示,跌倒与住院患者年龄、护士照护时间等密切相关,其使用场景更侧重于医护管理,而本研究则聚焦于脑梗死慢性期且多病共存的老年患者这一特殊群体,纳入慢性病共病数量、营养状况、平衡与步态评估指标构建跌倒的列线图预测模型,ROC曲线分析显示,该模型预测患者跌倒的曲线下面积为0.894(95%CI: 0.840~0.948),敏感度为77.80%,特异度为90.30%;Hosmer-Lemeshow拟合优度检验结果显示,该列线图模型拟合良好(χ2=9.612,P=0.293),可较为准确地预测患者跌倒风险;列线图预测模型阈值在0.01~0.99时,可提供临床净收益。既往有研究对中国≥45岁群体多病共存(共存≥2种慢性病)与跌倒(近2年发生跌倒≥1次)风险的关系进行分析,结果显示,共病数量越多,其发生跌倒的风险越高(合并1、2、3、4、≥5种慢性病患者的调整后OR值分别为1.60、2.08、2.22、3.15、4.55;均P<0.01)[46]。安然等[47]研究表明,与非多病共存老年人(≥60岁)比较,多病共存(≥2种疾病)使老年人过去1年发生跌倒的风险增加24%(OR=1.24,95% CI:1.15 ~ 1.34)。上述研究虽揭示了跌倒与共病的关系,但并未进一步构建发生跌倒的预测模型。本研究以“脑梗死”“跌倒”“多病共存”“预测模型”为关键词组合,检索中国知网、万方医学网、中华医学期刊全文数据库中2020年1月1日—2025年8月31日收录的中文文献;以“cerebral infarction”“falls”“coexistence of multiple diseases”“prediction model”为关键词组合,检索PubMed数据库中2020年1月1日—2025年8月31日收录的英文文献,未见近5年关于老年脑梗死慢性期多病共存患者与跌倒关系及相关预测模型的研究,多为脑梗死患者与跌倒的关系研究。本研究则聚焦多病共存与脑梗死2个关键特征,系统性整合骨质疏松、营养风险等关键指标,结果表明,多病共存是影响脑梗死患者发生跌倒的关键因素,本研究创新性地将肌少症纳入老年脑梗死慢性期多病共存患者跌倒的列线图预测模型,且预测模型在预测效能及临床获益方面均具有一定优势。本研究关注脑梗死慢性期多病共存患者入院后随访6个月的跌倒情况,未将脑梗死发病后至本次入院前的跌倒史作为研究变量,主要考虑本研究为回顾性研究,脑梗死病程较长,患者跌倒史获取准确性不足。
本研究的局限性:首先本研究为单中心回顾性分析,所有患者均来自同一机构,可能存在选择偏倚;其次,研究可能未涉及部分潜在重要影响因素,如既往跌倒史;此外,本研究的随访期为入院后6个月内,未能对长期跌倒风险变化趋势进行分析。未来可开展多中心前瞻性研究,纳入更多相关指标及延长随访时间进一步深入探究。
综上所述,老年脑梗死慢性期多病共存患者以共病高血压病、糖尿病为主;患者跌倒与伴骨质疏松症、肌少症及共病数量多、营养风险高、Tinetti POMA量表评分低有关,基于上述因素构建的列线图预测模型具有良好的预测效能,可为临床预测老年脑梗死慢性期多病共存患者跌倒及制定预防策略提供量化工具。
*本文转载自微信公众号“中国脑血管病杂志”,脑医汇获授权转载
声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。
投稿邮箱:NAOYIHUI@163.com
未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。
投稿/会议发布,请联系400-888-2526转3。





