通信作者:郭津,Email:guojin8002@163.com
基金项目:2024年度黑龙江省自然科学基金联合基金培育项目(PL2024H014);黑龙江省教育厅创新团队项目(2024-KYYWF-0611);黑龙江省教育厅基本科研业务费基础科研项目(2022-KYYWF-0653)
DOI:10.3760/cma.j.cn113694-20250603-00328
引用本文:孔德明,郭津,刘家豪,等.丘脑底核脑深部电刺激治疗难治性癫痫的研究进展[J].中华神经科杂志,2026,59(1):76-83.DOI:10.3760/cma.j.cn113694-20250603-00328.
【摘要】癫痫是一种由脑神经元异常放电引发的慢性疾病,约1/3患者会发展为难治性癫痫,其中部分患者因致痫灶弥漫或位于功能区而无法接受切除手术,神经调控疗法如脑深部电刺激(DBS)或成为重要替代选择。丘脑底核作为皮质-基底神经节运动回路的关键节点,在运动障碍性疾病治疗中已得到广泛应用,近年来,其在运动皮质区域癫痫发作中的疗效逐渐受到关注。文中将从丘脑底核-DBS治疗难治性癫痫的临床疗效、影响因素、作用机制及不良反应等方面进行综述。
【关键词】丘脑底核;深部脑刺激法;难治性癫痫

癫痫是一种常见的慢性疾病,是由脑神经元异常放电引发大脑电活动紊乱,导致的短暂性脑功能障碍及癫痫发作反复出现[1]。尽管有30多种获批的抗癫痫发作药物(anti-seizure medications,ASMs),但仍有约1/3的确诊后患者对药物治疗无明显效果,继而发展为难治性癫痫[2-3]。在这类患者中,确定致痫病灶并实施切除手术或许能减少甚至完全控制癫痫发作。然而,尽管50%的难治性癫痫患者可从手术切除中获益,但癫痫手术仍具挑战性,实际上,不少患者无法接受切除手术,原因在于疑似癫痫发作病灶较弥漫、定位不清或位于易因损伤导致神经功能缺损的高风险区域[4-5]。因此,并非所有难治性癫痫患者都能通过手术切除获益,急需其他治疗方式介入[6]。对于存在手术禁忌证、致痫区(epileptogenic zone)位于功能区或手术失败的癫痫患者,神经调控疗法可作为一种有效的替代选择。脑深部电刺激(deep brain stimulation,DBS)是神经调控疗法的重要组成部分,通过对脑内特定靶点施加电刺激,能够调节相应核团及神经回路的兴奋性,并且在过去几十年中已被开发为一种替代疗法[7-8]。丘脑前核(anterior nucleus of thalamus)是海马环路中的一个重要节点,是目前治疗癫痫最常用的刺激靶点,丘脑前核-DBS对颞叶癫痫发作的控制效果令人满意,但对其他区域引发的癫痫发作控制效果较差[9]。因此,针对起源于运动皮质相关区域的难治性癫痫,有必要探索新的刺激治疗靶点。
丘脑底核(subthalamic nucleus)在皮质-基底神经节运动回路中起着关键作用,已广泛用于帕金森病、特发性震颤等各种运动障碍性疾病的神经调控[10-11]。丘脑底核是局灶性运动性癫痫的网络核心,针对源于运动皮质的难治性癫痫,采用丘脑底核-DBS疗法可取得一定的疗效[12]。我们分别以“癫痫”“难治性癫痫”“深部脑刺激法”“丘脑底核”为中文检索词,以“epilepsy”“refractory epilepsy”“deepbrain stimulation”“subthalamic nucleus”为英文检索词,在中国知网、万方医学、PubMed、Web of Science数据库(检索发表时间为2002—2025年的相关文献)进行文献检索,从丘脑底核-DBS治疗难治性癫痫的临床疗效、影响因素、作用机制及不良反应等方面进行综述。

一、DBS及丘脑底核的介绍
1.DBS的原理:DBS作为一种神经调控技术,通过将电极精准植入大脑内的特定靶点,由与之相连类似起搏器的装置供能,可持续或间歇性地向靶点传输电流[13]。虽作用机制尚未完全明确,但有学者认为,DBS是通过调节大脑特定功能回路中的病灶来发挥疗效[14]。临床研究结果显示,相同的DBS参数和刺激目标能让多种神经系统疾病患者受益,这表明该疗法并非仅针对特定疾病的病理机制,而是调节已存在且活跃的病变脑回路,耐受性良好[14]。目前,全球已有上万名不同类型的神经系统疾病患者接受过DBS治疗,如帕金森病、癫痫、强迫症、神经性疼痛和药物成瘾等,该疗法采用双侧或单侧电极,治疗不同疾病时选择的靶点不同。DBS治疗难治性癫痫时的靶点主要包括丘脑前核、丘脑中央中核、丘脑底核、海马和小脑等[15-16]。DBS的最终目标是在最大限度提高治疗效果的同时减少不必要的不良反应,提升患者生活质量[17]。
2.丘脑底核的解剖和功能:丘脑底核是一种位于丘脑腹侧的椭圆形间脑结构,与基底神经节和中脑结构关系密切。其背侧与未定带相邻,背外侧和背内侧分别被ForelH2(豆状袢)和ForelH1区(丘脑袢)的纤维束所包绕;腹侧,其头端区域与内囊背内侧相连,尾端位于黑质(substantia nigra)头端背外侧,尤其与黑质网状部(substantia nigra reticulata,SNr)相邻;内侧与豆状袢相关联,外侧通常与内囊后肢相邻[18]。从细胞结构看,啮齿动物、非人类灵长类动物和人类的丘脑底核主要由兴奋性谷氨酸能神经元构成,还存在少量γ-氨基丁酸(γ-aminobutyric acid,GABA)能神经元[19]。
丘脑底核是基底神经节回路的重要组成部分,在运动控制、认知和情感调节等方面发挥关键作用。它与基底神经节的苍白球、纹状体、黑质等结构有广泛的纤维联系,参与神经信号的传递和整合。丘脑底核主要接收来自苍白球外侧部(external segment of the globus pallidus)的抑制性投射,并将谷氨酸能投射至SNr和苍白球内侧部(internal segment of the globus pallidus,GPi)[20]。在运动功能上,丘脑底核与基底神经节协同工作,基底神经节的直接通路(促进运动)和间接通路(抑制运动)相互拮抗共同控制运动。丘脑底核是间接通路的关键节点,通过调节间接途径的运动,增加对GPi的谷氨酸能输出,刺激GPi的GABA能神经元释放,导致丘脑兴奋减少和运动减少。当丘脑底核被激活时,通过间接通路抑制运动;受抑制时则促进运动[21-22]。研究结果显示,丘脑底核参与难治性运动性癫痫的发作,或可作为DBS治疗的潜在靶点[23]。

二、丘脑底核-DBS的临床疗效
丘脑底核-DBS适用于致痫区与感觉运动皮质相关的癫痫患者,术前需通过头皮视频脑电图、立体定向脑电图、高分辨率磁共振成像等手段进行评估定位,依据Morel立体定向图谱确定丘脑底核背外侧靠近SNr的运动相关亚区为靶点,通过微电极记录验证神经元高频放电等电活动特征,最终完成电极植入[24-25]。
Benabid等[26]首次报道采用丘脑底核-DBS治疗局灶性顶叶发育不良所致无法手术的癫痫患者,可使其发作频率降低80.7%。其后续研究结果显示,5例接受治疗的患者中,其中3例为感觉运动皮质引发的部分症状性发作,这3例患者的发作频率降低了67.0%~80.0%,且其中2例患者的运动功能也得以改善[27]。Shan等[24]报道了首例丘脑底核-DBS治疗全面性发作的耐药性肌阵挛性癫痫患者,该患者接受了双侧植入术,术后1年随访结果显示发作频率降低87.5%,严重程度和生活质量均得到有效改善,且无不良反应。Wille等[28]对5例进行性肌阵挛性癫痫(progressive myoclonic epilepsy,PME)患者进行了双侧单级SNr/丘脑底核的DBS治疗,1年随访后结果显示癫痫发作强度和频率降低30%~100%,部分患者出现癫痫发作加剧或明显不良反应,调整刺激参数后可恢复初始治疗效果。徐欣等[29]对5例局灶性运动性癫痫患者的丘脑底核进行长期刺激(平均周期>2年),结果显示所有患者的发作频率均较术前降低50%以上,其中平均发作频率减少87.6%,1例实现了6个月以上无发作Wang等[23]报道了1例局灶性肌阵挛性癫痫患者,病史为6年,MRI显示左额叶和中央区域轻微萎缩,经单侧丘脑底核-DBS治疗后随访5年,其发作频率较术前降低70.0%。这表明该疗法具有良好的长期疗效,证实其在难治性癫痫中的安全性和有效性,为癫痫治疗提供了重要依据。Ren等[30]对7例难治性局灶性运动性癫痫患者展开研究,探究丘脑底核-DBS不同刺激频率的调节作用,发现低频(20Hz)刺激会增加运动区域的癫痫活动,而高频(100/130Hz)刺激则可减少该区域癫痫活动。Cui等[31]对6例药物难治性癫痫患者研究显示,丘脑底核-DBS使发作频率平均下降64.0%,1例患者实现无发作;在癫痫发作类型、ASMs使用及认知功能方面,术前与术后无显著差异;5例对慢性丘脑底核刺激耐受性良好,仅1例出现右臂运动障碍。Yan等[25]对16例伴有运动性发作且致痫区与感觉运动皮质相关的难治性癫痫患者进行丘脑底核-DBS治疗,发现该疗法能显著减少癫痫发作,13例(81%)对治疗有效果,平均发作频率降低87.1%,其中2例可保持至少6个月无发作;但也有部分患者出现发作频率增加或治疗效果不佳,可能与刺激参数、电极接触不当的因素有关。Yang等[32]对3例难治性癫痫患者展开研究,探究丘脑底核-DBS在不同癫痫类型中的治疗作用,发现对于2例全面性肌阵挛性发作以及1例发作起始于辅助运动区的患者,将丘脑底核作为DBS的靶点之一进行多靶点治疗后,所有患者癫痫发作负担均显著降低,具体表现为发作聚集减少、严重程度降低和持续时间缩短。丘脑底核-DBS治疗各种类型难治性癫痫的临床疗效见表1。

综合上述研究可见,丘脑底核-DBS是一种治疗难治性癫痫有效的神经调控疗法。从癫痫发作类型来看,该疗法可能对耐药性肌阵挛性癫痫及感觉运动皮质引发的部分症状性癫痫治疗效果较为显著,能使其发作强度和频率明显降低,且部分患者运动功能得以改善。从致痫灶位置而言,起源于运动皮质相关区域(如顶叶、额叶、感觉运动皮质、辅助运动区等)的难治性癫痫患者疗效较为突出[24,26,32]。因此,多项研究结果证实,丘脑底核-DBS对上述患者的疗效具有持久性,并且可能不会对认知功能产生影响,但仍需更大样本量、更长时间的随访研究,以进一步明确其在不同临床特征患者中的有效性和安全性。

三、丘脑底核-DBS效率的影响因素
1.靶点选择:既往针对丘脑底核-DBS在运动障碍性疾病领域的研究结果显示,对丘脑底核及其邻近脑区的刺激可能产生不同效果,这或为癫痫临床治疗提供新的思路[33]。受刺激电极周围被激活组织的体积(volume of tissue activated,VTA)直接决定刺激结果的有效性。鉴于丘脑底核亚核的不同功能及周围复杂的邻接关系,与VTA相邻或受其涉及的脑区在功能调控中尤为关键,且VTA受电极接触位置和刺激参数影响[34]。研究结果证明,对丘脑底核背外侧区域进行DBS,不仅可有效改善帕金森病临床症状,该区域作为皮质-基底神经节运动回路的关键节点,还可通过调节异常神经同步化抑制癫痫发作[35-36]。另一项研究结果表明,癫痫患者与帕金森病患者使用的丘脑底核靶点相比更偏向于外侧和背侧,并且最有效的靶点位于丘脑底核的下部,靠近SNr[31]。近期研究显示,针对PME患者,单独SNr高频DBS效果优于刺激丘脑底核或两者的过渡区[37]。无论丘脑底核最佳刺激靶点是下外侧区域还是背外侧区域,在治疗癫痫时,效果不会因靶点不同而出现较大差异[38]。
2.刺激参数:丘脑底核-DBS抗癫痫作用还受刺激参数的影响,如频率、脉宽、电流或电压等。一项评估丘脑底核刺激调节作用的研究结果显示,以2A电流、10~130Hz递增频率刺激60s发现:20Hz刺激时运动区发作间期棘波(interictal intermittent spike)较非运动皮质增多,高频振荡(high-frequency oscillations)率高于基线;100Hz刺激降低高频振荡率;130Hz刺激可减弱亚临床癫痫患者发作期节律性放电,且抑制作用持续整个刺激期间。进一步研究证实,130Hz的丘脑底核刺激还能有效减轻运动皮质的节律性癫痫放电,抑制其引发的进展性发作期放电[30,38]。Xue等[39]的研究结果显示,在青霉素诱导的小鼠模型中,丘脑底核的低频(10Hz)、中频(60Hz)刺激不会减弱癫痫发作的钙信号,对癫痫发作控制无改善或缓解作用,而高频(130Hz)丘脑底核-DBS减轻了癫痫发作,能深度缓解运动皮质癫痫活动,这意味着丘脑底核可能是DBS治疗难治性运动性癫痫的首选目标。因此,丘脑底核的常规刺激频率为130Hz,建议将刺激电压从低设置逐渐提高到较高水平,以减轻潜在的不良反应[24]。
3.单侧或双侧刺激:关于丘脑底核-DBS单侧和双侧刺激的效果存在争议,研究结论不一。部分研究认为单侧和双侧刺激均有效果,另一些研究结果则表明只有双侧刺激有效[23-25,30,39]。在一项难治性癫痫患者治疗中,部分患者接受双侧刺激,另一部分接受单侧刺激,从治疗效果看,尽管刺激方式不同,但均有一定成效,差异并无统计学意义[31]。因此,这意味着两种刺激方式在临床中各有其价值,还需根据患者的情况选择更为合适的方式。
4.间歇性或持续性刺激:研究结果表明,高频持续性刺激显著降低癫痫发作的频率、振幅等指标,显示出控制癫痫发作方面的明显效果;同样,高频间歇刺激(如130Hz,30s开-关)也可有效抑制丘脑底核兴奋性神经元及丘脑底核-SNr回路,减少癫痫活动,且避免连续性刺激可能导致的神经适应性[39]。另一项研究结果显示,针对肌阵挛性癫痫患者进行双侧丘脑底核-DBS时,鉴于功耗差异选择间歇性刺激模式,该模式已显示出令人满意的治疗效果[24]。目前丘脑底核-DBS的间歇性刺激与持续性刺激在癫痫治疗效果上尚无明确差异。临床中,刺激方式的选择需结合患者病情特点、个体生理差异等因素进行个性化调整,以实现最优治疗效果[40]。

四、丘脑底核-DBS的作用机制
1.丘脑底核的抑制:丘脑底核是皮质-皮质下网络的一部分,可整合感觉运动活动,并通过直接和间接途径调节运动皮质的兴奋功能。动物研究通过多种方法证实了丘脑底核与运动皮质之间存在连接,这为丘脑底核-DBS调节运动皮质癫痫活动提供了神经通路基础[38,41]。丘脑底核除了通过单突触谷氨酸能输入调节SNr和GPi的抑制外,还能降低癫痫发作易感性。因此,可能对难治性癫痫的靶向治疗具有研究价值和应用潜力;它已是帕金森病DBS的既定神经外科靶点,这为向癫痫患者的临床转化应用提供了可行性基础[42]。研究发现,丘脑底核兴奋性神经元在运动性癫痫模型中双向调节癫痫发作幅度,激活该神经元会放大癫痫发作,抑制则能减轻其发作。高频丘脑底核电刺激对丘脑底核兴奋性神经元或丘脑底核-SNr回路的抑制作用相似,因此可推测,丘脑底核-DBS通过抑制该回路的投射改善小鼠的癫痫活动[39]。另外,丘脑底核刺激能通过延迟首次癫痫发作发生和减少发作次数来改善难治性癫痫的发作[30]。
2.黑质控制系统:黑质系统与丘脑底核保持密切的空间和功能关系,还能调节癫痫中的神经元传递[43]。SNr通过直接途径接收来自纹状体的GABA能投射,通过间接途径接收丘脑底核的谷氨酸能投射,同时将自身释放的GABA能投射到运动丘脑核(如腹外侧和腹内侧)[44]。同步活动是癫痫发作开始的先行决定因素,相反,抑制黑质会使下游区域去抑制,导致皮质活动不同步,从而提高癫痫发作阈值。因此,直接抑制SNr本身,或通过抑制其直接神经支配来源的丘脑底核间接抑制SNr,可产生抗惊厥作用[42]。大脑皮质与丘脑底核存在特定的神经传导通路,丘脑底核神经元能够将神经信号投射到SNr,并与上丘[中脑背侧抗惊厥区(dorsal midbrain anticonvulsant zone,DMAZ)]存在功能联系[45]。DMAZ受到来自SNr的GABA投射的强直抑制,而SNr则受到丘脑底核谷氨酸能投射的强直兴奋,研究假设DBS抑制丘脑底核,可降低SNr活性,消除对DMAZ的抑制,进而抑制癫痫发作[31]。
3.皮质-丘脑底核通路:最近一项针对癫痫患者的丘脑底核-DBS研究观察到,癫痫发作期的异常放电可从运动皮质迅速扩散至丘脑底核,表明其参与癫痫发作期的形成。同时记录到丘脑底核和癫痫发作区之间的皮质诱发电位,为皮质-丘脑底核回路的相互关系提供了有力证据[30]。在运动性癫痫发作的患者中,丘脑底核-DBS可抑制与运动相关的皮质异常兴奋性,调节运动皮质-丘脑底核回路,从而减轻癫痫发作[40]。研究发现,丘脑底核的刺激以逆向传导的方式激活该通路,从而降低皮质兴奋性并诱导抗癫痫作用[31]。另外,在癫痫大鼠模型的实验观察中也发现,丘脑底核-DBS可以显著抑制癫痫发作,表明其抗癫痫作用机制可能与逆向激活皮质-丘脑底核通路密切相关[12]。
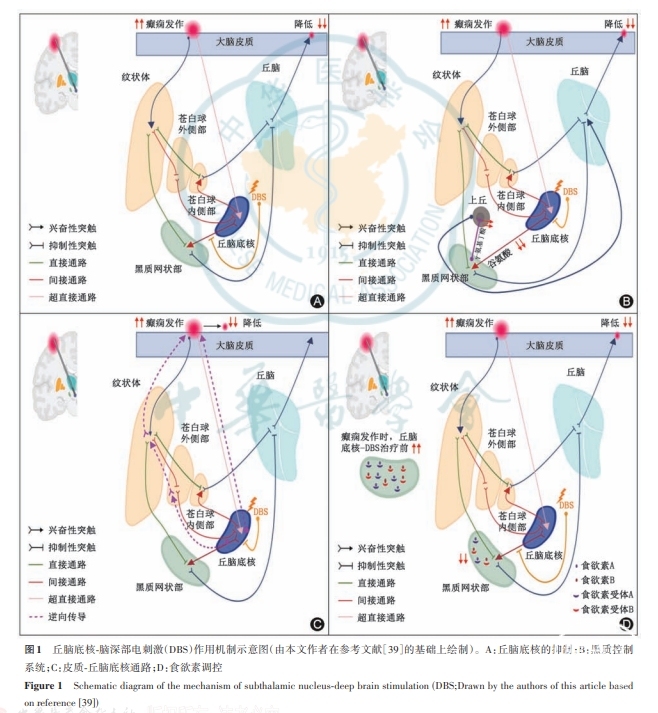
4.食欲素的调控:食欲素(也称为下丘脑分泌素)是一种兴奋性下丘脑肽,分为食欲素A和食欲素B两个亚型,由下丘脑中一组神经元分泌。这些神经元位于最靠近丘脑底核的区域,且投射到丘脑底核和SNr。此外,丘脑底核和SNr存在1型(OX1R)和2型(OX2R)两种类型的食欲素受体,且二者共定位于这两个区域[46]。内源性食欲素A/B维持丘脑底核谷氨酸能神经元和SNrGABA能神经元的生理性放电[47]。研究发现,外源性食欲素A/B可增加青霉素诱导的癫痫活性。此外,在多种癫痫模型中,DBS能影响食欲素及受体的表达,以减少癫痫的发作[48],同时,食欲素受体拮抗剂也可发挥相似的抗癫痫作用[39]。多项研究结果表明,食欲素通路在各类癫痫发作中(如阵挛性、失神性、创伤后癫痫等)发挥关键作用[49-51]。因此,丘脑底核-DBS降低癫痫发作活性可能与食欲素通路的调节相关。进一步研究显示,癫痫发作时食欲素及其受体表达增强,而高频丘脑底核-DBS可下调SNr中与癫痫发作相关的食欲素及其受体的升高水平,可能减少二者的结合,其机制与抑制丘脑底核-SNr回路相关[39]。此外,OX1R和OX2R拮抗剂能发挥与丘脑底核-DBS相似的作用,减轻难治性癫痫的发作:选择性抑制OX1R可显著降低癫痫发作的尖峰频率、振幅和脑电图功率;双重抑制OX1R和OX2R除上述作用外,还能显著延长局灶性癫痫发作和全身性癫痫发作的潜伏期,减少发作次数并延缓发作进展[39,50,52]。由此可见,食欲素受体拮抗剂在抑制癫痫发作活动方面具有潜力,未来可能成为一种有前景的治疗选择。丘脑底核-DBS的作用机制参见图1。

五、丘脑底核-DBS的不良反应
目前关于丘脑底核-DBS治疗癫痫的不良反应报道较少。与装置相关的常见并发症包括DBS植入部位不良反应、植入侧疼痛和感染[53]。例如开机时,刺激发生器植入部位可能出现对侧手臂数分钟刺痛感,或植入部位有刺痛、震动感、双上肢震颤等皮肤感觉异常。研究结果显示,术后5年内,约12.7%的患者发生植入部位感染,9.1%出现植入部位不适感,6.4%出现记忆障碍;其他不良反应还有短暂性失写、眩晕等[54-55]。
一项针对6例难治性癫痫患者的丘脑底核-DBS治疗过程中,5例患者耐受性良好,仅1例出现右臂运动障碍并发症,但可通过调整刺激参数解决[31]。另有报道指出,经过1年随访,丘脑底核-DBS对癫痫发作的治疗作用持久,能显著提高生活质量,且对认知功能无不利影响[24]。相关研究还提到,丘脑底核-DBS治疗癫痫可能出现运动收缩、感觉异常、眼睛偏差等与运动相关的常见并发症,这些可通过调整刺激接触点和刺激参数减轻[40]。总体来看,植入永久性刺激装置的风险较低,刺激相关不良反应与刺激参数和靶点选择有关,且可通过调整参数解决[56-57]。

六、小结与展望
综上所述,丘脑底核-DBS作为一种神经调控疗法,为起源于运动皮质的难治性癫痫患者提供了新的治疗选择。该疗法在长期疗效和安全性方面均有一定优势,但仍存在局限性。因此,未来需开展更多大样本、多中心随机对照临床试验,以积累更多临床证据,为其在癫痫治疗中的应用提供更可靠、更全面的支持。此外,丘脑底核-DBS的抗癫痫机制仍需深入研究,以优化其在癫痫患者中的应用,例如可尝试联合使用食欲素受体拮抗剂与丘脑底核-DBS,以增强治疗效果。同时,探索非侵入性DBS技术,如经颅磁刺激结合其他技术模拟DBS效果,可减少手术创伤和并发症,提高治疗的可及性和安全性。随着成像技术的进步,借助功能磁共振成像等手段能更精准地定位丘脑底核及其亚核结构,实现个性化靶点定位,从而提升治疗效果、减少不良反应。另外,基于生物标志物的反馈系统等闭环装置,已在迷走神经刺激、反应性神经刺激等其他神经调控疗法中被证实有效,但目前丘脑底核-DBS治疗癫痫仍以开环刺激为主,闭环刺激尚未广泛应用。未来需研究最佳脑电图生物标志物,以实现闭环刺激,进而提升治疗的精准性与安全性。
作者贡献声明 孔德明:酝酿、设计、撰写论文;刘家豪、傅如婷、刘媛媛、方立雅、李佳蔚、曾佩:文献收集、分析整理;郭津:研究指导、论文修改、经费支持
利益冲突 作者声明不存在利益冲突
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。





