中国医疗保健国际交流促进会肿瘤内科学分会 中国医师协会肿瘤医师分会
通信作者:石远凯,国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室,北京100021,Email:syuankai@cicams.ac.cn,航天中心医院肿瘤中心,北京100049,Email:shiyuankai@asch.net.cn
基金项目:国家重大新药创制科技重大专项(2017ZX09304015)
实践指南注册:国际实践指南注册与透明化平台(PREPARE-2025CN844)
DOI:10.3760/cma.j.cn112152-20250610-00267
引用本文:中国医疗保健国际交流促进会肿瘤内科学分会,中国医师协会肿瘤医师分会.肺癌脑转移中国治疗指南(2026版)[J].中华肿瘤杂志,2026,48(1):44-78.DOI:10.3760/cma.j.cn112152-20250610-00267.
【摘要】肺癌是中国发病率和死亡率最高的恶性肿瘤。2022年中国肺癌新发病例约106.06万例,死亡约73.33万例。肺癌患者脑转移发生率高、预后差、自然生存期短。近年来,随着外科手术、放射治疗和内科治疗等治疗水平的不断提高,肺癌脑转移患者的治疗选择越来越多,生存时间得以延长。为了及时反映国内外肺癌脑转移治疗的新进展,进一步提高中国肺癌脑转移患者的规范化治疗水平,在《肺癌脑转移中国治疗指南(2021年版)》基础上,中国医疗保健国际交流促进会肿瘤内科学分会和中国医师协会肿瘤医师分会组织专家编写了《肺癌脑转移中国治疗指南(2026版)》,对指南方法学、流行病学数据、临床表现、辅助检查、外科手术治疗、放射治疗、2025年8月31日之前获得中国国家药品监督管理局批准上市的新药、新治疗方案和新适应证等方面进行了系统、全面地更新,增加了治疗推荐意见和推荐级别,涵盖了肺癌脑转移患者诊治过程中常见的临床问题,以便更好地为肺癌脑转移患者的规范化治疗提供帮助。
【关键词】肺肿瘤;脑转移;治疗;指南

原发性肺癌(以下简称肺癌)是中国最常见的恶性肿瘤,根据国家癌症中心2024年发布的统计数据,2022年中国新发肺癌病例约为106.06万例,发病率为75.13/10万,位于恶性肿瘤发病率排名第1位;2022年中国肺癌死亡人数约为73.33万例,死亡率为51.94/10万,位于恶性肿瘤死亡排名第1位[1]。肺癌常见的远处转移部位之一是脑部,肺癌脑转移患者预后差,自然平均生存时间仅1~3个月[2]。外科手术、放射治疗技术和内科治疗的迅速发展为肺癌脑转移患者提供了越来越多的治疗选择,特别是靶向治疗和免疫治疗[3-4]。中国Ⅳ期原发性肺癌的治疗水平在不断提高,改善了肺癌脑转移患者的治疗效果,延长了生存时间,提高了生活质量。为了进一步规范中国肺癌脑转移患者的治疗,在《中国肺癌脑转移诊治专家共识(2017年版)》[5]《肺癌脑转移中国治疗指南(2021年版)》[6]《Ⅳ期原发性肺癌中国治疗指南(2024版)》[7]基础上,中国医疗保健国际交流促进会肿瘤内科学分会和中国医师协会肿瘤医师分会组织专家编写了《肺癌脑转移中国治疗指南(2026版)》,以便更好地为临床应用提供参考。
一、方法学
1.指南专家组构成:本指南专家组成员由来自肿瘤科、肿瘤内科、呼吸与危重症医学科、呼吸内科、胸外科、放疗科、病理科、感染科等科室专家构成。
2.文献检索、文献纳排标准:本指南以“lung cancer”和“brain metastases”为关键词在中国知网、万方数据知识服务平台、Pubmed、American Association for Cancer Research Annual Meeting、American Society of Clinical Oncology Annual Meeting、European Society for Medical Oncology Congress和World Conference on Lung Cancer进行检索,纳入了截至2025年8月31日关于肺癌脑转移的Ⅰ~Ⅲ期临床研究、荟萃分析、病例报告等文献。
3.证据级别和推荐类别标准:本指南的证据级别和推荐类别标准参考美国国家综合癌症网络指南,详见表1。
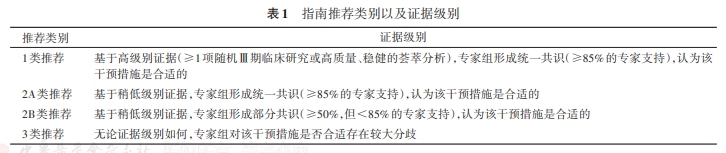
4.指南推荐意见的形成与确定:本指南专家均通过电子邮箱参与共识意见的投票,若超过2/3的专家同意该条推荐意见,则达成共识;对于未达成共识的推荐意见,则根据专家意见修改后进行第2轮专家投票,直到达成共识。
5.指南使用者和目标人群:本指南供中国的肿瘤科医师和涉及肺癌脑转移患者诊疗的相关学科医师参考。
二、流行病学特点
脑转移瘤包括脑实质转移和脑膜转移。脑实质转移瘤最常见的发生部位为大脑半球,其次为小脑和脑干[8]。脑膜转移较脑实质转移少见,但预后更差。近年来,随着肺癌发病率的上升,诊疗技术不断发展,使患者生存时间延长。肺癌脑转移发生率明显高于黑色素瘤、乳腺癌、肾癌及结直肠癌[9],20%~65%的肺癌患者在病程中会发生脑转移,是脑转移性肿瘤中最常见的类型[10-11]。各组织学类型肺癌脑转移的发生率存在差异,美国国立癌症研究所监测、流行病学和最终结果数据库的一项长期随访结果显示,在非转移性非小细胞肺癌(non-small cell lung cancer,NSCLC)中,肺腺癌、鳞癌和大细胞癌发生脑转移的风险分别为11%、6%和12%[12]。小细胞肺癌(small cell lung cancer,SCLC)患者首次就诊时脑转移的发生率为10%[13],诊疗过程中脑转移的发生率为40%~60%[14-15],是影响SCLC患者生存和生活质量的重要因素之一。
三、临床表现
肺癌脑实质转移和脑膜转移临床表现有共性,又各有特点。
(一)脑实质转移
脑实质转移瘤的临床表现主要包括共性的颅内压增高、特异性的局灶性症状和体征。
1.颅内压增高:颅内压增高的症状和体征主要表现为头痛、呕吐和视神经乳头水肿。头痛多为持续性钝痛,晨起加重,咳嗽、弯腰或体位改变时加剧。呕吐呈喷射状,呕吐后头痛可暂时缓解。眼底检查可见视神经乳头水肿,可伴随视力模糊、视野缺损等。除这3个主要症状外,还可出现复视、黑朦、视力减退、头晕、淡漠、意识障碍、认知障碍、二便失禁、脉搏徐缓和血压增高等征象。上述症状常呈进行性加重,当转移瘤囊性变或瘤内卒中时可出现急性颅内压增高症状。严重时出现意识障碍、嗜睡、反应迟钝甚至昏迷。
2.局灶性症状和体征:大脑半球功能区附近的转移瘤早期可出现局部刺激症状,晚期则出现神经功能破坏性症状,且不同部位肿瘤可产生不同的定位症状和体征。(1)认知与精神症状:常见于额叶或颞叶肿瘤,可表现为认知功能下降、记忆力减退、注意力不集中、执行力差、性情改变、反应迟钝、痴呆等,精神行为异常,如情绪波动、抑郁、焦虑、人格改变、幻觉或妄想等;(2)癫痫发作:额叶肿瘤较多见,其次为颞叶、顶叶肿瘤,可为全身阵挛性大发作或局限性发作;(3)感觉障碍:为顶叶转移瘤的常见症状,表现为两点辨别觉、实体觉及对侧肢体的位置觉障碍;(4)运动障碍:表现为肿瘤对侧肢体肌力减弱或完全性上运动神经元瘫痪;(5)失语症:见于优势大脑半球语言中枢区转移瘤,可表现为运动性失语、感觉性失语、混合性失语和命名性失语等;(6)视野损害:枕叶和顶叶、颞叶深部肿瘤因累及视辐射而引起对侧同象限性视野缺损或对侧同向性偏盲;(7)丘脑转移瘤可产生丘脑综合征,主要表现为对侧感觉缺失和/或刺激症状,对侧不自主运动,并可有情感和记忆障碍;(8)垂体或下丘脑转移相关症状,主要表现为内分泌紊乱,如尿崩症、性功能减退、体温调节异常等。
小脑转移瘤的临床表现:(1)小脑半球肿瘤:可出现爆破性语言、眼球震颤、患侧肢体协调动作障碍、同侧肌张力减低、腱反射迟钝、易向患侧倾倒等;(2)小脑蚓部肿瘤:主要表现为步态不稳、行走困难、站立时向后倾倒;(3)肿瘤阻塞第四脑室的早期即出现脑积水和颅内压增高表现。
脑干转移瘤大都出现交叉性瘫痪,即病灶侧脑神经周围性瘫痪、对侧肢体中枢性瘫痪和感觉障碍。根据受损脑神经可定位转移瘤的位置,如第Ⅲ对脑神经麻痹则肿瘤位于中脑;第Ⅴ、Ⅵ、Ⅶ、Ⅷ对脑神经麻痹则肿瘤位居脑桥;第Ⅸ、Ⅹ、Ⅺ、Ⅻ对脑神经麻痹则肿瘤侵犯延髓。
(二)脑膜转移[16-20]
脑膜转移患者的临床表现常因肿瘤细胞侵犯部位不同而复杂多样,缺乏特异性,有时很难与脑实质转移引起的症状和治疗原发肿瘤出现的不良反应相鉴别;部分患者因颈肩部疼痛进行性加重而被确诊为脑膜转移。
脑膜转移的主要临床表现有:(1)脑实质受累及脑膜刺激表现:头痛、呕吐、颈项强直、脑膜刺激征、精神状态改变、意识朦胧、认知障碍、癫痫发作和肢体活动障碍等;(2)颅神经受累表现:常见的受累脑神经有视神经、动眼神经、滑车神经、外展神经、面神经、听神经等,表现为视力下降、复视、面部麻木、味觉和听觉异常、吞咽和发音困难等;(3)颅内压增高表现(头痛、呕吐、视乳头水肿)和脑积水压迫脑组织引起的进行性脑功能障碍表现(智力障碍、步行障碍、尿失禁)等;(4)若同时伴有脊膜播散则可出现脊髓和脊神经根刺激表现,如神经根性疼痛、节段性感觉缺损、肢体麻木、感觉性共济失调、腱反射减弱或消失、括约肌功能障碍等,这些有助于脑膜转移的诊断。
(三)急性并发症
1.脑疝:(1)小脑幕切迹疝:意识障碍加重、昏迷、瞳孔不等大、对侧肢体偏瘫等。(2)枕骨大孔疝:突发呼吸骤停、昏迷。
2.肿瘤卒中:肿瘤出血或坏死可导致急性神经功能严重损伤、病情急剧恶化。
四、辅助检查
(一)头颅MRI
在无禁忌证的前提下,MRI是诊断肺癌脑转移的首选影像学检查方法。常规扫描序列包括:T1加权成像(T1-weighted imaging,T1WI)、T2加权成像(T2-weighted imaging,T2WI)或液体衰减反转恢复序列(fluidattenuated inversion recovery,FLAIR)、扩散加权成像(diffusion weighted imaging,DWI)及T1WI增强序列。对于临床怀疑脑膜转移的患者,在常规FLAIR与增强扫描基础上增加黑血技术更利于观察。
1.脑实质转移瘤MRI表现:约80%的脑实质转移发生于大脑半球,15%发生于小脑半球,脑干受累者约5%[21]。瘤细胞主要经血行播散,灰白质交界区因血管管径变细造成肿瘤栓子易于滞留,故易形成转移灶,是转移瘤最常发生的部位,且以多发转移常见。典型脑实质转移瘤MRI表现为圆形或类圆形、边界清楚,大小不一,平扫T1WI多为稍低信号或等信号,当病灶内伴出血时可表现为高信号,T2WI或FLAIR序列多为稍高信号,也可为等信号,DWI序列呈等或稍高信号,增强扫描呈明显强化,随着转移瘤增大,病灶中心常见无强化坏死区。瘤周伴程度不等的水肿带,T2WI或FLAIR序列易于观察水肿情况。转移瘤伴随的脑水肿常是引起临床症状的主要原因。当水肿明显时,需注意观察周围组织受压、中线移位,以及有无脑疝等需临床紧急处理的情况。
较大的单发脑实质转移需与原发性脑肿瘤如高级别胶质瘤、脑膜瘤等进行鉴别。高级别胶质瘤相较于转移瘤发病年龄较轻,症状出现时间相对较长,因其浸润性生长的特性,MRI表现为边界不清,可跨叶或跨裂生长,呈不均匀明显强化,可与转移瘤进行鉴别;脑膜瘤发生于颅内邻近脑膜部位,宽基与脑膜贴邻,边界清楚。与转移瘤相比,脑膜瘤信号均匀,少有坏死,T1WI与T2WI以近等信号多见,呈均匀明显强化,可伴“脑膜尾征”。
多发性转移瘤需与淋巴瘤、脑脓肿等进行鉴别。脑淋巴瘤以近中线位置多见,常呈均匀明显强化,形态不规则,表现为“梳齿征”、“脐凹征”、“握雪征”等,DWI呈明显高信号、对应表观弥散系数值减低是其重要特征之一。脑脓肿多表现为环形强化,且强化的脓肿壁厚度均匀,内部坏死在DWI呈明显高信号为其特征性表现,同时结合临床有无感染指标有利于鉴别诊断。
2.脑膜转移MRI表现:脑膜转移根据受累部位不同分为硬脑膜转移及柔脑膜转移,以柔脑膜转移最常见,后者包括软脑膜及蛛网膜转移、蛛网膜下腔转移及脑室转移。硬脑膜转移可因颅骨转移累及硬脑膜或血行转移所致。FLAIR序列表现为颅骨下方、大脑镰或小脑幕的条带状高信号影,不延伸至脑沟内,增强扫描呈明显强化。以软脑膜及蛛网膜受累为主的柔脑膜转移,在FLAIR序列表现为沿脑沟走行的多发条线样高信号或类结节影,增强扫描呈明显强化。脑室转移相对少见,多同时伴软脑膜及蛛网膜转移,表现为沿脑室壁的条带状、结节状异常信号及明显强化,脑室系统可不同程度扩张,脑室压力增高可同时继发脑室旁间质性脑水肿。在常规FLAIR与增强扫描基础上增加黑血技术,从而抑制血管与静脉窦的高信号,更利于观察脑膜转移的情况。需要注意的是,MRI表现为脑膜转移时,腰穿脑脊液检查可以为阴性;同样,脑脊液检查阳性时,MRI也可受颅内高压的影响表现为假阴性,此时需结合临床综合考虑。
脑膜转移需与脑梗塞、脑膜炎等疾病进行鉴别。脑梗塞多急性起病,沿脑血管供血区分布,亚急性或慢性脑梗塞由于血管壁损伤或侧支循环建立,在增强MRI出现沿脑回走行的强化带,此时需与脑膜转移进行鉴别。脑梗塞导致相应脑实质出现异常信号,DWI呈明显高信号是重要的鉴别点。脑膜炎多发病年龄较轻,因感染微生物的病种不同呈现不同的临床与影像特征。
(二)头颅CT
头颅CT是肺癌脑转移诊断和评估的基础且重要的影像学手段。平扫脑转移瘤多表现为等或低密度灶,少数可表现为高密度(如出血性或钙化性转移);增强扫描病灶多呈环形或结节状明显强化,周围常伴低密度水肿带,小强化结节伴大范围水肿带引起的占位效应是脑转移瘤的特征性CT影像表现。CT凭借其快速成像能力(摆位+扫描通常<5min)、广泛普及性及对急性出血、钙化的高敏感性,成为临床实践中不可替代的辅助评价工具,尤其在急诊评价(如疑似脑疝、急性颅内压增高)或存在MRI禁忌证(如金属植入物、幽闭恐惧症)时具有重要价值。
在肺癌脑转移全程管理中,CT的应用贯穿多个环节:初诊筛查可快速识别颅内占位及其并发症(如出血、脑积水);治疗过程中可用于监测内科治疗或放疗后病灶体积变化及水肿缓解情况;随诊阶段则能动态追踪术后或放疗后并发症(如放射性坏死、出血)。需要注意的是CT评价脑转移瘤具有局限性,对微小转移灶(<5mm)或脑膜转移的敏感性低于MRI,特别是CT平扫较难发现微小转移瘤,因此在条件允许时仍需结合MRI进一步评价,以实现更精准的诊疗决策。
(三)正电子发射断层成像-计算机断层扫描(positron emission tomography-computed tomography,PET-CT)
PET-CT最常用的显像剂为18F-脱氧葡萄糖(18F-fluorodeoxyglucose,18F-FDG),恶性肿瘤细胞由于大量摄取18F-FDG,表现为对18F-FDG的高摄取,因此PET-CT能够区分肿瘤和正常组织的代谢差异,有助于肿瘤的定性诊断,对多数转移灶的检测优于CT。但是由于正常脑组织对18F-FDG亦呈高摄取,所以18F-FDGPET-CT对脑转移瘤、尤其是小的或低代谢的脑转移灶以及脑膜转移不敏感,应该结合头颅MRI(首选)或增强CT扫描增加检出率。近年来随着11C-蛋氨酸、成纤维细胞活化蛋白抑制剂等新型肿瘤PET-CT显像剂的出现,提高了PET-CT对于肺癌脑转移的检出率。
(四)腰椎穿刺和脑脊液检查
腰椎穿刺可测量脑脊液压力,收集脑脊液并进行脑脊液常规、生化和细胞病理学检查,脑转移尤其是脑膜转移的患者可以出现脑脊液压力增高、蛋白含量增高。如细胞学检查发现肿瘤细胞可明确诊断。
(五)血清肿瘤标志物
肺癌相关的血清肿瘤标志物包括癌胚抗原、细胞角蛋白片段19、鳞状上皮细胞癌抗原等。SCLC具有神经内分泌特征,可以有促胃泌素释放肽前体、神经元特异性烯醇化酶、肌酸激酶BB以及嗜铬蛋白A等异常升高。上述肺癌相关的血清肿瘤标志物可以作为监测疗效和病情变化的辅助指标。
(六)分子病理检测
对于腺癌或含有腺癌成分的其他类型肺癌,应该在进行病理诊断的同时常规进行表皮生长因子受体(epidermal growth factor receptor,EGFR)基因突变、间变性淋巴瘤激酶(anaplastic lymphoma kinase,ALK)融合基因、ROS1融合基因、KRAS基因突变、BRAF基因V600E突变、人表皮生长因子受体2(human epidermal growth factor receptor-2,HER-2)基因突变、MET基因14号外显子跳跃缺失突变及MET基因扩增、NTRK融合基因、RET融合基因检测,进行程序性死亡受体配体1(programmed cell death-ligand 1,PD-L1)蛋白表达、HER-2蛋白表达等免疫组织化学检测。脑脊液标本经细胞病理学诊断后,如查见肿瘤细胞,可以应用脑脊液标本中肿瘤细胞和/或无细胞脑脊液上清作为基因检测的标本[22]。
五、治疗
(一)治疗原则
肺癌脑转移患者的治疗应该在全身治疗基础上进行针对脑转移的治疗,包括外科手术、全脑放疗(whole brain radiotherapy,WBRT)、立体定向放疗(stereotactic radiotherapy,SRT)和内科治疗在内的多学科综合治疗,其目的是控制转移病灶、改善患者症状和生活质量,最大程度地延长患者生存时间。
1.NSCLC患者脑转移的治疗:对于无症状脑转移患者,可以先行全身治疗,需要根据患者病理类型、驱动基因变异情况、PD-L1表达水平及全身状况选择合适的治疗方案。对于驱动基因阳性患者,选择对应的靶向药物。发生靶向药物耐药后需要根据耐药机制选择后线治疗方案,优先选择血脑屏障渗透率高的药物。对于驱动基因阴性或变异情况不明的患者,需要根据PD-L1表达状态分层治疗,若无程序性死亡受体1(programmed cell death protein 1,PD-1)/PD-L1单抗治疗禁忌,一线推荐PD-1/PD-L1单抗联合含铂双药方案治疗。对于无法一线应用PD-1/PD-L1单抗的患者,应当采用含铂双药方案化疗;合适的患者还可联合贝伐珠单抗或重组人血管内皮抑素治疗(非鳞状NSCLC)。对于不适合铂类药物治疗的患者,可考虑非铂方案化疗。一线治疗结束时无进展的非鳞状NSCLC患者可以考虑培美曲塞±贝伐珠单抗维持治疗。一线联合免疫治疗的患者,也可考虑免疫维持治疗。一线治疗进展的患者,后线治疗需要根据一线治疗方案和患者全身状况充分权衡治疗利弊,选择无交叉耐药的方案,详见《Ⅳ期原发性肺癌中国治疗指南(2026版)》[23]。
对于有症状脑转移而颅外病灶稳定的NSCLC患者,应该积极行局部治疗,详见“外科手术治疗”和“放射治疗”部分。
2.SCLC患者脑转移的治疗:对于初治无症状的SCLC脑转移患者,可先行全身化疗后再行WBRT;对于有症状的SCLC脑转移患者,应该积极行WBRT。对于脑转移灶较少的患者,应该在充分权衡利弊后决定是否选择SRT。对于既往接受过全脑预防照射后出现脑转移的患者,经严格放疗剂量评估后,弥漫性脑转移的患者可考虑再次WBRT,寡进展患者优先选择SRT。
(二)外科手术治疗
推荐意见1:肺癌脑转移瘤患者是否适合手术切除需考虑组织学类型、肿瘤个数、肿瘤大小、肿瘤部位、患者全身状况等,以上因素要单独评估,但手术选择应该整合所有因素、综合权衡。值得注意的是,肺癌脑转移的患者都是Ⅳ期患者,手术选择应该谨慎(1级推荐)。
与内科治疗和放疗相比,外科手术具有如下优点:(1)全部切除转移瘤可以迅速缓解颅内高压症状,消除转移灶对周围脑组织的刺激;(2)获得肿瘤组织,从而明确组织病理和分子病理诊断;(3)手术能通过切除全部肿瘤达到局部治愈。
1.外科手术适应证
(1)活检术:明确组织病理和分子病理诊断,以指导下一步治疗。①肺原发灶隐匿或虽然原发灶明确但取材困难;②肺原发灶病理明确,但脑部病变不典型或难于诊断;③明确是肿瘤坏死或复发,评价前期放疗或内科治疗效果。
(2)手术切除:①脑内单发、部位适合、易于切除,且肿瘤或其水肿占位效应重或导致脑积水的患者适合外科手术切除。虽然为单发转移灶但对放、化疗敏感的病理类型,如SCLC等可不首选手术,但下列情况除外:转移瘤和(或)水肿体积大、颅内压失代偿、肿瘤卒中等濒临脑疝、危及生命者应该急诊手术,为下一步放疗或内科治疗争取时间和空间。②多发脑转移瘤手术治疗目前尚存在争议,但一般认为:如果转移瘤病灶数目≤3个,并且手术能够完全切除,则与单发脑转移瘤患者行外科手术切除一样也能获得满意的治疗效果。>3个脑转移病灶治疗应该首选WBRT或SRT,但如果出现肿瘤卒中、梗阻性脑积水等危及生命的情况时,应该进行手术减压。③肿瘤大小:肿瘤最大径>3cm者,一般不适合放射治疗,宜首选手术;肿瘤最大径<5mm,尤其位于脑深部(丘脑、脑干等)宜首选放疗或内科治疗;如果肿瘤最大径为1~3cm,则根据患者全身状况、手术风险等综合评估后,再决定首选手术还是其他治疗手段。④肿瘤部位:尽管目前借助神经导航、术中功能定位等技术,神经外科医师的技术可以到达颅内任何一个部位,但脑深部或功能区转移瘤手术的致残率总体上较浅表或非功能区的手术致残率高。因此,对位于脑干、丘脑、基底节的脑转移瘤,原则上不首选外科手术治疗。
2.外科手术方法
(1)手术辅助技术:目前,多模态神经影像技术、神经导航、术中超声以及术中电生理监测等辅助措施能最大限度地减少手术副损伤,对功能区转移瘤手术十分重要。
(2)手术入路:①大脑皮质下转移瘤:经皮质入路,环形切开肿瘤表面薄层脑组织,全切肿瘤。但是如果肿瘤位居功能区,则严禁此术式,应该在肿瘤表面皮质或脑沟进行纵向切口,先瘤内分块切除,再全切肿瘤,尽量减少手术对瘤周脑组织的损伤。②位于脑沟两侧或脑沟深部的转移瘤:经脑沟入路,分开脑沟,在其侧面或底部切除肿瘤。③脑白质深部转移瘤,可经皮质或经脑沟入路切除。④岛叶转移瘤应该分开侧裂切除肿瘤。⑤中线部位转移瘤最好经纵裂入路切除。⑥脑室肿瘤可以经胼胝体或皮层入路切除。⑦小脑转移瘤切除以最短的经小脑实质径路为佳。
(3)对于脑膜转移的患者:可植入Ommaya储液囊行脑室内化疗。对合并交通性脑积水的患者可行脑室-腹腔分流术以降低颅内压、缓解症状,但脑室-腹腔分流术可能增加肿瘤腹腔转移的机会,宜审慎取舍。
(4)复发脑转移瘤的再次手术:脑转移瘤术后复发有两种情况:手术残留、肿瘤在原位复发和原发部位以外的新发脑转移瘤,如经肿瘤个数、全身状况等因素整体评估后适合手术,则再次手术能够改善患者的生活质量和预后。
3.手术治疗新进展
(1)激光间质热疗:MRI引导的激光消融技术能精准摧毁病灶,适用于深部或常规手术难以到达的病灶。
(2)术中导航与影像技术:术中实时MRI/CT导航确保病灶被精准、完全切除,消灭残留。
(3)机器人辅助手术:机器人系统如机器人无框架立体定向手术辅助系统可以提高手术精度,减少并发症。
(4)荧光引导手术:用荧光素钠或5-氨基乙酰丙酸(5-ALA)标记肿瘤边界,提高完整切除率。
(三)放射治疗
肺癌脑转移瘤的放疗需要综合考虑肿瘤的病理类型、数量、大小、位置以及患者全身状况等因素来综合制定最优方案。卡氏评分(Karnofsky performance status,KPS)<50分或<70分且无全身治疗选择的脑转移患者,不会从放疗中获益[24]。随机对照研究结果显示,分级预后评估(graded prognostic assessment,GPA)评分<2.5分,或预期生存<3个月的患者,脑部放疗对比最佳支持治疗未能带来生存获益[25]。
1.NSCLC脑转移患者的放疗
推荐意见2:对于脑转移灶数量≤4个的NSCLC患者,脑部放疗首选SRT(1类推荐);对于脑转移灶数量>4个的NSCLC患者,目前最佳放疗方案仍有争议,需结合患者情况充分权衡;对于接受脑转移瘤切除术后的患者,推荐行SRT(1类推荐)。
(1)脑转移病灶数量≤4个的放疗:SRT凭借精准定位、高剂量聚焦以及对周围正常组织损伤小的优势,成为治疗≤4个脑转移瘤的首选手段。SRT包括单次立体定向放射外科治疗(stereotactic radiosurgery,SRS)、分次立体定向放射治疗(fractionated stereotactic radiotherapy,FSRT)和大分割立体定向放射治疗(hypofractionated stereotactic radiotherapy,HSRT)。多项研究结果显示,对≤4个脑转移瘤进行单纯SRT,相较于单独WBRT具有生存优势,能够显著提高局部控制率,同时更好地保护神经认知功能[26-27]。多项随机对照研究在主要纳入了1~4个脑转移瘤的患者中,对比了使用WBRT联合SRS与单独使用SRS在脑转移瘤(包括NSCLC)的疗效,结果显示,尽管WBRT联合SRS可以改善颅内疾病控制率(intracranial disease control rate,iDCR),但并未改善生存率[28-30]。对于远离重要脑组织结构的转移灶,推荐依据病灶长径制定SRS放疗剂量。RTOG90-05研究确立了不同长径肿瘤的单次SRS耐受剂量:≤2cm为24Gy,2.1~3cm为18Gy,3.1~4cm为15Gy[31]。对于接受>12Gy单次分割SRS,V12Gy>5cm3、>10cm3或>15cm3时引起症状性放射性坏死的风险分别约为10%、15%和20%,建议将SRS的V12Gy限制在10cm3以内[32]。对于较大体积脑转移病灶(长径3.1~4cm),单次SRS治疗不良反应明显增加,容易导致放射性坏死,并且难以获得良好的局部控制效果,因此也可以采用FSRT,剂量建议27Gy/3次或30Gy/5次[33]。对于难治性脑转移灶,包括长径>4cm的转移瘤、位于关键结构(如脑干、视神经、视交叉和内囊)之内或附近、WBRT后出现的多个复发或进展病灶等,利用HSRT治疗不仅可以保证肿瘤局部控制率,还可以减少治疗相关不良反应[34],单次剂量建议3.5~4Gy,在保证正常组织限制剂量的同时总剂量达到52.5~60Gy;必要时可以采用分段治疗模式,通过HSRT给予40~50Gy剂量后休息1~2个月,待肿瘤缩小后再进行补量[35]。
(2)脑转移病灶数量>4个的放疗:超过4个脑转移灶患者的最佳放疗方案仍有争议[36]。WBRT作为基础方案,常用剂量为30Gy/10次、37.5Gy/15次或40Gy/20次[37-38]。20Gy/5次短疗程方案仅限于预后较差、老年患者(>75岁)或体能状态不佳的患者(KPS评分<70分)。不建议在初诊未行全身治疗前行脑转移病灶的放疗,原因是全身治疗可能对脑转移病灶同样敏感,放疗对生存期较长的患者可能带来较重的远期不良反应[39]。采用海马保护性全脑放疗(hippocampal avoidance whole brain radiotherapy,HA-WBRT)联合美金刚已经成为降低神经不良反应的重要治疗策略[40]。在多项探索HA-WBRT的研究中,当转移灶距海马≥5mm时,采用调强放射治疗或者螺旋断层调强技术,将海马区最大剂量限制在9~16Gy,可以降低神经认知功能下降的发生率,并且治疗后海马区出现转移的概率仅为1.4%~4.5%[41-44]。NRGCC001研究结果显示,接受HA-WBRT+美金刚治疗组较传统WBRT+美金刚组认知障碍发生率降低26%(P<0.01),并且在生存期≥4个月或基线认知功能较好的亚组中获益更显著[45-46]。
近年来的研究结果显示,SRT在多发转移灶中的应用获益显著。针对4~10个脑转移灶的前瞻性研究结果显示,SRT组较WBRT组显著延长颅内无进展生存时间(intracranial progression free survival,iPFS)和总生存时间(overall survival,OS),并且未观察到Ⅲ级不良反应[47];对于4~10个脑转移灶以及肿瘤体积<15ml的脑转移瘤患者,可考虑优先采用SRS治疗[36,48]。长期随访结果显示,即使脑转移灶≥10个,SRT仍然可以达到与总体积类似的单发灶的生存获益(中位OS:15~19.2个月对比12个月,P=0.3),并且不良反应无明显增加[49-50],提示脑转移病灶体积参数可能较数量更具预后指导价值。
WBRT仅能延缓新发病灶出现0.5~1年,30%~50%患者治疗后出现颅内进展,约半数多发脑转移患者最终仍需挽救性治疗[51]。即使采用HA-WBRT联合治疗,仍有患者在6个月后出现认知功能下降,因此对预期生存期较长者应该考虑推迟WBRT而将其作为挽救治疗手段[52]。对于随诊方便的患者,推荐优先采用SRT,延迟采用WBRT的策略。接受单纯SRT的患者颅内远处失败率高于WBRT,所以对多发性脑转移瘤患者在进行初程SRT后需要进行密切随诊,一般2~3个月复查1次,监测颅内新发病灶。
WBRT同步加量(simultaneous integrated boost,SIB)技术整合了全脑控制与局部强化的优势,在给予全脑30~40Gy常规剂量的同时对转移灶同步加量至50~60Gy。回顾性研究结果显示,对于多发脑转移患者,该方案较单独WBRT显著提升局部控制率,并且患者可以耐受[53-54];与SRS相比,WBRT+SIB的中位iPFS延长8个月(20和12个月,P=0.0069),但是OS相近(32和28个月,P=0.195),适用于无法进行SRT而预期生存期较长的多发脑转移患者[55]。HA-WBRT+SIB方案在多项研究中展现出双重优势:神经认知损伤发生率较传统WBRT降低,同时提高iDCR、延长OS[56-57]。
(3)术后放疗:对于接受手术切除的脑转移瘤患者,术后辅助放疗是降低复发风险的关键措施。基于颅内肿瘤难以完整切除的特性,单纯手术切除后局部复发风险高,1~2年复发率可达50%,因此推荐所有脑转移瘤切除术后的患者接受放射治疗,尤其对于体能状态良好和颅外疾病控制良好的患者[58]。前瞻性研究结果显示,针对孤立性脑转移病灶最大径<5cm的患者,术后SRT组神经认知功能恶化速度较WBRT组明显减缓,6个月的认知功能障碍发生率降低33.6%(85%对比52%,P<0.00031)[59]。因此,SRS已经被确立为术后首选放疗模式。对于瘤腔较大的脑转移瘤,大分割立体定向放疗可能更具优势。根据瘤腔体积制定SRT放疗剂量,常用剂量分割方案为:单次照射:12~20Gy/1次、24~27Gy/3次、30Gy/5次[60]。
2.SCLC脑转移患者的放疗
推荐意见3:对于SCLC伴脑转移患者,推荐进行WBRT,并且进行海马区保护(1类推荐)。对于脑转移灶数量较少的患者,SRT存在争议,需要结合患者具体情况充分权衡后再做决定。
SCLC具有高度侵袭性,早期即可发生隐匿性脑微转移,因此WBRT是SCLC脑转移的标准治疗,即使影像学显示脑转移灶数量较少也倾向于选择WBRT,旨在覆盖潜在微转移并预防新发病灶。WBRT推荐剂量同NSCLC,建议采用HA-WBRT技术(海马区5mm范围内有转移灶、有脑膜转移等高风险特征者除外),并且在放疗期间及结束后加用美金刚。SCLC患者的SRT治疗,最主要的担忧是如果省略WBRT会增加颅内复发风险并且降低OS率。但是,近期多项研究结果显示,对于转移灶数量较少的患者SRT可能是更合适的选择[61-63]。正在进行的NRGCC009研究比较SRT与HA-WBRT联合美金刚在此类患者中的疗效。对于预防性WBRT后出现弥漫性脑转移的患者,在进行严格的剂量评估后可以考虑再次进行WBRT,而对于出现寡进展的患者则优先选择SRT。
(四)内科治疗
1.NSCLC脑转移患者的化疗
推荐意见4:非鳞状NSCLC脑转移患者的全身化疗方案以培美曲塞和铂类为基础。替莫唑胺也可以作为NSCLC脑转移患者全身化疗的药物选择(3类推荐)。
尽管传统观点认为,化疗药物由于分子量较大、携带电荷并且容易与白蛋白结合,因此很难穿透血脑屏障对颅内转移病灶发挥抗肿瘤作用[64-65],但化疗仍然是NSCLC脑转移患者重要且不可或缺的综合治疗手段。以顺铂、卡铂为主的铂类药物为基础,联合培美曲塞可以给NSCLC脑转移患者带来生存获益[66-68]。
培美曲塞在非鳞状NSCLC中有良好的抗肿瘤活性,是非鳞状NSCLC患者一线治疗和维持治疗的重要药物。培美曲塞联合铂类对NSCLC脑转移患者的颅内病灶也有控制作用,化疗组患者的OS明显长于自然生存时间。GFPC07-01研究纳入初治的NSCLC脑转移患者,应用标准剂量顺铂联合培美曲塞方案化疗6周期,化疗结束或者脑转移进展时进行WBRT治疗,颅内客观缓解率(intracranial objective response rate,iORR)为41.9%,颅外病灶的客观缓解率(objective response rate,ORR)为34.9%,中位OS为7.4个月[67]。培美曲塞可以成为NSCLC脑转移患者一个有效的治疗选择[68-69]。替莫唑胺是一种新型咪唑四嗪类烷化剂,可在人体内转化成有活性的烷化剂前体,能透过血脑屏障,对于控制NSCLC脑转移有较好的疗效。对于既往接受过WBRT或全身化疗的NSCLC脑转移患者,可以应用替莫唑胺以延长OS[70]。替莫唑胺单药或联合其他化疗药物与WBRT序贯或同步应用,尤其是同步应用,可以提高iDCR。目前多为Ⅱ期临床研究,结果显示,替莫唑胺在NSCLC脑转移患者的治疗中安全、有效,但由于样本量较少,尚需大规模的Ⅲ期研究进一步证实[71-72]。
2.SCLC脑转移患者的化疗
推荐意见5:SCLC脑转移患者的全身化疗方案首选以铂类、依托泊苷、伊立替康和拓扑替康为基础的药物(3类推荐)。
化疗是SCLC脑转移患者综合治疗的一种有效手段。铂类联合依托泊苷或伊立替康双药方案是SCLC患者的标准一线全身化疗方案,对颅内转移病灶也有一定疗效。对于基线伴脑转移的SCLC患者,伊立替康联合卡铂化疗的iORR为65%[73]。依托泊苷联合顺铂化疗的iORR为30%[74]。因此,对广泛期SCLC伴有无症状脑转移患者,一线治疗可优先考虑全身化疗,在全身化疗结束后或脑转移进展时再考虑WBRT。Ⅱ期临床研究结果显示,拓扑替康二线治疗SCLC脑转移患者的iORR为33%[75]。
3.鞘内注射
推荐意见6:对于脑膜转移且经全身治疗后无法有效控制的患者,培美曲塞鞘内注射可以作为一种治疗选择(3类推荐)。
鞘内注射化疗是将药物直接注入蛛网膜下腔,提高脑脊液内药物浓度,从而杀伤肿瘤细胞。给药途径包括:经腰椎穿刺蛛网膜下腔注射化疗药物和经Ommaya储液囊行脑室内化疗。与经腰椎穿刺鞘注给药相比,经Ommaya储液囊给药安全性更好,可以避免鞘注误将药物注射到硬膜外间隙的风险;对于伴有血小板减少症的患者,可以避免硬膜外和硬膜下血肿的发生[76]。鞘内注射常用的化疗药物包括:培美曲塞、甲氨蝶呤、阿糖胞苷和塞替派。鞘内注射化疗药物同时给予糖皮质激素可减轻化疗药物的神经不良反应、缓解症状[77-78]。腰椎穿刺时行脑脊液常规、生化及细胞学检查有助于监测疗效并且指导治疗。鞘内化疗是NSCLC脑膜转移的重要治疗手段,Ⅱ期临床研究结果显示,鞘内注射培美曲塞治疗伴有脑膜转移、EGFR-TKI耐药NSCLC患者的iORR为80.3%和84.6%,中位OS为12和9个月[79-80]。回顾性研究结果显示,鞘内注射培美曲塞治疗108例肺癌脑膜转移患者的中位OS为14个月,56例患者出现神经系统症状好转。KPS评分>60分、接受EGFR-TKI治疗是OS的独立预后保护因素;合并脑实质转移是OS的独立危险因素[81]。对于脑实质转移,目前尚无明确支持证据。
4.分子靶向治疗
近年来多项临床研究结果显示,分子靶向药物为驱动基因变异阳性NSCLC脑转移患者提供了新的有效的治疗选择。
推荐意见7:对于EGFR-TKI初治NSCLC脑转移患者,优先推荐佐利替尼(1类推荐)、埃克替尼(1类推荐)、奥希替尼(2A类推荐)、阿美替尼(2A类推荐)、伏美替尼(2A类推荐)、贝福替尼(2A类推荐)、瑞齐替尼(2A类推荐)、瑞厄替尼(2A类推荐)、利厄替尼(2A类推荐)、奥希替尼+化疗(2A类推荐)、阿美替尼+化疗(2A类推荐)、埃万妥单抗+兰泽替尼(2A类推荐);对于EGFR-TKI经治并伴有EGFRT790M突变的NSCLC脑转移患者,优先推荐奥希替尼(2A类推荐)、阿美替尼(3类推荐)、伏美替尼(3类推荐)、贝福替尼(3类推荐)、瑞齐替尼(3类推荐)、瑞厄替尼(3类推荐)、利厄替尼(3类推荐)。
(1)EGFR-TKI:亚洲晚期肺腺癌EGFR基因敏感突变发生率为46.3%[82]。中国晚期肺腺癌EGFR基因敏感突变发生率为46.7%[83]。第一代EGFR-TKI包括吉非替尼、厄洛替尼、埃克替尼和佐利替尼。吉非替尼或厄洛替尼用于EGFR基因敏感突变阳性NSCLC脑转移患者的疗效数据多来源于回顾性研究、Ⅱ期临床研究或与其他药物对比的Ⅲ期临床研究中脑转移患者的亚组分析结果,不同研究间的iORR差异较大,吉非替尼的iORR为63%~87.8%[84-89];厄洛替尼的iORR为68.2%[90]。BRAIN研究是埃克替尼对比WBRT±化疗分别用于NSCLC脑转移患者的Ⅲ期随机对照临床研究,研究结果显示,埃克替尼显著提高了EGFR基因敏感突变阳性晚期NSCLC脑转移患者的iORR(分别为65%和37%,P=0.001)和中位iPFS(分别为10和4.8个月,HR=0.56,P=0.014)[91]。
第二代EGFR-TKI包括阿法替尼和达可替尼,在EGFR基因敏感突变阳性NSCLC脑转移患者的颅内疗效数据均较少。阿法替尼后线治疗EGFR基因敏感突变阳性NSCLC脑转移患者的iORR为35%(11/31)[92]。阿法替尼一线治疗EGFR基因敏感突变阳性NSCLC脑转移患者的iORR为72.9%[90]。LUX-Lung7研究的脑转移患者亚组分析结果显示,阿法替尼对比吉非替尼分别治疗基线伴脑转移的EGFR基因敏感突变阳性NSCLC患者的OS差异无统计学意义[93]。ARCHER1050研究中未纳入脑转移患者,达可替尼治疗NSCLC脑转移患者的研究多为小样本回顾性研究或Ⅱ期临床研究,达可替尼一线治疗EGFR敏感突变阳性NSCLC脑转移患者的iORR为85.7%和87.5%[94-95]。
第三代EGFR-TKI包括奥希替尼、阿美替尼、伏美替尼、贝福替尼、瑞齐替尼、瑞厄替尼和利厄替尼,其在控制NSCLC患者脑转移病灶方面均显示出较好的疗效。FLAURA研究中脑转移亚组患者的事后分析结果显示,奥希替尼较吉非替尼或厄洛替尼一线治疗EGFR基因敏感突变阳性NSCLC脑转移患者可显著延长中位iPFS(分别为未达到和13.8个月,HR=0.48,P=0.014),iORR分别为91%(20/22)和68%(13/19;OR=4.6,P=0.066)[96]。FLAURA2研究中脑转移亚组患者的事后分析结果显示,奥希替尼联合培美曲塞和铂类较奥希替尼单药一线治疗EGFR基因敏感突变阳性NSCLC脑转移患者可显著延长中位iPFS(分别为未达到和17.3个月,HR=0.40,P=0.0157),iORR分别为88%(35/78)和87%(33/78;OR=1.06,P=0.9308)[97]。AURA3研究中脑转移亚组患者的事后分析结果显示,奥希替尼较培美曲塞联合铂类化疗二线治疗EGFR-TKI耐药后EGFRT790M突变阳性NSCLC脑转移患者可显著延长中位iPFS(分别为11.7和5.6个月,HR=0.32,P=0.004)、改善iORR[分别为70%(21/30)和31%(5/16),OR=5.13,P=0.015][98]。APOLLP研究结果显示,奥希替尼二线治疗EGFR-TKI耐药后EGFRT790M突变阳性NSCLC脑转移患者的iORR为68.8%(22/32)[99]。奥希替尼对脑膜转移的NSCLC患者也显示出良好疗效,BLOOM研究结果显示,奥希替尼二线治疗既往应用第一代或第二代EGFR-TKI治疗后进展伴或不伴EGFRT790M突变NSCLC脑膜转移患者的iORR为62%(23/37),颅内缓解持续时间(intracranial duration of response,iDoR)为15.2个月[100]。AURA系列研究的回顾性汇总结果显示,奥希替尼二线治疗EGFR-TKI耐药后伴EGFRT790M突变NSCLC脑膜转移患者的iORR为55%(12/22)[101]。另外一项针对EGFR基因敏感突变阳性NSCLC脑膜转移患者的研究结果显示,奥希替尼治疗组较其他治疗组(包括其他EGFR-TKI、化疗、鞘内注射化疗、免疫治疗、WBRT等)的OS显著延长(分别为17.0和5.5个月,HR=0.36,P<0.001),并且与EGFRT790M的突变状态无关[102]。阿美替尼、伏美替尼、贝福替尼、瑞齐替尼、瑞厄替尼和利厄替尼均为国产第三代EGFR-TKI,在EGFR基因敏感突变阳性NSCLC脑转移患者中显示出良好疗效。AENEAS研究中脑转移亚组事后分析结果显示,阿美替尼较吉非替尼一线治疗EGFR基因敏感突变阳性NSCLC脑转移患者可显著延长中位iPFS(分别为29.0和8.3个月,HR=0.26,P<0.001),iORR分别为85.7%(24/28)和75.0%(24/32,P=0.312)[103]。AENEAS2研究脑转移亚组分析结果显示,阿美替尼联合培美曲塞和铂类较阿美替尼单药一线治疗EGFR敏感基因突变阳性NSCLC脑转移患者可显著延长中位PFS(分别为26.3和18.0个月,HR=0.56,P<0.001)[104]。阿美替尼二线治疗EGFRT790M突变阳性NSCLC脑转移患者的iORR为60.9%(14/23),iDCR为91.3%(21/23),iDoR为12.5个月[105]。FURLONG研究中脑转移亚组事后分析结果显示,伏美替尼一线治疗EGFR基因敏感突变阳性NSCLC脑转移患者的中位iPFS获益显著优于吉非替尼(分别为20.8和9.8个月,HR=0.40,P=0.0011),iORR也显著提高[分别为91%(21/23)和65%(24/37),OR=6.82,P=0.028][106-107]。伏美替尼160mg二线治疗EGFR-TKI耐药后伴EGFRT790M突变阳性脑转移患者的iORR为65%(22/34),iDCR为97%(33/34),中位iPFS为19.3个月[108-110]。与吉非替尼相比,伏美替尼可以显著改善患者生活质量[111]。贝福替尼较埃克替尼一线治疗EGFR基因敏感突变阳性伴NSCLC脑转移患者的中位iPFS分别为未达到和15.2个月(HR=0.69,P=0.26);iORR分别为70.0%和50.0%(OR=2.33,P=0.37)[112]。贝福替尼二线治疗EGFR-TKI耐药后EGFRT790M突变阳性脑转移患者在75~100mg剂量组的iORR为57.1%(12/21),iDCR为100%(21/21),中位iPFS未达到(95%CI:16.5个月~无法评估)[113]。REZOR研究中脑转移亚组事后分析结果显示,瑞齐替尼较吉非替尼一线治疗EGFR基因敏感突变阳性NSCLC患者的中位iPFS分别为22.5和15.2个月(HR=0.61,P=0.074)[114-115]。瑞齐替尼治疗EGFRT790M突变阳性NSCLC脑转移患者的iORR为68.9%(31/45),iDCR为100%(45/45),中位iPFS为16.5个月(95%CI:13.7个月~无法评估)[116-118]。利厄替尼一线治疗研究中脑转移亚组事后分析结果显示,利厄替尼较吉非替尼一线治疗EGFR基因敏感突变NSCLC脑转移患者可显著改善中位iPFS(分别为20.7和7.1个月,HR=0.28,P=0.0136),iORR分别为89%(16/18)和73%(16/22;P=0.2579)[119]。利厄替尼治疗EGFRT790M突变阳性NSCLC脑转移患者的iORR为56.1%(23/41),iPFS为10.6个月[120]。瑞厄替尼治疗EGFRT790M突变阳性NSCLC脑转移患者的iORR为35.5%(11/31),iDCR为93.5%(29/31),中位iPFS为4.3个月[121]。埃万妥单抗联合兰泽替尼一线治疗研究中脑转移亚组事后分析结果显示,埃万妥单抗联合兰泽替尼较奥希替尼一线治疗EGFR基因敏感突变NSCLC脑转移患者PFS的HR为0.69(95%CI:0.53~0.92)[122]。
佐利替尼是一款专为NSCLC脑转移患者研发的EGFR-TKI,具有完全透过血脑屏障的能力。EVEREST研究结果显示,佐利替尼较吉非替尼/厄洛替尼一线治疗EGFR基因敏感突变阳性局部晚期或转移性NSCLC伴有未经过放疗的有症状或无症状脑转移患者可显著提高iORR(分别为74.3%和62.8%;OR=1.710,P=0.0393)、显著延长中位iPFS(分别为15.2和8.3个月,HR=0.395,P<0.001)[123]。佐利替尼Ⅰ期临床研究结果显示,佐利替尼后线治疗NSCLC伴脑转移患者的iORR为52%(11/21)[124]。
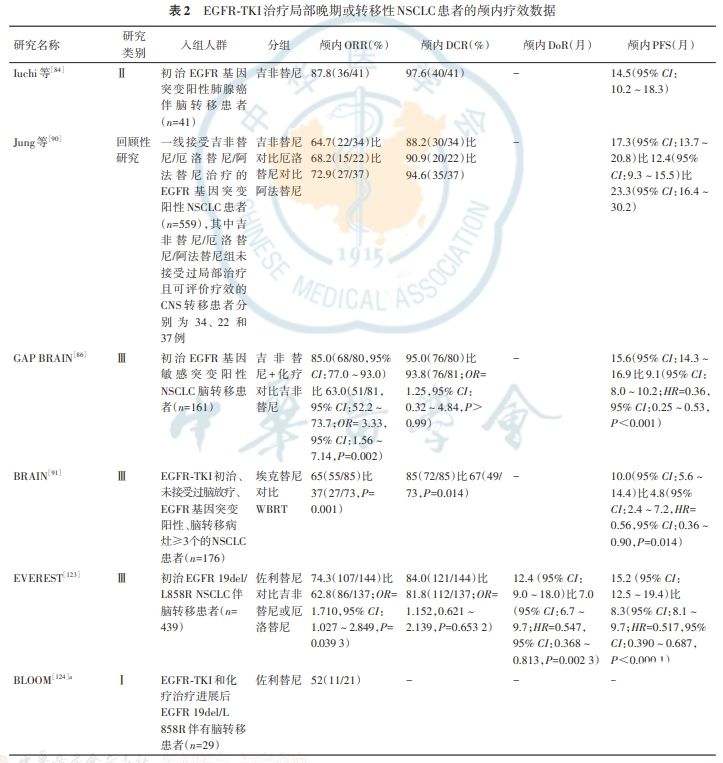
EGFR-TKI的颅内疗效数据汇总见表2。


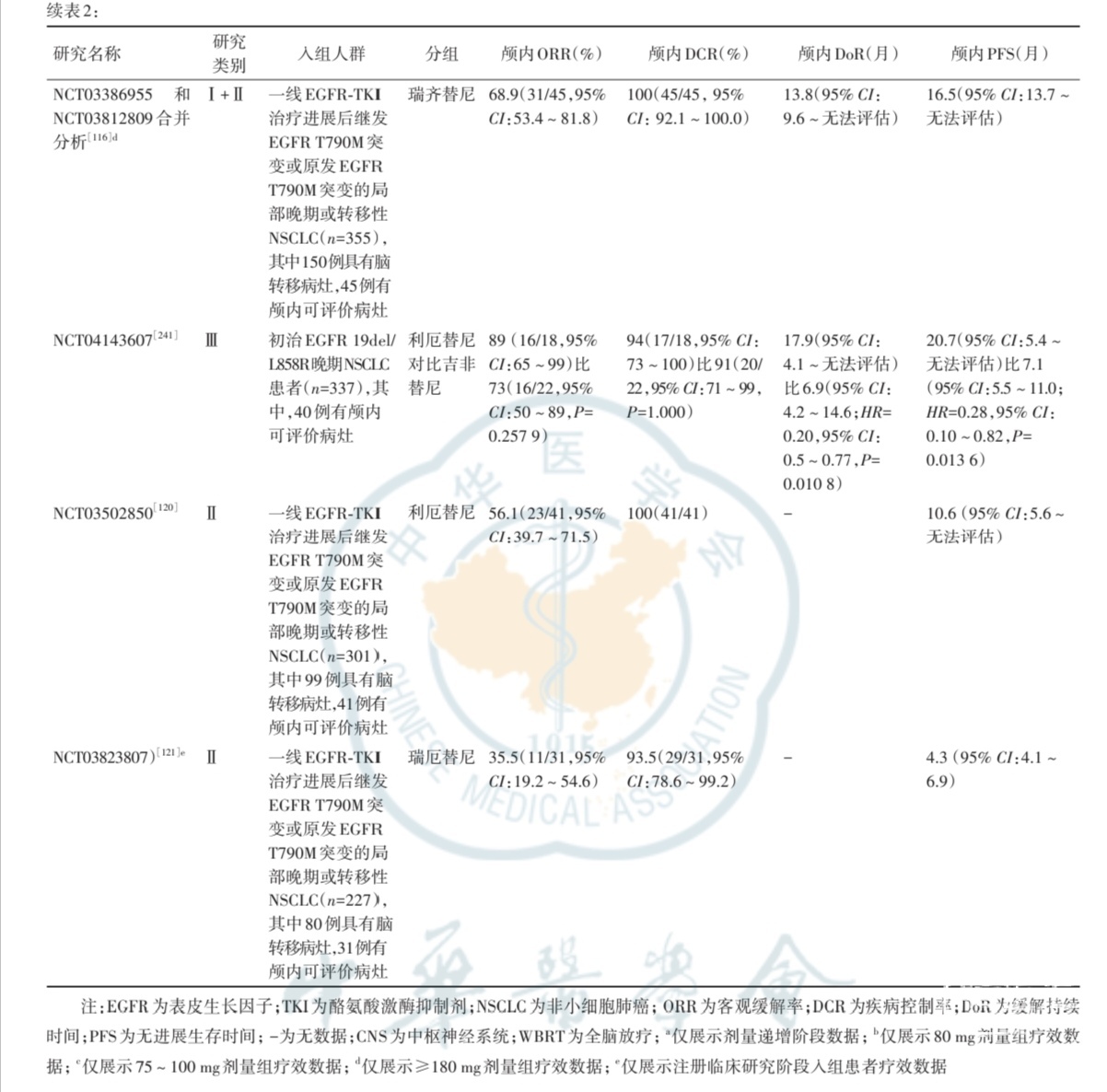
推荐意见8:对于ALK-TKI初治NSCLC脑转移患者,优先推荐新一代ALK-TKI治疗,包括:阿来替尼(2A类推荐)、布格替尼(2A类推荐)、洛拉替尼(2A类推荐)、伊鲁阿克(2A类推荐)、依奉阿克(2A类推荐)和地罗阿克(2A类推荐);对于ALK-TKI经治NSCLC脑转移患者,优先推荐塞瑞替尼(2A类推荐)、阿来替尼(3类推荐)、恩沙替尼(3类推荐)、布格替尼(3类推荐)、洛拉替尼(3类推荐)、伊鲁阿克(3类推荐)、依奉阿克(3类推荐)。
(2)ALK-TKI:ALK融合基因是NSCLC另一个明确的治疗靶点。中国NSCLC患者ALK融合基因的阳性率约为4.9%[125]。获得中国国家药品监督管理局(National Medical Products Administration,NMPA)批准上市的ALK-TKI包括克唑替尼、塞瑞替尼、阿来替尼、恩沙替尼、布格替尼、洛拉替尼、伊鲁阿克、依奉阿克和地罗阿克。
PROFILE1014研究脑转移亚组分析结果显示,克唑替尼较培美曲塞联合铂类方案一线治疗ALK融合基因阳性的NSCLC脑转移患者可显著改善iORR[77%(30/39)对比28%(11/40),P<0.001]和中位iPFS(分别为9.0和4.0个月,HR=0.4,P<0.001)[126]。新一代ALK-TKI对分子量、疏水性、氢键等进行了改造,血脑屏障穿透力更强,颅内疗效更佳。ASCEND-1研究结果显示,在ALK-TKI初治、ALK融合基因阳性NSCLC脑转移患者中,塞瑞替尼的iORR和iDCR分别为62.5%(5/8)和62.5%(5/8);在ALK-TKI经治、ALK融合基因阳性NSCLC脑转移患者中,塞瑞替尼的iORR和iDCR分别为35.7%(10/28)和60.7%(17/28),但是部分患者既往曾接受过脑部放疗[127]。ASCEND-4研究脑转移患者亚组分析结果显示,塞瑞替尼对比培美曲塞联合铂类方案治疗ALK融合基因阳性的初治NSCLC脑转移患者的中位PFS分别为10.7和6.7个月(HR=0.70,95%CI:0.44~1.12),iORR分别为72.7%(16/22)和27.3%(6/22),iDoR分别为16.6个月和无法评估[128]。ASCEND-5研究结果显示,塞瑞替尼对比培美曲塞或多西他赛治疗含铂双药和克唑替尼耐药的ALK融合基因阳性NSCLC脑转移患者的中位PFS分别为4.4和1.4个月(HR=0.50,95%CI:0.33~0.76);iORR分别为35%(6/17)和5%(1/20),中位iDoR分别为6.9个月和无法评估[129]。ALEX研究结果显示,阿来替尼对比克唑替尼一线治疗ALK融合基因阳性NSCLC脑转移患者的中位PFS分别为25.4和7.4个月(HR=0.37,95%CI:0.23~0.58),iORR分别为81%(17/21)和50%(11/22),中位iDoR分别为17.3和5.5个月[130-131]。针对日本患者的J-ALEX研究结果显示,阿来替尼对比克唑替尼一线治疗ALK融合基因阳性NSCLC脑转移患者的中位PFS的HR为0.08(95%CI:0.01~0.61)[132]。针对亚洲患者的ALESIA研究结果显示,阿来替尼对比克唑替尼一线治疗ALK融合基因阳性NSCLC脑转移患者的中位PFS分别为42.3和9.2个月(HR=0.17,95%CI:0.09~0.33),iORR分别为94%(16/17)和29%(2/7)[133-134]。此外,一项研究汇总分析了两项阿来替尼治疗克唑替尼耐药的ALK融合基因阳性NSCLC脑转移患者的Ⅱ期临床研究,结果显示,iORR为64%(32/50),iDoR为10.8个月[135]。ALUR研究结果亦显示,阿来替尼治疗含铂双药耐药和克唑替尼耐药/不耐受的ALK融合基因阳性NSCLC患者颅内疗效优于培美曲塞或多西他赛单药,iORR分别为66.7%(16/24)和0(0/17;P<0.001)[136-137]。eXalt3研究结果显示,恩沙替尼对比克唑替尼一线治疗ALK融合基因阳性NSCLC脑转移患者的中位PFS分别为11.8和7.5个月(HR=0.55,95%CI:0.30~1.01,P=0.05)[138]。恩沙替尼Ⅱ期研究结果显示,恩沙替尼治疗克唑替尼耐药的ALK融合基因阳性NSCLC脑转移患者的iORR为70%(28/40)[139]。ALTA-1L研究结果显示,布格替尼对比克唑替尼一线治疗ALK融合基因阳性NSCLC脑转移患者的iORR分别为78%(14/18)和29%(6/21;OR=11.67,P=0.0014),中位iPFS分别为24和5.5个月(HR=0.29,P<0.001)[140-141]。ALTA研究结果显示,布格替尼90mg剂量组治疗克唑替尼耐药NSCLC脑转移患者的iORR为42%(11/26),180mg剂量组的iORR为73%(11/15)[142];CROWN研究结果显示,洛拉替尼对比克唑替尼一线治疗ALK融合基因阳性NSCLC脑转移患者的中位iORR分别为92%(11/12)和33%(2/6;OR=15.0);中位iDoR分别为未达到和10.2个月;中位至颅内进展时间(central nervous system time to progression,CNS-TTP)分别为未达到和16.4个月(HR=0.06,95%CI:0.03~0.12)[143-145]。洛拉替尼治疗克唑替尼耐药脑转移患者的iORR为80.6%和87.0%[146-147]。
INSPIRE研究结果显示,伊鲁阿克对比克唑替尼一线治疗ALK融合阳性NSCLC脑转移患者的iORR分别为90.9%(10/11)和60.0%(9/15;P=0.097);中位iDoR分别为20.1和9.3个月,18个月的累积中枢进展率分别为3.2%和12.2%(HR=0.39,P=0.0081)[148]。伊鲁阿克治疗克唑替尼耐药脑转移患者的iORR为64%[149]。依奉阿克Ⅲ期临床研究结果显示,依奉阿克对比克唑替尼一线治疗ALK融合基因阳性NSCLC脑转移患者的iORR分别为78.95%(15/19)和23.81%(5/21)(P=0.0012);中位iDoR分别为25.82和7.39个月(P=0.0030);中位CNS-TTP分别为26.68和6.34个月(P=0.0008)[150]。XZP-3621-3001研究结果显示,地罗阿克对比克唑替尼一线治疗初治ALK融合基因阳性NSCLC脑转移患者的中位PFS分别为未达到和9.23个月(HR=0.32,95%CI:0.143~0.704),iORR分别为92.3%(12/13)和11.1%(1/9;P=0.0004),中位iDoR分别为未达到和3.55个月(P=0.0008)(药品说明书)。ALK-TKI的颅内疗效数据汇总见表3。

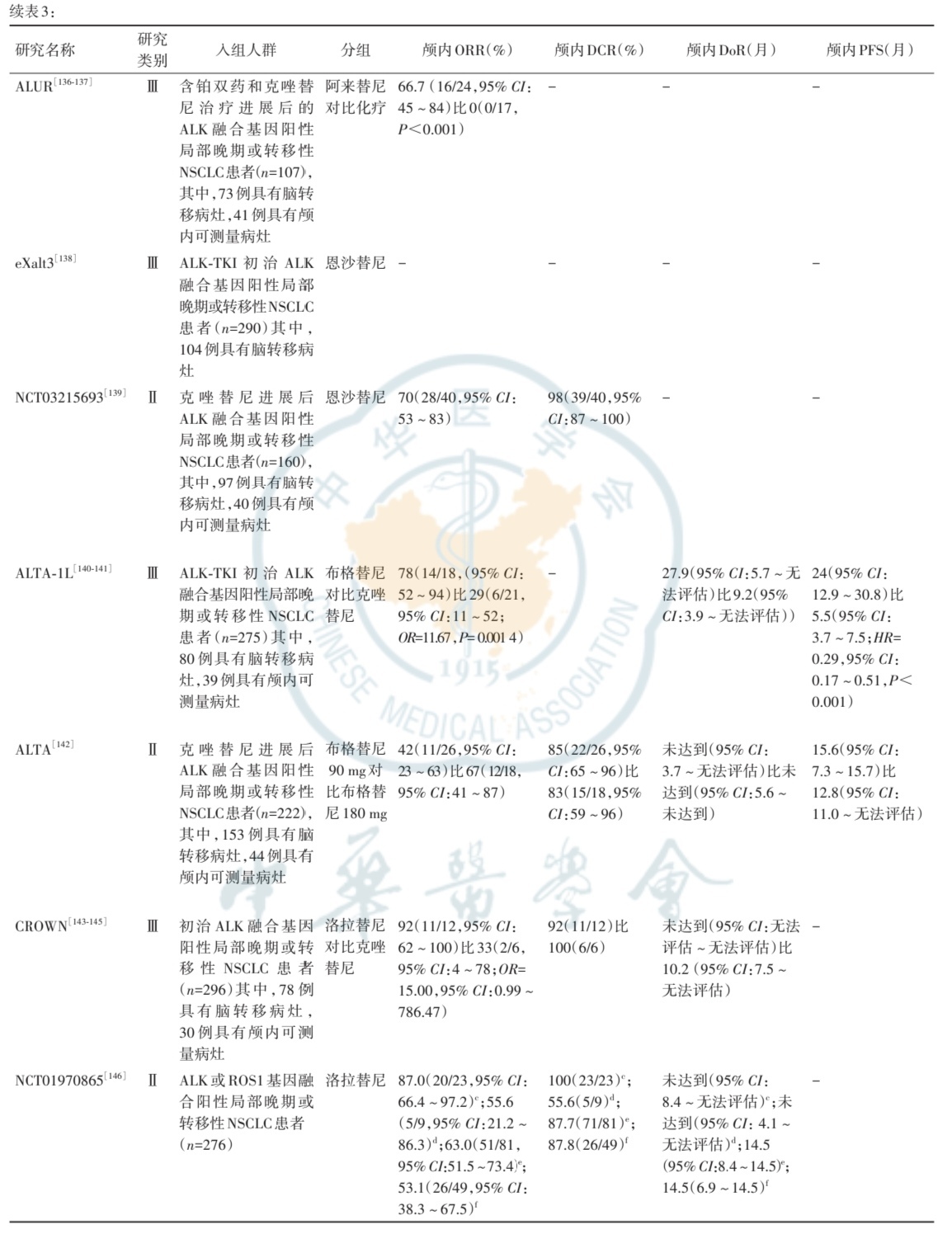
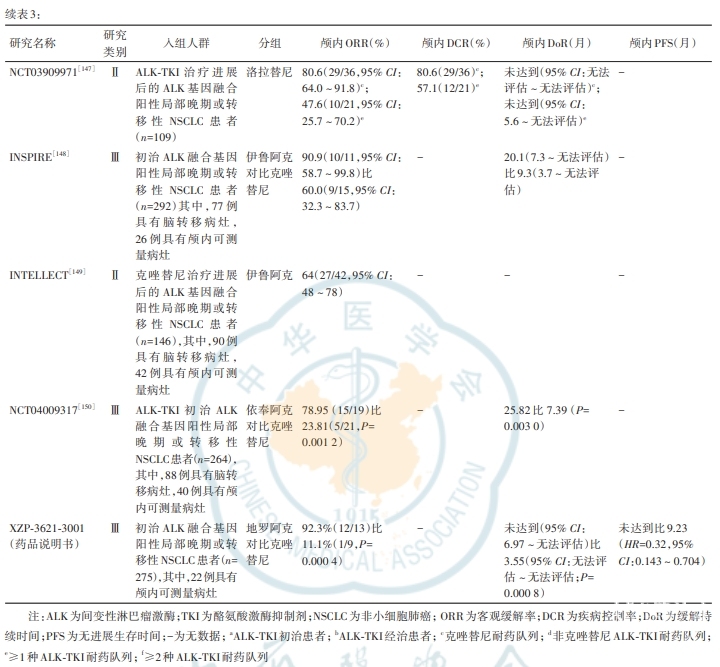
推荐意见9:对于ROS1-TKI初治的NSCLC脑转移患者,优先推荐恩曲替尼(3类推荐)、瑞普替尼(3类推荐)、安奈克替尼(3类推荐)和他雷替尼(3类推荐);对于ROS1-TKI经治的NSCLC脑转移患者,优先推荐恩曲替尼(3类推荐)、瑞普替尼(3类推荐)和他雷替尼(3类推荐)。
(3)ROS1-TKI:ROS1基因和ALK基因均同属胰岛素样受体酪氨酸激酶超家族成员,二者的氨基酸序列具有近49%的相似性,在激酶催化区的ATP结合位点同源性达77%[151]。ROS1融合基因在NSCLC中的阳性率大约为1%~3.4%[152],获中国NMPA批准上市的ROS1-TKI包括克唑替尼、恩曲替尼、瑞普替尼、安奈克替尼和他雷替尼。参考克唑替尼在ALK融合基因阳性NSCLC脑转移患者中的临床研究数据,尽管颅内病灶缓解情况优于化疗,但由于颅内渗透率低,颅内疗效并不理想。恩曲替尼是广谱抗肿瘤靶向药,在ROS1融合基因阳性NSCLC患者的治疗中取得了进展。BFAST研究结果显示,恩曲替尼一线治疗ROS1融合基因阳性NSCLC患者的12个月中枢神经系统无事件生存率为86.4%,中位CNS-TTP未达到[153]。对ALKA-372-001、STARTRK-1和STARTRK-2三项临床研究的汇总结果显示,恩曲替尼后线治疗ROS1融合基因阳性NSCLC脑转移患者的iORR为79.2%(19/24),中位iDoR为12.9个月,中位iPFS为12个月[154]。TRIDENT-1研究结果显示,瑞普替尼治疗ROS1融合基因阳性ROS1-TKI初治NSCLC脑转移患者的iORR是89%(8/9),治疗既往接受过1种ROS1-TKI但未接受过化疗的iORR是38%(5/13)[155]。安奈克替尼的Ⅰ/Ⅱ期临床研究结果显示,安奈克替尼治疗ROS1融合基因阳性ROS1-TKI初治NSCLC脑转移患者的iORR为72.7%(8/11),中位iPFS为10.1个月[156]。TRUST-I和TRUST-Ⅱ研究的汇总分析结果显示,他雷替尼治疗ROS1融合基因阳性ROS1-TKI初治NSCLC脑转移患者的iORR为76.5%(13/17),治疗既往接受过一种ROS1-TKI患者的iORR为62.5%(20/32)[157]。
推荐意见10:对于RET融合基因阳性的NSCLC脑转移患者,推荐普拉替尼(3类推荐)和塞普替尼(3类推荐)。
(4)RET基因:NSCLC中RET融合基因阳性的发生率约为2.0%[158]。中国NMPA批准上市的RET抑制剂有普拉替尼和塞普替尼。ARROW研究结果显示,在伴有可测量脑转移病灶的9例NSCLC患者中(既往均接受过治疗),普拉替尼的iORR为56%(5/9)[159]。LIBRETTO-321研究结果显示,在伴有可测量脑转移病灶的5例NSCLC患者中(4例既往接受过治疗,1例为初治),塞普替尼的iORR为80%(4/5)[160]。
推荐意见11:对于MET基因14号外显子跳跃突变阳性NSCLC脑转移患者,推荐赛沃替尼(3类推荐)、谷美替尼(3类推荐)、伯瑞替尼(3类推荐)、特泊替尼(3类推荐)和卡马替尼(3类推荐)。
(5)MET基因14号外显子跳跃突变:NSCLC患者MET基因14号外显子跳跃突变的发生率为3%~4%[161]。中国NMPA批准上市的MET抑制剂有赛沃替尼、谷美替尼、伯瑞替尼、特泊替尼和卡马替尼。赛沃替尼的Ⅱ期临床研究纳入了15例MET基因14号外显子跳跃突变伴有基线脑转移的肺肉瘤样癌和其他NSCLC患者,尽管这15例患者的脑转移病灶未被独立评审委员会(independent review committee,IRC)选为靶病灶,但事后分析发现这15例患者的脑转移病灶均能得到控制,这些患者颅外ORR为46.7%,颅外DCR为93.3%,中位PFS为6.9个月。3例患者的脑转移病灶被研究者选为靶病灶,均达到部分缓解(partial response,PR)[162]。谷美替尼的Ⅰb/Ⅱ期临床研究纳入了13例MET基因14号外显子跳跃突变的NSCLC脑转移患者,但这13例患者的脑转移病灶未被IRC选为靶病灶,其颅外ORR为85%。5例患者的脑转移病灶被研究者选为靶病灶,均达到PR[163]。伯瑞替尼Ⅱ期临床研究纳入了5例MET基因14号外显子跳跃突变的NSCLC脑转移患者,全身ORR为100%[164]。特泊替尼Ⅱ期临床研究纳入了11例MET基因14号外显子跳跃突变的NSCLC脑转移患者,但这11例患者的脑转移病灶未满足靶病灶标准,其全身ORR为55%,中位DoR为9.5个月,中位PFS为10.9个月[165]。卡马替尼Ⅱ期研究纳入了13例MET基因14号外显子跳跃突变的NSCLC脑转移患者(10例既往接受过治疗,3例为初治),iORR为53.8%,iDCR为92.3%[166]。
推荐意见12:对于BRAFV600E突变阳性NSCLC脑转移患者,推荐达拉非尼+曲美替尼(3类推荐)。
(6)BRAFV600E基因突变:NSCLC患者BRAF基因突变的发生率为2%[167],其中V600E突变约占45%[168]。达拉非尼联合曲美替尼已经获中国NMPA批准用于BRAFV600E阳性晚期NSCLC患者的治疗。一项Ⅱ期临床研究纳入了1例经治BRAFV600E阳性NSCLC脑转移患者,但这1例患者的脑病灶为非靶病灶,疗效评价为非CR非疾病进展(progressive disease,PD)[169]。另一项Ⅱ期临床研究纳入了2例初治BRAFV600E阳性NSCLC脑转移患者,但这2例患者的脑病灶均为非靶病灶,疗效评价均为非CR非PD[170]。达拉非尼联合曲美替尼治疗BRAFV600E突变阳性NSCLC患者的中国注册临床试验纳入了5例BRAFV600E阳性NSCLC脑转移患者,但未公布这5例患者的颅内疗效数据[171]。一项真实世界研究纳入了34例BRAFV600E阳性NSCLC脑转移患者(27例既往接受过治疗,7例为初治),全身ORR为80.6%,中位PFS为7.5个月,中位OS为24.1个月[172]。
推荐意见13:对于EGFR20ins阳性NSCLC脑转移患者,一线治疗推荐埃万妥单抗+化疗(2A类推荐)、舒沃替尼(不耐受铂类化疗者,3类推荐);后线治疗推荐舒沃替尼(3类推荐)。
(7)EGFR基因20号外显子插入突变(20ins):NSCLC患者EGFR20ins的发生率为2.4%[82]。中国NMPA批准上市的EGFR20ins抑制剂有舒沃替尼和埃万妥单抗。舒沃替尼Ⅱ期临床研究纳入了31例EGFR20ins阳性NSCLC脑转移患者,这31例患者的全身ORR为48%[173]。埃万妥单抗是一个靶向EGFR和MET受体的双特异性抗体。PAPILLON研究评价了埃万妥单抗联合化疗对比单纯化疗一线治疗EGFR20ins阳性NSCLC患者的疗效,埃万妥单抗联合化疗组和单纯化疗组分别纳入了35例和36例伴有脑转移的患者,脑转移患者亚组分析结果显示,埃万妥单抗联合化疗组较化疗组的IRC和研究者评估PFS的HR分别为0.63(95%CI:0.38~1.06)和0.47(95%CI:0.28~0.80)[174]。
推荐意见14:对于KRASG12C突变阳性NSCLC脑转移患者,二线治疗推荐氟泽雷塞(3类推荐)、格索雷塞(3类推荐)和戈来雷塞(3类推荐)。
(8)KRASG12C突变:亚洲NSCLC患者KRASG12C突变发生率为1.4%~4.3%[175]。中国NMPA批准上市的KRASG12C抑制剂有氟泽雷塞、格索雷塞和戈来雷塞。氟泽雷塞Ⅱ期临床研究纳入了35例既往接受过标准方案治疗(≤3线)后进展的KRASG12C突变阳性NSCLC脑转移患者(11例既往接受过放疗),这部分患者的全身ORR为48.6%[176]。格索雷塞Ⅱ期临床研究纳入了18例PD-1单抗和含铂方案治疗失败或不耐受的KRASG12C突变阳性NSCLC脑转移患者,但这部分患者的颅内疗效数据未单独披露[177]。戈来雷塞Ⅱ期临床研究纳入了20例免疫检查点抑制剂(immune check point inhibitor,ICI)和含铂方案治疗失败的KRASG12C突变阳性NSCLC脑转移患者,这部分患者的全身ORR为35%[178]。
推荐意见15:对于HER-2基因突变阳性NSCLC脑转移患者,二线治疗推荐德曲妥珠单抗(3类推荐)、瑞康曲妥珠单抗(3类推荐)和宗艾替尼(3类推荐)。
(9)HER-2基因突变:HER-2基因突变在NSCLC患者的发生率为1.7%[179]。中国NMPA批准上市的用于HER-2基因突变阳性NSCLC患者的治疗药物有德曲妥珠单抗、瑞康曲妥珠单抗和宗艾替尼。德曲妥珠单抗Ⅱ期临床研究5.4mg/kg剂量组纳入了32例HER-2突变晚期NSCLC脑转移患者,这部分患者的全身ORR为60.0%;6.4mg/kg剂量组纳入了19例HER-2突变晚期NSCLC脑转移患者,这部分患者的全身ORR为45.5%[180]。瑞康曲妥珠单抗Ⅱ期临床研究纳入了24例HER-2突变晚期NSCLC脑转移患者,这部分患者的全身ORR为87.5%[181]。宗艾替尼Ⅰb期临床研究纳入了28例HER-2酪氨酸激酶结构域突变、既往接受过治疗的晚期NSCLC脑转移患者,这部分患者的全身ORR为64%,其中27例患者伴有可测量脑转移病灶,这部分患者的iORR为41%[182]。
5.免疫治疗
ICI在肺癌治疗中具有重要地位。中国NMPA已经批准用于肺癌治疗的PD-1有纳武利尤单抗、帕博利珠单抗、卡瑞利珠单抗、替雷利珠单抗、信迪利单抗、特瑞普利单抗、斯鲁利单抗和派安普利单抗;PD-L1单抗包括度伐利尤单抗、阿替利珠单抗、舒格利单抗和贝莫苏拜单抗。双特异性抗体包括依沃西单抗。
推荐意见16:对于驱动基因阴性的NSCLC脑转移患者,一线治疗推荐帕博利珠单抗[PD-L1肿瘤细胞阳性评分(tumor proportion score,TPS)≥1%患者,2A类推荐]、帕博利珠单抗+培美曲塞+铂类(非鳞癌,2A类推荐)、帕博利珠单抗+紫杉醇/紫杉醇(白蛋白结合型)+卡铂(鳞癌,2A类推荐)、卡瑞利珠单抗+培美曲塞+卡铂(非鳞癌,2A类推荐)、替雷利珠单抗+培美曲塞+铂类(非鳞癌,2A类推荐)、替雷利珠单抗+紫杉醇/紫杉醇(白蛋白结合型)+铂类(鳞癌,2A类推荐)、信迪利单抗+培美曲塞+铂类(非鳞癌,2A类推荐)、信迪利单抗+吉西他滨+铂类(鳞癌,2A类推荐)、特瑞普利单抗+培美曲塞+铂类(非鳞癌,2A类推荐)、斯鲁利单抗+培美曲塞+铂类(非鳞癌,2A类推荐)、斯鲁利单抗+紫杉醇(白蛋白结合型)+卡铂(鳞癌,2A类推荐)、派安普利单抗+紫杉醇+卡铂(鳞癌,2A类推荐)、阿替利珠单抗+培美曲塞+铂类(非鳞癌,3类推荐)、舒格利单抗+培美曲塞+卡铂(非鳞癌,2A类推荐)、舒格利单抗+紫杉醇+卡铂(鳞癌,2A类推荐)、纳武利尤单抗+伊匹木单抗(PD-L1TPS≥1%患者,2A类推荐);后线治疗推荐纳武利尤单抗(2A类推荐)、替雷利珠单抗(2A类推荐)、依沃西单抗+培美曲塞+卡铂(EGFR-TKI耐药后患者,2A类推荐)、信迪利单抗+贝伐珠单抗生物类似药+培美曲塞+顺铂(EGFR-TKI耐药后患者,2A类推荐)、埃万妥单抗+培美曲塞+卡铂(EGFR-TKI耐药后患者,2A类推荐)、埃万妥单抗+兰泽替尼+培美曲塞+卡铂(EGFR-TKI耐药后患者,2A类推荐)。
(1)NSCLC脑转移患者的免疫治疗:CheckMate-017和CheckMate-057研究结果显示,无论晚期鳞状NSCLC还是非鳞状NSCLC患者,纳武利尤单抗二线治疗均较多西他赛显著延长患者的中位OS。这2项研究均允许脑转移患者入组,CheckMate-017研究纳入的脑转移患者中,纳武利尤单抗组(n=9)和多西他赛组(n=8)的中位OS分别为4.99和3.86个月[183]。CheckMate-057研究纳入的脑转移患者中,纳武利尤单抗组(n=34)和多西他赛组(n=34)的中位OS分别为7.61和7.33个月(HR=1.04,95%CI:0.62~1.76)[184]。另一项研究结果显示,纳武利尤单抗后线治疗非鳞状NSCLC脑转移患者(n=409)的ORR和DCR分别为17%和39%,中位PFS和OS分别为3.0和8.6个月[185]。回顾性研究结果显示纳武利尤单抗后线治疗NSCLC脑转移患者(n=43)的iORR和iDCR分别为9%和51%,中位iPFS为3.9个月,中位OS为7.5个月[186]。KEYNOTE-001、KEYNOTE-010、KEYNOTE-024和KEYNOTE-042研究结果均显示了帕博利珠单抗单药在晚期NSCLC患者中的疗效,这4项研究均允许脑转移患者入组。KEYNOTE-001研究纳入了58例NSCLC脑转移患者,初治患者的全身ORR为0(0/3),经治患者的全身ORR为21.8%(12/55)[187]。KEYNOTE-010研究纳入了152例PD-L1TPS≥1%的NSCLC脑转移经治患者,但未进行脑转移亚组分析[188]。KEYNOTE-024研究纳入了28例PD-L1TPS≥50%的NSCLC脑转移初治患者,脑转移患者亚组分析结果显示,帕博利珠单抗组较化疗组患者PFS的HR为0.55(95%CI:0.20~1.56)[189]。KEYNOTE-042研究纳入了70例PD-L1TPS≥1%的NSCLC脑转移初治患者,脑转移患者亚组分析结果显示,帕博利珠单抗组患者的OS较化疗组的HR为0.64(95%CI:0.38~1.10)[190]。这4项研究中脑转移患者的汇总分析结果显示,在PD-L1TPS≥50%的NSCLC脑转移患者(n=160)中,帕博利珠单抗和化疗组的ORR分别为33.9%和7%;中位PFS分别为4.1和4.6个月(HR=0.70,95%CI:0.47~1.03);中位OS分别为19.7和9.7个月(HR=0.67,95%CI:0.44~1.02)。在PD-L1TPS≥1%的NSCLC脑转移患者(n=293)中,帕博利珠单抗和化疗组的ORR分别为26.1%和18.1%;中位PFS分别为2.3和5.2个月(HR=0.96,95%CI:0.73~1.25);中位OS分别为13.4和10.3个月(HR=0.83,95%CI:0.62~1.10)[191]。KEYNOTE-189研究结果显示,帕博利珠单抗+培美曲塞+铂类较安慰剂+培美曲塞+铂类方案可显著延长患者的PFS和OS。该研究纳入了108例初治非鳞状NSCLC脑转移患者,脑转移患者亚组分析结果显示,帕博利珠单抗+培美曲塞+铂类组较安慰剂+培美曲塞+铂类组患者PFS的HR为0.42(95%CI:0.26~0.68),OS的HR为0.36(95%CI:0.20~0.62)[192]。KEYNOTE-407研究结果显示帕博利珠单抗+紫杉醇/紫杉醇(白蛋白结合型)+卡铂方案较安慰剂+紫杉醇/紫杉醇(白蛋白结合型)+卡铂方案可显著延长患者的PFS和OS。该研究纳入了44例初治鳞状NSCLC脑转移患者,但未单独进行脑转移亚组分析[193]。CameL和CameL-Sq研究结果显示,无论晚期鳞状NSCLC还是非鳞状NSCLC患者,卡瑞利珠单抗联合化疗方案较单纯化疗方案均可显著延长患者的中位PFS,这两项研究均允许脑转移患者入组。CameL研究脑转移患者(n=17)的亚组分析结果显示,PFS的HR为0.14(95%CI:0.01%~0.88%);CameL-Sq研究未单独进行脑转移患者亚组分析[194-195]。一项Ⅱ期临床研究结果显示,卡瑞利珠单抗+化疗方案一线治疗NSCLC脑转移患者(n=45)的iORR为52.5%(95%CI:36.1%~68.5%),中位iPFS为7.6个月(95%CI:4.6个月~未达到)[196]。RATIONALE304和RATIONALE307研究结果显示,无论晚期鳞状NSCLC还是非鳞状NSCLC患者,替雷利珠单抗联合化疗方案较单纯化疗方案一线治疗均可显著延长患者的中位PFS。RATIONALE304研究入组了18例脑转移患者,RATIONALE307研究入组了6例脑转移患者,这两项研究均允许脑转移患者入组,但均未单独进行脑转移亚组分析[197-198]。一项Ⅱ期临床研究结果显示,替雷利珠单抗联合化疗方案一线治疗NSCLC脑转移患者(n=36)的iORR为46.7%[199]。RATIONALE-303研究结果显示,无论是鳞癌还是非鳞癌,替雷利珠单抗较多西他赛二线治疗均可显著延长患者的OS。该研究纳入了57例脑转移患者,但未进行脑转移亚组分析[200]。ORIENT-11研究和ORIENT-12研究结果显示,无论晚期鳞状NSCLC还是非鳞状NSCLC患者,信迪利单抗联合化疗方案较单纯化疗方案均可显著延长患者的中位PFS,这两项研究均允许脑转移患者入组。ORIENT-11研究脑转移患者(n=33)的亚组分析结果显示,PFS的HR为0.578(95%CI:0.283~1.180,P=0.132);ORIENT-12研究未单独进行脑转移患者亚组分析[201-202]。ORIENT-31研究结果显示,信迪利单抗+贝伐珠单抗生物类似药+培美曲塞+顺铂方案较单纯培美曲塞+顺铂方案治疗EGFR-TKI耐药后的非鳞状NSCLC患者可显著延长PFS。该研究入组了160例脑转移患者,脑转移患者亚组分析结果显示中位PFS分别为7.2和4.3个月(HR=0.48,95%CI:0.29~0.79)[203]。CHOICE-01研究结果显示,特瑞普利单抗联合化疗方案较单纯化疗方案可以显著延长NSCLC患者的中位PFS和中位OS。该研究纳入了5例NSCLC脑转移患者,未单独进行脑转移患者亚组分析[204]。ASTRUM-002和ASTRUM-004研究结果显示,无论是鳞癌还是非鳞癌,斯鲁利单抗联合化疗方案较单纯化疗方案均可显著延长患者的中位PFS和中位OS。ASTRUM-002研究将是否具有脑转移作为患者的入组分层因素,全组636例患者中共有119例患者具有基线脑转移(18.7%),斯鲁利单抗联合化疗方案相比单纯化疗方案可以显著延长患者中位PFS(8.1个月对比4.1个月,HR=0.51,P=0.0115)[205-207];ASTRUM-004研究允许脑转移患者入组,脑转移患者(n=38)亚组分析结果显示,PFS的HR为0.37(95%CI:0.14~0.96)[208]。AK105-302研究结果显示,派安普利单抗+紫杉醇+卡铂方案较安慰剂+紫杉醇+卡铂方案可以显著延长鳞状NSCLC患者的中位PFS。该研究纳入了10例鳞状NSCLC脑转移患者,未单独进行脑转移患者亚组分析[209]。OAK研究脑转移患者事后分析结果显示,阿替利珠单抗(n=61)和多西他赛(n=62)治疗既往接受过治疗的无症状NSCLC脑转移患者的中位OS分别为16.0和11.9个月(HR=0.74,95%CI:0.49~1.13)[210]。IMPOWER110研究结果显示,阿替利珠单抗较化疗一线治疗可以显著延长PD-L1高表达[肿瘤细胞≥50%或免疫细胞≥10%]驱动基因阴性非鳞状或鳞状NSCLC患者的PFS和OS。但该研究排除了未经治疗的和症状性NSCLC脑转移患者[211-212]。另一项Ⅱ期临床研究结果显示,阿替利珠单抗+培美曲塞+卡铂方案一线治疗非鳞状NSCLC伴脑转移患者(n=40)的iORR为42.7%,中位iPFS为6.9个月[213]。IMpower132研究结果显示,阿替利珠单抗+培美曲塞+铂类较培美曲塞+铂类方案一线治疗非鳞状NSCLC可以显著延长PFS,但该研究排除了未经治疗的脑转移患者[214]。GEMSTONE-302研究结果显示,无论是晚期鳞状NSCLC还是非鳞状NSCLC患者,舒格利单抗联合含铂方案一线治疗较单纯化疗方案均可以显著延长患者的中位PFS和OS。该研究允许脑转移患者入组,脑转移患者亚组事后分析结果显示,舒格利单抗联合含铂方案组(n=50)和单纯化疗方案组(n=17)的中位PFS分别为8.9和4.5个月(HR=0.29,95%CI:0.15~0.56);中位OS分别为22.1和9.0个月(HR=0.45,95%CI:0.23~0.88)[215-216]。HARMONi-A研究结果显示,依沃西单抗+培美曲塞+卡铂方案治疗EGFR-TKI耐药后NSCLC患者较培美曲塞+卡铂方案可以显著延长患者中位PFS。该研究允许脑转移患者入组,脑转移患者亚组分析结果显示,依沃西单抗+培美曲塞+卡铂方案组(n=35)和培美曲塞+卡铂方案组(n=37)患者的中位PFS分别为5.75和4.14个月(HR=0.40,95%CI:0.22~0.73)[217]。MARIPOSA-2研究脑转移患者亚组分析结果显示,对于奥希替尼耐药后的患者,埃万妥单抗+培美曲塞+卡铂方案(n=58)较培美曲塞+卡铂方案(n=120)可以显著延长脑转移患者的中位PFS(HR=0.52,95%CI:0.35~0.78);埃万妥单抗+兰泽替尼+培美曲塞+卡铂方案(n=120)较培美曲塞+卡铂方案(n=120)也可以显著延长脑转移患者的中位PFS(HR=0.48,95%CI:0.35~0.78)[218]。CheckMate-227研究脑转移患者亚组分析结果显示,对于PD-L1≥1的Ⅳ期NSCLC肺癌患者,纳武利尤单抗+伊匹木单抗方案较化疗方案一线治疗PFS的HR为0.68(95%CI:0.41~1.1)[219]。
推荐意见17:对于SCLC脑转移患者,一线治疗推荐阿替利珠单抗+卡铂+依托泊苷(2A类推荐)、度伐利尤单抗+依托泊苷+铂类(2A类推荐)、阿得贝利单抗+卡铂+依托泊苷(2A类推荐)、斯鲁利单抗+依托泊苷+卡铂(2A类推荐)、特瑞普利单抗+依托泊苷+铂类(2A类推荐)、替雷利珠单抗+依托泊苷+铂类(2A类推荐)、贝莫苏拜单抗+安罗替尼+依托泊苷+卡铂(2A类推荐)。
(2)SCLC脑转移患者的免疫治疗:IMPOWER133研究结果显示,阿替利珠单抗+卡铂+依托泊苷方案一线治疗广泛期SCLC患者较卡铂+依托泊苷方案可以显著延长中位PFS和OS。该研究入组了35例脑转移患者,脑转移患者亚组PFS的HR为0.98(95%CI:0.49~2.00);脑转移患者亚组OS的HR为1.07(95%CI:0.47~2.43)[220]。CASPIAN研究结果显示,度伐利尤单抗+依托泊苷+铂类方案一线治疗广泛期SCLC较卡铂+依托泊苷方案可以显著延长中位OS。该研究允许脑转移患者入组,脑转移患者亚组OS的HR为0.69(95%CI:0.35~1.31)[221]。CAPSTONE-1研究结果显示,阿得贝利单抗+卡铂+依托泊苷方案一线治疗广泛期SCLC较卡铂+依托泊苷方案可以显著延长患者的中位PFS和OS。该研究允许脑转移患者入组,但未单独进行脑转移患者亚组分析[222]。ASTRUM-005研究结果显示,斯鲁利单抗+依托泊苷+卡铂方案一线治疗广泛期SCLC较依托泊苷+卡铂方案可以显著延长患者中位OS。该研究允许脑转移患者入组。脑转移患者亚组OS的HR为0.61(95%CI:0.33~1.13)[223]。EXTENTORCH研究结果显示,特瑞普利单抗+依托泊苷+铂类方案一线治疗广泛期SCLC较依托泊苷+铂类方案可以显著延长中位PFS和OS。该研究允许脑转移患者入组,但未单独进行脑转移亚组分析[224]。RATIONALE-312研究结果显示,替雷利珠单抗+依托泊苷+铂类方案一线治疗广泛期SCLC较依托泊苷+铂类方案可以显著延长中位PFS和OS。该研究允许脑转移患者入组,但未单独进行脑转移亚组分析[225]。ETER701研究结果显示,贝莫苏拜单抗+安罗替尼+依托泊苷+卡铂方案一线治疗广泛期SCLC患者较依托泊苷+卡铂方案可以显著延长患者的中位PFS和OS。该研究允许脑转移患者入组,脑转移患者亚组的HR为0.64(95%CI:0.29~1.41)[226]。
6.抗血管生成药物
推荐意见18:对于非鳞状NSCLC脑转移患者,一线治疗推荐含贝伐珠单抗的联合化疗方案(3类推荐);后线治疗推荐安罗替尼(2A类推荐)。
贝伐珠单抗是抗血管内皮生长因子(vascular endothelial growth factor,VEGF)的重组人源化单克隆抗体。贝伐珠单抗联合化疗对于非鳞状NSCLC脑转移患者是安全、有效的[227-229]。一项贝伐珠单抗治疗NSCLC脑转移患者的荟萃分析结果显示,与对照组相比,贝伐珠单抗治疗组的疗效更好,经贝伐珠单抗治疗的患者颅内病灶的ORR和DCR均优于颅外病灶,且不增加脑转移患者的出血风险[230]。贝伐珠单抗对于放射治疗导致的脑坏死及脑水肿也有一定效果,贝伐珠单抗可以在一定程度上减轻脑水肿[231-232]。BRAIN研究结果显示,贝伐珠单抗+紫杉醇+卡铂方案一线治疗伴有脑转移的非鳞状NSCLC患者的iORR为61.2%,中位iDoR为8.1个月[233]。安罗替尼是靶向VEGFR2/3、FGFR1-4和PDGFRα/β等靶点的小分子多靶点TKI[234],ALTER0303研究脑转移患者亚组事后分析结果显示,三线及以上治疗后进展的NSCLC脑转移患者安罗替尼治疗的iORR为14.3%,iDCR为85.7%,安罗替尼较安慰剂可以显著延长患者的中位CNS-TTP(HR=0.11,95%CI:0.03~0.41,P=0.001)[235]。
(五)对症治疗
肺癌脑转移患者常伴有颅内压升高导致的头痛、恶心、呕吐等症状,颅内高压属于肿瘤急症,首先应该积极给予脱水和利尿治疗以降低颅内压,可选择的药物包括甘露醇、甘油果糖和呋塞米。糖皮质激素,尤其是地塞米松可减轻脑水肿、改善脑转移患者的生活质量,但并不能改善预后。其次是控制症状,包括抗癫痫和镇痛治疗,由于抗癫痫药物不能减少NSCLC脑转移患者的癫痫发作次数,因此一般仅用于有发作症状的患者,不预防性应用[236-237]。头痛明显患者可予止痛对症治疗。
1.甘露醇:20%甘露醇125~250ml静脉滴注,依据症状每6~8h1次,同时严密监测血浆电解质和尿量。甘露醇通过提高血浆渗透压,导致包括脑、脑脊液等组织内的水分进入血管内,从而减轻组织水肿,降低颅内压和脑脊液容量及其压力,可用于治疗脑转移瘤引起的脑水肿和颅高压,预防脑疝的发生。既往国内外动物及临床研究表明,甘露醇具有暂时性开放血脑屏障,促进肿瘤化疗药物向患者颅脑病灶渗透,提高颅内血药浓度及疾病缓解率的作用[238]。
2.糖皮质激素:糖皮质激素是治疗脑转移瘤周围水肿的重要药物,具有改善肿瘤颅内转移相关症状的作用。其中地塞米松应用最为广泛,常与甘露醇联合使用。对于没有占位效应的无症状脑转移患者,目前没有足够的证据支持应用激素治疗。对于轻微症状性脑转移患者,推荐使用激素以暂时缓解继发性颅内压增高和脑水肿引起的症状,建议地塞米松起始剂量为4~8mg/d。有中度至重度占位效应相关症状的脑转移患者,建议提高地塞米松剂量,如16mg/d及以上[239]。手术切除脑转移瘤前应用糖皮质激素可减轻术前及术后脑水肿,放疗时应用糖皮质激素可减轻早期放疗反应。需警惕糖皮质激素的不良反应,防止消化性溃疡、血糖升高等。糖尿病患者必须慎用糖皮质激素。
3.利尿剂:呋塞米20~40mg静脉推注,依据颅内压增高程度、临床症状和24h尿量调整剂量和频次,但须严密监测血浆电解质变化,尤其是低钠和低钾血症。
4.抗癫痫治疗:部分肺癌脑转移患者在确诊前出现癫痫,亦有部分患者在病情发展过程中出现癫痫发作。应该根据患者病情适时应用抗癫痫药物,并警惕抗癫痫治疗潜在的不良反应,如肝功能异常、认知障碍和共济失调等。
六、预后
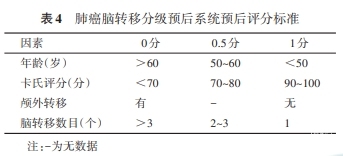
在GPA基础上,根据不同原发肿瘤脑转移的差异进一步提出了诊断特异性分级预后系统(diagnosis-specific graded prognostic assessment,DS-GPA)。在DS-GPA中,肺癌脑转移的预后因素包括年龄、KPS评分、颅外转移和脑转移数目,具体评分标准如表4。0~1分、1.5~2分、2.5~3分和3.5~4分NSCLC患者的中位OS分别为3.02、5.49、9.43和14.78个月;而0~1分、1.5~2分、2.5~3分和3.5~4分SCLC患者的中位OS分别为2.79、4.90、7.67和17.05个月。NSCLC和SCLC脑转移患者的中位OS分别为7.0和4.9个月[240]。肺癌脑转移分级预后系统预后评分标准见表4。
七、随诊
肺癌脑转移患者诊治后应该定期随诊并进行相应检查。检查方法包括病史、体格检查、血清肿瘤标志物检查、影像学检查等,频率一般为治疗后每2~3个月随诊1次,病情变化时随时就诊,以便根据病情变化及时采取相应的诊疗措施。
本指南参考了国际权威肺癌诊疗指南和最新研究进展,并结合中国国情制定。由于临床实践中肺癌脑转移患者存在较大的个体差异,需要根据具体情况决定每位患者的治疗策略,本指南仅供参考,不具有法律效力。
专家组成员
组长 石远凯(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室,航天中心医院肿瘤中心)
执笔人
总执笔人 石远凯(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术 北京市重点实验室,航天中心医院肿瘤中心)
头颅MRI部分执笔人 张红梅(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院影像诊断科)、万丽娟(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院影像诊断科)
头颅CT部分执笔人 王建卫(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院影像诊断科)
PET-CT部分执笔人 刘瑛(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院核医学科)
分子病理检测部分执笔人 王征(国家老年医学中心 北京医院病理科)
血清肿瘤标志物部分执笔人 韩晓红(中国医学科学院北京协和医院临床药理中心 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)
外科手术治疗部分执笔人 李学记(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院神经外科)
放射治疗部分执笔人 邓垒(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院放射治疗科)
内科治疗部分执笔人 石远凯(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室,航天中心医院肿瘤中心)
专家组成员(按姓氏汉语拼音字母排序) 艾斌(北京医院肿瘤内科)、仓顺东(河南省人民医院肿瘤内科)、陈军(天津医科大学总医院胸外科)、陈骏(大连医科大学附属第二医院肿瘤内科)、崔久嵬(吉林大学白求恩第一医院肿瘤内科)、邓垒(国家癌症中心国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院放射治疗科)、董晓荣(华中科技大学同济医学院附属协和医院肿瘤内科)、丁翠敏(河北医科大学第四医院呼吸内科)、顾康生(安徽医科大学第一附属医院肿瘤内科)、桂琳(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)、郭其森(山东省肿瘤医院肿瘤内科)、郭人花(南京医科大学第一附属医院肿瘤科)、韩晓红(中国医学科学院北京协和医院临床药理中心 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)、郝学志(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)、何志勇(福建省肿瘤医院肿瘤内科)、胡兴胜(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)、胡长路(安徽省肿瘤医院肿瘤内科)、黄鼎智(天津市肿瘤医院肿瘤内科)、黄建安(苏州大学附属第一医院呼吸与危重症医学科)、林冬梅(北京大学肿瘤医院病理科)、林华(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院病案室)、刘鹏(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)、刘尚梅(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院病理科)、刘晓晴(解放军总医院第五医学中心肿瘤内科)、刘雨桃(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)、刘云鹏(中国医科大学附属第一医院肿瘤内科)、刘瑛(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院核医学科)、刘文杨(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院放射治疗科)、刘基巍(大连医科大学附属第一医院肿瘤科)、柳江(新疆维吾尔自治区人民医院肿瘤内科)、李学记(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院神经外科)、李恩孝(西安交通大学第一附属医院肿瘤内科)、李醒亚(郑州大学第一附属医院肿瘤科)、李蒙(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院影像诊断科)、万丽娟(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院影像诊断科)、聂立功(北京大学第一医院呼吸与危重症医学科)、马克威(吉林大学白求恩第一医院肿瘤内科)、马丽(北京胸科医院肿瘤科)、潘跃银(安徽省立医院肿瘤内科)、郏博(北京大学肿瘤医院暨北京市肿瘤防治研究所胸部肿瘤内一科恶性肿瘤发病机制及转化研究教育部重点实验室北京大学肿瘤医院内蒙古医院内蒙古医科大学附属肿瘤医院胸部肿瘤内科内蒙古自治区癌症中心)、曲宝林(解放军总医院放射治疗科)、沈波(江苏省肿瘤医院肿瘤内科)、石建华(临沂市肿瘤医院肿瘤内科)、史美祺(江苏省肿瘤医院肿瘤内科)、石远凯(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室,航天中心医院肿瘤中心)、宋霞(山西省肿瘤医院呼吸内科)、宋之乙(中日友好医院胸外科)、宋飞雪(兰州大学第二附属医院肿瘤内科)、陶丹(重庆大学附属肿瘤医院肿瘤放射治疗中心)、陶云霞(徐州医科大学附属医院肿瘤内科)、王彩莲(东南大学附属中大医院肿瘤科)、王长利(天津医科大学附属肿瘤医院肺部肿瘤科)、汪麟(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)、王东(陆军军医大学大坪医院肿瘤科)、王华庆(天津市人民医院肿瘤内科)、王佳蕾(复旦大学附属肿瘤医院胸部肿瘤内科)、王孟昭(中国医学科学院北京协和医院呼吸与危重症医学科)、王章桂(航天中心医院肿瘤中心)、王征(北京医院病理科)、王子平(北京大学肿瘤医院胸部肿瘤内科)、王建卫(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院影像诊断科)、王希成(广东药科大学附属第一医院放疗科)、吴世凯(北京大学第一医院肿瘤内科)、吴密璐(青海大学附属医院肿瘤内科)、吴宁(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院影像诊断科、核医学科)、伍钢(华中科技大学同济医学院附属协和医院肿瘤中心)、信涛(哈尔滨医科大学附属第二医院肿瘤内科)、邢镨元(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)、肖文华(解放军总医院第一附属医院肿瘤内科)、杨建良(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)、杨磊(甘肃省肿瘤医院呼吸内科)、杨晟(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)、杨树军(河南省肿瘤医院肿瘤内科)、杨向红(中国医科大学附属第二医院病理科)、杨润祥(云南省肿瘤医院肿瘤内科)、余萍(四川省肿瘤医院肿瘤内科)、于雁(哈尔滨医科大学附属肿瘤医院肿瘤内科)、姚煜(西安交通大学附属第一医院肿瘤内科)、于国华(潍坊市人民医院肿瘤内科)、藏爱民(河北大学附属医院肿瘤内科)、曾瑄(北京协和医院病理科)、张贺龙(空军军医大学唐都医院肿瘤内科)、张俊萍(山西白求恩医院肿瘤内科)、张兰军(中山大学附属肿瘤医院胸外科)、张力(中国医学科学院北京协和医院呼吸与危重症医学科)、张沂平(浙江省肿瘤医院肿瘤内科)、张红梅(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院影像诊断科)、张雯杰(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院核医学科)、赵仁(宁夏医科大学总医院肿瘤医院放疗科)、赵琼[树兰(杭州)医院胸部肿瘤中心]、赵艳秋(河南省肿瘤医院肿瘤内科)、周生余(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)、钟巧凤(福建省肿瘤医院胸部肿瘤内科)、周宗玫(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院放射治疗科)
学术秘书(按姓氏汉语拼音字母排序) 陈馨蕊(解放军总医院第二医学中心肿瘤科)、高茹云、黄莉玲、唐乐、谢祖成、杨梦薇(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院内科 重大疾病创新药早期临床试验评价关键技术北京市重点实验室)、朱豪华(航天中心医院肿瘤中心)
利益冲突 作者声明不存在利益冲突
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。





