中华医学会神经病学分会头痛协作组 中国卒中学会头痛分会
通信作者:张锐,郑州大学第一附属医院神经内科,郑州450052,Email:ruizhangyy@126.com;王永刚,首都医科大学附属北京天坛医院神经病学中心头痛科,北京100070,Email:w100yg@163.com
DOI:10.3760/cma.j.cn113694-20250818-00486
引用本文:中华医学会神经病学分会头痛协作组,中国卒中学会头痛分会.药物过度使用性头痛诊断与治疗中国专家共识2025(中华医学会神经病学分会第一版)[J].中华神经科杂志,2026,59(1):18-33.DOI:10.3760/cma.j.cn113694-20250818-00486
【摘要】药物过度使用性头痛是由于原发性头痛预防性治疗不充分所导致的继发性头痛,致残性强、经济负担重。我国药物过度使用性头痛患病率高、诊断率低。中华医学会神经病学分会头痛协作组、中国卒中学会头痛分会专家结合国内外临床研究制订本共识,旨在提高以神经科医生为主体的临床医生对药物过度使用性头痛的认识,规范药物过度使用性头痛的全程化管理。
【关键词】头痛;药物过度使用性头痛;诊断;治疗;共识

药物过度使用性头痛(medication overuse headache,MOH)是一种常见的慢性继发性头痛[1-2],是指由于原发性头痛未及时启动预防性治疗或者预防治疗无效导致患者频繁应用急性止痛药,导致头痛发作频率增加及慢性化。MOH作为头痛疾病中经济负担最重的类型,其疾病成本是偏头痛的3倍,是紧张型头痛的10倍[3]。2017年发表的全球神经系统疾病负担调查结果显示,MOH是导致伤残调整寿命年(disability-adjusted life-years)增加的第6大原因[4]。
MOH一般人群年患病率约为0.5%~7.2%[5]。我国MOH诊断率较低[6],导致MOH发生的部分原因是临床医生对该疾病的概念及风险认识不足。基于目前国内MOH诊疗现状,中华医学会神经病学分会头痛协作组、中国卒中学会头痛分会各位专家参考近年来多个临床研究及国外多部指南共识,结合我国国情撰写本共识,旨在指导以神经科为主体的临床医生开展对MOH的全程管理、进行规范化诊疗、降低MOH的疾病负担、减少医疗资源消耗、改善患者的生活质量。
中华医学会神经病学分会头痛协作组、中国卒中学会头痛分会遵循循证医学原则,参考中华医学会指南及共识制订方法与标准[7],并根据我国MOH诊断治疗的国情制订本共识(推荐强度和证据等级标准详见表1)。

病理生理机制
原发性头痛若未得到及时或有效的预防性治疗,易进展为MOH。预防性治疗疗效不佳的常见因素包括合并精神障碍、睡眠障碍、肥胖和痛觉过敏等共病。MOH的病理生理机制主要涉及奖赏系统失调与痛觉中枢敏化,二者通过多系统交互形成恶性循环,遗传与环境因素也参与其中。

一、奖赏系统失调
中脑多巴胺奖赏系统(mesolimbic dopamine reward system)是调控奖励、动机、愉悦感和强化学习的核心神经网络。主要由中脑腹侧被盖区(ventral tegmental area,VTA)及其投射的多巴胺能神经元组成,这些神经元通过释放多巴胺调节与奖赏相关的行为。影像学研究结果显示:MOH患者负责高级决策行为的腹内侧前额叶皮质及多巴胺能神经元富集的黑质/腹侧被盖区复合体呈现显著功能减退[8]。静息态功能磁共振成像研究发现:MOH的形成与伏隔核及背侧吻侧壳核功能连接异常有关,这两个脑区分别在奖赏驱动通路及习惯形成中发挥重要作用。楔前叶作为情景记忆存储与自我状态监控的关键脑区,在MOH患者中出现功能连接重组。基础研究证实:药物通过激活VTA多巴胺神经元,短期内增加伏隔核多巴胺释放,产生愉悦感和疼痛缓解,但长期使用引发多巴胺D2受体下调,需增加药量以缓解头痛。阿片类药物过度使用还可干扰内源性阿片肽的生理平衡,从而使得镇痛阈值增高[9-10]。而前额叶皮质神经元突触可塑性损伤会削弱其对冲动用药的抑制作用,形成“失控性用药”行为[9]。

二、中枢敏化
MOH患者外周伤害感受器阈值下降,中枢上行伤害感受传递通路敏化,下行疼痛调节功能障碍,从而导致头痛慢性化。影像学研究结果显示:MOH患者海马、皮质后联合、小脑、眶额叶皮质等多脑区结构改变。导水管周围灰质、丘脑和腹侧纹状体等疼痛相关区域灰质体积更大[11]。基础研究证实,慢性药物暴露导致三叉神经尾核(trigeminal nucleus caudalis)和脊髓背角神经元N-甲基-D-天冬氨酸受体(N-methyl-D-aspartic acid receptor)磷酸化,从而使谷氨酸能信号增强,增强钙内流,引发神经元超兴奋[12]。长期使用止痛药导致降钙素基因相关肽(calcitonin gene related peptide,CGRP)释放反弹性升高,促进头痛慢性化。下行抑制系统包括中脑导水管周围灰质及延髓头端腹内侧区功能受损,使得5-羟色胺(serotonin)和去甲肾上腺素(norepinephrine)减少,促痛物质如CGRP、P物质等释放增加,导致痛觉抑制失效。星形胶质细胞和小胶质细胞释放促炎因子(IL-1β、TNF-α),通过Toll样受体4(Toll-like receptor 4,TLR4)、核因子κB(nuclear factor kappa-light-chain-enhancer of activated B cells,NF-κB)通路增强谷氨酸能突触传递,加剧中枢敏化[13]。

三、遗传因素
血管紧张素转换酶(angiotensin-converting enzyme,ACE)、脑源性神经营养因子(brain-derived neurotrophic factor,BDNF)、儿茶酚-O-甲基转移酶(catechol-O-methyltransferase,COMT)、5-羟色胺转运体(serotonin transporter,SLC6A4)等基因与单胺类神经递质代谢通路异常、5-羟色胺和多巴胺传递或药物依赖相关。研究结果显示上述基因多态性可能与MOH相关[5]。

四、行为与心理因素
MOH的形成涉及多方面的行为与心理因素交互作用:(1)患者对急性药物反应不佳、担心头痛影响重要活动及停药后症状反弹,促发心理依赖和仪式性用药行为[14];(2)危险因素(痛觉超敏、精神障碍、低教育水平)和异常用药行为(如联用滴眼液等非头痛药物)加重药物依赖风险[15];(3)适应不良认知模式(疼痛灾难化、预期焦虑、强迫用药)及头痛恐惧症(对头痛发作/加重的病态恐惧)导致过早、过量用药[16-17]。这些因素通过降低用药阈值,共同导致MOH的发生发展。
分类
2018年《国际头痛分类-第三版》(International Classification of Headache Disorders,3rdedition,ICHD-3)[18]根据过度使用药物的种类将MOH分为麦角胺过度使用性头痛、曲普坦过度使用性头痛、非阿片类止痛药过度使用性头痛、阿片类药物过度使用性头痛、复方止痛药过度使用性头痛、缘于多种并非单一种类药物的MOH、缘于未经证实的多种药物种类的MOH和缘于其他药物的MOH共8个类型(表2)。
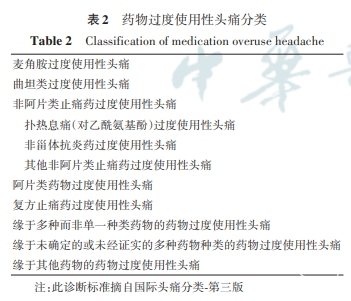
诊断和鉴别诊断
MOH的诊断主要基于病史、原发性头痛类型以及急性期药物应用的时间、种类和剂量。在诊断MOH之前,需明确急性期止痛药物过度使用(medication overuse,MO)的概念。过度使用是指使用单纯成分的非甾体抗炎药(non-steroidal anti-inflammatory drugs,NSAIDs)或对乙酰氨基酚≥15d/月,或使用复方止痛药、曲普坦类、麦角胺类或阿片类药物≥10d/月[19],但尚未导致原发性头痛的慢性化。

一、MOH临床表现
MOH患者女性多见,男女比例约为1∶1.4~1∶4.7[20],发病高峰在40岁左右,并呈现一定的地区差异。MOH患者罹患的原发性头痛以偏头痛为主,其次是紧张型头痛。MOH临床特征具有一定的异质性,患者MOH类型与原发头痛类型及过度使用药物类型有关。麦角胺类药物过度使用多表现为紧张型头痛特征,进展为MOH的时间平均约为2.7年;曲普坦类药物过度使用则更倾向于偏头痛样表现且头痛持续时间较长,其进展时间较短,平均为1.7年;而含巴比妥类的复方止痛药具有较高的MOH发生风险,进展时间相对较长,平均需4.8年[21]。详细的问诊对MOH的诊断至关重要,可通过依赖严重程度量表(Severity of Dependence Scale,SDS)评估原发性头痛患者出现MOH的风险,问诊内容见表3和表4。

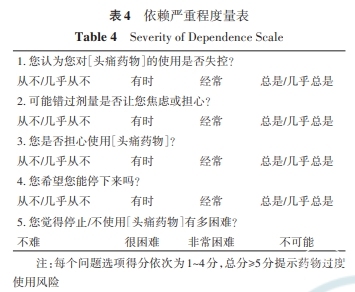

二、MOH合并症
MOH患者容易合并焦虑和(或)抑郁,这些精神心理共病不仅与MOH的致残性密切相关,更是治疗反应不良的重要预测因素[22-23]。强迫症人格特征在MOH患者中常见[24]。一些患者也表现出成瘾行为,成瘾行为的存在是MOH不良预后的预测因素[25-26]。MOH患者更容易出现慢性肌肉骨骼疾病、甲状腺功能减退、消化系统疾病(出血或溃疡、肠易激综合征)、代谢综合征、高血压、肥胖等[27-29]。

三、诊断标准
参照ICHD-3诊断标准:A.原发性头痛患者每月头痛发作的天数≥15d;B.规律服用过量的头痛急性治疗或对症治疗药物3个月以上;C.不能用ICHD-3中的其他诊断更好地解释。
诊断原则:(1)需首先诊断原发性头痛;(2)是否达到了慢性原发性头痛的诊断标准;(3)按照诊断标准明确不同急性止痛药物每月服用天数是否符合诊断标准。
常见的慢性原发性头痛如下。
1.慢性偏头痛(chronic migraine):临床最常见的导致MOH的慢性原发性头痛,发生于有发作性偏头痛史的患者。每月至少15d出现头痛,持续至少3个月,且每月符合偏头痛特点的头痛天数至少8d。约半数以上的慢性偏头痛患者合并有药物过度使用[30]。
2.慢性紧张型头痛(chronic tension type headache):从频发性紧张型头痛进展而来,每月至少15d出现头痛,持续至少3个月。典型的头痛为轻到中度双侧压迫性或紧箍样头痛,时间持续几小时到几天或不间断。日常体力活动不受影响,可合并MOH。
诊断标准见表5。不同亚型MOH诊断标准见表6。

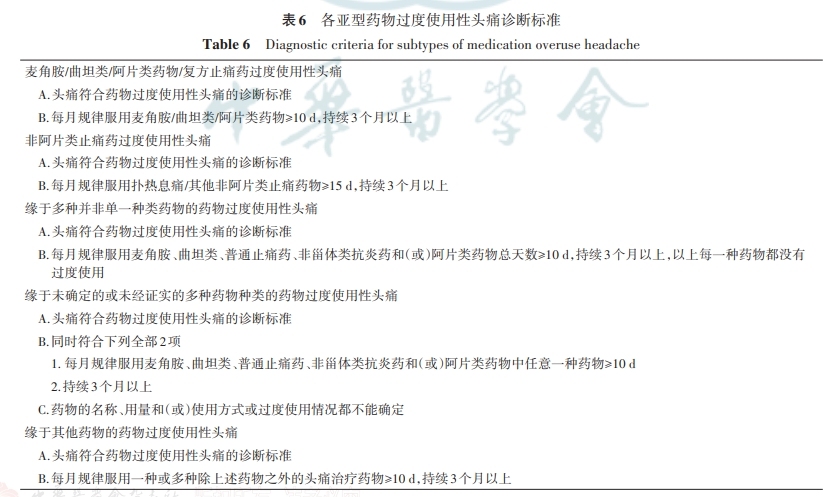

四、鉴别诊断
(一)其他继发性头痛
MOH需要与其他继发性头痛鉴别,特别是存在一些“预警征象”时提示可能存在其他继发性头痛。“预警征象”包括:包括发热在内的全身症状;肿瘤病史;神经功能缺损(包括意识下降);头痛的突然发作(霹雳头痛);老龄(比如65岁以后发病);头痛模式改变或头痛新发;体位性头痛;因喷嚏、咳嗽(Valsalva动作)或运动加重;视乳头水肿;进展性头痛和非典型表现;妊娠和产褥期;伴自主神经症状的眼痛;创伤后发作头痛;免疫系统的病变(如HIV感染);头痛发作时使用新药[31]。
(二)与原发性头痛鉴别
1.持续性偏侧头痛(hemicrania continua):严格单侧的持续性头痛,伴同侧头面部自主神经症状,有时伴偏头痛症状,吲哚美辛治疗有效。在三叉自主神经痛患者中,仅在合并偏头痛或有偏头痛家族史的患者中观察到MOH。
2.新发每日持续性头痛(new daily persistent headache):多数患者可准确地描述其头痛开始的确切日期,且发病24h内头痛持续不缓解,患者通常无既往头痛史。
预防
在原发性头痛患者诊疗过程中,识别导致MOH的危险因素及不同类型止痛药物的危险分层,及时启动原发性头痛的预防性治疗是预防MOH发生的关键。

一、MOH危险因素
导致MOH的危险因素包括:女性、每月头痛天数大于10d、社交活动少、其他慢性疼痛、压力、缺乏锻炼、肥胖、吸烟、物质滥用、合并焦虑或抑郁[32-33]。对于合并危险因素的原发性头痛患者,建议尽早启动个体化预防性治疗。

二、急性止痛药物危险分层
MO患者发展成为MOH的时间,取决于所应用止痛药类型。研究结果显示与对乙酰氨基酚相比,阿片类及巴比妥类复方制剂可使MOH风险增加2倍左右,应用曲普坦类、阿片类和复方止痛药过量的患者更早出现MOH[34]。将易导致MOH药物进行危险分层:高风险药物包括阿片类、巴比妥类及曲普坦类药物;中风险药物包括含有咖啡因、阿司匹林和(或)对乙酰氨基酚的复方止痛药;低风险药物为非甾体抗炎药及对乙酰氨基酚。诊疗过程中注意随访原发性头痛患者每月急性止痛药使用频率与数量。
治疗
MOH患者治疗包括健康教育、停用过度使用药物、预防性治疗和非药物治疗。需根据患者原发头痛类型、过度使用药物的种类及合并症进行个体化管理,治疗流程见图1。
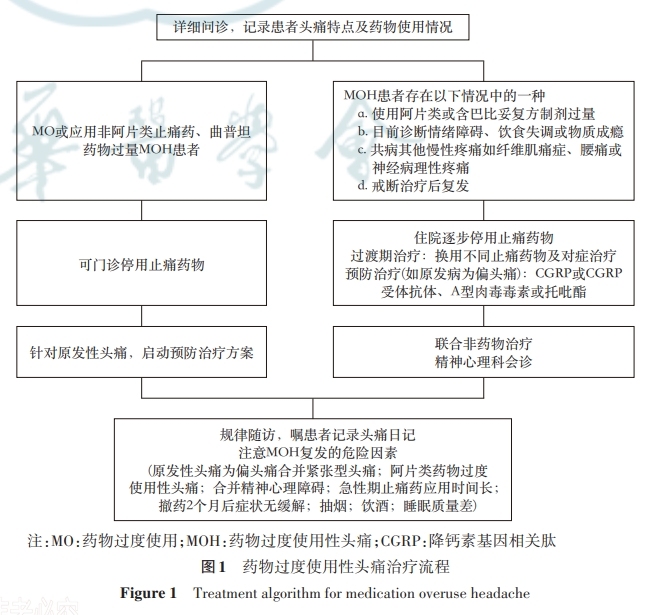

一、健康教育
原发性头痛患者教育是MOH管理的基石。研究结果显示,健康教育可显著减少MOH患者的头痛频率和止痛药物的应用次数[35],健康教育的效果可持续16个月[36]。对于过度使用非阿片类药物、苯二氮䓬类药物以及巴比妥类药物的MOH患者而言,单纯强化健康教育在减少头痛频率以及减少药物过度使用方面的效果,与传统的一般健康教育加上早期使用激素以及预防性药物的方案效果相近[37]。
MOH患者教育需包括:(1)告知MOH的概念,以及药物过度使用导致MOH的可能机制;(2)告知停用过度使用药物对于治疗MOH的重要性,以及停药之后可能出现的症状;(3)告知MOH患者在治愈(即不再符合ICHD-3中MOH的诊断标准)后仍有复发风险,1年内复发风险最高,应该注意加强随访[20]。
推荐意见:建议所有MOH患者接受健康教育,单纯患者教育可改善患者症状(Ⅱ级推荐,B级证据)。

二、撤药管理
(一)撤药方案
停用过度使用的药物是MOH治疗成功的重要干预策略。一项纳入27项随机对照试验(randomized controlled trial,RCT)的系统评价结果表明,完全撤药联合预防性治疗的疗效优于单纯撤药方案[38]。Carlsen等[39]通过RCT研究比较了3种撤药方案,即完全撤药联合预防性治疗、单纯撤药、单纯预防性治疗后6个月和12个月时的疗效,结果表明完全撤药联合预防性治疗组每月偏头痛天数减少≥50%的患者比例显著高于其他两组。推荐意见:完全撤药同步启动预防性治疗可作为MOH患者首选方案(Ⅰ级推荐,A级证据)。
(二)撤药速度
对于立即停药和逐步撤药目前尚无统一方案。在过度使用曲普坦类、麦角胺类、对乙酰氨基酚、NSAIDS和复方止痛药的MOH患者中,Engelstoft等[40]比较了立即停药和逐步撤药(允许每周使用2次急性止痛药物)2种不同的撤药方案,结果表明立即停药的有效性优于逐步撤药组;另一项RCT研究结果也表明,立即停药组6个月时的每月头痛天数减少比例显著高于逐步撤药组(46%比22%)[41]。
推荐意见:对于过度使用曲普坦类、麦角胺类、对乙酰氨基酚、NASIDs和复方止痛药的MOH患者,可立即停药(Ⅰ级推荐,B级证据)。但是,对于阿片类药物或巴比妥类药物过度使用的MOH患者,早期完全停药后可能出现严重戒断反应,推荐采用逐步撤药的方式。
(三)住院指征
撤药初期可能会诱发戒断反应,从而导致MOH患者依从性降低甚至撤药失败。因此,是否需要住院治疗也是撤药时医患共同关注的问题。研究结果表明,对于合并严重精神症状、药物成瘾/滥用、多种类型止痛药过度使用、既往撤药失败的MOH患者,住院治疗的撤药成功率显著高于门诊治疗[42];但是,对于无合并上述危险因素的MOH患者,门诊和住院患者的慢性偏头痛转化为发作性偏头痛的比例,以及MOH终止率相近[42-43]。
推荐意见:对于无合并危险因素的MOH患者首选门诊撤药,而对于合并严重精神症状、药物成瘾/滥用、多种类型止痛药过度使用、既往撤药失败的MOH患者推荐住院撤药治疗(Ⅱ级推荐,B级证据)。
(四)过渡期治疗
撤药初期可能会导致MOH患者头痛加剧、恶心呕吐、心悸、焦虑、睡眠障碍等戒断症状,头痛加剧的发生率约70%,胃肠道症状约20%~40%,情绪波动或失眠约40%~60%,这个过程通常维持2~7d[44]。因此,这段时间通常需要药物缓解戒断症状、降低MOH复发风险,称之为“过渡期治疗”。目前临床上治疗方法包括:皮质类固醇激素、急性止痛药、补液支持、镇静剂和止吐药。
1.戒断性头痛:(1)皮质类固醇激素:一项开放标签研究结果显示,60mg/d泼尼松(每2天减少20mg)可减少撤药初期6d内严重头痛发作次数、1个月内头痛发作次数和急性止痛药物使用[45];另一项回顾性研究结果显示,甲泼尼龙联合地西泮静脉注射5d可减少撤药3个月时头痛发作次数和急性止痛药物使用频率[46]。(2)急性止痛药物:急性止痛药可用于戒断性头痛,但是需选择与原有过度使用药物机制不同的药物,如曲普坦药物过度使用则选择对乙酰氨基酚、萘普生、布洛芬等。目前尚无针对撤药期间戒断性头痛使用急性止痛药物频率的相关研究报道,临床上建议急性止痛药物使用少于2次/周[44,47]。CGRP受体拮抗剂如瑞美吉泮等不会增加MOH风险[48]。真实世界研究结果显示,按需应用瑞美吉泮49~52周可显著降低使用止痛药患者比例[49]。一项RCT研究比较了口服塞来昔布(400mg/d)和泼尼松(75mg/d)在MOH戒断期间的疗效,结果表明,与泼尼松组相比,塞来昔布组撤药后3周内头痛发作程度明显减轻[50]。(3)丙戊酸盐:研究报道丙戊酸盐静脉注射负荷剂量15mg/kg,每8小时序贯注射5mg/kg的方案,对于80%的MOH患者戒断性头痛有效并且耐受性良好[51]。
推荐意见:(1)急性止痛药需选择与原有过度使用药物机制不同的药物,瑞美吉泮可用于偏头痛合并MOH患者戒断性头痛的急性止痛治疗(Ⅱ级推荐,B级证据);(2)塞来昔布(400mg/d)连续使用5d,可用于减少戒断性头痛发作(Ⅲ级推荐,B级证据);(3)皮质类固醇激素、丙戊酸盐可用于减少戒断性头痛发作(Ⅲ级推荐,C级证据)。
2.胃肠道症状:一项纳入16项临床研究的荟萃分析结果表明[52],甲氧氯普胺10mg肌内注射/口服可显著改善偏头痛患者恶心、呕吐等胃肠道症状,其不良反应主要包括嗜睡和潜在锥体外系反应风险,如急性肌张力障碍或静坐不能。
推荐意见:甲氧氯普胺可用于戒断时胃肠道症状(Ⅱ级推荐,A级证据),但是需警惕其不良反应。
3.情绪和睡眠障碍:回顾性研究结果表明,氯丙嗪25~50mg肌内注射/口服可改善慢性偏头痛合并MOH患者撤药期间焦虑和睡眠障碍,但因其可能导致低血压和过度镇静,应避免长期使用[53]。观察性研究结果表明,三环类药物阿米替林(6.25~12.50mg)能够改善撤药初期的焦虑和抑郁症状,其不良反应包括口干、嗜睡、注意力减退等[54];还有研究报道另一种三环类药物多塞平对缓解戒断时睡眠障碍和焦虑症状有效,但需要警惕用药期间潜在不良反应(如体重增加和低血压)[55]。
推荐意见:三环类药物(阿米替林、多塞平)、氯丙嗪可用于戒断时睡眠障碍和焦虑抑郁症状(Ⅲ级推荐,C级证据),但是需小剂量起始、个体化治疗,注意随访和监测不良反应。

三、预防性治疗
预防性治疗的目标:停用过度使用药物,且原发性头痛天数控制在每月4d以内。预防性治疗的原则:根据患者原发性头痛的类型、对药物的耐受性、药物使用便利性、经济学成本、共患疾病以及特殊人群等因素,个性化选择治疗方案。
(一)预防性治疗应用时机
COMOESTAS研究中,376例患者戒药同时添加预防性治疗。6个月后2/3的患者不再符合MOH诊断标准,47%的慢性头痛患者转化为发作性头痛[56]。一项系统评价纳入27项研究,结果显示与单戒药及未接受治疗相比,戒药同时联用预防性治疗患者获益最大。12个月头痛天数减少50%以上比例达53%,而单戒药组仅25%[57]。
推荐意见:建议MOH患者戒药同时联用预防性治疗药物(Ⅰ级推荐,A级证据)。
(二)预防性治疗药物
应根据MOH患者原发性头痛类型选择预防性治疗药物。因现有临床研究纳入人群多为偏头痛合并MOH患者,因此本共识主要针对偏头痛合并MOH患者预防性治疗给出建议。在临床应用中应充分评估个体差异与长期安全性。
1.CGRP类药物:具体种类如下。
(1)CGRP单克隆抗体:具体药物如下。
a.依普奈珠单抗(eptinezumab):一项随机、双盲、安慰剂对照研究(PROMISE-2)的亚组分析结果显示,依普奈珠单抗(100mg或300mg静脉输注,间隔3个月,共2次)可显著改善慢性偏头痛合并MOH患者的头痛频率和急性用药次数,且用药后1d即见疗效[58-59]。此外,对其他CGRP单抗疗效不佳的患者,依普奈珠单抗仍可能有效[60]。一项随机、双盲、安慰剂对照研究(DELIVER)预先设定的MOH亚组分析结果显示,在既往预防性治疗失败2~4次的偏头痛合并MOH患者中,依普奈珠单抗每季度100mg和300mg仍可分别显著减少第1~12周每月偏头痛天数5.6和7.3d(安慰剂组2.3d)[61]。
一项3期、单臂、开放标签研究(PREVAIL)预先设定的MOH亚组分析结果显示,依普奈珠单抗每季度300mg能显著且在2年内持续改善患者失能[62]。在此基础上,RESOLUTION研究(随机、双盲、多中心4期临床试验)进一步证实,结合简要教育干预后,100mg依普奈珠单抗在慢性偏头痛合并MOH患者中疗效显著。608例患者按1∶1比例接受治疗,596例完成双盲期,基线每月偏头痛天数为20.9d。结果显示,第1~4周每月偏头痛天数较基线减少6.9d(对比安慰剂3.7d),第1~12周持续改善(7.3d比4.4d),疼痛强度和急性用药频率亦明显下降[63-64]。同时,患者报告的头痛负担、生活质量和工作效率等也较安慰剂组显著改善[65]。
b.瑞玛奈珠单抗(fremanezumab):一项随机、双盲、安慰剂对照研究(HALO-CM研究)的亚组分析评估了瑞玛奈珠单抗对慢性偏头痛合并MO患者的预防性治疗效果[66]。该研究共分3组:第一组为瑞玛奈珠单抗675mg皮下注射,随后每月225mg;第二组为瑞玛奈珠单抗675mg皮下注射,随后每月注射安慰剂;第三组为安慰剂组。共随访3个月。结果表明,两种用法的瑞玛奈珠单抗与安慰剂相比均可显著改善头痛频率及止痛药物使用次数,但是第一组可能效果更好。
c.加卡奈珠单抗(galcanezumab):三项随机、双盲、安慰剂对照研究的亚组分析评估了加卡奈珠单抗对偏头痛伴MO(EVOLVE-1研究和EVOLVE-2研究)或慢性偏头痛(REGAIN研究)合并MOH患者的预防性治疗效果[67]。加卡奈珠单抗用法为120/240mg,每月1次,皮下注射。随访时间为3或6个月。与安慰剂相比,两种剂量的加卡奈珠单抗均可改善患者头痛频率及急性止痛药物应用次数。
(2)CGRP受体单克隆抗体:依瑞奈尤单抗(erenumab):一项随机、双盲、安慰剂对照研究的亚组分析评估了依瑞奈尤单抗对慢性偏头痛合并MOH患者的预防性治疗效果[68]。依瑞奈尤单抗的用法为每次70/140mg,每月1次,皮下注射,随访期为3个月。与安慰剂相比,两种剂量的依瑞奈尤单抗均可相似地改善MOH患者头痛频率及急性止痛药物使用次数。延长至1年的随访进一步证实了依瑞奈尤单抗长期应用的有效性和安全性[69]。此外,对于既往多次预防性治疗失败的患者,140mg的剂量的疗效优于70mg的剂量[70-71]。一项4期随机安慰剂对照研究评估了依瑞奈尤单抗治疗慢性偏头痛合并非阿片类MOH的安全性和有效性,结果显示24周治疗期间,70mg和140mg依瑞奈尤单抗组的持续MOH缓解率均显著高于安慰剂组(49.5%比37.6%,P=0.02;61.3%比37.6%,P<0.001),70mg和140mg依瑞奈尤单抗组患者每月平均急性止痛药物天数较基线均显著下降,且变化幅度显著优于安慰剂组(-7.83d,P=0.033;-9.35d,P<0.001)[72]。
(3)CGRP受体拮抗剂:具体药物如下。
a.阿托吉泮(atogepant):一项随机、双盲、安慰剂对照研究的亚组分析评估了阿托吉泮对慢性偏头痛合并MOH患者的预防性治疗效果。阿托吉泮的用法为每次30mg,每日2次,或每次60mg,每日1次[73]。与安慰剂相比,两种用法的阿托吉泮均可显著改善患者头痛频率及急性止痛药物使用次数,但是每日2次的用法可能更有优势。
b.瑞美吉泮(rimegepant):一项真实世界研究数据分析结果显示,瑞美吉泮治疗6个月内,38.3%的患者完全停止使用阿片类药物[74]。瑞美吉泮治疗49~52周,使用镇痛药和止痛药的患者比例较基线下降47.7%。另一项研究结果显示,瑞美吉泮治疗3个月后,在不同随访时间点,MOH患病率均下降18.0%~29.2%[49]。
推荐意见:依普奈珠单抗可用于慢性偏头痛合并MOH的预防性治疗。推荐用法为100mg静脉输注,每3个月1次,对于效果不佳或既往多次预防性治疗失败的患者,可将剂量增至300mg静脉输注,每3个月1次(Ⅰ级推荐,A级证据)。(2)瑞玛奈珠单抗可用于慢性偏头痛合并MO的预防性治疗。
推荐治疗开始时的负荷剂量为675mg,之后每月给药225mg,皮下注射(Ⅱ级推荐,A级证据)。(3)加卡奈珠单抗可用于慢性偏头痛合并MO的预防性治疗。推荐治疗开始时的负荷剂量为240mg,之后每月给药120mg,皮下注射(Ⅱ级推荐,A级证据)。(4)依瑞奈尤单抗可用于慢性偏头痛合并MOH的预防性治疗。推荐剂量为70mg,皮下注射,每月1次,对于效果不佳或既往多次预防性治疗失败的患者,可将剂量增至140mg,每月1次(Ⅰ级推荐,A级证据)。(5)阿托吉泮可用于慢性偏头痛合并MOH的预防性治疗。推荐剂量每次30mg,每日2次口服(Ⅱ级推荐,A级证据)。(6)瑞美吉泮可用于慢性偏头痛合并MOH的预防性治疗。推荐剂量75mg,隔日服用(Ⅲ级推荐,C级证据)。
在临床应用CGRP类药物时,应充分评估个体差异与长期安全性。
2.注射用A型肉毒毒素:两项随机、双盲、安慰剂对照研究(PREEMPT1和PREEMPT2研究)的亚组分析评估了注射用A型肉毒毒素对慢性偏头痛合并MOH患者的预防性治疗效果。结果显示,治疗组每月头痛减少天数、每月偏头痛减少天数、中重度头痛减少天数等均显著优于安慰剂组[75]。一项纳入68例患者的RCT的亚组分析结果表明,注射用A型肉毒毒素可能对伴有颅周肌压痛的MOH患者效果更明显[76]。一项共纳入179例患者的随机、双盲、安慰剂对照试验结果显示,注射用A型肉毒毒素有降低慢性偏头痛合并MOH患者月头痛天数的趋势,但是结果差异无统计学意义(P=0.15)[77]。
推荐意见:局部注射用A型肉毒毒素可用于慢性偏头痛合并MOH的预防性治疗,特别适用于伴颅周肌肉压痛患者(Ⅱ级推荐,B级证据)。注射方法为:头颈部7块肌肉31个位点共注射155U,每个位点5U,隔12周1次。注意合并有重症肌无力、Lambert-Eaton综合征、肌萎缩侧索硬化等患者禁用。
3.托吡酯:一项多中心、随机、双盲、安慰剂对照研究,共纳入59例慢性偏头痛患者,其中合并MOH的患者占80.0%。结果显示托吡酯50~200mg/d可显著减少头痛天数[78]。合并MOH的亚组分析结果仍显示,托吡酯组头痛减少天数优于安慰剂组。托吡酯组不良事件发生率增高。最常见的不良反应为感觉异常,其次为恶心、头晕、消化不良、疲劳、认知功能下降等。另一项共纳入50例慢性偏头痛合并MOH患者的研究结果同样显示托吡酯100mg/d可显著减少每月头痛天数和每月止痛药物的服用量[79]。
推荐意见:托吡酯25~200mg/d口服可用于慢性偏头痛合并MOH的预防性治疗(Ⅱ级推荐,B级证据)。注意从低剂量开始逐渐加量,并注意相关不良反应,育龄期女性慎用。
4.丙戊酸盐(丙戊酸镁/丙戊酸钠):一项多中心、随机、双盲、安慰剂对照研究,共纳入88例无先兆偏头痛合并MO患者,干预组给予丙戊酸钠800mg/d,对照组给予安慰剂,两组均建议停用原过度使用的止痛药物,主要结局为第3个月头痛天数减少50%的患者比例。结果表明,干预组达到主要终点的患者比例、每月头痛减少的天数、每月使用止痛药减少的天数显著优于对照组,两组不良反应无显著差异[80]。
推荐意见:丙戊酸盐500~1500mg/d口服可用于偏头痛合并MOH的预防性治疗,注意育龄期女性慎用(Ⅲ级推荐,C级证据)。
5.阿米替林:阿米替林也常被应用于MOH的预防性治疗,且显示出一定的效果,但是研究中阿米替林只是用药方案之一或未进行随机对照设计[39,81-84]。
推荐意见:阿米替林(12.5~75.0mg/d)可用于MOH的预防性治疗,但需要进一步的证据支持(Ⅲ级推荐,C级证据)。
6.其他药物:一项开放标签的随机对照研究将120例MOH患者按1∶1∶1随机分为撤药加预防性药物治疗组、单独预防性药物治疗组和单纯撤药组。约一半的患者应用坎地沙坦作为预防性药物。3组6个月时头痛频率、止痛药物应用等均有所改善,但是撤药加预防性药物组在MOH治愈率上更有优势[39]。
普萘洛尔、美托洛尔、文拉法辛等也被用于MOH的预防性治疗[84],但是没有针对性的临床研究证实其效果。
推荐意见:坎地沙坦8~16mg/d口服可用于MOH的预防性治疗(Ⅲ级推荐,B级证据);普萘洛尔(50~200mg/d)、美托洛尔(50~200mg/d)、文拉法辛(75~150mg/d)等可尝试用于MOH的预防性治疗,但需要进一步的证据支持(Ⅲ级推荐,C级证据)。详见表7。
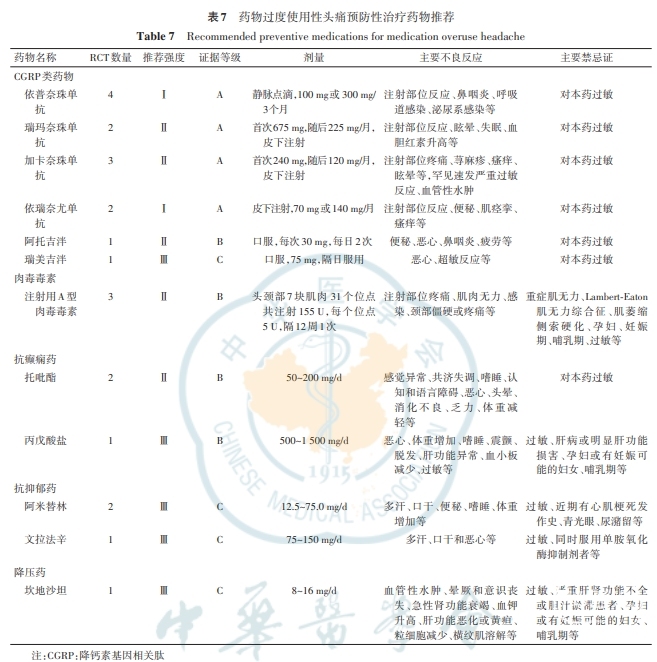
如原发性头痛为慢性紧张型头痛,则应根据《中国紧张型头痛诊断与治疗指南》[85]选择预防性药物。

四、非药物治疗
(一)针刺
一项随机对照研究的亚组分析结果表明,与托吡酯(25mg起始,增加至每天100mg)相比,持续12周共24次的针刺治疗(双侧攒竹穴、风池穴、太阳穴和印堂穴,得气后留针30min)可以显著降低MOH患者的头痛天数(针灸组50%反应率为70.8%,托吡酯组为20.0%)和止痛药物使用次数[86]。
(二)神经调控技术
虽然小样本(n=20)的临床研究结果表明阳性经颅直流电刺激偏头痛对侧初级运动皮质(每日1次,持续5d,每次20min,阳极刺激强度2mA)可降低MOH患者的头痛发作频率(50%反应率为70%,安慰剂组为20%)[87],但是另一项更大样本(n=135)的临床研究发现无论是阳性或者是阴性经颅直流电刺激,均不能降低MOH患者头痛频率及止痛药物应用次数[88]。
重复经颅磁刺激(repetitivetranscranialmagneticstimulation,rTMS)对MOH的效果不确切[89-90]。一项真实世界的前瞻性研究结果表明,单脉冲经颅磁刺激(设备放置在枕部,6Hz的0.9T脉冲,两次连续脉冲每天2次,递增至6次脉冲每天3次)治疗持续3个月可以将MOH的比例从52%降低到19%,持续12个月可以降低到8%。然而,RCT研究未能证明联合使用高频rTMS的效果优于单纯戒断治疗;但高频rTMS可诱发安慰剂效应,从而改善疼痛程度。
非侵入性神经调节技术,包括眶上经皮神经刺激、枕神经刺激、非侵入性迷走神经刺激等,均可有效预防和治疗偏头痛[91-95],并不受到是否存在MOH的影响。但这些方法是否对MOH有效尚缺乏有力证据,仍需要更大规模的随机试验来证实[96-97]。
(三)神经阻滞治疗
一项开放标签随机对照研究证实,枕大神经封闭(1ml2%利多卡因和1ml曲安奈德40mg/ml)效果优于常规治疗,进一步降低了MOH患者3个月后的头痛频率、时间和强度。一项对照试验结果表明,接受多次枕大神经阻滞(1%利多卡因)的曲普坦类MOH患者,出现了头痛天数和强度以及止痛药使用量的减少[98]。
(四)认知行为疗法
一项RCT证实,在MOH患者接受常规治疗之外,使用动机性访谈(motivationalinterviewing)方法进行12周的患者教育可以提高患者应对疼痛的能力,9个月随访可见痛觉应对量表评分的改善。另一项RCT结果显示,加入行为干预后MOH患者戒断成功率达86%,强化行为干预(包括在戒断疗法12周期间的健康教育、动机访谈和目的明确的活动计划)可提升有效率至93%,延长治疗时间有利于产生长期效果,并且强化行为干预可以减少6个月止痛药物使用天数[99]。另外,正念疗法及生物反馈技术可在常规预防性治疗的基础上进一步降低头痛频率和止痛药物应用次数[100-101]。
推荐意见:(1)针刺可用于MOH的辅助治疗(Ⅱ级推荐,B级证据);(2)经颅直流电刺激、rTMS等无创神经调控技术可尝试用于MOH的辅助治疗,但需要更多的证据支持(Ⅲ级推荐,C级证据);(3)枕大神经阻滞有助于MOH的治疗(Ⅲ级推荐,C级证据);(4)提倡综合系统的认知行为疗法(动机访谈、目的明确的活动计划、正念疗法、生物反馈技术等)作为MOH患者的合并治疗手段(Ⅱ级推荐,B级证据)。

五、MOH复发的预防
MOH短期预后较好,60%~83%的患者撤药1年后仍可保持无药物过度使用。10%~40%的患者出现复发[102],且大部分复发发生于撤药后1年内。
导致复发的高危因素包括:原发性头痛为偏头痛合并紧张型头痛、阿片类药物过度使用性头痛、合并精神心理障碍、急性期止痛药应用时间长、撤药2个月后症状无缓解、抽烟、饮酒、睡眠质量差等[103]。需早期识别危险因素,并建议患者坚持记录头痛日记,长期规律随访,降低复发风险。
(一)心理治疗
两项小型前瞻性观察研究分析了心理治疗的重要性。随访6个月(P=0.016)和12个月(P=0.047)后,接受短期心理治疗联合药物预防组的复发率明显低于仅接受药物预防组[104]。
(二)健康咨询及头痛日记
两项研究评估了健康咨询的重要性[105-106]。一项随机试验(n=60,完全随访100%)评估了与常规护理相比,在研究开始时(早期短暂干预)或6个月后(晚期短暂干预)由训练有素的普通专业人员进行短暂干预后的复发率。早期组在6个月时的复发率为4%,在16个月时为8.3%。晚期组未见复发。在接受过专门培训的护士参与的多学科治疗计划和密切随访的情况下,既往戒药不成功的患者复发率较低(15%)。通过纸质头痛日记和电子日记监测药物摄入以及密切随访(每2个月,包括电话),复发率非常低(6.5%)[107]。
(三)注重原发性头痛预防治疗
研究结果显示,原发性头痛预防用药不足是导致MOH复发的重要原因之一,两项应用肉毒毒素治疗慢性偏头痛合并MOH的观察性研究结果表明,规律应用肉毒毒素治疗,或联合其他预防性药物,经过2年的随访,患者均没有复发[108-109]。
推荐意见:(1)高复发风险患者接受心理治疗(Ⅲ级推荐,C级证据);(2)开展健康咨询(Ⅱ级推荐,B级证据),定期随访(Ⅲ级推荐,C级证据);(3)注重原发头痛管理,足量足疗程应用原发性头痛预防药物(Ⅲ级推荐,C级证据)。
MOH致残性高,疾病负担重,但原则上可防可治。本共识通过回顾相关临床研究,并结合国际指南及共识,对MOH的全流程管理提出推荐意见,旨在加强以神经科为主体的临床医生对该疾病的认识,减少MOH的发生,改善患者预后,减少社会及经济负担。
主要执笔者 张锐(郑州大学第一附属医院)、王永刚(首都医科大学附属北京天坛医院)、赵红如(苏州大学附属第一医院)、刘恺鸣(浙江大学医学院附属第二医院)、渠文生(华中科技大学同济医学院附属同济医院)、龚骊(上海交通大学医学院附属同仁医院)、雷琦(陕西省人民医院)、桂韦[中国科学技术大学附属第一医院(安徽省立医院)]
编写组成员(按姓名汉语拼音排序) 曹克刚(北京中医药大学东直门医院)、陈兰兰(江苏省苏北人民医院)、陈宁(四川大学华西医院)、陈玉娟(上海市第十人民医院)、程敏(北京大学人民医院)、董铭(吉林大学第一医院)、段智慧(郑州大学附属洛阳中心医院)、范秉林(广西壮族自治区人民医院)、方杰(厦门大学附属第一医院)、冯娟(中国医科大学附属盛京医院)、冯鹏(山西医科大学第二医院)、傅国恵(南阳市中心医院)、葛朝莉(深圳市第二人民医院)、谷文萍(中南大学湘雅医院)、郭继东(北华大学附属医院)、韩登峰(新疆医科大学第一附属医院)、黄培坚(上海交通大学医学院附属瑞金医院海南医院)、黄雪融(瑞安市人民医院)、黄永锋(榆林市第一医院)、焦燕(新疆维吾尔自治区人民医院)、经屏(武汉市中心医院)、李磊(哈尔滨医科大学附属第二医院)、李俐涛(河北省人民医院)、李强(淄博市中心医院)、李霞(浙江大学医学院附属第一医院)、李雅博(巴音郭楞蒙古自治州人民医院)、李云(大理大学第一附属医院)、廖松洁(中山大学附属第一医院)、刘斌(内蒙古自治区人民医院)、刘昌云(福建医科大学附属协和医院)、刘喷飓(首都医科大学附属北京安贞医院)、刘强(宁夏医科大学总医院)、刘小利(浙江医院)、刘怡(南昌大学第一附属医院)、刘永辉(广西中医药大学第一附属医院)、刘源香(山东中医药大学附属医院)、刘志勤(西安市中心医院)、满玉红(吉林大学第二医院)、孟召友(陆军军医大学第二附属医院)、牟英峰(徐州医科大学附属医院)、牛建平(厦门医学院附属第二医院)、潘晓华(包头市中心医院)、彭忠兴(广东药科大学附属第一医院)、任潇(南昌大学第一附属医院)、邵卫(武汉市第一医院)、沈航(中国医学科学院北京协和医院)、唐春花(陆军军医大学陆军特色医学中心)、唐鹤飞(首都医科大学附属北京天坛医院)、陶涛(西南医科大学附属医院)、童秋玲(温州医科大学附属第一医院)、汪敬业(安徽医科大学第一附属医院)、王发明(杭州医学院附属天台医院)、王彦(唐山市人民医院)、王毅(天津市天津医院)、王幼萌(阜阳市人民医院)、王哲(大连医科大学附属第一医院)、魏慧星(福建医科大学附属第一医院)、吴成斯(南昌大学第一附属医院)、吴春华(昆明医科大学第一附属医院)、吴珊(贵州医科大学附属医院)、吴伟(南昌大学第二附属医院)、武衡(南华大学附属第一医院)、熊永洁(华中科技大学同济医学院附属同济医院)、颜洋(三峡大学附属仁和医院)、燕兰云(江苏省人民医院)、杨嘉君(上海市第六人民医院)、杨俊峰(天津医科大学总医院)、杨瑞瑞(山东第一医科大学附属省立医院)、杨西爱(安康市中心医院)、于学英(首都医科大学附属北京天坛医院)、余传勇(南京脑科医院)、袁梅(南华大学附属第二医院)、张洁(中南大学湘雅二医院)、张平(新乡医学院第一附属医院)、张清秀(南京大学医学院附属鼓楼医院)、张昱雯(复旦大学附属中山医院)、张振昶(兰州大学第二医院)、张忠玲(哈尔滨医科大学附属第一医院)、赵凌(成都中医药大学)、赵秀丽(青海大学附属医院)、赵元琛(温州市中西医结合医院)、赵仲艳(海南省人民医院)、郑峥(福州大学附属省立医院)、郑智婷(福州大学附属省立医院)、周道友(广东省中医院)、朱佳佳(南方医科大学南方医院)、朱琳(南京大学医学院附属鼓楼医院)、朱莹(上海国际医学中心)、邹东华(广西医科大学第二附属医院)
学术秘书 熊中华(首都医科大学附属北京天坛医院)、牛朋朋(郑州大学第一附属医院)
利益冲突 所有作者声明不存在利益冲突
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。





