急性呼吸窘迫综合征(ARDS)与各类急性脑损伤(ABI)的不良神经功能结局及死亡率相关。据报道,其发生率在心搏骤停后患者中高达48%,在创伤性脑损伤(TBI)患者中为30%,在非创伤性蛛网膜下腔出血(SAH)患者中为38%,在自发性颅内出血(ICH)患者中为28%[1-6]。然而,由于对颅内高压的担忧,ABI患者在里程碑式的ARDS临床试验中代表性不足。俯卧位通气被认为是中重度ARDS最有效的干预措施之一,尤其是自PROSEVA试验证明每日≥16小时俯卧位通气可使28天死亡率绝对降低17%以来[7]。尽管如此,一项2024年纳入120项评估ARDS俯卧位通气研究的系统评价显示,75%的研究无理由地排除了脑损伤患者,12%未报告ABI相关数据[8]。尽管PROSEVA试验未明确排除ABI患者(仅将颅内压>30 mmHg或脑灌注压<60 mmHg列为排除标准),但未具体说明脑损伤患者的比例[7]。
2020年欧洲重症监护医学会(ESICM)关于ABI机械通气的共识指南指出,该人群缺乏俯卧位通气的高质量证据。指南强烈建议对合并ARDS与ABI但无明显颅内压升高的患者考虑俯卧位通气,但专家小组承认无法对合并ARDS与显著颅内压升高的患者提供推荐意见[9]。由于文献指导不足,俯卧位通气在ABI患者中的应用率偏低。一项2018-2019年针对687名重症医师与麻醉医师的调查显示,超过三分之一(37%)的受访者表示未将俯卧位通气作为ABI合并难治性呼吸衰竭的救治策略[10]。
本文简要综述俯卧位通气对颅内压影响的证据,指出ABI患者的特殊临床挑战,并提出该人群俯卧位通气的实用实施方案。
俯卧位通气对颅内压的影响
俯卧位可能通过降低床头高度、颈静脉受压导致脑静脉回流受阻以及腹压升高等机制增加颅内压[11]。现有评估俯卧位对颅内压影响的研究结果不一。这些研究的主要局限包括样本量小、纳入病理生理机制各异的ABI亚型、俯卧位持续时间短(多数约4-8小时——这被认为是PROSEVA之前试验未显示结局获益的主要原因之一)以及缺乏长期结局数据。
目前唯一一项针对ABI患者的俯卧位随机对照试验于2002年开展,纳入51例因昏迷(格拉斯哥昏迷评分≤9分,多为TBI或ICH)需有创机械通气的患者。值得注意的是,该试验排除了氧合指数≤150及基线颅内压>20 mmHg的患者。研究发现俯卧位组(25例)肺部恶化(肺损伤评分增加≥1分)发生率较低。对其中6例患者的监测显示,0°俯卧位时的颅内压较20°仰卧位显著升高,但在4小时俯卧位期间呈下降趋势。俯卧位组3个月良好神经功能结局(格拉斯哥预后评分4-5分)比例更高(60% vs. 46%),28天死亡率更低(28% vs. 46%),但差异无统计学意义[12]。一项2021年系统评价筛选出10项明确描述俯卧位通气方案的神经科患者研究,包括上述随机对照试验、两项前瞻性与两项回顾性单中心队列研究、一项病例系列及四项病例报告;俯卧位患者数从1例至29例不等[13]。多项研究显示俯卧位期间颅内压升高(颅内压变化中位数3-12.7 mmHg[12,14-16]),而脑灌注压大多维持稳定;部分研究报道动脉血氧分压(如从92.9±11.9 mmHg升至129.2±24.4 mmHg[15])或氧合指数(从135.4±43升至339.8±93.6,即使采用改良135°俯卧角度[16])显著改善。随后一项纳入11例患者的前瞻性观察研究显示,俯卧位使颅内压中位数升高8.6 mmHg,但同时氧合指数显著改善,经颅多普勒搏动指数或舒张末期流速提示脑血流无变化;研究使用血管活性药物维持脑灌注压[8]。一项2023年针对30例SAH患者的研究报道,97次俯卧位操作中有5次因药物难治性颅内压危象提前终止;这些事件与 younger age 及 higher baseline ICP 相关[17]。另一项近期对28例患者颅内压数据的回顾性分析提示,脑顺应性受损者更易在俯卧位期间出现颅内高压[18]。
ABI患者实施俯卧位通气的实践要点
综上,这些数据强调需结合脑血流与基线颅内压解读颅内压数值,同时也凸显俯卧位通过改善气体交换降低继发性脑损伤风险的潜力。
在脑水肿高峰期、颅内血肿扩大期或血管痉挛/迟发性脑缺血期等关键时间窗,需加强神经监测。应权衡连续神经功能评估的重要性与使用镇静剂、神经肌肉阻滞剂以实施肺保护性通气、降低脑代谢需求之间的平衡。对存在颅内高压风险且无法进行可靠临床检查者,应考虑有创颅内压监测以制定个体化血流动力学目标、支持脑自动调节功能并缓解颅内压危象。当无法立即实施或资源有限时,视神经鞘直径测量、经颅多普勒等无创监测技术可作为替代工具[19]。经颅多普勒自动调节研究可指导个体化平均动脉压与二氧化碳分压目标值的设定,以优化脑血流与脑血管反应性(图1)。
图1 急性脑损伤患者俯卧位通气的临床考量要点。AOD 寰枢椎脱位,ARDS 急性呼吸窘迫综合征,CPP 脑灌注压,CSF 脑脊液,DO₂ 氧输送量,HOB 床头高度,IAP 腹内压,ICP 颅内压,IJ 颈内静脉,MAP 平均动脉压,N/A 不适用,PaCO₂ 二氧化碳分压,PaO₂ 氧分压,PbtO₂ 脑组织氧分压,PEEP 呼气末正压,PP 俯卧位,Vt 潮气量(对CPP存在影响):
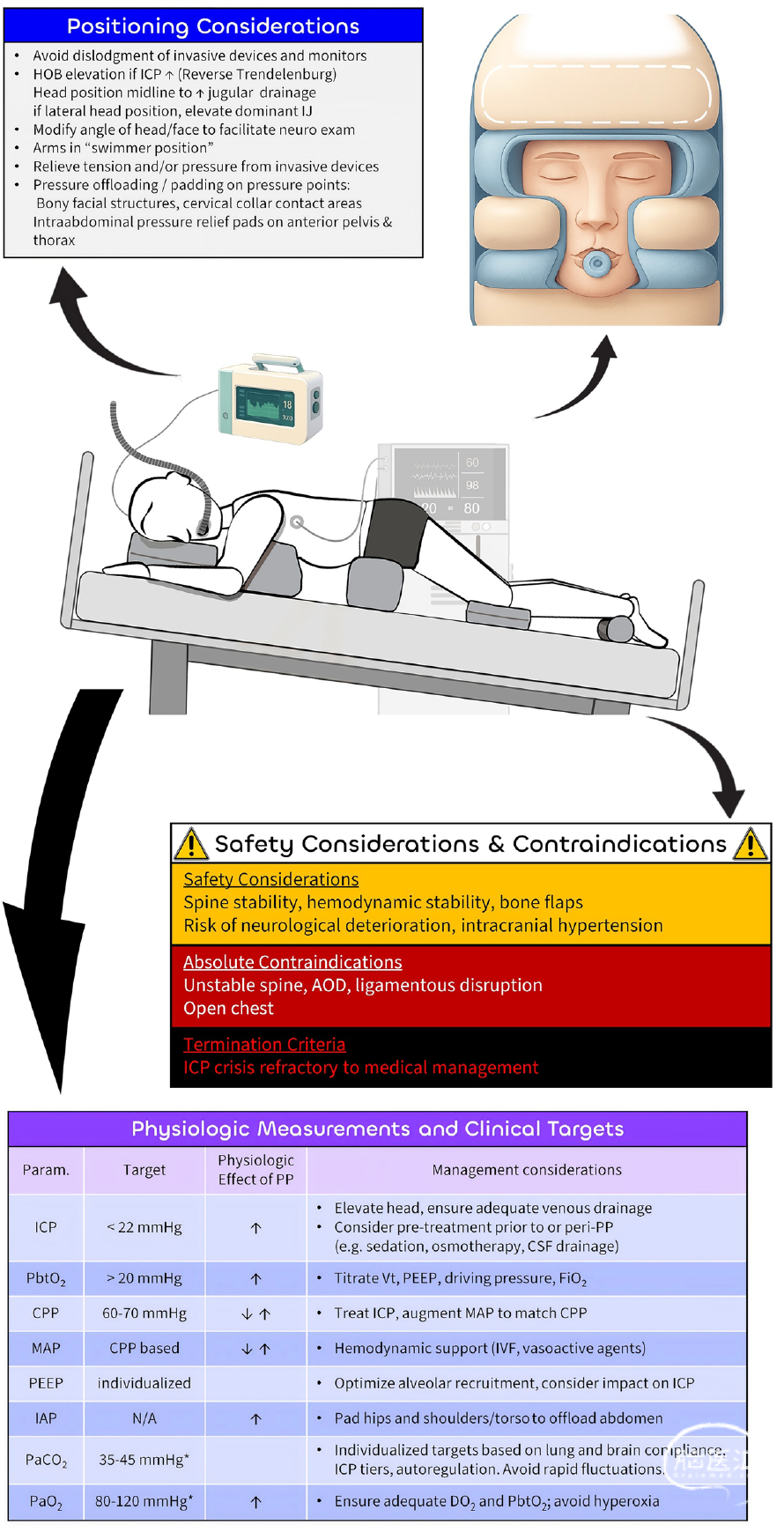
体位摆放考量要点:
避免有创装置与监测设备移位
若存在颅内高压,抬高床头(反Trendelenburg体位)
头部保持中立位以利于颈静脉回流;若采用侧头位,抬高优势侧颈内静脉
调整头/面部角度以方便神经功能检查
手臂呈"游泳姿势"
解除有创装置产生的张力或压力
压力卸载/骨突部位加垫:
面部骨性结构
颈托接触区域
骨盆前侧及胸廓处放置腹压减压垫
安全考量:
脊柱稳定性、血流动力学稳定性、骨瓣状态
神经功能恶化风险、颅内高压风险
绝对禁忌症:
不稳定脊柱、寰枢椎脱位、韧带断裂
开放性胸腔损伤
终止标准:
药物难治性颅内压危象
翻身过程中,最佳体位应旨在保护颈静脉回流(如优先保持头颈中立位,或将优势颈静脉侧朝上)并降低腹压(如使用肩髋垫)[11]。需注意避免俯卧位期间颅内压监测探头移位或脑脊液过度引流。脑室外引流管可能需要重新调零以确保颅内压测量准确。去骨瓣患者可考虑头侧偏位,尤其对存在骨瓣凹陷者,亦有使用防护头盔的报道[20]。需关注脊髓稳定性问题,尤其在TBI人群中。俯卧位的绝对禁忌证包括不完全性不稳定脊髓损伤、寰枕关节脱位或韧带断裂/不稳。在特定病例中,经脊柱团队会诊后可采用俯卧位,翻身时使用轴线翻身技术并加用衬垫,佩戴颈托时需预防压力性损伤。
对基线颅内压升高者,可在俯卧位前通过高渗疗法、镇静或脑脊液引流进行预处理,并可提升平均动脉压以维持脑灌注压。若氧合允许,可尝试俯卧位时抬高床头(“反Trendelenburg位”,(“reverse Trendelenburg)。同时需特别关注二氧化碳分压波动对脑血流及颅内压的影响,尤其在调整潮气量实施肺保护性通气时。类似地,较高呼气末正压滴定可能通过增加胸内压导致颅内高压,且其血流动力学效应会影响脑灌注压。肺组织弹性被认为影响呼气末正压向颅内的传导,结合神经、呼吸及血流动力学监测进行精细的呼气末正压滴定对指导个体化管理至关重要[21,22]。对于经一、二级治疗仍存在俯卧位难治性颅内压升高者,可根据风险评估与预期预后,考虑升级至去骨瓣减压手术或静脉-静脉体外膜肺氧合。由具备神经专长的重症医师、神经外科医生、护士及呼吸治疗师组成的多学科团队及时讨论,有助于快速制定个体化方案。
结论
俯卧位通气在ABI患者中具有可行性,对于合并中重度ARDS者应考虑使用。对颅内高压的担忧并非绝对禁忌证,但需警惕并积极支持脑自动调节、优化脑血流。有创及无创神经监测的使用阈值应降低,尤其当连续神经功能评估受限且神经功能恶化风险较高时。鉴于ARDS与ABI均包含一系列异质性病症,需根据潜在的肺与脑病理生理学权衡俯卧位通气的获益与风险。最终,临床医生需平衡颅内压分级管理与ARDS严重程度,并基于先进的神经与呼吸监测技术进行个体化管理(23)。未来需要开展结合生理学测量与长期结局的多中心试验,以进一步指导这一高危人群的治疗。
Intensive Care Med
. 2025 Oct;51(10):1909-1912. doi: 10.1007/s00134-025-08097-4. Epub 2025 Sep 11.
Head up, face down-a practical framework for proning brain-injured patients with ARDS
*本文转载自微信公众号“脑血管病及重症文献导读”,脑医汇获授权转载
![]()
声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。
投稿邮箱:NAOYIHUI@163.com
未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。
投稿/会议发布,请联系400-888-2526转3。




