重要性
卵圆孔未闭(PFO)是正常胎儿发育期间左右心房之间的通道,在出生后未能闭合,约25%的成年人存在此现象。反常栓塞是指静脉血栓栓塞通常通过PFO进入体循环,约占所有卒中的5%,在较年轻卒中患者中占比可达10%。
观察结果
约50%的60岁及以下不明原因栓塞性卒中(隐源性卒中)患者存在PFO,而一般人群的PFO患病率为25%。反常栓塞风险(RoPE)评分结合临床特征(年龄、卒中或短暂性脑缺血发作史、糖尿病、高血压、吸烟、影像学显示皮质梗死)来预测不明原因栓塞性卒中由PFO引起的可能性。在RoPE评分最低类别(评分<3分)的患者中,PFO患病率与一般人群相似(23%),而RoPE评分9-10分的患者中PFO患病率高达77%。PFO相关卒中因果可能性(PASCAL)分类系统结合RoPE评分和超声心动图解剖学标准(大分流、房间隔动脉瘤),将PFO导致隐源性卒中的可能性分类为"很可能"、"可能"或"不太可能"。
PFO封堵术可减少60岁及以下隐源性卒中患者的复发性缺血性卒中。对6项试验(3740例患者)的汇总分析显示,中位随访57个月期间,PFO封堵组的年化卒中发生率为0.47%(95%CI 0.35%-0.65%),而药物治疗组为1.09%(95%CI 0.88%-1.36%)(调整后风险比0.41 [95%CI 0.28-0.60])。然而,封堵术的获益和危害在不同试验人群间存在高度异质性。在PASCAL分类为"很可能"的患者中(即无血管危险因素且具有高风险PFO解剖特征的较年轻患者),PFO封堵术后2年复发性缺血性卒中的相对风险降低了90%(风险比0.10 [95%CI 0.03-0.35];绝对风险降低2.1% [95%CI 0.9%-3.4%])。而PASCAL分类为"不太可能"的患者(如具有血管危险因素且无高风险PFO解剖特征的老年患者)未因PFO封堵术降低卒中复发风险,反而面临更高的手术和装置相关不良事件(如房颤)风险。
结论与意义
卵圆孔未闭存在于约25%的成年人中,是青中年患者卒中的常见原因。PASCAL分类系统有助于指导PFO封堵术的患者选择。对于经过严格筛选的60岁以下隐源性卒中患者,经皮PFO封堵术可显著降低卒中复发风险。
卵圆孔未闭(PFO)是胎儿循环中残留的持续性小通道,允许血液发生右向左的房水平分流,约25%的成年人存在此现象,可能在心脏超声检查中被偶然发现。然而,高达30%的卒中属于隐源性卒中,即经过全面病因评估后仍无法解释的卒中。在隐源性卒中患者中,约50%存在PFO,这可能引发反常栓塞——静脉系统中的栓子直接进入脑动脉循环。过去数十年间,研究表明专门设计用于封堵PFO的器械,在经过严格筛选的青中年PFO患者中能有效预防卒中复发[1-6]。2020年,一个国际卒中专家工作组建议更新卒中命名法,将PFO相关性卒中从隐源性类别中移除[7]。
本综述阐述了PFO相关性卒中的流行病学特征,比较了器械封堵与药物治疗的疗效,并讨论了鉴别PFO是病因性还是偶然性的概率算法,以支持临床决策。同时,也回顾了PFO相关性卒中临床管理的其他方面(见专栏)。
专栏:关于卵圆孔未闭(PFO)与卒中的常见问题
如何确诊隐源性卒中?
卒中的初步评估包括头部CT血管成像或脑部MR血管成像以评估大动脉粥样硬化、心电图检测房颤,以及心脏超声检查以评估心源性栓塞可能。若上述检查均未发现明确病因,则可诊断为隐源性卒中。若神经影像学提示梗死灶为栓塞性,则归类为不明原因栓塞性卒中。
在PFO相关性卒中患者中,哪些因素提示PFO是病因而非偶然发现?
缺乏糖尿病、高血压及吸烟等血管疾病危险因素,且神经影像学显示存在皮层梗死(尤其在60岁以下患者中),提示PFO可能是卒中病因。其他增加此可能性的因素包括:存在大分流量的PFO或房间隔动脉瘤,以及在Valsalva动作期间或存在深静脉血栓时发生的脑梗死。
所有合并PFO的隐源性卒中患者都能从PFO封堵术中获益吗?
随机试验证实,经过筛选的60岁及以下隐源性卒中患者,封堵PFO可降低卒中复发率。然而,根据PASCAL(PFO相关性卒中因果可能性)系统分类为"不太可能"由PFO引起卒中的患者,似乎不能从封堵术中获益,且面临更高的装置相关不良事件(如房颤)风险。
方法
与大学图书馆员合作制定了全面的检索策略,在PubMed中检索了2014年1月1日至2025年5月17日期间发表的关于PFO与卒中的英文研究(补充材料)。对检索到的文章及其相关参考文献进行了人工评估,并纳入了其他关键出版物和临床试验。共识别出867篇文章,其中我们纳入了79篇(27篇系统评价/荟萃分析、23项队列研究、15项随机临床试验、8篇专家声明或立场文件以及6篇指南)。
卵圆孔未闭的胚胎学
在正常的产前发育过程中,卵圆孔由胎儿房间隔中的两个结构——原发隔和继发隔——未完全闭合所形成。卵圆孔使得来自胎盘的含氧血能够绕过无功能的胎儿肺部,进入胎儿动脉循环。出生时,流经肺血管的血流增加,导致左心房压力显著升高,将原发隔推向继发隔,从而实现卵圆孔的功能性闭合,并在出生后第一年内完成解剖性闭合。然而,约25%的个体其原发隔和继发隔边缘未能完全融合,留下一个小开口,即形成PFO。
PFO相关性卒中的病理生理学
大多数PFO直径较小(平均4.9毫米,范围1-19毫米),不会引起有血流动力学意义的血液分流。然而,其尺寸足以让静脉血栓产生的栓子绕过肺血管的过滤作用,进入体动脉循环。这种"反常栓塞"可通过阻塞脑动脉循环的分支导致症状性卒中(图1)。PFO相关性卒中的另一个潜在机制是房间隔隧道周围形成原位血栓,从而引发脑栓塞[8,9]。
图1.PFO的机制:

PFO相关性卒中的临床流行病学
在增强超声心动图技术问世之前,反常栓塞被认为是卒中的罕见原因,1972年之前仅报告了128例[6]。随后的流行病学研究报告显示,在隐源性卒中患者中PFO的患病率增高[10,11]。一项对23项病例对照研究(n=1154例病例,1852例对照)的荟萃分析显示,隐源性卒中患者与已知病因的缺血性卒中对照组相比,存在PFO的汇总比值比为2.9(95% CI, 2.1-4.0)[11]。然而,在55岁以下人群中,存在PFO的比值比高达5.1(95% CI, 3.3-7.8)。利用这些关联性估计,在隐源性卒中患者中,PFO是卒中可能原因(而非偶然发现)的比例,在55岁以下患者中约为80%(95% CI, 75%-84%),而在老年患者中约为52%(95% CI, 34%-66%)[11,12]。据估计,约5%的全部缺血性卒中以及约10%的青中年缺血性卒中可归因于PFO[12]。
PFO相关性卒中的评估与诊断
PFO相关性卒中的诊断需要满足以下三点:(1) 确定卒中为隐源性;(2) 检测到PFO;(3) 判断PFO是卒中的可能病因还是偶然发现。
卒中是否为隐源性?
"隐源性卒中"是一个排除性诊断,指经过全面检查仍未发现卒中病因[13]。卒中病因评估包括病史、体格检查以及以下检查:(1) 通过脑部磁共振成像或头部计算机断层扫描评估梗死的位置、体积和数量,这些信息常可提示病因(例如,腔隙性梗死提示小血管疾病);(2) 通过CT血管成像、磁共振血管成像或颈动脉超声评估大血管通畅性;(3) 通过经胸超声心动图评估瓣膜或心房疾病,包括左心房血栓;(4) 通过心电图和心电遥测评估心律;(5) 全血细胞计数和凝血功能实验室检查[14]。额外检查可能包括:数字减影血管造影(一种利用荧光透视直接观察血管的血管内技术)、经颅多普勒检测右向左分流、如果心电图或遥测未发现房颤则进行长时程心脏节律监测(如动态心电图或植入式循环记录器)、若怀疑血管炎则进行腰椎穿刺、评估隐匿性恶性肿瘤(如胸腹盆CT)、以及进行与卒中风险增加相关的基因变异检测(例如CADASIL——伴有皮质下梗死和白质脑病的常染色体显性遗传性脑动脉病)。这些检查有助于确定卒中的病因,最常见的病因包括房颤导致的心源性栓塞(27.7%)、小血管疾病(23.7%)、大动脉粥样硬化(23.3%)[15]以及其他更罕见的原因如烟雾病和血管炎(5.3%)[16-18]。如果未发现任何卒中病因,则被视为隐源性(20.0%)[7]。
"不明原因栓塞性卒中"这一术语于2014年被提出,旨在标准化定义那些神经影像学表现为栓塞性、但经诊断性检查后无明确机制的卒中[19]。不明原因栓塞性卒中可能由隐匿性阵发性房颤、非狭窄性颅内和颅外大动脉粥样硬化形成的栓子引起,并且可能影响伴有或不伴有PFO的患者[20,21]。
在患有隐源性卒中且合并PFO的患者中,为检测隐匿性房颤(定义为常规心电图未检测到的房颤)所需进行的心脏监测时长尚不确定[22]。此外,尽管更长时长的心脏监测(长达3年)与房颤检出率的增加相关,但尚不清楚在长期随访中首次发现的房颤是否应被视为初始卒中的原因[23-27],特别是当阵发性房颤负荷(即患者在房颤状态下的总监测时间比例)极低时,例如低于0.1%[28-31]。2021年美国心脏协会/美国卒中协会指南建议,缺血性卒中后应进行至少24小时的心脏监测以评估房颤[32]。相比之下,一个由8个欧洲学会组成的联盟建议,对于房颤高风险的隐源性卒中患者(例如,未控制的高血压或糖尿病、左心室肥厚、左心房扩大或心力衰竭),在决定进行PFO封堵术前,应进行长达6个月的心脏监测[33,34]。
PFO的识别
在高收入国家,大多数卒中患者最初会接受经胸超声心动图检查,以评估结构性心脏病或血栓,PFO可能在此检查中被发现。为评估PFO是否为卒中病因的患者,通常需接受经胸超声心动图结合发泡试验检查,该试验通过在患者进行Valsalva动作(以增加右心房压力)时,静脉注射震荡生理盐水来完成。若在3个心动周期内于左心房观察到微气泡,即可诊断PFO,表明存在经房间隔的右向左分流。
经胸超声心动图结合发泡试验检测PFO的汇总敏感性为71%(95%CI, 50%-86%),特异性为99%(95%CI, 93%-100%)[35],但被认为不足以排除PFO。经颅多普勒超声结合发泡试验是另一种无创检查,可检测右向左分流,其检测PFO的汇总敏感性为96%(95%CI, 93%-98%),特异性为90%(95%CI, 83%-95%)[35]。然而,由于经颅多普勒检测的是脑循环内的微气泡,它不能直接显示房间隔,也无法区分PFO与其他分流。
识别PFO的金标准是经食管超声心动图结合发泡试验(参见相关视频),用以评估分流大小、PFO的解剖结构以及周围结构(如房间隔动脉瘤或欧式瓣——一种右心房内的胚胎残留结构,可能增加通过PFO的血流)。经食管超声心动图需将超声探头置入食道以显示心脏,通常在有意识镇静下进行。一项比较经食管超声心动图结合发泡试验与通过尸检、心脏手术或心导管检查识别PFO的荟萃分析(包含4项前瞻性研究,n=164)显示,其敏感性为89%(95%CI, 81%-95%),特异性为91%(95%CI, 82%-97%)[36]。然而,某些PFO仍可能被漏诊,原因包括患者因焦虑或无法控制的咽反射而不能耐受TEE探头、镇静状态下难以有效完成Valsalva动作,或操作者经验有限。
判断PFO是病因性还是偶然性
在隐源性卒中患者中,PFO更常见于那些没有典型卒中危险因素的患者[37]。反常栓塞风险评分(Risk of Paradoxical Embolism (RoPE) score)(表1上部)是基于对8个数据库(包含3023名经过系统性PFO评估的隐源性卒中患者)的分析而制定的[3,8]。RoPE评分包含6项临床特征(年龄、卒中或短暂性脑缺血发作史、糖尿病、高血压、吸烟、影像学显示皮层梗死),分值范围0-10(表1上部;图2)[38]。根据贝叶斯定理,不同RoPE评分层级的PFO患病率差异可用于估算PFO归因分数——即在隐源性卒中患者中发现的PFO与卒中存在因果关系的可能性(图2)。在RoPE评分最低类别(评分<3分,即具有多种卒中危险因素的老年患者)中,PFO患病率为23%,与普通人群相似,表明PFO归因分数接近于零[38]。而在RoPE评分为9或10分的隐源性卒中患者中,PFO患病率为77%,表明在这些患者中PFO归因分数约为90%[38]。
表1.RoPE评分和PASCAL分级的计算方法:

图2.在接受经食管超声或经颅多普勒检测PFO的隐源性卒中患者中,RoPE评分与PFO的关联性
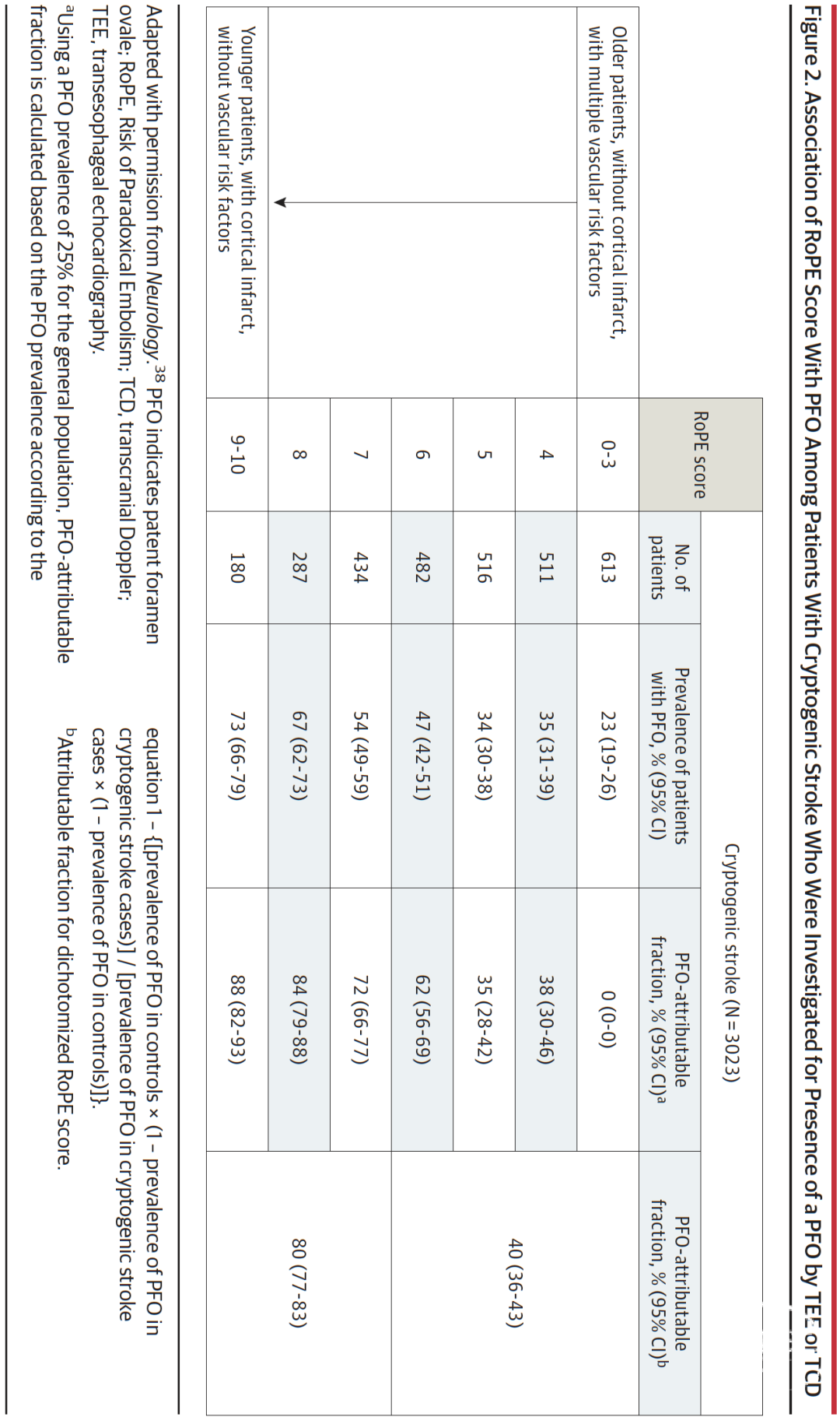
RoPE评分已在针对隐源性卒中患者的各项研究中得到独立验证[42,43]。例如,在ASTRAL数据库纳入的455名PFO隐源性卒中患者中,各RoPE评分层级的PFO患病率与RoPE数据库的结果高度吻合——从RoPE评分≤3分患者的23%(95%CI 21%-26%)到评分≥9分患者的72%(95%CI 68%-75%)[43]。由于归因分数属于估算值而非直接观测指标,其验证需要随机数据来考察不同RoPE分层中PFO归因分数与观察到的PFO封堵相对疗效之间的一致性。
值得注意的是,RoPE评分存在若干局限性。研究表明,高RoPE评分患者的卒中复发风险可能较低[38]。一项针对1324名PFO相关性卒中患者的研究显示,RoPE评分≥9分患者的卒中/TIA两年复发率的Kaplan-Meier估计值仅为2%(95%CI 0%-4%),这意味着对最可能发生PFO归因性卒中复发的患者而言,PFO封堵的绝对获益可能有限。此外,RoPE评分未纳入与反常栓塞风险升高相关的PFO解剖特征[44,45]——即大分流(静脉注射震荡盐水后3个心动周期内右心房出现>20个微气泡)和房间隔瘤(房间隔从中线位置的移动幅度≥10毫米)。
PFO相关性卒中因果可能性分类系统(PFO-Associated Stroke Causal Likelihood (PASCAL))整合了RoPE评分和超声心动图发现,其中高风险解剖特征定义为大分流和/或房间隔瘤(表1下部)。根据该分类系统,PFO被视为隐源性卒中的"很可能"、"可能"或"不太可能"病因。
反常栓塞的其他潜在风险因素:未纳入RoPE评分但可能增加反常栓塞风险的其他临床因素包括:卒中发作时的Valsalva动作、近期长途旅行、睡眠呼吸暂停、就诊时存在深静脉血栓或肺栓塞、高凝状态、偏头痛,以及其他解剖特征如Chiari网或欧式瓣的存在[11,46-49]。
PFO相关性卒中的治疗
经皮PFO封堵术通过股静脉将封堵器经导管置入右心房。封堵器在PFO处展开,覆盖缺损部位,并随时间推移与心脏组织融合(图1)。
早期三项比较PFO封堵+阿司匹林与单纯药物治疗的随机试验,在2年、2.5年和4年随访时均未发现主要终点(卒中、TIA或栓塞事件)存在统计学显著差异[39,1,41,50]。然而,RESPECT试验延长随访至平均5.9年时发现,PFO封堵组的复发性缺血性卒中发生率为3.6%,显著低于药物治疗组的5.8%(风险比0.55)[1]。2017年公布的RESPECT、REDUCE和CLOSE试验延伸研究,以及2018年的DEFENSE-PFO试验,均证实了PFO封堵对特定患者的获益[51,2,3,40]。对6项随机试验的荟萃分析显示,在中位随访57个月时,PFO封堵组的复发性缺血性卒中发生率显著低于单纯药物治疗组(相对风险0.44)[33,52-54]。基于这些证据,现行指南推荐对经过选择的患者(如年龄<60岁的隐源性卒中)行PFO封堵术[32,33,55]。
由于各临床试验中与器械封堵联用的抗栓方案存在异质性,目前难以推荐适用于所有患者的统一方案(表2)。欧洲卒中组织指南建议封堵后给予1-6个月的双联抗血小板治疗,后续长期单药抗血小板治疗,部分原因在于卒中病因往往难以完全明确[35]。
表2.PFO封堵术的临床试验:
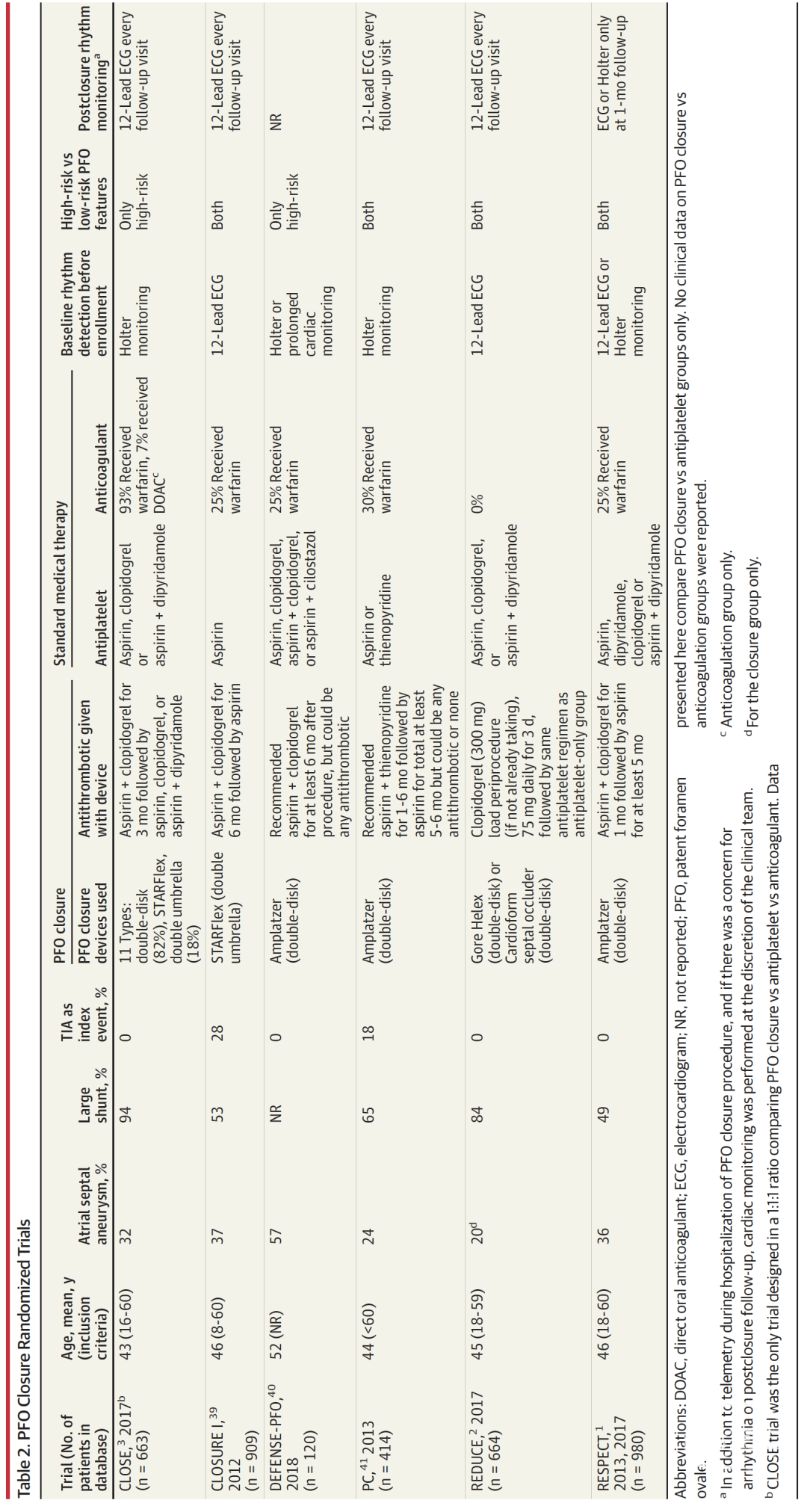
需要强调的是,即使成功实施PFO封堵,隐源性卒中伴PFO患者在术后4年的卒中风险仍显著高于普通人群,这一风险与年龄、高血压、糖尿病、血脂异常及吸烟等心血管危险因素密切相关[56,57],凸显了即使 after PFO封堵仍需要持续管理血管危险因素的重要性。
PFO封堵术的不良反应
PFO封堵术通常被认为是安全的,但可能发生严重不良事件。一项基于1887例患者理赔数据的回顾性队列研究显示:房颤/房扑发生率为3.7%,需外科修补的血管并发症(出血/血肿)为3.0%,血肿/出血为2.7%,心脏压塞/穿孔为0.5%,气胸/血胸为0.1%,死亡为0.3%[58]。对6项卒中后PFO封堵随机临床试验的个体患者数据合并分析显示,在中位随访57个月期间,PFO封堵组与药物治疗组发生任何严重不良事件的患者比例相近(28.7% vs 26.4%)[59]。然而,封堵组房颤发生率更高(5.0% vs 1.1%),其中超过半数的风险差异源于围术期房颤(通常呈一过性)[60]。术后远期(>45天)的房颤风险,封堵组为2.4%,药物治疗组为0.8%[59]。此外,封堵组静脉血栓栓塞发生率为1.4%,高于药物治疗组的0.5%;两组出血事件发生率相似(1.4% vs 1.7%)[59]。这些试验未量化的其他罕见器械相关并发症包括镍暴露引起的镍钛合金过敏反应,以及器械移位、断裂和感染。
基于RoPE评分和PASCAL分类的封堵疗效差异
对6项RCT的个体患者荟萃分析探讨了不同RoPE评分和PASCAL分类患者的封堵获益[59]。合并分析显示,中位随访57个月期间,封堵组年化卒中发生率为0.47%,显著低于药物治疗组的1.09%。对于反常栓塞可能性更高的患者(RoPE评分≥7),封堵降低卒中复发的相对风险显著优于评分<7的患者[59]。卒中复发的风险降幅与计算得出的归因分数相符(RoPE<7分者约40%,≥7分者约80%)[59,61,62]。
采用PASCAL分类系统(表1下部),在兼具高风险解剖特征和高RoPE评分而被列为"很可能"类的患者中,PFO封堵使卒中复发风险相对降低90%(中位随访57个月)[59]。PASCAL"可能"类患者也有中等程度的相对获益,在具有临床意义的绝对风险降低方面与"很可能"类患者相似——封堵后2年卒中复发的风险差异在这两类患者中均约为2%[59]。相比之下,PASCAL"不太可能"类患者未从封堵术中获益[59]。不同PASCAL分层间的疗效差异具有高度统计学显著性[59]。
据报道,PASCAL"不太可能"组的器械相关安全性事件发生率高于"很可能"或"可能"组。例如,在6项RCT的合并分析中,中位随访57个月期间,与药物治疗相比,封堵导致术后远期房颤的绝对风险增加幅度在"不太可能"类中最高[59]。"不太可能"类患者接受器械治疗后房颤风险增高,可能与其年龄较大、血管危险因素较多(这些因素与手术相关房颤有关)有关[43]。
虽然PASCAL分类系统将大分流或房间隔瘤视为PFO的高风险解剖特征,但6项试验的合并分析表明,同时具备这两种高风险特征的患者从PFO封堵中获益最大[63]。这些患者在药物治疗下的复发率最高(2年时5.9%),而封堵后的复发率最低(2年时0.4%)。2年时,他们的卒中复发绝对风险降低了5.5%,远高于仅具备一个或无高风险特征的患者(绝对风险降低1.0%)[63]。
药物治疗(抗凝药与抗血小板药)
一项纳入6项RCT的荟萃分析比较了抗凝药与抗血小板药对PFO相关性卒中患者的疗效[64]。综合分析显示,与抗血小板治疗相比,使用华法林或直接口服抗凝药进行抗凝治疗可降低复发性缺血性卒中风险[64]。在6项比较PFO封堵与药物治疗预防卒中复发的随机试验中,约四分之三的药物治疗患者接受了抗血小板治疗。因此,PFO封堵与单纯抗凝治疗的相对有效性仍不确定,值得进一步研究。
对60岁以上患者行PFO封堵的考量
尽管PFO封堵可降低60岁及以下PFO相关性卒中患者的卒中风险,但其对老年患者的潜在获益尚不明确。在6项随机试验中,仅1项纳入了60岁以上患者,且样本量过小无法得出确凿结论[65]。PFO封堵对老年患者的潜在获益是一个活跃的研究领域,至少有一项RCT正在进行中[66]。
已有两项观察性研究采用了倾向评分方法[67,68]。其中一项分析显示,PFO封堵与显著较低的缺血性卒中或TIA复合结局风险相关[66]。另一项纳入5508名医保受益人的倾向匹配队列研究也报告,封堵组的复发性缺血性卒中风险显著低于药物治疗对照组[68]。然而,这两项研究均存在可能偏向器械组的偏倚。前者存在" immortal time bias "[69],后者使用的"真实世界数据"无法识别隐源性卒中,且组间存在不平衡。
在缺乏明确证据的情况下,一些指南(如美国神经病学学会的指南)建议,对于年龄60至65岁、具有高风险PFO特征(如大分流、房间隔瘤)的患者,即使RoPE评分<7,考虑PFO封堵也可能是合理的[55,70]。
封堵器械选择与未来方向
目前大多数PFO封堵器为双盘封堵器。尚无试验比较美国FDA批准的不同器械的疗效和安全性;观察性数据和荟萃分析未能得出一致性结论支持某一种器械更优[71-75]。
几种新型器械正在研发中,包括可在植入后内皮化和生物降解的生物可吸收双盘器械[76]。此外,一种新的缝线介导技术正在评估中,该技术可能避免镍钛合金过敏反应以及其他器械相关并发症(如移位、断裂、感染和房颤)[77]。该技术也可用于封闭器械封堵失败后的残余缺损[78]。
不确定领域与实践考量
首先,PFO封堵与围术期房颤风险增加相关,后者常为一过性并可自行缓解;目前尚不清楚这些患者是否应接受抗凝治疗[79]。其次,也不确定TIA患者是否应接受PFO封堵,因为大多数PFO封堵RCT未纳入这类个体。第三,由于PFO导致右向左分流,发现静脉血栓栓塞可能会增加PFO与卒中存在因果关联的可能性。在接受检查的PFO伴隐源性卒中患者的研究中,深静脉血栓频率在7%至27%之间[79]。目前DVT的存在并未纳入PFO相关性卒中的风险分层评分,也缺乏关于筛查这些患者DVT效用的高质量数据。然而,学会指南推荐对DVT进行早期评估,包括下肢多普勒检查和考虑盆腔磁共振静脉造影[32]。
局限性
本综述存在局限性。首先,未对纳入研究的质量进行正式评估。其次,可能遗漏了相关研究。第三,纳入研究在缺血性卒中的诊断检查方面存在差异,导致研究间存在显著的异质性。
结论
PFO存在于约25%的成年人中,是青中年患者卒中的常见原因。经皮PFO封堵术可显著降低较年轻隐源性卒中患者的卒中复发风险。PASCAL分类系统有助于指导患者选择进行PFO封堵,以优化获益并最小化不良事件。
JAMA
. 2025 Oct 28;334(16):1463-1473. doi: 10.1001/jama.2025.10946.
Patent Foramen Ovale and Stroke: A Review
*本文转载自微信公众号“脑血管病及重症文献导读”,脑医汇获授权转载
![]()
声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。
投稿邮箱:NAOYIHUI@163.com
未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。
投稿/会议发布,请联系400-888-2526转3。




