摘 要
脑动静脉畸形合并颅内动脉瘤为高风险脑血管病变组合,二者因血流动力学异常、结构发育缺陷等机制存在复杂关联,显著升高颅脑出血风险并大幅增加临床诊疗决策难度。当前临床实践中,针对该联合病变缺乏明确统一的诊疗指导标准,各中心诊疗流程及治疗策略不同,患者预后差异较大。故中国医师协会神经介入专业委员会等学术组织联合领域专家,遵循循证医学证据、结合临床实践经验,共同制定了本共识。共识围绕病因机制、诊断流程、风险评估及个体化治疗路径等核心内容,提出针对性推荐意见,旨在为各级医院临床医师提供参考,提升诊疗流程规范性与安全性,改善患者长期预后。
前 言
脑动静脉畸形(brain arteriovenous malformation,bAVM)合并颅内动脉瘤(intracranial aneurysm,IA)是一类高风险的脑血管病变组合,病理机制复杂,临床诊治依赖于精确的影像学评估、综合风险分层与多学科协作[1-3]。目前,相关的治疗策略包括药物治疗、血管内治疗、外科手术治疗和放射治疗等,其中血管内治疗因其操作简便、创伤小、安全性高等特点,逐渐成为bAVM合并IA的主要治疗方式之一[4-6]。但临床上仍存在治疗方案不一致、患者预后差异较大等现象,故本共识结合最新临床研究成果和专家意见,围绕病因机制、诊断流程、风险评估与个体化治疗路径等核心问题提供了相关领域专家的一致性意见,以期提高此类患者的诊疗流程规范性与安全性,进一步改善患者长期预后。
一、共识制定过程及方法学
(一)共识发起机构及工作流程
本共识由中国医师协会神经介入专业委员会、脑血管病诊疗技术与器械教育部工程研究中心发起和组织撰写,共识编写组成员包括神经外科、神经内科、神经介入科、放射介入科等相关领域专家。通过文献检索、证据总结及专家临床实践经验,形成共识框架及拟推荐意见,采用改良德尔菲法进行多轮论证及投票后形成最终推荐意见及共识内容。
(二)文献检索
共识编写组以脑动静脉畸形、颅内动静脉畸形、颅内动脉瘤、脑动脉瘤、血流相关型动脉瘤、brain arteriovenous malformation、intracranial arteriovenous malformation、cerebral arteriovenous malformatiom、intracranial aneurysm、cerebral aneurysm、flow-related aneurysm等中英文检索词在Pubmed、Web of Science、PsychoInfo、Cochrane library、Embase、万方数据知识服务平台和中国知网等中英文数据库中进行了系统检索。检索时间范围为各数据库建库时间至2025年7月30日。纳入文献类型包括指南、共识、系统综述、回顾性或前瞻性临床研究、高质量病例系列以及具有代表性的专家观点类文献。剔除重复文献、无法获取全文的文献。
(三)推荐强度
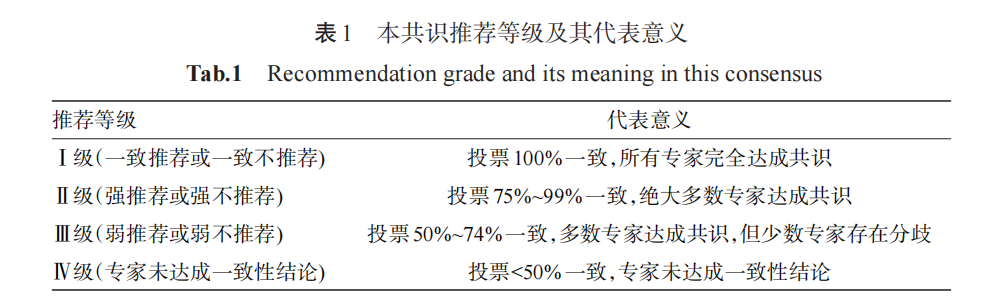
本共识采用专家组投票的形式决定推荐意见的分级,投票设置5个选项:(1)强推荐;(2)弱推荐;(3)无明确推荐意见;(4)弱不推荐;(5)强不推荐。通过统计投票结果中不同选项及组合的投票比例,将推荐等级分为I、II、III、IV级,具体代表意义见表1。
二、流行病学
bAVM破裂占出血性卒中的2%~4%,是导致青少年出血性卒中的重要原因[7-9]。10%~20%的bAVM患者合并IA,该组合显著增加了出血性卒中风险[1,3,10]。bAVM合并IA患者的平均年龄为38.3岁,男女比例大约为0.98∶1[2]。在破裂bAVM合并IA病例中,IA作为出血来源的比例可高达49.2%,其中血流相关型IA是最常见的破裂类型(78.5%)[2]。2025年一项纳入了2 440例未破裂bAVM患者的国际多中心研究显示,IA合并率达19%(457例);中位随访4.65年,首次颅内出血发生率为1.40%/年(95%CI:1.20~1.64)。校正COX模型证实,合并IA显著增加出血风险(HR=1.66,95%CI:1.06~2.59,P=0.030)[1]。在中国人群中,Lv等[5]回顾性分析了1999~2009年间在北京天坛医院就诊的366例bAVM患者,其中86例(23.5%)合并IA。患者的平均年龄为31.8岁,男性占64%,女性占36%。大多数(87.2%)患者的bAVM位于小脑幕上,80.2%患者因出血就诊。孙丰兵等[11]分析了2000~2019年间上海交通大学附属新华医院的352例bAVM患者,结果显示供血动脉近端IA(APIA)组患者年龄较高,后循环供血率明显高于非APIA组(51.6%比22.7%)。
在伴有IA的bAVM患者中,IA的平均数量为1.5个,其中约75%为幕上IA,25%为幕下IA[2,6]。另一方面,幕下bAVM合并IA的发生率显著高于幕上病例(45.4%比20.1%),多变量Logistic回归分析结果显示幕下bAVM合并IA的发生几率是幕上bAVM的2.9倍[12]。Orning等[13]研究也显示幕下bAVM中供血IA的总体发生率相对幕上bAVM较高(34.4%比18.5%),2组bAVM畸形血管团内IA的发生率相似(9.2%比8.8%),供血IA是幕下bAVM出血源的可能性远高于幕上bAVM(30.0%比7.6%)。在bAVM合并IA患者中,IA(包括破裂和未破裂)的直径(最大径)平均值为5.34 mm,其中发生破裂出血患者中IA的的直径(最大径)平均值为5.77 mm。血流相关型IA的发生率为42.1%~76.8%;畸形近端IA、畸形远端IA、畸形血管团内IA和血流不相关IA的比例分别为40.7%~61.2%、24.8%~38.8%、22.2%~42.9%以及4.0%~6.3%[2,6]。IA分布广泛,主要位于大脑中动脉(11.6%~23.5%)、大脑前动脉/前交通动脉(18.5%~25.0%)、颈内动脉(7.4%~32.6%)、大脑后动脉(3.7%~11.8%)、椎基底动脉系统(3.7%~9.6%)以及小脑动脉(小脑后下动脉3.7%~18.8%,小脑上动脉4.2%~25.0%,小脑前下动脉0.4%~17.5%)[2,6]。
三、发病机制及破裂出血的危险因素
(一)发病机制
目前关于bAVM合并IA的关联机制,主要存在3种理论解释。
1. 先天性理论:由Arieti和Gray[14]提出,该理论认为bAVM与IA可能具有共同的先天性或遗传背景,从而导致两种病变同时存在,但具体的遗传调控机制仍有待进一步研究证实。bAVM基础研究最重要的进展在于发现了RAS-丝裂原活化蛋白激酶(MAPK)通路基因的体细胞突变[15-18]。通路中KRAS/BRAF突变在bAVM中的检出率为81%,在脊髓动静脉畸形中达100%[19]。然而,这些基因突变导致bAVM形成的机制仍是未知。大多数家族性bAVM病例与遗传性出血性毛细血管扩张症(HHT)相关[15,20]。超过90%的HHT患者存在转化生长因子β(TGFβ)家族受体相关基因、内皮素(ENG)或活化素受体样激酶1基因(ALK1,又称ACVLR1)的突变[21-23]。另外,Zhou等[24]提出,血小板衍生生长因子-D(PDGFD)基因启动子DNA甲基化与IA或bAVM发生风险存在显著相关性。
2. 血流动力学理论:由McKissock和Paterson[25]提出并不断发展,目前已得到学界的广泛关注。该理论认为,bAVM的存在可导致局部血流灌注增加,进而引起主要供血血管承受异常压力,最终诱发IA形成。这一理论可通过临床病例得到支持,例如对侧颈动脉结扎后出现颈内动脉IA的病例报告。Shakur等[26]通过评估bAVM合并IA患者的血流动力学变化发现,与无IA的供血动脉相比,伴IA的供血动脉虽流速相近,但血管直径更小,导致壁面剪切力显著升高。据此提出,壁面剪切力异常升高可能是bAVM合并IA发生的重要血流动力学机制,这一发现既证实了血流改变是触发血管重塑的关键生物力学刺激因素,也揭示了其对bAVM供血血管的潜在影响。
3. 巧合理论:最初由Boyd-Wilson[27]提出,该理论认为bAVM与IA的共存可能是偶然发现的结果。这一理论较为简单,主要认为这两种病变并无直接关联,而是因偶然因素同时存在于同一患者体内。
值得关注的是,这3种理论并不相互排斥。事实上,先天性因素与血流动力学改变的相互作用,似乎更能合理解释大多数临床病例的发病机制。
(二)危险因素
多项研究探讨了bAVM合并IA患者出血风险增高的危险因素。Redekop等[28]发现,合并畸形血管团内IA亚组的出血发生率(72%)显著高于无IA(36%)或其他部位IA亚组(40%)。Hung等[3]发现年龄较大、bAVM尺寸较小和bAVM位于小脑位置是血流相关型IA破裂率升高的危险因素。此外,高血压也被认为是出血风险增加的危险因素[10]。相比之下,癫痫史、年龄、性别、浅静脉引流及高Spetzler-Martin分级等因素与出血风险的关联尚缺乏明确证据支持。
四、分型
bAVM合并IA的分型系统逐步发展,主要基于bAVM相关IA与病灶之间的血流动力学关系或解剖位置关系进行分型。Sun等[29]将bAVM相关IA分为畸形血管团前IA或畸形血管团内IA;而Piotin等[30]则依据解剖位置,将其分为位于供血动脉近端的IA和供血动脉远端的IA。
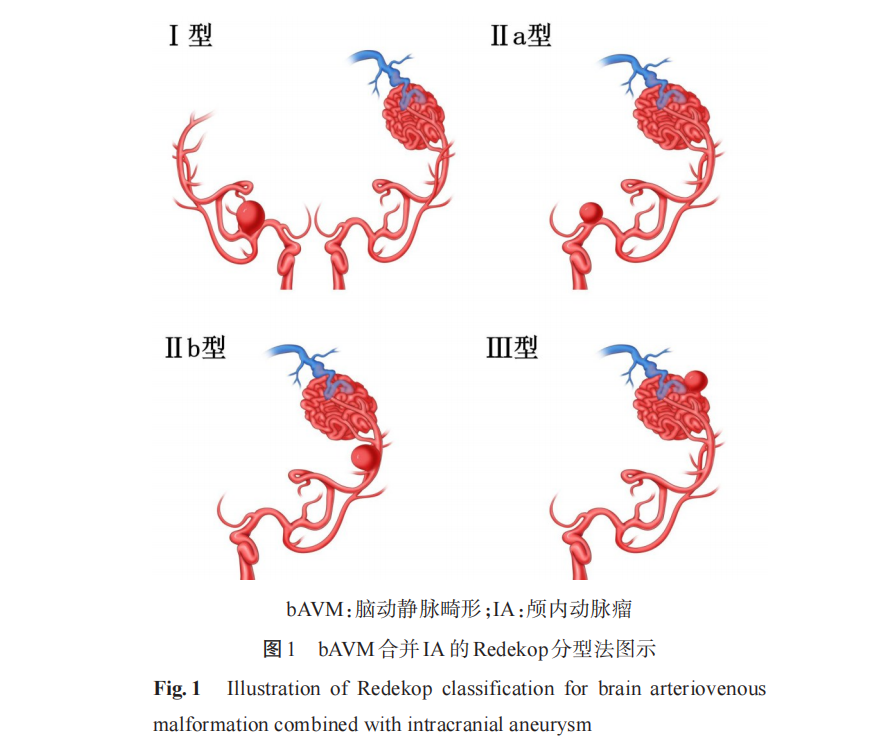
目前,Redekop分型法被较多国内外学者认可,该分型法将bAVM合并IA分为3型[28]:(1)I型(与bAVM供血动脉无关型):IA位于bAVM的非供血动脉上,与畸形血管团的血流供应无直接关联。(2)II型(供血动脉血流相关型IA):囊状IA起源于最终供应bAVM的动脉,其形成与供血动脉的血流动力学改变密切相关,进一步分为2个亚型:IIa型(供血动脉近端血流相关型)与IIb型(供血动脉远端血流相关型)。(3)III型(畸形血管团内型IA):IA位于bAVM的血管团内部,在血管造影早期(大量静脉充盈前)即显影;诊断时需排除单纯动脉扩张、漏斗样结构、静脉袋及静脉扩张等类似表现,以明确为真性IA。该分型法具体内容见表2、图1。

五、影像学诊断
(一)DSA
DSA是诊断bAVM合并IA的金标准,可高分辨率显示IA-bAVM复合体的供血动脉、畸形血管团及静脉引流,并定量评估动静脉分流程度[31-33]。四维DSA(4D DSA)进一步提升了时间分辨率,在观察畸形血管团内IA、瘘口等细节方面更具优势[31,34]。
(二)头颅CT/CTA
常规CT对未破裂的bAVM敏感性有限。若合并急性出血,其血肿及占位效应也会干扰对bAVM本身的准确定位。但若血肿内伴发钙化,则可视为提示潜在bAVM的重要间接征象[33]。
CTA具有无创、快速、成本较低及风险较小的优势,在紧急手术场景中可作为DSA的可靠替代方案。CTA结合容积渲染、最大密度投影(MIP)、多平面重建(MPR)等多模式后处理技术,可一次性清晰显示bAVM与IA的供血动脉、引流静脉、病灶位置、大小、形态,以及伴发的血栓或钙化,为术前精准评估提供关键的解剖与血流动力学信息[35]。CTA的局限性主要表现为静脉显影易受干扰,尤其在颅底区域(如海绵窦),骨性结构产生的伪影常导致静脉轮廓辨识困难。
(三)头颅MRI及MRA
头颅MRI可在T2WI中清晰显示bAVM特征性的“扩张血管流空”信号,是筛查未破裂bAVM的首选检查手段;但其对畸形血管团内IA的识别能力有限。在急性出血期,MRI对新鲜出血的敏感性较低;其核心价值在于识别陈旧性出血(表现为皮质/皮质下含铁血黄素沉积形成的弧形或窦状低信号),从而判断患者既往是否存在破裂史。MRA的空间分辨率略低于CTA,但具有无创、无辐射的特点,适用于儿童、孕妇及需长期随访患者的复查。然而,其对供血动脉、引流静脉及IA显示的敏感性与特异性仍不及DSA,因此不能单独作为指导治疗决策的依据。
(四)对比增强MRA及四维血流MRI
对比增强MRA(contrast-enhanced magnetic resonance angiography,CE-MRA)在评估bAVM合并IA时,对畸形血管团的检出率与时间飞跃法MRA(time-of-flight magnetic resonance angiography,TOF-MRA)相当,而对供血动脉及引流静脉的显示更优[36]。CE-MRA对治疗后bAVM的随访具有良好的诊断灵敏度及特异度,有助于识别残留bAVM并减少随访期间过度使用DSA[37]。
四维血流MRI(4D-flow MRI)可无创评估bAVM复杂的血流动力学,其在诊断和分型方面与DSA具有良好一致性[38];该技术能弥补TOF-MRA及单相CE-MRA时间分辨率不足的局限,清晰区分动静脉期,有助于风险分层与治疗计划优化。治疗后,4D-flow MRI检测残留bAVM的特异性高而敏感性低,阴性结果不能等同于治愈[39-40]。对于放射外科术后患者,可考虑以其随访至畸形血管团消失,再以DSA确认。
高分辨率MRI(high-resolution magnetic resonance imaging,HR-MRI)可清晰显示IA的壁层细节与邻近关系,对评估IA壁结构异常、炎症及不稳定性具有潜在价值[41-43]。然而,仍需进一步研究证实HR-MRI对bAVM本身不稳定性及破裂风险的预测效能[44]。
推荐意见1:(1)增强CT和(或)CTA为重要的辅助检查工具,有助于定位出血患者的出血源,为紧急救治提供重要参考(推荐等级:I级)。(2)MRI及MRA是筛查未破裂bAVM的重要手段,也可用于陈旧性出血评估及长期随访(推荐等级:I级)。(3)HR-MRI对评估合并IA的瘤壁炎症或不稳定性具有潜在价值,可作为风险评估的补充手段(推荐等级:II级)。
六、治疗现状与原则
目前,关于bAVM合并IA的治疗尚未形成统一标准,缺乏强有力的循证医学证据支持。不过,随着显微外科、血管内介入技术及放射外科的不断发展,治疗选择已显著拓宽。临床实践中,治疗方案的制定需综合考虑医疗机构的技术条件、术者的专业经验,并审慎评估干预的风险与收益比。系统综述及ARUBA研究显示,针对bAVM的外科手术(29.0%,范围1.5%~54.0%)、血管内治疗(25.0%,范围7.6%~55.0%)和放射外科治疗(13.0%,范围0.0%~63.0%)均存在不可忽视的并发症风险。[45-49]
(一)治疗目标
(1)预防出血:通过积极干预,降低病变破裂出血的风险,避免病情因急性出血而急剧恶化。(2)改善症状:缓解因病变导致的进行性神经功能损害,减轻临床症状(如头痛、癫痫、神经功能缺损等),提升患者的生活质量。(3)降低远期风险:减少复发性出血的潜在可能性,保障患者长期安全,降低疾病对远期生存及功能预后的不良影响。
(二)治疗原则
(1)风险评估优先:制定治疗方案前,必须全面细致评估干预措施的风险,确保其不超过病变本身所致的长期致残或致死风险,以实现治疗效益最大化。(2)个体化治疗决策:现有证据未显示IA分布与bAVM的Spetzler-Martin分级存在显著相关性。因此,治疗决策应基于个体化风险评估,而非单纯依据bAVM的解剖复杂性;尤其对于急性破裂出血患者,准确识别出血源对预后判断及治疗方案制定至关重要[28,50]。
(三)出血性病例的治疗
对于出血性病例,其处理应遵循个体化原则,核心目标在于优先处理已破裂的出血责任病灶(明确为bAVM血管团或IA):若为浅表病灶破裂,在开颅血肿清除术时可考虑同期联合实施病变切除或IA夹闭;若为深部病灶破裂,则可优先行血肿清除或考虑血管内干预。方案选择需紧密结合病灶位置、患者基础状况等个体特征。必须强调的是,临床上目前尚无单一、可靠的方法能完全准确地鉴别出血责任病灶(bAVM血管团或IA),这一不确定性是导致诊疗决策复杂化的核心。
现有的判断主要依赖于对影像学特征的专业解读与临床经验的综合分析(准确性存在局限):CT显示出血部位距离bAVM血管团越远,IA破裂可能性越大[51];单纯蛛网膜下腔出血(subarachnoid hemorrhage,SAH)而无脑内血肿(intracerebral hematoma,ICH)强烈提示IA破裂[3];邻近IA的局灶性血肿合并SAH,也提示IA为出血源;当存在ICH(伴或不伴SAH)时,需分析出血中心与bAVM血管团内血管结构的关系。动态CTA有助于阐明IA与出血的空间关系[50]。因此,在治疗破裂出血患者时,必须对二者进行全面的风险评估,综合考虑影像学提示的高危因素(如形态不规则的IA、畸形血管团内IA、假性IA等),以制定最为安全有效的个体化策略。
1. IA确定为出血源时:应尽早参照孤立囊性IA标准,采用外科手术或血管内技术处理;若IA邻近bAVM且bAVM本身可手术切除,可考虑同期处理两处病灶;供血动脉近端血流相关型IA,根据其位置、形态及术者经验选择手术或血管内治疗[30,52-53]。
2. 穿支假性IA确定为出血源时:需及时干预或密切影像学随访。假性IA缺乏完整血管壁,急性期常呈“动态”变化(早期易扩张再破裂,亦可能自发消退);因其多位于深部穿支,手术难度大。若能在假性IA近端建立安全的血管内通路,血管内技术具有优势[50]。
3. bAVM为出血源时:建议参考目前bAVM最新指南或专家共识优先处理bAVM,对于表浅病变,在开颅血肿清除术时,可以考虑同时进行切除或夹闭;深部病变在急性期可能需要优先进行血肿清除或采取血管内干预措施。若手术或介入可及,可考虑同期处理IA[54-56]。
推荐意见2:(1)明确出血源:应结合CT/MRI影像,综合评估出血特征及其与病变的解剖关系,出血部位距离bAVM血管团越远,IA破裂可能性越大;邻近IA的局灶性血肿合并SAH,也提示IA可能为出血源(推荐等级:III级)。(2)IA破裂:可参照单纯IA原则急诊处理。若计划行血管内治疗,需评估支架植入的必要性;若必须植入支架,应权衡其抗血小板治疗可能带来的出血风险。在此情况下,可考虑选择手术夹闭(推荐等级:III级)。(3)bAVM破裂:建议按照bAVM现有指南或专家共识优先处理bAVM,若手术或介入可及,可考虑同期处理IA(推荐等级:III级)。
(四)未破裂病例的处理
对于未破裂的bAVM合并IA,最佳治疗策略存在显著争议。国际ARUBA研究[45,57]提示未破裂bAVM干预风险可能高于其自然病史风险,倾向于保守观察;而国内临床实践则更多基于对病变高出血风险的担忧,倾向于积极干预。目前缺乏专门针对此复合病变的高级别前瞻性研究证据,以精确量化干预与保守治疗的长期获益风险比,这使得治疗决策难以完全规避主观性。
1. 供血动脉远端血流相关型IA:研究表明,bAVM根治性治疗后,此类IA可能缩小甚至消失。长期随访显示,bAVM完全闭塞后,80%的远端IA消退,且未发生与之相关的SAH。因此,若bAVM已获根治,对于小而远的IA可考虑保守管理[28]。
2. 供血动脉近端血流相关型IA:bAVM治疗后,多数(78.3%)保持稳定,少数缩小(17.4%)或闭塞(4.3%)[28]。
3. Redekop分型法指导治疗决策:Redekop分型法为未破裂bAVM合并IA的个体化治疗提供了重要框架,但在面对具体患者时,治疗顺序(如同期处理与分期处理的选择、IA与bAVM的优先处理次序)的决策异常复杂,高度依赖于多学科团队对个体解剖特点、血流动力学、技术可行性及患者意愿的综合权衡,尚无普适的标准化路径。
(1)I型(与bAVM无关的IA):对于出血患者,治疗顺序依据出血来源确定:若明确bAVM是责任出血灶,则优先处理bAVM;若IA破裂,则需立即处理IA,之后再处理bAVM[50]。对于未破裂I型IA,治疗顺序应基于综合风险评估:低风险者通常保守处理,优先治疗bAVM直至其风险显著降低。当需对IA行支架辅助栓塞时,必须审慎评估抗血小板治疗对未处理bAVM出血风险的潜在影响。部分患者可在支架植入前接受分阶段多轮血管内栓塞以降低bAVM出血风险,且观察到此策略下无出血事件发生[58]。
(2)IIa型IA(位于主要供血动脉近端):因解剖位置复杂及相对较高的出血风险,常需更积极的治疗策略[3,59]。当bAVM与IIa型IA位于相同血管路径时,可考虑同期治疗。为规避bAVM根治术后供血区血流动力学改变引发IA破裂的风险,通常优先处理IA:采用血管内栓塞供血动脉及IA,或显微外科术中优先夹闭IA。
(3)IIb型IA(位于主要供血动脉远端):IIb型IA若与bAVM血管团紧邻,可在一期显微外科治疗或血管内治疗bAVM时同步夹闭或栓塞IA;若邻近Willis环,则先行处理bAVM以降低血流冲击,待血流动力学负荷缓解后再二期处理IA[60]。
(4)III型(畸形血管团内IA):畸形血管团内型IA结构是病灶的薄弱点,可能是血流动力学以及局部炎症反应共同作用于畸形血管壁的结果,需要积极干预,可通过血管内栓塞bAVM时同期栓塞IA,或在显微外科切除bAVM时同期处理IA,介入栓塞时通常使用液体栓塞剂进行填塞[61]。
4. 放射外科治疗:既往研究发现合并IA会增加出血性bAVM立体定向放射外科(SRS)治疗后再出血的风险。Kano等[62]通过对其机构近30年数据的回顾性分析发现,伴有IA的bAVM发生率为11%。在SRS治疗后5年内,合并IA患者的bAVM再出血率是无IA患者的5倍(分别为26.7%、5.2%),而IA被夹闭或栓塞的bAVM患者再出血率为6.2%。因此建议在SRS治疗前对bAVM合并IA采取更积极的干预,以最大限度降低再出血风险。然而Ding等[63]研究发现合并IA的bAVM患者SRS术后的年出血率(3.3%)虽高于未合并IA的bAVM患者(2.0%),但差异无统计学意义(P>0.05)。Tsuei等[64]研究了bAVM合并血流相关型IA经SRS治疗后的形态学变化,发现较小的血流相关型IA(<5 mm)在bAVM闭塞后倾向于自发闭塞。这些提示医疗人员可能要充分评估bAVM和IA的形态与相互关系后再制定治疗方案。
推荐意见3:(1)I型(bAVM供血动脉无关型IA)需按照常规未破裂IA的管理原则进行处理,重点在于综合评估IA自身的破裂风险(需考量其大小、形态、位置及瘤壁是否强化等特征)与bAVM的出血风险(可基于Spetzler-Martin分级等工具),并进行审慎权衡(推荐等级:I级)。(2)II型(供血动脉血流相关型IA):无论IIa还是IIb型都需谨慎评估和权衡IA与bAVM的破裂风险,对于非常靠近畸形血管团,尤其是细小供血动脉上、形态不规则且直径(最大径)大于供血动脉的IA,应积极治疗IA,尽可能在治疗bAVM时同期栓塞;排除高破裂风险IA后,多数该类型IA保持稳定,可考虑采取保守治疗随访观察,若后续出现形态或血流动力学变化,则需积极干预(推荐等级:III级)。(3)III型(畸形血管团内型IA):在对bAVM进行治疗时,可考虑同期处理该类型IA(可采用栓塞或外科手术方式)(推荐等级:I级)。
(五)复合手术技术的应用
复合手术室是实现多模式无缝衔接的重要平台,其术中实时血管成像技术为复杂bAVM合并IA的手术提供了全方位支持。对于出血起病患者,术中DSA结合动态CT能有效鉴别出血来源(畸形血管团或IA),并对责任病灶进行精确定位,从而指导血肿清除与靶向处理;术中DSA能三维重现病变血管构筑,为手术路径规划与实时调整提供解剖学依据。此外,在处理IA后,可即刻验证其是否被完全夹闭或栓塞,并评估载瘤动脉通畅性。在切除畸形血管团后,术中DSA作为判断有无残留的“金标准”,可在术中发现残留灶时同期进行补充处理,力争实现解剖学治愈,有效规避二次手术风险。
推荐意见4:复合手术室(术中DSA/动态CT)是复杂bAVM合并IA的重要治疗平台,可实现以下术中实时影像功能:(1)责任灶判定:协助定位出血源(bAVM/IA破裂),辅助血肿清除及靶向处理;(2)三维影像支持:术中脑血管造影、重建血管结构(供血动脉/引流静脉/IA),辅助手术规划与执行;(3)通过即时DSA评估切除与栓塞效果,为同期处理残留病变提供支持,避免二次手术(推荐等级:II级)。
(六)颅内支架的应用
在合并IA的bAVM患者中,植入颅内支架后的双重抗血小板治疗(DAPT)与未处理的bAVM之间存在冲突。DAPT是预防支架内血栓形成的关键措施,尤其在植入后前3~6个月的内皮化关键期不可或缺。然而,抗血小板药物也可能增加bAVM的出血风险。目前,尚缺乏大规模前瞻性研究证据指导该类患者DAPT的安全实施,抗栓强度与疗程亦无明确标准,临床实践中需结合个体出血风险与抗栓获益进行审慎权衡。
现有少数病例报告为血流导向装置(FD)在此类患者中的应用提供了有限的安全性提示。文献显示,部分bAVM合并IA患者(包括急性出血期及儿童病例)在FD治疗及相应抗血小板方案后未发生bAVM再出血或出血加重,且预后良好[58,65-66],提示在严格围术期管理下,FD治疗可能具有一定的安全性。尽管如此,基于当前极低等级的证据,本共识仍认为应对该技术持高度谨慎态度。
总体而言,颅内支架(包括普通辅助支架与FD)在bAVM合并IA治疗中的证据基础极为薄弱。因此,不推荐将颅内支架(特别是FD)作为常规治疗选择。如经多学科团队评估后确有必要使用,必须在术前向患者及家属充分告知现有证据的缺乏与治疗相关的不确定性。
推荐意见5:(1)bAVM合并IA的治疗中,FD或普通支架辅助栓塞仅可作为其他治疗方式失败或不可行时的备选方案,且需经多学科团队评估确认(推荐等级:II级)。(2)实施颅内支架治疗前必须个体化评估抗血小板治疗对未处理bAVM出血风险的潜在影响,并在知情同意谈话中明确告知患者相关风险(推荐等级:I级)。
七、结论与展望
bAVM合并IA是神经外科领域极具挑战性的疾病之一,应综合考量病变的Redekop分型、血流动力学特征、患者的临床状况(如是否破裂、神经功能状态)以及医疗机构的技术条件,进行审慎的权衡与决策。
当前,该领域的临床实践仍面临诸多挑战,包括出血责任病灶判定的不确定性、未破裂病例治疗策略的分歧,以及对FD等新技术应用长期安全性与有效性的未知。本共识对此均予以了探讨,并对颅内支架(尤其是FD)等证据不足的技术持高度谨慎态度,旨在最大限度地保障患者安全。本共识仅代表参与编写专家的学术性共识意见,不具备法律效力,临床应用时应参考其他循证医学证据及患者个体情况综合判断。本共识内容将依据临床实践的改进及研究进展不定期修订。
本共识专家组成员
执笔:冯欣、李西锋(南方医科大学珠江医院);邓剑平(空军军医大学唐都医院);何旭英(广东省第二人民医院)
专家组成员(按姓氏汉语拼音排序):曹文锋(江西省人民医院)、曹毅(昆明医科大学第二附属医院)、柴尔青(甘肃省人民医院)、陈锷(厦门大学附属中山医院)、陈光忠(广东省人民医院)、陈文伙(福建医科大学附属协和医院)、陈左权(同济大学附属第十人民医院)、程道宾(广西医科大学第一附属医院)、邓剑平(空军军医大学唐都医院)、段传志(南方医科大学珠江医院)、冯欣(南方医科大学珠江医院)、宫崧峰(深圳市第二人民医院)、顾宇翔(复旦大学附属华山医院)、管生(郑州大学第一附属医院)、韩建峰(西安交通大学医学院第一附属医院)、何旭英(广东省第二人民医院)、洪韬(首都医科大学宣武医院)、黄昌仁(西南医科大学附属医院)、姜长春(包头市中心医院)、焦力群(首都医科大学宣武医院)、李西锋(南方医科大学珠江医院)、李永利(哈尔滨医科大学附属第二医院)、刘建民(海军军医大学第一附属医院)、买买提力·艾沙(新疆医科大学第一附属医院)、南光贤(吉林大学中日联谊医院)、彭亚(常州市第一人民医院)、石忠松(中山大学孙逸仙纪念医院)、史怀璋(哈尔滨医科大学附属第一医院)、宋冬雷(上海冬雷脑科医院)、苏世星(南方医科大学珠江医院)、孙钦建(山东第一医科大学附属省立医院)、万杰清(上海交通大学医学院附属仁济医院)、汪阳(首都医科大学附属北京朝阳医院)、王东海(山东大学齐鲁医院)、王峰(大连医科大学附属第一医院)、王君(中国人民解放军总医院第一医学中心)、王培明(广东三九脑科医院)、吴红星(新疆维吾尔自治区人民医院)、徐翔(唐山工人医院)、许璟(浙江大学医学院附属第二医院)、杨鹏飞(海军军医大学第一附属医院)、杨新健(首都医科大学附属北京天坛医院)、姚声涛(遵义医科大学附属医院)、于加省(华中科技大学同济医学院附属同济医院)、喻孟强(中南大学湘雅二医院)、张鸿祺(首都医科大学宣武医院)、张猛(陆军军医大学大坪医院)、张猛(深圳市第二人民医院)、张品元(河北医科大学第三医院)、张天(四川省人民医院)、张炘(南方医科大学珠江医院)、赵沃华(华中科技大学同济医学院附属同济医院)、郑洪波(四川大学华西医院)、钟书(中山大学附属第一医院广西医院)、朱刚[陆军军医大学第一附属医院(西南医院)]、朱良付(河南省人民医院)
参考文献略
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。











