
四川大学华西医院神经外科关俊文教授团队与疾病系统遗传研究院张定坤副研究员团队合作,于2025年3月在Chemical Engineering Journal(IF:13.3)发表文章“Nanometabolomics elucidated biological response of 3D printed vascular stents: Towards metabolic reprogramming of metabolome and lipidome”(扫描下方二维码阅读原文)。3D打印血管支架(3D-PVS)为血管相关疾病治疗提供了卓越的解决方案,但其应用过程中的详细分子机制尚不清楚。本研究利用纳米代谢组学(包括基于纳米材料的非靶向/靶向水溶性代谢组学、脂质组学和空间代谢组学)技术阐明了3D-PVS的生物响应特性,揭示其在应用过程中对糖酵解、氨基酸代谢及脂质稳态的调节作用,为其深入的生物医学应用提供了新思路。

3D打印技术有诸多优点且在多领域有广泛应用,3D-PVS(图1)是其在生物医学领域的典型应用之一。血管疾病是发达国家死亡和残疾主要原因,商用血管支架是治疗血管狭窄的有效器械,但传统方法制造的标准支架存在因血管形态异质性、稳定性和生物相容性不理想等导致的问题。相比之下,3D-PVS有生物相容性更好等优点。然而,目前基于3D-PVS的生物响应特性分析大多停留在表型水平,缺乏深入的分子机制研究。幸运的是,纳米代谢组学为解析“3D-PVS-生物体”相互作用的分子机制提供了新途径,但此前对3D-PVS诱导的代谢机制变化在分子水平了解甚少,因此基于纳米代谢组学开展血管支架相关研究具有重要意义与应用前景。

图1 基于纳米代谢组学探索3D-PVS生物响应特性的研究流程
本研究围绕3D-PVS与人脐静脉内皮细胞(HUVECs)和SD大鼠的多维相互作用展开(图2),通过体外和体内建模与分析,利用纳米代谢组学系统探讨了3D-PVS对生物体代谢过程的影响,并验证了其在体内环境的治疗效果。
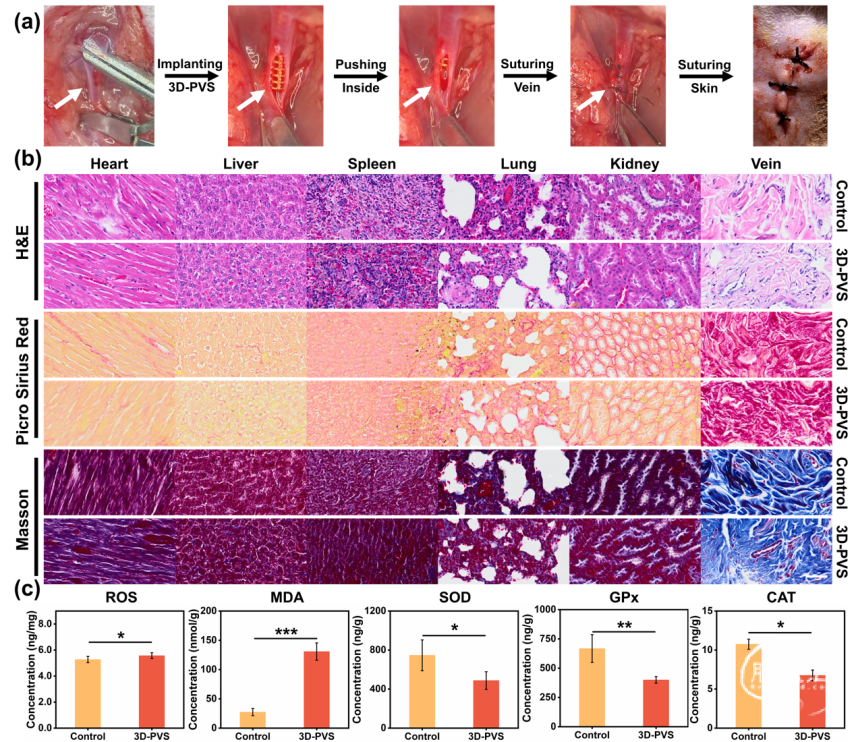
图2 基于体内模型的病理学、影像学和生物化学研究
本研究首先对细胞模型进行非靶向纳米代谢组学分析,以初步分析3D-PVS诱导的细胞代谢变化,然后在大鼠模型中进行靶向纳米代谢组学研究,基于上述非靶向纳米代谢组学结果,深入探究3D-PVS诱导的代谢重编程(图3)。本研究是首次使用纳米代谢组学方法在代谢水平上研究3D-PVS生物学效应的尝试。
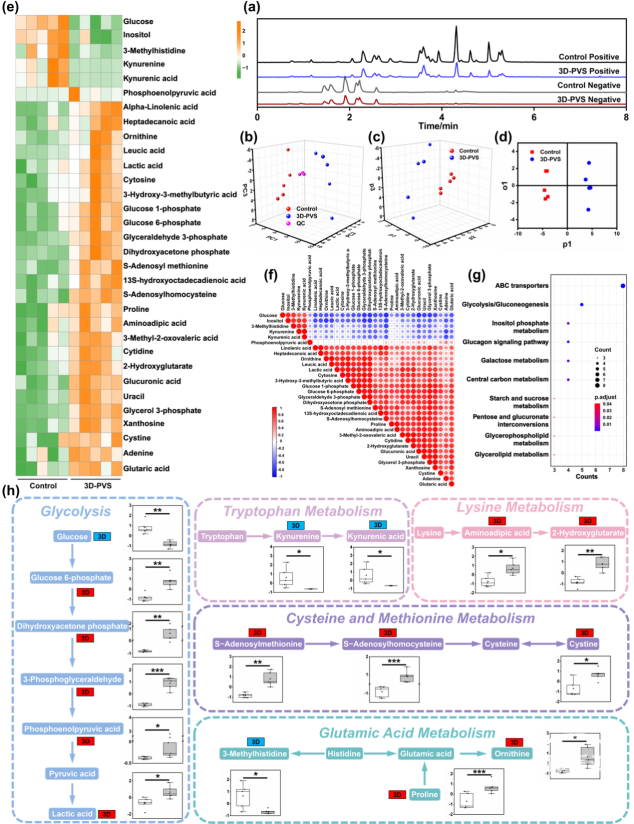
图3 基于体内模型的靶向水溶性代谢组学研究
非靶向纳米代谢组学结果显示,3D-PVS的体外安全浓度范围(<15 mg/mL)对氨基酸或有机酸相关代谢,以及磷脂、鞘脂或甘油脂相关代谢过程有一定影响。此外,靶向纳米代谢组学结果进一步揭示了体内3D-PVS诱导的糖酵解和氨基酸代谢(包括色氨酸代谢、半胱氨酸和甲硫氨酸代谢、谷氨酸代谢以及赖氨酸代谢)的改变,以及一些脂族(包括PC、PE、PS、MAG、DAG、Cer、SM、CE、Car和FFA)的稳态改变(图4)。基于纳米代谢组学结果,相信这项工作将成为在代谢水平上对3D-PVS的创新性探索,为其在生物化学、医学和工业领域的潜在应用和发展提供思路。此外,基于3D-PVS的纳米代谢组学可被视为对经典代谢组学方法的创新,进一步推动了纳米代谢组学在解析基于3D打印纳米材料的生物响应特性方面的技术和方法不断进步。
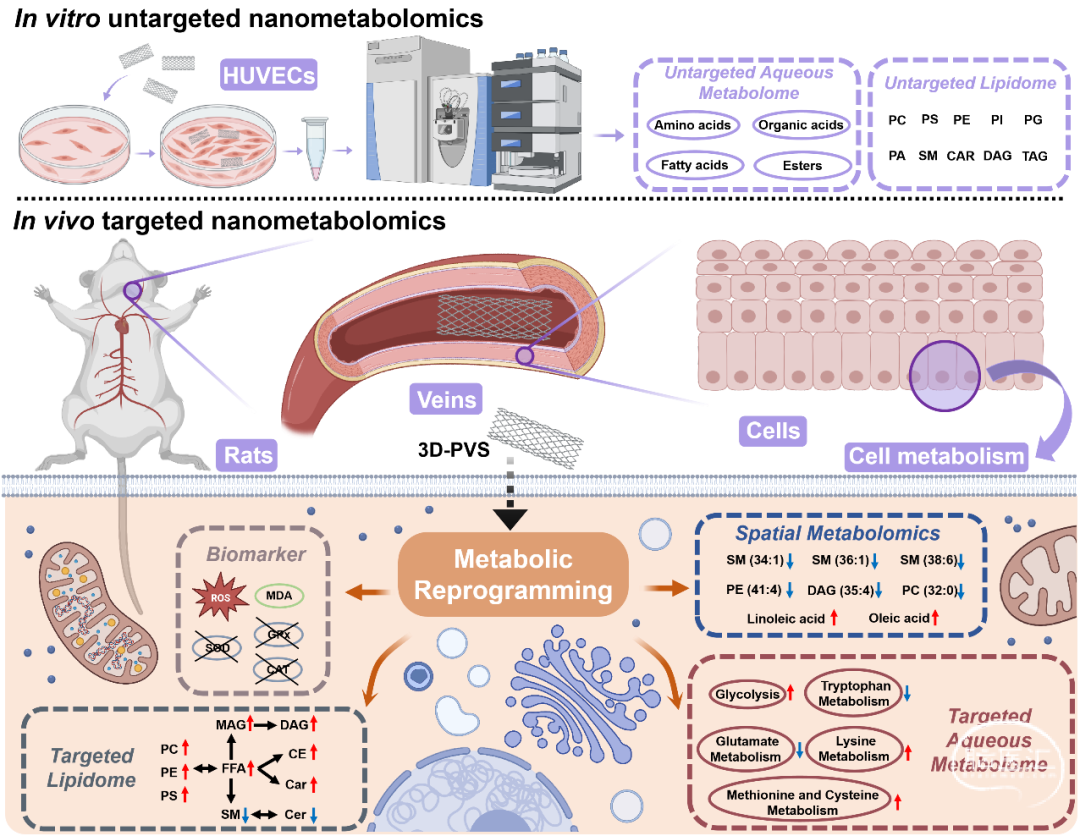
图4 “3D-PVS-生物体”相互作用中生物学过程与通路
专家点评
徐建国教授:研究团队通过多层次的研究设计,结合了体外细胞模型和体内动物模型,采用非靶向和靶向代谢组学、脂质组学以及空间代谢组学技术,从细胞水平到组织水平全面评估3D-PVS的生物相容性和其对糖酵解、氨基酸代谢和脂质代谢的代谢调控作用,这种从微观到宏观的研究策略确保了结果的可靠性和普适性。研究采用了多维度技术手段,包括非靶向和靶向代谢组学、脂质组学以及空间代谢组学,特别是空间代谢组学技术的应用,直观展示了代谢物的空间分布变化,为机制研究提供了直接证据。研究团队运用了PCA、PLS-DA、OPLS-DA等多变量统计分析方法,结合热图、火山图等可视化手段,提高研究的科学性,为生物材料与细胞代谢相互作用的研究提供了新的技术路径。

徐建国,教授,主任医师,博士生导师,四川大学华西医院神经外科主任,四川大学神经疾病研究所所长。四川省学术和技术带头人,中国医师协会神经外科分会副会长、颅底外科学组副组长,中国医疗保健国际交流促进会颅底外科分会副主委。擅长颅底外科(如垂体腺瘤、颅咽管瘤、鞍结节和蝶骨嵴脑膜瘤、前床突脑膜瘤、错构瘤、脊索瘤等),能够高质量完成颅底神经外科各类复杂的高难度手术,效果达到国际先进水平。以第一/通讯作者身份发表论文300余篇,250篇发表在Neurosurgery、J Neurosurg、J Neurooncol、Neurology 等期刊。主持国家自然基金面上项目4项,获得中华医学科技进步奖一等奖、教育部科技进步奖二等奖,“王忠诚医师奖”。
专家点评
沈百荣教授:本研究具有重要的转化潜力,证实了3D-PVS在低浓度下具有良好的生物相容性,为其在血管支架植入和修复中的临床应用提供了安全性依据。同时,研究深入解析了3D-PVS的代谢调控机制,为优化血管支架的设计和功能提供了理论支持,有助于开发更高效的血管修复材料。团队通过代谢组学技术评估了3D-PVS对代谢状态的影响,为临床决策提供科学依据,更为重要的是,3D打印技术的引入使得个性化定制血管支架成为可能,这不仅满足紧急手术的需求,还为复杂病例提供了新的解决方案。总体而言,本研究为临床实践和生物材料领域的创新提供了新的思路和技术支持。

沈百荣,教授、博士生导师,四川大学华西医院疾病系统遗传研究院院长,兼任西雅图系统生物学研究所和西班牙巴斯克等大学教授;教育部101计划“医学数据采集与分析”虚拟教研室负责人,四川省“十四五”规划“数字健康”专家组组长等。2008年回国至今主持基金委等国家级项目10多项、培养研究生100余人,在医学、生物学和信息学国际期刊上发表交叉学科研究论文280余篇,任主编出版《转化信息学》等中英文著作和规划教材10余部。
作者心得
本研究发表于化学工程领域知名期刊Chemical Engineering Journal(CEJ),该期刊是一本专注于化学工程及相关交叉领域的权威国际刊物,影响因子13.4,2023年JCR学科类别“工程、生物医学”98种期刊中排名第4位。在化学工程与生物材料交叉领域认可度极高,对论文的创新性、科学性和实用性有着严苛要求,收录的论文广泛覆盖了化学工程技术在生物材料设计、生物医学应用等多方面涉及的物理、化学和生物科学内容。
本研究聚焦于3D打印聚合物血管支架在生物医学领域的应用,不仅开发出制造薄壁支架的潜在方法,还利用代谢组学深入阐明了其生物响应特性并揭示相关分子机制,与CEJ所关注的前沿研究方向高度契合,所以我们首选它作为投稿期刊。投稿过程中,两位审稿人充分肯定了研究的创新性和价值,同时也提出了诸多专业且中肯的意见和建议。我们认真对待每一条反馈,经过反复修改和补充实验,对研究进行了全方位的充实和完善,最终论文得以在CEJ顺利发表。在此衷心感谢四川大学和华西医院对生物医学研究平台的大力支持,同时也特别感谢各位领导和专家在研究过程中的悉心指导和教诲,让我们能够不断突破自我,取得更优异的科研成果。
通信作者

关俊文,教授,硕士生导师,四川大学华西医院神经外科主任医师,一级专家。现任四川省医学会神经外科专委会创伤组组长、四川省生理科学会神经损伤与修复专业委员会主委等职务。从事神经外科专业30余年,主要擅长手术治疗各种急慢性复杂颅脑创伤以及颅脑创伤后并发症、各种慢性意识障碍的评估和促醒治疗、脑积水等脑脊液循环障碍、前中颅底损伤的手术治疗。团队每年手术治疗促醒和颅脑创伤及相关疾病500余台次。获省部级科研基金项目多项、医学成果奖以及专利,多次参加国内外专业学术交流并在大会主持和发言。已发表论文50余篇,其中在Neurology,Brain Res、Neurosciences 等期刊发表论文30余篇。
通信作者

张定坤,清华大学博士,东京大学博士后,四川大学华西医院疾病系统遗传研究院副研究员。四川省海外高层次留学人才。主要研究方向为基于代谢组学技术的生物医学材料应用与疾病分子机制研究。主持国家自然科学基金青年项目、四川省科技厅重大项目、四川省科技厅青年项目等。发表SCI论文23篇,其中以第一/共同第一作者在Biomaterials、ACS Nano、Chem Eng J、Carbon 等期刊发表论文16篇。第一作者身份拥有授权专利2项,受理专利8项,参加国内外学术会议20余次并作现场汇报。以第一参与人获得北京市级奖励1项,获得HK Tech 300创新创业千万大赛全国决赛10强,“蓉漂杯”高层次人才创新创业大赛成都赛区30强等荣誉。
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。





