
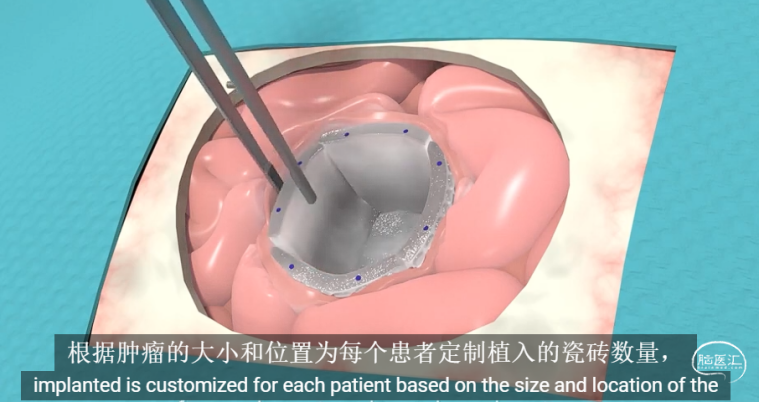
美国GT Medical Technologies, Inc.(GT MedTech)医疗器械公司主力研发的创新产品——GammaTile®(伽玛贴)是一种嵌入铯-131粒子的生物可吸收胶原植入物。铯-131是一种常用于低剂量率(LDR)近距离放射治疗的放射性同位素,其微小的放射性粒子可直接植入肿瘤内或其邻近部位。GammaTile疗法适用于手术靶向放射治疗(STaRT),在肿瘤切除时能立即对病灶部位进行高强度剂量的放射治疗。该疗法能够向癌细胞释放高放射剂量,同时最大程度地减少对周围健康组织的损伤。目前,该产品已通过美国食品与药品监督管理局(FDA)认证,用于治疗新确诊的恶性颅内肿瘤患者以及复发性颅内肿瘤患者。


2024年11月13日,GT MedTech公司宣布,其已达成两项有助于拓展GammaTile®应用的临床里程碑。第一项里程碑,是位于德克萨斯州布鲁克陆军医疗中心(BAMC)完成的第1500例GammaTile植入手术。该手术由该中心Ryan Morton博士完成,患者是一例复发性胶质母细胞瘤。
第二项里程碑,是针对GammaTile安全性和有效性开展的第一项大型多中心、观察性注册研究——“STaRT(手术靶向放射疗法)应用于脑肿瘤患者的登记研究(NCT04427384)”,已经成功招募了第400例患者。入组的患者将在脑肿瘤切除术后立即接受GammaTile放射治疗永久性植入。

该研究的目标是通过评估真实世界中的临床结局和患者报告的结果,评估STaRT疗法的临床效果、安全性,及其对患者的潜在风险和益处。研究预计纳入600例手术切除后接受STaRT治疗的脑肿瘤患者(涵盖所有病理类型),主要终点是转移性肿瘤患者治疗后12个月内的无复发生存期(RFS)、脑膜瘤患者治疗后3年内的RFS,以及高级别胶质瘤患者治疗后9个月的总生存期(OS)。此外,研究计划在未来5年内收集术后随访信息,包括局部控制情况、OS、生活质量、功能状态,以及与手术和放射治疗相关的不良事件。该研究于2020年9月11日启动,预计将在2028年10月31日完成主要研究部分,2028年12月31日完成全部研究。
纳入标准:
√ 接受最大程度安全切除术并植入GammaTile的脑肿瘤患者(年龄不限);
√ 签署知情同意书并参与所有评估的患者。
排除标准:
√ 无法进行术前、术后影像学检查以评估病情和植入情况的患者;
√ 由研究者评估患有严重医学或精神疾病,且会影响治疗完成情况、完成入组评估的能力和/或随访过程的患者;
√ 因缺乏英语流利性而无法完成英文版神经认知和生活质量(QOL)评估测试的患者。
GT MedTech公司首席医疗官兼临床开发部主任Michael Garcia博士表示:“全美多家独立医疗机构已相继发表了关于使用GammaTile治疗脑转移瘤、胶质母细胞瘤和脑膜瘤的临床经验。这些研究结果一致表明,GammaTile疗法在疗效和安全性方面表现出色,并具有高度可重复性。基于这些实践数据与注册研究的结果,GammaTile疗法已在美国医生中获得了越来越多的认可和采用。”
关于GT MedTech医疗技术公司

GT MedTech(www.gtmedtech.com),一家由脑肿瘤领域专家团队创立的医疗技术公司,专注于提高脑肿瘤治疗标准并提升患者的生活质量。公司研发的GammaTile®贴片已获得FDA认证,适用于治疗新确诊的恶性颅内肿瘤患者以及复发性颅内肿瘤患者。自2020年3月在美国全面上市以来,GammaTile已被100多家顶尖医疗机构采用,而且每月还有更多的医疗中心加入使用行列。
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。




