
Pearls
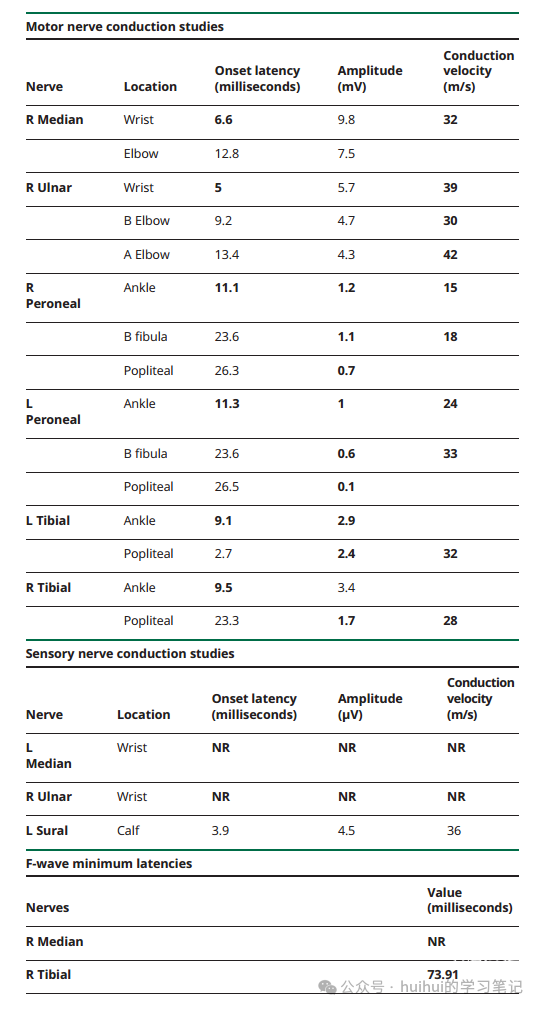
本研究符合欧洲神经病学学会/周围神经学会慢性炎症性脱髓鞘性多神经根神经病变的电诊断标准。右正中、右尺、双侧腓骨和右胫骨运动反应有传导速度减慢(低于正常下限≥30%且振幅保留)。右尺、双侧腓骨和双侧胫骨运动反应的远端潜伏期延长(高于正常上限≥50%)。排除右侧正中运动反应,因为该神经远端潜伏期延长可由手腕正中神经病变引起。右正中和右胫骨运动反应f波潜伏期延长(高于正常上限20%)。双侧腓骨和右胫骨运动反应存在传导阻滞(近端相对远端负峰复合肌动作电位振幅降低≥30%)。左尺神经、左正中神经和左腓肠神经感觉反应异常。
加粗部分为异常值。正常值:中尺运动发作潜伏期<4.2毫秒,幅值>5 mV,传导速度>50 m/s。
腓骨和胫骨运动发作潜伏期<6毫秒,振幅>2.5 mV,传导速度>40 m/s。中位感觉潜伏期<3.6毫秒,振幅10 μV,传导速度>45 m/s。尺感觉开始潜伏期<3.6毫秒,振幅15 μV,传导速度>45 m/s。
正中神经f波最小潜伏期<33毫秒。胫神经波最小潜伏期<61毫秒。
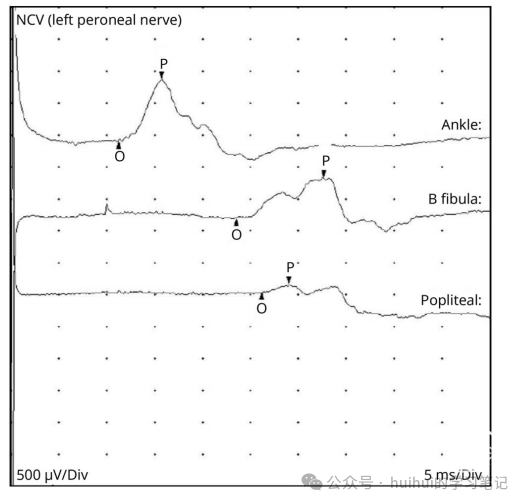
图像显示传导阻滞,其特征是近端刺激比远端刺激复合肌动作电位(CMAP)幅度降低30%以上,而时间弥散表现为近端刺激比远端刺激CMAP持续时间延长
自身免疫性节蛋白病(AN)是由抗体靶向连接周围神经节区和副神经区的胶质细胞和轴突的细胞粘附分子引起的。这些抗体靶向NF155、CNTN1、CASPR1和泛神经束蛋白(NF186/NF140和NF155),通过破坏来自轴膜的髓磷脂环和减慢传导导致致病作用。这些抗体一般属于IgG4亚类,缺乏激活补体系统的能力,对Fc受体的亲和力最低,导致对IVIG的反应较差。
AN的表现与CIDP相似,急性至亚急性发作,病程进行性或复发性。然而,由于潜在的病理,独特的临床特征,对治疗的反应,AN于2021年被EAN/PNS分类为一个独立的实体。每种AN抗体具有不同的临床特征。抗nf155是引起AN最常见的自身抗体。抗nf155相关AN患者通常较年轻,主要表现为远端感觉运动无力;感觉性共济失调;以及舌头、声音和四肢的高振幅、低频姿势性/有意性震颤。NF155也存在于中枢神经系统中,因此除了周围神经脱髓鞘外,还可引起中枢神经系统脱髓鞘病变。抗接触素-1(CNTN1)相关AN患者有急性至亚急性发作,伴有明显的感觉性共济失调、神经性疼痛、颅神经受累(主要是面神经)、体位性震颤和呼吸衰竭。抗接触素1阳性患者也存在肾病综合征。抗caspr相关AN的临床表现与抗接触相关AN相似。然而,它最初可表现为单相gbs样病程,与肾病综合征无关。考虑到IgG3抗体在病程早期介导发病机制,出现抗接触素-1或抗caspr抗体的AN病例也可能在急性期表现出对IVIG的初始反应。然而,向慢性期的转变涉及到类切换到IgG4,使IVIG的有效性降低最后,抗泛神经束蛋白相关AN伴抗nf155和抗nf186 /140表现为侵袭性急性-亚急性多神经病变,累及四肢脑神经、呼吸和自主神经一些分离。抗inf186也被报道,并模仿远端获得性脱髓鞘神经病变伴感觉性共济失调。
除临床表现外,脑脊液蛋白水平极高,神经影像学观察到神经根增强或增厚,表明血-神经屏障破坏,常支持AN的诊断基于电诊断测试很难区分AN和CIDP,因为两者都会显示获得性脱髓鞘的证据。如果进行神经活检,将显示末梢髓鞘袢脱离,轴周间隙变宽,神经内膜水肿,无炎症浸润,这可以区分AN和CIDP。
总之,AN是一个相对较新的实体,很容易被忽略。因此,对于节蛋白抗体的早期发现,尤其是具有不典型特征的难治性CIDP病例,如震颤、严重的感觉共济失调、脑脊液蛋白非常高,临床高度怀疑是必不可少的。当对免疫球蛋白治疗缺乏反应时,早期检测这些抗体是很重要的,因为AN可以用b细胞消耗剂逆转。
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。




