
运动功能障碍是脑卒中后最常见的后遗症,也是导致卒中后残疾的关键因素。虽然许多患者在经历卒中后得以幸存,但在随后的几年里不得不面对残疾带来的困扰。其中,至少有一半的患者需要依靠他人协助来进行日常的生活能力——如进食、自理和活动。
目前,物理康复是卒中后运动功能障碍的治疗方式,鉴于康复治疗的物理特性,主要作用于外周神经系统和肌肉组织,但对于大脑受损区域仅能产生间接影响,因此物理康复治疗的效果存在一定的局限性。
在此背景下,研究人员逐渐将目光投向了脑-机电生理康复疗法,通过对大脑皮层或皮层通路使用电生理刺激,期望借此促进卒中后患者的大脑神经元的修复,并且改善大脑结构与功能的可塑性。
其中,德国医疗科技公司CorTec旗下的核心产品——大脑交换系统(Brain Interchange,BIC),是一款完全植入体内的脑-机接口系统装置,能够实现神经刺激与测量感知的功能。该系统致力于发掘针对中枢神经系统的创新疗法,并探索脑-机接口技术的应用潜力。作为一款研究性设备,BIC系统目前共有32条专为试验设计的通路,拟用于中枢和外周神经的长期性电刺激和测量。据悉,BIC系统已于2024年5月获得了美国食品药品监督管理局(FDA)的试验用器械豁免(IDE)批准。
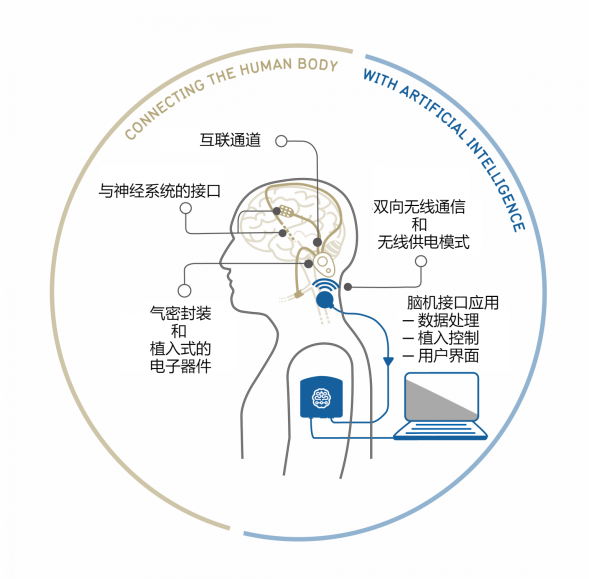
大脑交换系统(BIC)由多个组件构成,旨在连接外部与神经系统的信息互通,并通过这些组件,以实现对神经系统的功能调节。BIC系统的核心设备包括植入式的封装电子部件,主要负责放大和过滤神经信号,并将神经信号数字化。其次,系统采用了外部感应式供电技术,并配备了无线网络连接功能。最终,通过计算机上的软件执行遥测任务(包括参数控制、数据处理及传输),以便对脑-机互相接收的信号和参数进行分析以及管理。
据CorTec的首席技术官Martin Schuettler博士称,这种脑-机闭环式系统为高度个性化的治疗开辟新的途径。他指出:“我们所提供的BIC系统实现了生物学与技术、大脑与计算机之间的信息交流,可以为需要运用脑-机接口技术的创新疗法提供关键性的技术支持。”

“通过皮质神经刺激诱导可塑性运动功能的恢复(MRPICS)”(NCT06506279)是CorTec BIC系统的首个IDE临床试验,这项前瞻性、开放标签、介入式、单组试验研究,旨在通过BIC系统刺激大脑皮层,以促进大脑的神经重塑。该研究将应用CorTec BIC系统评估神经可塑性的效果,来验证对缺血性脑卒中后上肢运动功能障碍患者的康复疗效如何。
根据美国ClinicalTrials.gov官网最新公布的消息,MRPICS研究预计纳入4例22~75岁具有缺血性脑卒中后遗症的受试者,并计划于2025年1月15日正式启动,2028年6月15日完成主要终点工作,2030年6月15日完成总体研究。首席研究员(PI)为美国华盛顿大学医学院神经外科副主任Jeffrey G. Ojemann,并与美国国立神经疾病和卒中研究院(NINDS)协作开展。
该研究主要终点指标着重于评估上肢功能障碍,以确保采用CorTec BIC系统装置的刺激不会对患者造成不利的影响。在患者的康复期间,研究人员将对所有患者执行每周一次的肢体功能障碍评估。并且,在每月一次的随访中采用Fuegl-Myer(UEFM)和沃尔夫运动功能测试(WMFT)评估肢体功能情况,以跟踪个体运动功能和运动改善的趋势。
纳入标准:
. 年龄22 ~ 75岁
. 缺血性脑卒中病史;
. 缺血性皮质卒中后至少6个月;
. 上肢功能的偏瘫程度达到需进行手术干预的标准;
. 上肢Fuegl-Myer(UEFM)定义评分为25~45分,并愿意有效地配合这一康复治疗;
. 改良Rankin量表评估残疾程度为3~4之间;
. MRI成像显示皮质脊髓束保留率至少为30%;
. 可观察到经颅磁刺激(TMS)传递至运动皮层的上肢运动输出;
. 同意参与为期54周的研究,并配合在植入后第38周、移除后第16周接受多次随访;
排除标准:
. 在术前7天、术后3天内无法停用抗血小板药物;
. 正在接受抗凝治疗;
. 具有无诱因的深静脉血栓或任何肺栓塞既往病史;
. 存在出血性疾病病史的患者,在研究过程中可能会显著增加出血性并发症的风险。
. 由研究者酌情决定,存在其他病史提示血栓风险增加的患者;
. 有任何癫痫发作史;
. 妊娠;
. 老年抑郁症量表评分>10分;
. 蒙特利尔认知评估(MoCA)<22分,除非经PI批准可归因于失语症的患者;
. 哥伦比亚自杀意念量表(C-SSRS)得分>1分;
. 具有失语或认知缺陷的患者,以避免在执行研究过程中,难以实现有关疼痛和不适感的询问流程,或难以理解运动测试或康复测试要求;
. 根据美国国立卫生研究院卒中量表(NIHSS)第11题评分为2分——代表严重的偏侧忽视或一种以上的偏侧忽视,患者不认识自己的手或只能对一侧空间定位;
. 经研究人员判断,患者心脏病发病率可能会增加安全风险的患者;
. 具有自发性出血性卒中病史;
. 具有严重的神经科和精神科共病的、并可能干扰研究进程的患者;
. 正在进行抗菌治疗的传染病患者;
. 无法参与康复治疗安排的患者;
. 佩戴其他植入设备(工耳蜗、起搏器等)的患者;
. 在本项研究中,除了研究方案所提供的治疗措施外,任何需要接受本研究范围之外治疗(包括职业治疗、物理治疗或言语治疗)的患者将不予纳入。
此外,如果患者有肩关节半脱位、粘连性关节囊炎或上肢挛缩,则必须接受运动范围疼痛的额外筛查,并得到临床招募医生的批准;如果患者需要服用任何未明确排除在安全标准之外的药物,则由参与本研究的临床工作人员决定是否应该排除该患者,以确保本研究的完整性。以上所有纳入和排除标准将在装置植入手术后的90天内进行评估,但根据MRI成像复查的进度,PI可能会决定推迟这一过程。
关于CorTec

CorTec公司(https://www.cortec-neuro.com/)成立于2010年,总部位于德国弗莱堡。该公司专注于为工业界和临床领域提供尖端的神经技术解决方案。CorTec致力于为工业和临床客户供应关键组件与系统,并为特定病症研发创新型的医疗器械,以助力全新临床应用领域的开拓。
![]()
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。
投稿邮箱:NAOYIHUI@163.com
未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。




