前段时间遇到了一个慢性主动脉夹层动脉瘤的病人,有一些很可惜的点!学习下慢性主动脉夹层的一些管理要点。
慢性主动脉夹层的并发症包括脑卒中。当慢性主动脉夹层动脉瘤病人出现卒中时,要考虑是否瘤内有血栓形成导致的栓塞。夹层病人内科治疗需要严格控制血压120mmHg以下,心率60以下;一些影像特征提示需要手术干预(直径、增长速率)。支架术后也可以发生内漏(导致相关夹层动脉瘤生成),当出现一些相关并发症时也是需要处理的。
慢性B型主动脉夹层是指无名动脉开口以远的主动脉内膜撕裂(1区或1区以远 (图 1))且持续超过90日。慢性B型主动脉夹层的治疗特别困难,随着血管腔内技术的进步,其治疗方式在不断发展。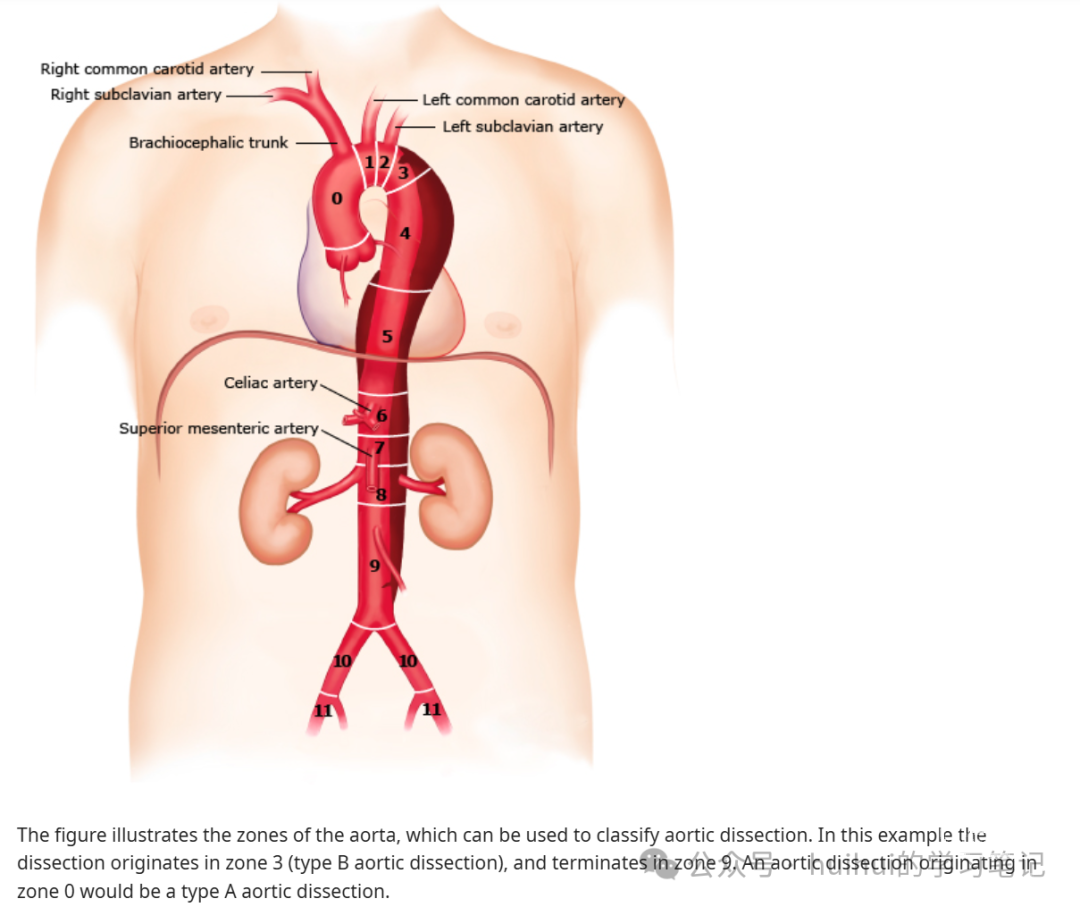
Figure1
慢性B型主动脉夹层的治疗主要基于临床特征。非复杂性慢性B型主动脉夹层通常采取内科治疗,并定期进行临床和影像学监测。若发生并发症(例如,动脉瘤样变性、灌注不良)或有明确高危特征,则需要干预。对于一些临床特征预示会发生并发症的非复杂性患者,早期(而非晚期)干预可能有益。对于符合解剖学要求且无结缔组织疾病的患者,一线治疗为胸主动脉腔内修复术。对于不适合腔内修复者,开放性手术修复是持久的治疗,但围术期并发症发生率和死亡率增加。主动脉夹层是指主动脉壁最内层(内膜)撕裂,导致高压血流进入主动脉层间,形成真腔和假腔。主动脉夹层的分类依据是初始撕裂口的解剖位置(A型、B型)、夹层的临床严重程度(非复杂性、复杂性、高危特征)和症状持续时间(超急性、急性、亚急性、慢性),这些都会影响治疗的方式和时机。慢性B型主动脉夹层是指源于无名动脉开口以远的主动脉部位的内膜撕裂(1区或1区以远且持续超过90日)。主动脉夹层的病因可为散发性(例如,高血压、感染/炎症)、基因介导(例如,马凡综合征、埃勒斯-当洛斯综合征、Loeys-Dietz综合征、二叶式主动脉瓣畸形、Turner综合征)或创伤性(例如,主动脉钝性损伤、医源性)。分类
●解剖–常用的DeBakey和Stanford主动脉夹层分类系统 (图 2)存在缺陷。两者对夹层的精确范围界定相对无特异性,对主动脉弓受累情况也定义模糊。血管外科学会和胸外科学会委派的工作组采用一种分类系统解决了这些问题,系根据初始撕裂口的位置来区分A型与B型主动脉夹层 (图 1)。A型主动脉夹层是指初始撕裂口位于0区,远端位于1-12区。B型主动脉夹层是指初始撕裂口位于1区及以远的位置,需记录其近端和远端范围。约2/3的急性主动脉夹层为A型,1/3为B型。
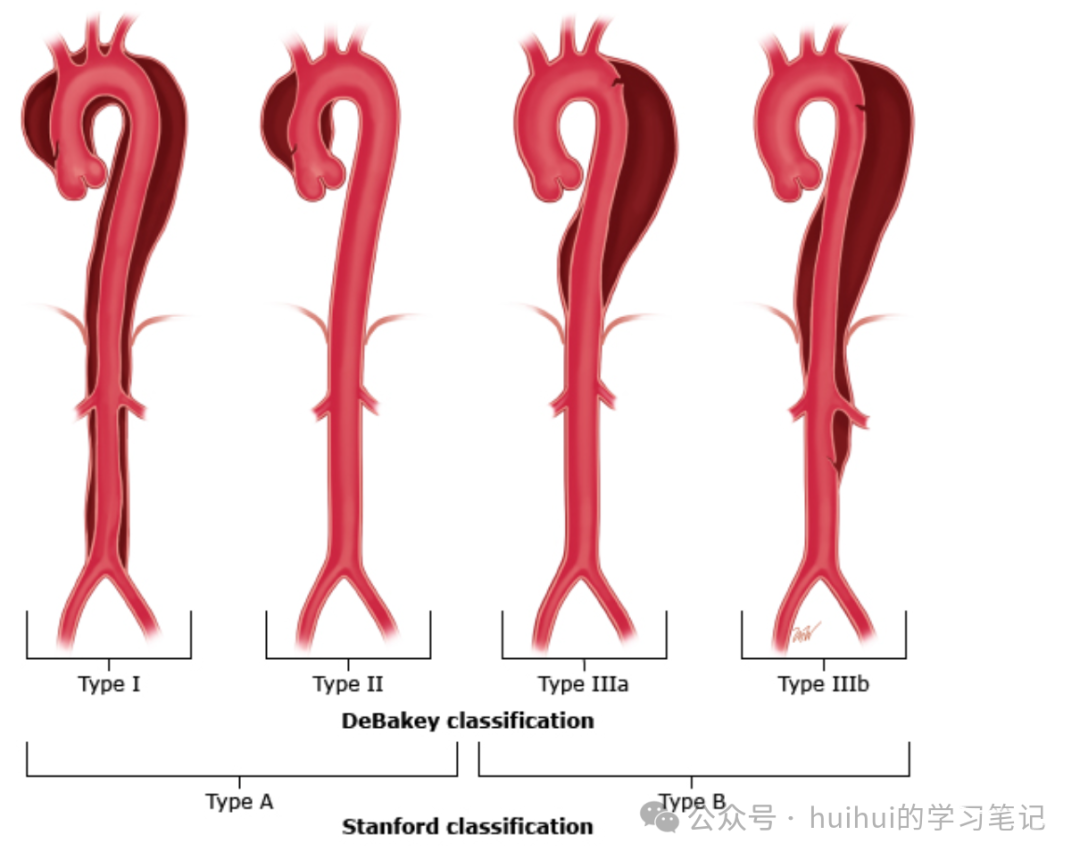

Figure2
对于已呈动脉瘤样的慢性B型主动脉夹层,Safi修正版Crawford分型 (图 3)有助于描述病变和胸腹主动脉置换的范围。
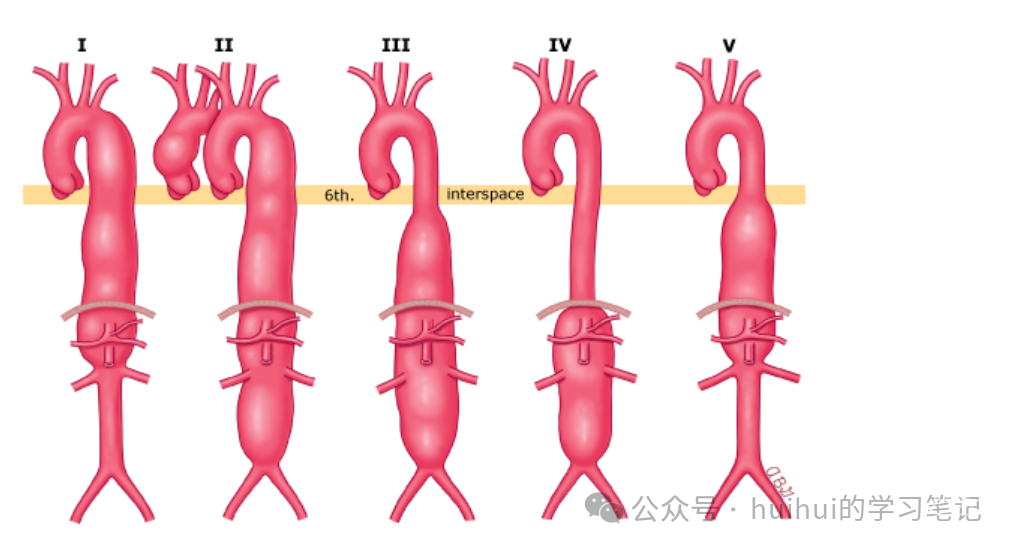

Figure3
●临床严重程度–主动脉夹层的临床严重程度分为复杂性、非复杂性或有高危特征。复杂性B型主动脉夹层有破裂和/或临床灌注不良的证据 (图 4 和 图 5)。高危特征包括:难治性或复发性疼痛(>12h);难治性高血压(3种以上最大剂量的降压药无效);影像学特征,如初始撕裂口位于小弯、主动脉直径>4cm、假腔直径>2.2cm、胸腔积血以及只有影像学证据的灌注不良。非复杂性是指没有破裂、临床灌注不良和高危特征。
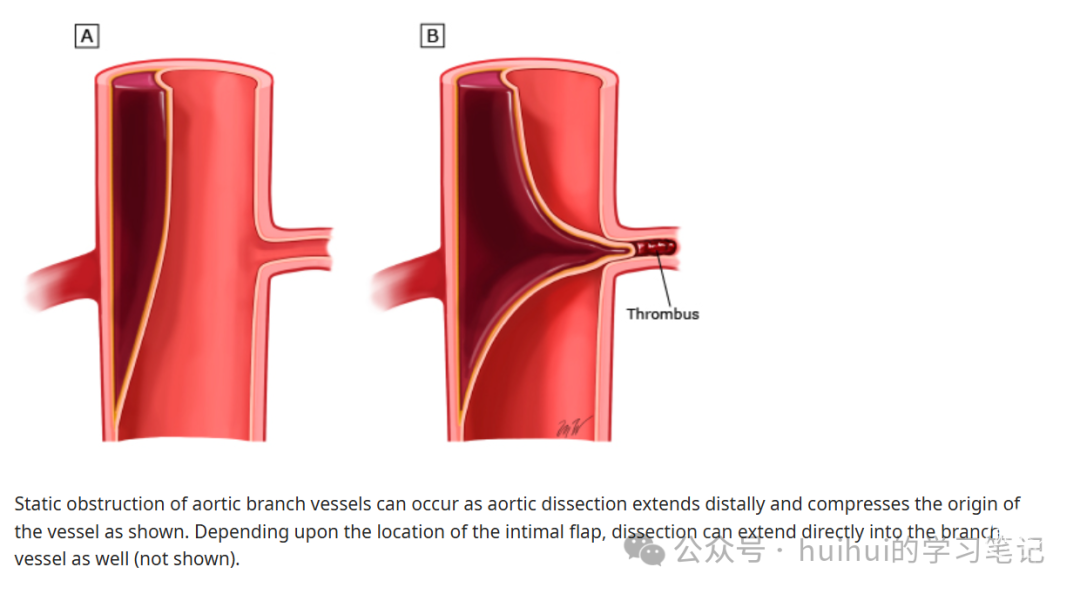
Figure4
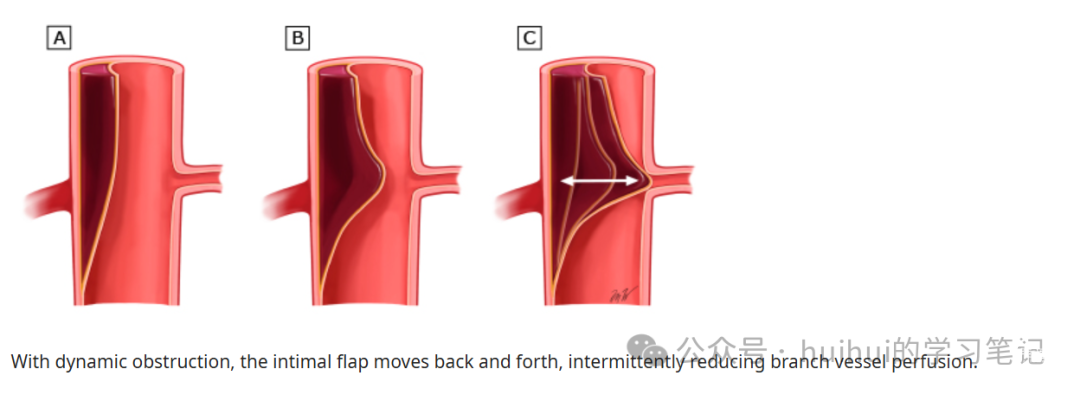
Figure5
●病程–在开放式手术时代,B型主动脉夹层仅根据死亡时间分为急性(<14日)或慢性(>14日)。血管外科学会/胸外科学会报告指南根据从症状发作算起的时间确定了如下分类:
•超急性–<24小时
•急性–1-14日
•亚急性–15-90日
•慢性–>90日
为了方便讨论慢性B型主动脉夹层,我们使用“急性”B型主动脉夹层来泛指≤90日的夹层,包括超急性期、急性期和亚急性期。
自然病程 — 从发病开始,随着主动脉重塑,主动脉夹层从急性转变为慢性状态。这种转变很复杂,可从夹层内膜瓣结构、假腔通畅性或血栓形成以及主动脉扩张的程度和速度来描述。主动脉重塑的自然病程对胸主动脉腔内修复的最佳治疗时机和临床结局有重要意义。
VIRTUE注册研究的一项分析发现,急性与慢性B型主动脉夹层的主动脉重塑有差异。主动脉的形态和可塑性在急性期里不随时间变化。在急性期,内膜瓣/隔膜和主动脉薄而脆,腔内修复期间出现A型夹层逆撕的风险升高,但由于内膜瓣/隔膜更加柔软/柔韧,胸主动脉腔内修复能比慢性B型主动脉夹层更充分扩张真腔。
不良主动脉事件的预测因素 — 几项研究试图确定B型主动脉夹层患者需要干预或有不良结局的危险因素。一项研究对294例患者平均随访3.7年发现,干预需求和死亡的预测因素包括年龄>60岁、就诊时主动脉直径>4.4cm以及近端降主动脉假腔直径>2.2cm。一项规模较小的研究对104例患者平均随访87.6个月发现,有46例发生1次或多次夹层相关事件。1年、5年、10年和20年时,无夹层相关事件生存率分别为95%、75%、53%和13%。单变量和多变量分析发现,初始主动脉直径≥4cm和假腔内血流量是夹层相关事件的重要危险因素。
一篇系统评价确定了非复杂性B型主动脉夹层患者发生主动脉扩张的几个预测因素。预测因素分为患者特征和影像学征象。
●发病年龄较小是主动脉扩张的临床预测因素。年龄<60岁与主动脉直径增加显著相关,原因为较年轻者的主动脉壁硬度较低,因此主动脉更易扩张。与主动脉扩张发生率增加有关的其他患者特征包括白人、马凡综合征和心率>60bpm。
●主动脉扩张的影像学预测因素包括急性期主动脉最大直径≥4cm、假腔通畅、假腔部分血栓化、初始影像学检查示假腔直径≥2.2cm、夹层近端的初始撕裂口≥1cm以及内膜撕裂口位于主动脉内弯侧。
B型主动脉夹层的治疗主要基于临床严重程度。通常只修复从非复杂性进展为复杂性的慢性B型主动脉夹层。对于大多数非复杂性慢性B型主动脉夹层患者,建议观察等待并持续药物治疗,而非干预。但若非复杂性B型主动脉夹层患者存在主动脉扩张或其他夹层相关事件的高危特征,则早期腔内修复可能有益,不要等到发生并发症。非复杂性夹层 — 非复杂性慢性B型主动脉夹层通常采取内科治疗(anti-impulse治疗)并定期进行临床和影像学监测。anti-impulse治疗 — 急性非复杂性B型主动脉夹层的主要治疗是严格控制心率和血压(也称anti-impulse治疗)与急性B型主动脉夹层时一样,anti-impulse治疗的目的仍是保持对主动脉壁的剪应力较低,以防夹层进展、灌注不良、动脉瘤样变性或破裂。指南推荐的目标心率为60-80bpm,收缩压为<120mmHg。务必还要恰当处理复发性疼痛,以限制心动过速和高血压。心率和收缩压控制良好者结局更佳,主动脉扩张和破裂的发生率降低。对于急性期后存活者,慢性B型主动脉夹层的治疗相似,最佳内科治疗的重点为长期控制血压和心率。β受体阻滞剂 可降低心肌收缩力和心率,从而有效降低血压和主动脉壁应力。除了β受体阻滞剂,观察性研究表明,钙通道阻滞剂维持治疗也可减少慢性B型主动脉夹层患者的主动脉扩张,并提高其生存率。可惜很多慢性B型主动脉夹层患者都不依从其anti-impulse药物治疗。一项小型研究(n=47)显示,有43%的患者依从性“高”,21%为“中等”,10%为“低”。依从性较高的相关因素包括既往主动脉手术、所用药物更多、感到治疗有益、记忆力好以及不太担心副作用。连续影像学检查 — 估计接受药物治疗的B型主动脉夹层患者有20%-50%最终需要干预。最佳内科治疗的失败率较高且可能发生严重并发症或死亡,因此务必要密切监测和识别出何时干预。对于确诊非复杂性B型主动脉夹层的患者,我们通常在夹层发作后1、6和12个月时行后续CT血管造影,此后每年复查1次,前提是患者仍适合外科干预.肾功能受损者适合磁共振平扫。肾功能正常者可交替使用CT血管造影和磁共振血管造影。经胸壁超声心动图不适用于监测,但在监测持续性瓣膜功能障碍时可能需要。有高危特征者的干预 — 有高危临床特征的非复杂性慢性B型主动脉夹层患者似乎可获益于早期而非晚期胸主动脉腔内修复,但尚未确定公认标准。最佳内科治疗的失败率非常高(6年内约为60%),慢性B型主动脉夹层的死亡率(5年时为20%-50%)归因于主动脉重塑失败。INSTEAD试验将非复杂性亚急性或慢性B型主动脉夹层患者(发病后2-52周)随机分配至接受单纯最佳内科治疗或联合胸主动脉腔内修复。随访2年发现,尽管存在有利主动脉重塑,胸主动脉腔内修复并不能改善总体生存率和不良事件发生率,而5年时腔内修复组的主动脉特异性生存率提高。由于腔内治疗结果喜人,有研究试图预测哪些患者可能获益于早期而非晚期胸主动脉腔内修复。高危特征包括主动脉最大直径>4cm、假腔直径>2.2cm、内膜撕裂位于主动脉内弯侧、胸腔积血、难治性疼痛或难治性高血压、只有影像学证据的灌注不良、主动脉夹层相关再次入院。一项针对美国血管外科学会血管质量倡议数据库的研究回顾了606例非复杂性急性B型主动脉夹层患者,发现在超急性期(<24小时)接受治疗者风险更高,术后并发症发生率也更高。这与B型夹层早期治疗的现有数据相一致。应注意,与亚急性期(15-90日)相比,急性期(1-14日)接受治疗者有死亡率降低的趋势,两组的再干预和术后并发症无差异。复杂性病变的干预 — 复杂性慢性B型主动脉夹层需要紧急腔内修复或开放性手术干预,以处理临床灌注不良或破裂。对于进展为出现高危特征的患者,如主动脉动脉瘤样变性>4cm、假腔扩张至>2.2cm、反复疼痛、影像学检查示灌注不良以及持续难治性高血压,应考虑干预。一些研究表明,对于某些后期出现并发症风险较高的患者,早期(而非晚期)干预可能有益。慢性与急性B型主动脉夹层相比,需干预并发症的发生率有一定差异,动脉瘤样变性是最常见的干预指征。●动脉瘤样变性–内科治疗B型主动脉夹层者中,5年动脉瘤样变性发生率为20%-55%。与胸主动脉疾病治疗指南一致,胸主动脉直径达到5.5-6cm时就应干预。有结缔组织病者应考虑在直径较小时修复。●破裂或即将破裂–与退变性(真性)主动脉瘤一样,破裂风险随主动脉直径增加而增加。一项研究根据571例B型主动脉夹层患者发现,主动脉直径为4-4.4cm、4.5-4.9cm、5-5.4cm、5.5-5.9cm和6-6.4cm时,破裂发生率分别为0、3.3%、15.3%、18.8%和28.6%。慢性B型主动脉夹层干预中仅不到10%是因明确破裂。但破裂相关死亡率较高,因此务必识别出即将破裂的征象并尽快治疗。如果内科期待治疗期间的2次后续CT检查发现主动脉周围血肿和胸腔积血增加,则提示即将破裂。根据国际急性主动脉夹层登记的数据,复发性疼痛和难治性高血压为重要预后因素,应予以重视,因为在亚急性期或慢性期这些临床特征可能预示即将发生破裂。●主动脉扩张率>0.5cm/年–系慢性期不稳定的征象,也是修复的指征。●复发性疼痛–系慢性B型主动脉夹层修复的第二常见指征,因为夹层引起的疼痛可能是将会破裂的不祥征兆。●灌注不良–灌注不良综合征也是修复的指征。约4%的慢性B型主动脉夹层患者因发生灌注不良综合征接受修复。与急性B型夹层相比,慢性B型夹层发生下肢灌注不良的可能性要低得多,下肢并发症发生率<5%。●难治性高血压–若需使用至少3种最大推荐剂量或最大耐受剂量的降压药,则应考虑干预;但应由外科医生根据临床情况决定是否干预,主要是依据有无上述特征。
●主动脉弓–应评估主动脉弓的所有解剖结构,包括其分支、角度、直径和初始撕裂入口的位置。如果计划覆盖主动脉分支,可能需要在腔内修复前进行主动脉弓去分支操作。分支型和开窗型腔内支架逐渐常用于治疗弓部病变。解剖学异常 (图 6),如右侧弓型或左/右锁骨下动脉异常,也可能改变术式。

Figure6
●入路血管–应评估股总动脉和髂总动脉,动脉直径必须足以支持递送系统通常较大的输送鞘。某些病例可能需要采用肱动脉入路。对于解剖结构不适合腔内修复的患者,例如近端或远端锚定区不足、重度弯曲或钙化、血管入路不足或主动脉直径过大,应尽可能考虑开放性手术修复。预防脊髓缺血 — 脊髓缺血是胸主动脉腔内修复和开放性手术修复都存在的严重并发症。脊髓血供来自主动脉直接发出的肋间动脉和腰动脉分支,以及锁骨下动脉和髂内动脉分支。如果计划广泛覆盖或置换主动脉,则发生脊髓缺血的风险增加,尤其是T8-L1区。75%个体中Adamkiewicz动脉源自该区域 (图 7)。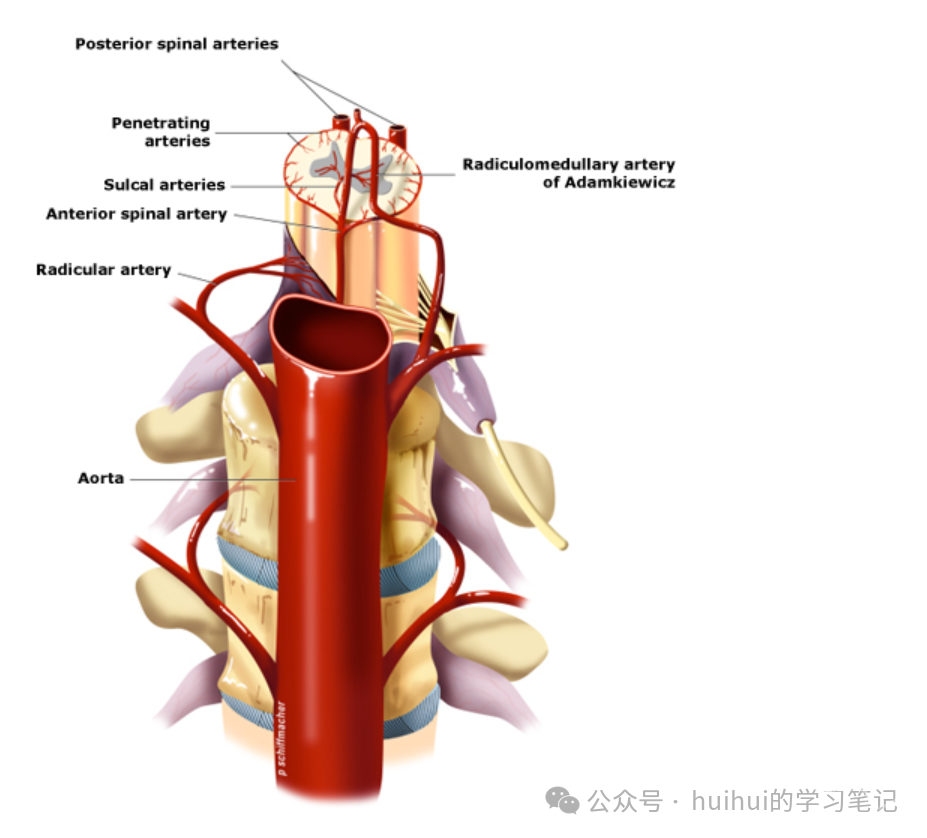
Figure7
●行胸主动脉腔内修复前,应对脊髓缺血风险较高的患者放置腰椎引流管。腔内修复胸腹主动脉瘤(动脉粥样硬化性、夹层后)时,胸主动脉覆盖范围是脊髓损伤最重要的决定因素。其他考虑因素包括既往主动脉手术、既存髂内动脉闭塞和/或计划覆盖左锁骨下动脉但不行血运重建。●所有接受开放性手术修复的慢性B型主动脉夹层患者都应放置腰椎引流管,因为与胸主动脉腔内修复相比,开放性手术修复的脊髓损伤风险显著更高。CrawfordⅠ/Ⅱ型胸腹主动脉置换的脊髓损伤风险最高 (图 8A-B)。一项研究根据2286例接受开放性手术修复的胸腹主动脉瘤患者(24%为慢性夹层)发现,下肢轻瘫/截瘫的总发生率为3.8%,接受Ⅱ型和Ⅰ型置换的患者中最高,分别为6.3%和3.3% (图 8D)。一项随机试验(n=145)发现脑脊液引流显著降低开放性手术修复的截瘫发生率,相对危险度降低80%。另一项研究发现,对胸腹主动脉瘤患者行开胸修复术时,脑脊液引流+远端主动脉灌注和适度低温可将脊髓损伤发生率从10%降至1%。Figure8A-B
辅助措施包括术中神经功能监测以及使用体感诱发电位检查和/或运动诱发电位检查,以识别脊髓损伤并立即开始治疗。升高平均动脉压和/或增加腰椎脑脊液引流都可改善脊髓灌注。对于接受腔内修复的高危患者以及接受开放性手术修复的所有患者,都应考虑体感诱发电位检查和/或运动诱发电位检查。
术后腰椎引流至少应持续48小时,目标脑脊液压力≤10mmHg。对于发生脊髓损伤的患者,推荐目标平均动脉压>80mmHg、目标血红蛋白水平>10g/dL,以增加脊髓灌注和氧输送。对于术后神经功能完好的患者,推荐以不超过15mL/h的速度引流脑脊液,以使目标压力<10mmHg。对于迟发性神经功能障碍患者,推荐遵守脑脊液引流状态/氧输送/患者状态(即“改良COPS”)方案。在这种情况下,患者保持平躺,脑脊液目标压力<5mmHg,不限最大引流速度和引流量,同时维持足够氧输送[氧饱和血红蛋白>10g/dL、心脏指数>2.5L/(min·m2)],以及通过使收缩压>140mmHg维持脊髓灌注压。●A型夹层逆撕–系胸主动脉腔内修复的严重并发症。腔内修复慢性B型夹层时,A型夹层逆撕的发生率为1.6%-5%[33,39,40]。此风险在B型主动脉夹层的急性期远高于慢性期,可能是因为病程较早期主动脉隔膜更脆弱且可塑性更大。不应使用近端金属支架或带金属倒钩支架、避免支架过大(oversizing不超过10%)、释放支架后不进行球囊扩张,以尽量降低风险。●支架相关并发症–支架再干预的原因为内漏及其他并发症,如支架断裂、压缩、塌陷或移位。内漏是最常见的早期并发症,发生率为4.8%-11.1%。一篇大型系统评价报道,在接受腔内修复的慢性B型主动脉夹层患者中,中期随访24个月时,内漏总发生率为8.1%,Ⅰ型内漏最常见。●支架植入后综合征–系一种全身炎症反应综合征,发生于支架植入后72小时内,发生率约为15%。临床特征包括发热(>38℃)、白细胞增多和C反应蛋白升高。血培养阴性且无临床感染。IL-6水平是重要的生物标志物,若在胸主动脉腔内修复术后24小时内出现升高,则将发生植入后综合征。植入后综合征为自限性,治疗主要为支持性。●B型主动脉夹层–慢性B型主动脉夹层是指仅累及降主动脉 (图 1)且病史超过90日的夹层。
●治疗方法–慢性B型主动脉夹层的治疗取决于夹层的临床严重程度(非复杂性、复杂性、高危特征)。
•非复杂性夹层–非复杂性慢性B型主动脉夹层通常采取内科治疗,并定期进行临床和影像学监测,监测有无进展为高危特征的征象。内科治疗包括持续控制心率和血压(即anti-impulse治疗),目标心率<60bpm、收缩压<120mmHg。慢性夹层患者应持续使用β受体阻滞剂作为维持治疗。慢性期加用钙通道阻滞剂有助于减少主动脉扩张,且可提高生存率。
我们对非复杂性病变的处理如下:
-无高危特征的患者–建议继续内科治疗,而非干预(Grade 2C)。但除了持续内科治疗,患者和医生还可选择腔内干预,以预防灌注不良或其他主动脉并发症,此时关注点是潜在改善主动脉长期结局胜过可能面临的围术期并发症(如脑卒中、脊髓缺血)。可能影响决策制定的因素包括患者年龄、预期寿命、医疗风险以及有无可能增加未来主动脉事件风险的某些解剖学因素。
-有高危特征的患者–对于存在或正进展为有高危特征的患者,建议干预(Grade 2C)。高风险特征包括:难治性或复发性疼痛(>12h);难治性高血压(3种以上最大剂量的降压药无效);影像学特征,如初始撕裂口位于小弯、主动脉直径>4cm、假腔直径>2.2cm、胸腔积血以及只有影像学证据的灌注不良。
•复杂性夹层–对于复杂性慢性B型主动脉夹层,包括进展为有临床意义的灌注不良和/或破裂,需要进行修复。近2/3的慢性B型主动脉夹层患者会出现并发症。这些并发症的发生率与急性B型主动脉夹层不同,最常见动脉瘤样变性。
•修复类型–对于有干预指征且解剖结构合适的慢性B型主动脉夹层患者(无结缔组织病),建议腔内修复,而非开放性手术修复(Grade 2C)。与开放性手术修复相比,胸主动脉腔内修复可降低围术期死亡率和主要并发症(如脑卒中、脊髓缺血、全身并发症)发生率,但再干预率更高。对于在大手术量中心接受治疗且手术风险较低的患者(肾和肺功能正常),开放性手术修复的效果更持久。
•预防脊髓缺血–对于接受修复的患者,应采取措施降低胸主动脉修复相关的脊髓缺血风险。腰椎引流适用于所有接受开放性手术修复的患者,以及接受胸主动脉腔内修复的高危患者,包括计划支架广泛覆盖远端胸主动脉(T8-L1)、既往主动脉手术、既存髂内动脉闭塞和/或计划覆盖左锁骨下动脉但不行血运重建。
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。
投稿邮箱:NAOYIHUI@163.com
未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。










![]()






