会议地点:腾讯会议
本期互动团队:
![]()
![]()
四川大学华西医院脑胶质瘤MDT团队
![]()
贵州医科大学附属医院暨肿瘤医院脑胶质瘤MDT团队
神经外科:出良钊教授、董明昊教授、李文衍教授、周兴旺教授
肿瘤科:金风教授、李媛媛教授
影像科:阮志兵教授
病理科:高勤教授
![]()
乐山市人民医院脑胶质瘤MDT团队
神经外科:卫正洪教授、张召教授、詹傲教授
影像科:邓磊教授
病理科:胡恒辉教授
肿瘤科:陈娟教授
![]()
专题分享:脑内多发胶质瘤影像诊断及多发病灶疾病的鉴别诊断——杨喜彪教授
华西医院杨喜彪教授:
![]()
多发胶质瘤指脑内同期或非同期出现2个及2个以上病灶,占总体弥漫性脑胶质瘤的20.8%,其中多灶胶质瘤约93.6%;多发脑胶质瘤在年龄上大于单发胶质瘤;在病理级别上以GBM和高级别胶质瘤为主。多发胶质瘤分为多灶性胶质瘤和多中心胶质瘤,多灶性胶质瘤是已知途径播散;可以沿着联合纤维、脑脊液、血液及肿瘤周边卫星状等播撒,多中心胶质瘤是不能通过上述播散途径转移。多中心胶质瘤广泛分布于不同脑叶;大多发生于幕上,但也可能同时发生于幕上及后颅窝。多中心胶质瘤发病机制尚不清楚,有多种学说,有两种主流的假说。第一个是中枢神经系统发展过程中出现一次广泛但低致癌能力的突变,这些突变后的细胞可能来源于同种或非同种的原始细胞,在其发育过程中,受到生化、激素、病毒或寄生虫等外界因素刺激下,最终发展成为胶质瘤。第二个是与细胞分子及遗传学特征有关,如p53突变广泛存在于多发性胶质瘤的肿瘤细胞中,并且与肿瘤的发生发展关系密切。目前没有针对多中心胶质瘤的定制治疗方案,预后比较差。经典的GBM播撒途径模式有:临近脑实质侵犯(最常见)、白质纤维束播撒(次之)、蛛网膜下腔或室管膜播撒、血管周围间隙播撒。多灶性胶质瘤影像特点表现为多发、多样,多发病灶表现为弥漫性(低-高级别)、局灶性胶质瘤特征;可同时具有1种、或2种及以上胶质瘤特征;征象越复杂,级别可能越高。脑皮层受累及征象突出,同时累及皮层区与室管膜下区的胶质瘤大多为多发,认为多发胶质瘤的可能与室管膜下区丰富的神经干细胞有关。病灶之间有高度影像异质性:形态学的异质性,功能影像的高度异质性(弥散、灌注及代谢等);与相应级别的单发胶质瘤表现相似,但多发胶质瘤病灶间可以有差异。多发胶质瘤需要与多灶性疾病进行鉴别,此处主要列举临床中容易误诊或诊断困难的几种疾病,有淋巴瘤、瘤样脱髓鞘、von Hippel-Lindau综合征(VHL)、结节性硬化、MELAS综合征。原发性中枢神经细胞淋巴瘤的影像特征多位于中线两旁脑白质、脑室周围、脑表面,幕上多见,可为单发或多发,局灶性或弥漫性浸润性生长,形态多样,多轻度/中度水肿,在CT呈等或稍高密度,MRI:T2WI呈稍低、等或高信号,增强后肿瘤明显增强。通常弥散明显受限,灌注增加或增加不明显。MRS中NAA下降,脂质、乳酸和胆碱峰增高。瘤样脱髓鞘影像特征为单发或多发,双侧较为常见以白质受累为主,还可累及皮层及皮层下白质;累及额叶为主,其次为颞叶、顶叶,可累及脊髓;体积大,大小与占位效应不匹配;、T1低(“黑洞”征),T2高,而且中央比周边更高(“煎蛋”征);强化:急性期,斑片状或结节状;亚急性期“开环样”、“闭合环样”或“花环样”;慢性期,强化变淡或消失,易与脑肿瘤相混淆。结节性硬化症为常染色体显性遗传性疾病,可以导致细胞增殖和分化失控,几乎累及所有器官和系统,尤以脑、皮肤、肾脏、心脏表现突出,病理改变是错构瘤。von Hippel-Lindau综合征是一种常染色体(3号染色体)显性遗传的家族性肿瘤综合征,伴有多发性小脑和视网膜血管母细胞瘤。不同器官多发肿瘤:脑血管母细胞瘤、视网膜血管母细胞瘤,伴胰腺囊肿和肾细胞癌(RCC)和/或多发性肾囊肿和肾上腺嗜铬细胞瘤。线粒体脑肌病是一组由于线粒体结构和/或功能缺陷引起的,以中枢神经和肌肉系统病变为主要表现、多系统受累的全身性疾病。MELAS综合征影像表现,部位:皮层及皮层下白质;枕>颞>顶>额;可出现脑萎缩;病灶单发或散在;病灶区与脑血管分布不一致,反复发作可见脑萎缩;平扫:T1稍低信号影,T2高信号影,FLAIR和DWI出现高信号;增强:呈脑回样强化(可强化或不强化);血管:增生或增粗,痉挛性狭窄;MRS:Lac双峰,NAA降低,Cho可升高;PWI:增加;或不明显。颅内多发病疾病影像诊断比较困难,我们可以先做加法,再做减法的方式思路。做加法是,根据此影像特点,把可能得诊断都加入进来。做加法是,把加入进来的疾病进行排序,最有可能是,可能的是,不排除的是。此时我们不能忽略的是全身影像特点:其他部位肿瘤,可多发的疾病,综合征等。目前对多灶性胶质瘤和多中心胶质瘤的治疗没有特别大差异,并且预后也基本一致,预后都比较差。对它们影像鉴别诊断,主要是给术前诊断提供更多的思考,更准确地诊断多发疾病,减少误诊。
![]()
临床病例讨论1——贵州医科大学附属医院暨肿瘤医院
<左右滑动查看更多>
讨论
![]()
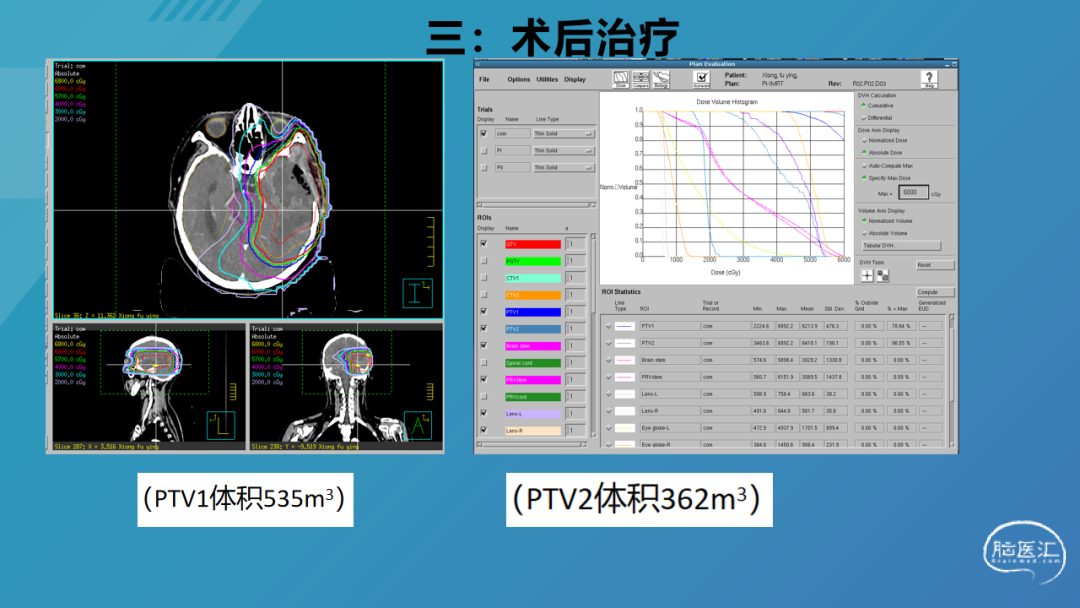
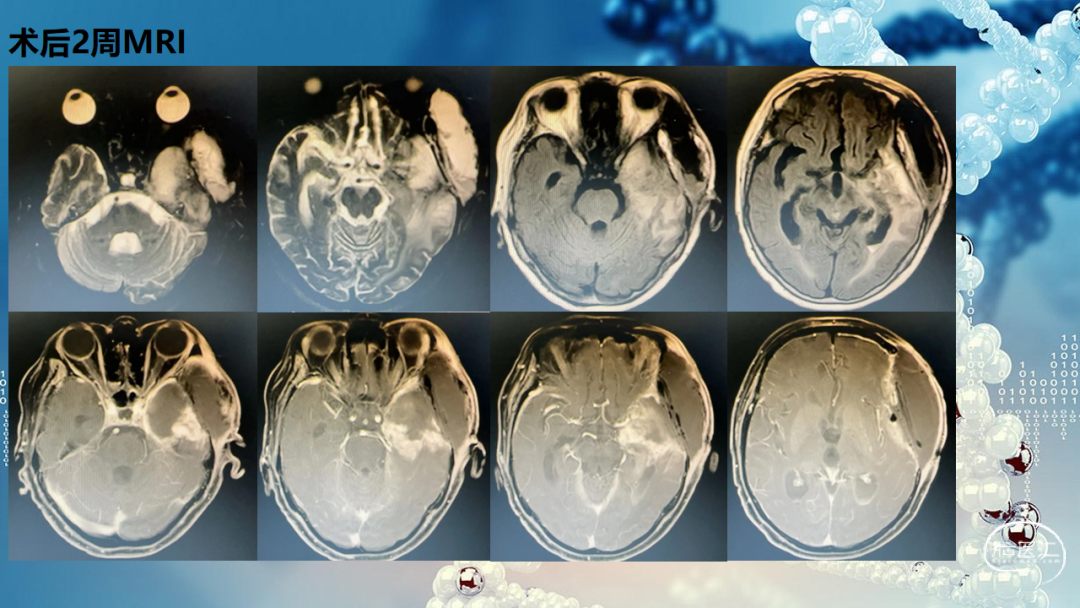
贵州医科大学附属医院暨肿瘤医院肿瘤科:考虑该病例病灶范围大,术后残留靠近颞叶海马及脑干,术后CT融合MRI勾画放疗靶区,放疗靶区GTV包含术腔、增强残留病灶、T2flair异常信号区域,给与剂量60Gy,外扩2cm时考虑脑干,脑干附近缩回0.5cm,给予50Gy剂量,术后标准化疗。该病例术后至复发共22月,复发后由于颅内压高致昏迷进行急诊手术,术后院GOSIV级,已出院,二次术后未进行再次放疗,考虑第一次放疗剂量较大且靠近脑干以及十二周期化疗,所以可以先用药物治疗,比如贝伐单抗联合化疗,以及免疫治疗。
华西医院神经外科:该病例总体来讲治疗效果不错,IDH野生型的胶质母细胞瘤4级第一次术后达到22月,复发后再次手术,从手术角度提出两点建议,第一是切除程度,手术将强化病灶切除的不错,病灶位于左颞海马,如果在功能监测下积极点可以再多切一些;第二是对于胶质瘤手术不建议去骨瓣减压,术中切除病灶后可以充分减压,骨瓣复位有助于后期综合治疗,现在的外科技术完全能够有效的进行病灶切除及彻底的止血,不需要预防去骨瓣减压。
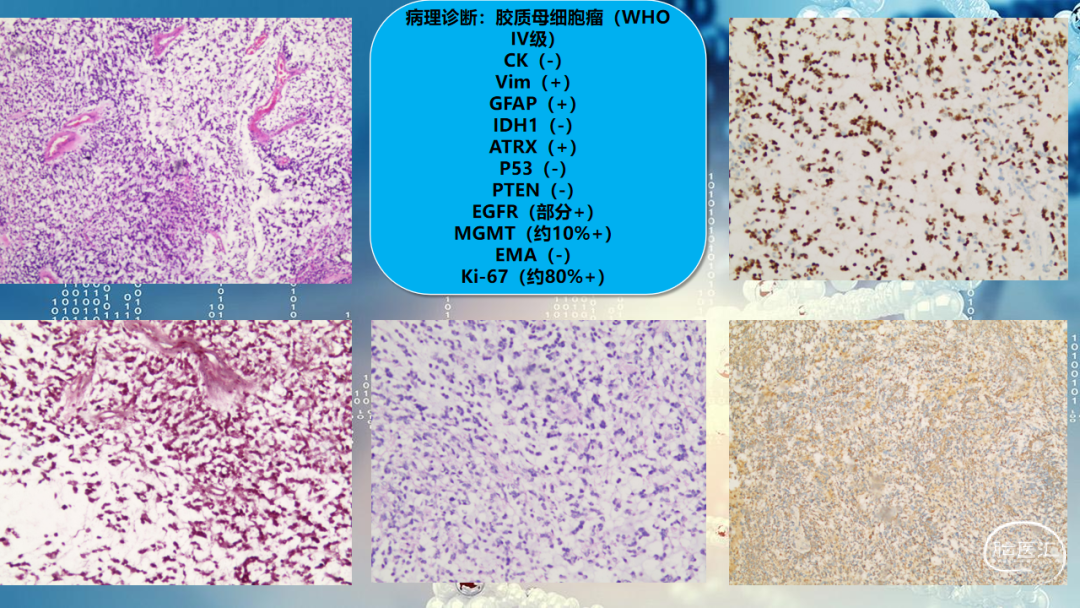
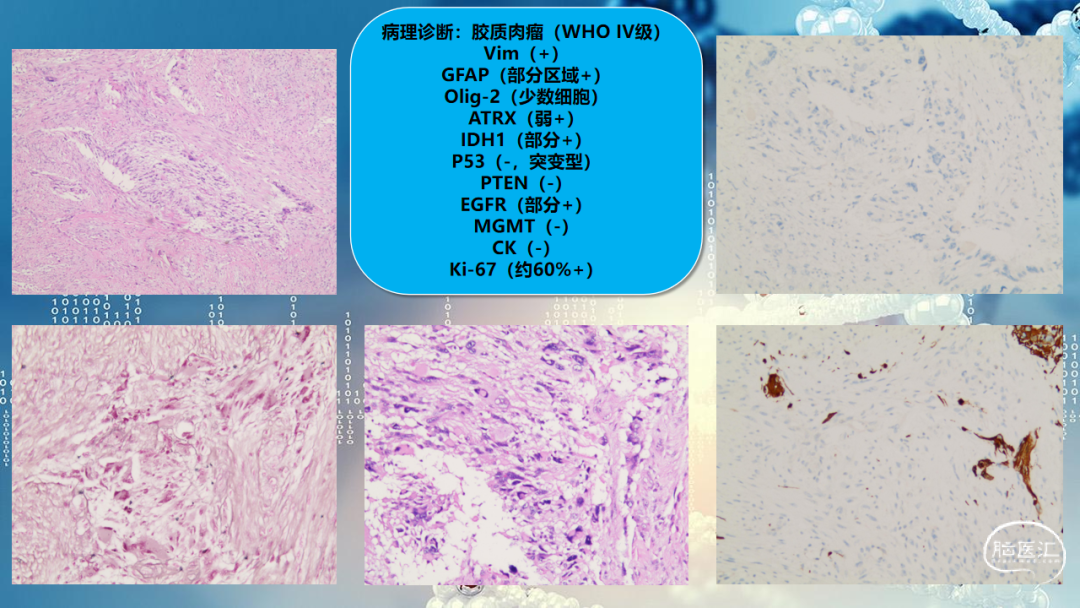
华西医院病理科:本例病理诊断明确。第一次是非常典型的胶质母细胞瘤,形态学细胞密度高,可见大量栅栏状坏死,TERT启动子突变,胶质母细胞瘤的诊断非常明确。复发后形态学朝肉瘤方向发展,呈胶质肉瘤形态,大范围还是属于胶质母细胞瘤,预后会更差一些。
华西医院肿瘤科:对于该病例是否再次放疗的问题同意金书记和李主任的意见。该病例第一次术后放疗范围很大,照射剂量60Gy,放疗时间不到2年,再程放疗的放射性坏死概率非常高。第二次术后如果影像学全切,建议使用电场加化疗,可与患者沟通,尝试加用免疫治疗;该病例目前未见明显水肿及占位效应,建议暂缓使用贝伐珠单抗;若第二次术后有小部分残留,建议可以伽马刀治疗。
华西医院神经外科:该病例的治疗是综合治疗的成果,因为该病例有MGMT甲基化,可以使用替莫唑胺剂量密度方案。
![]()
临床病例讨论2——乐山市人民医院
<左右滑动查看更多>
讨论:
![]()
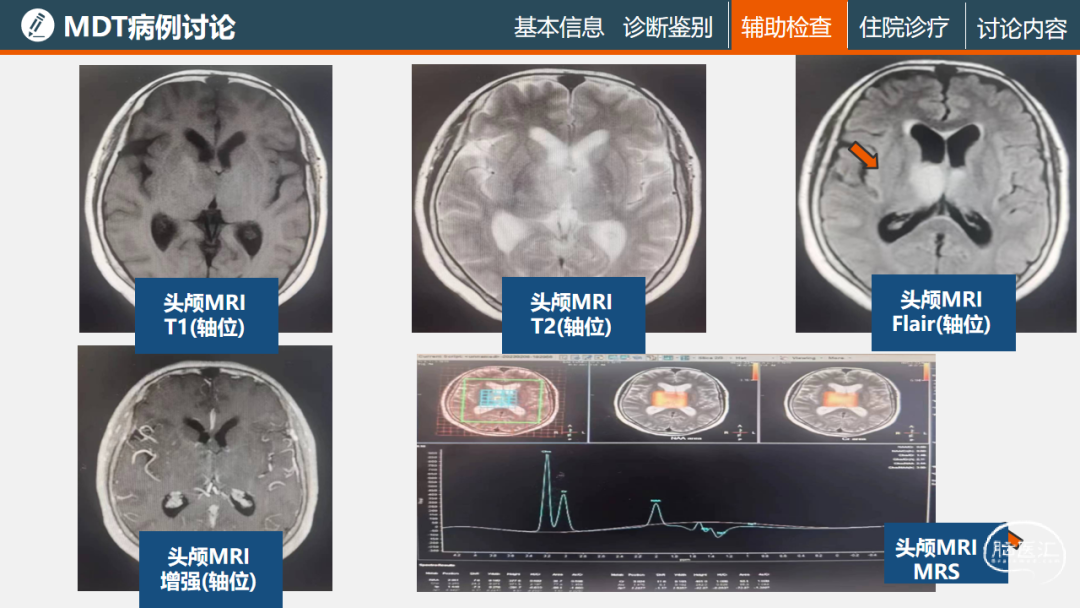
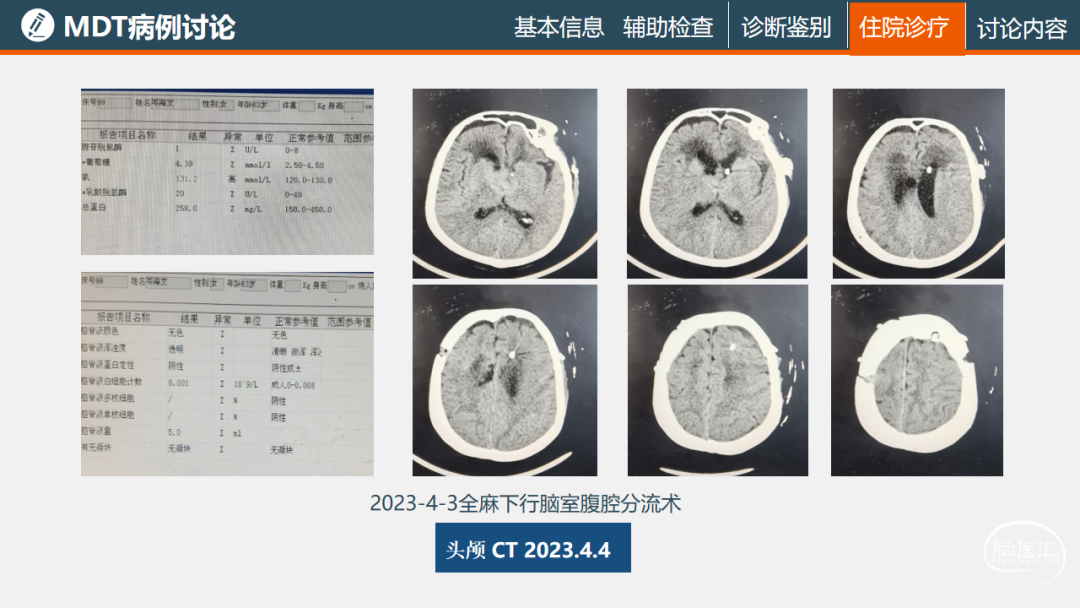
乐山市人民医院放射科:该病例病灶于T1呈低信号,T2及T2Flair呈高信号,累及双侧丘脑,以右侧居多,并伴有轻度瘤周水肿,增强序列呈轻度强化,边界不清楚,MRS提示Cho峰明显增高,NAA峰降低,影像诊断考虑胶质瘤可能性大。
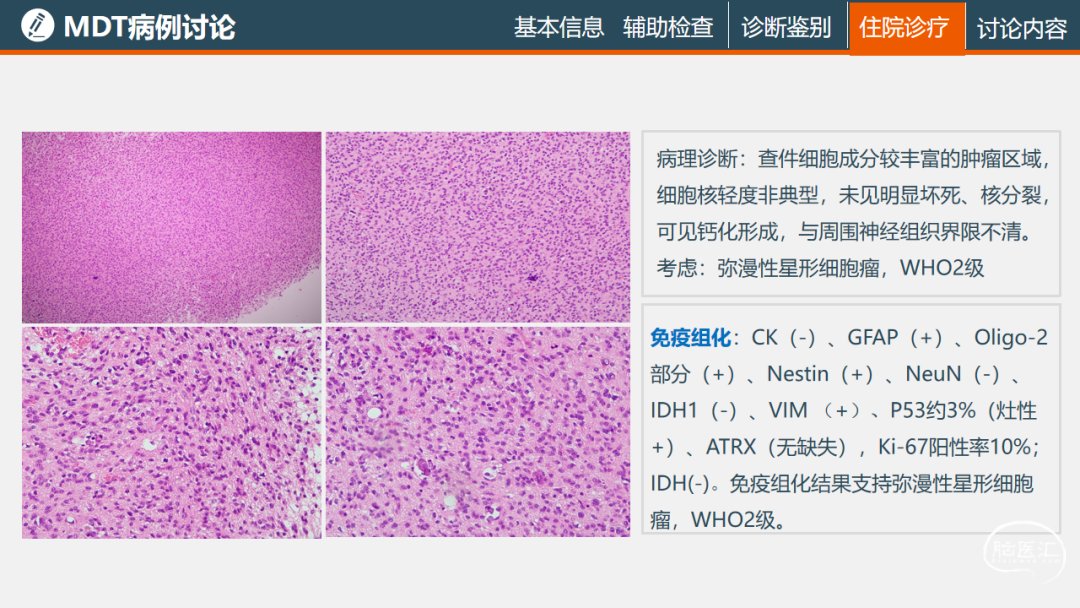
乐山市人民医院病理科:肿瘤细胞密度高,细胞异型性部分较明显,呈空泡状改变,未见明确坏死及微血管增生,与周围组织界限不清,首先考虑为弥漫性胶质瘤,在免疫组化之后,IDH阴性,ATRX缺失,Ki-67阳性率10%,考虑为IDH野生型的弥漫性星形细胞瘤,由于组织学形态不明显,诊断分级为2级,外院基因检测IDH野生型,TERT突变,综合诊断考虑为弥漫性胶质瘤4级。
华西医院病理科:该病例细胞密度稍高,未见典型坏死及微血管增生,组织学形态2-3级。该病变位于丘脑,首先需排除弥漫中线胶质瘤,丘脑肿瘤70%为H3K27M突变的弥漫中线胶质瘤。该病例H3K27M未突变,结合分子检测TERT启动子突变诊断为胶质母细胞瘤,WHO 4级。
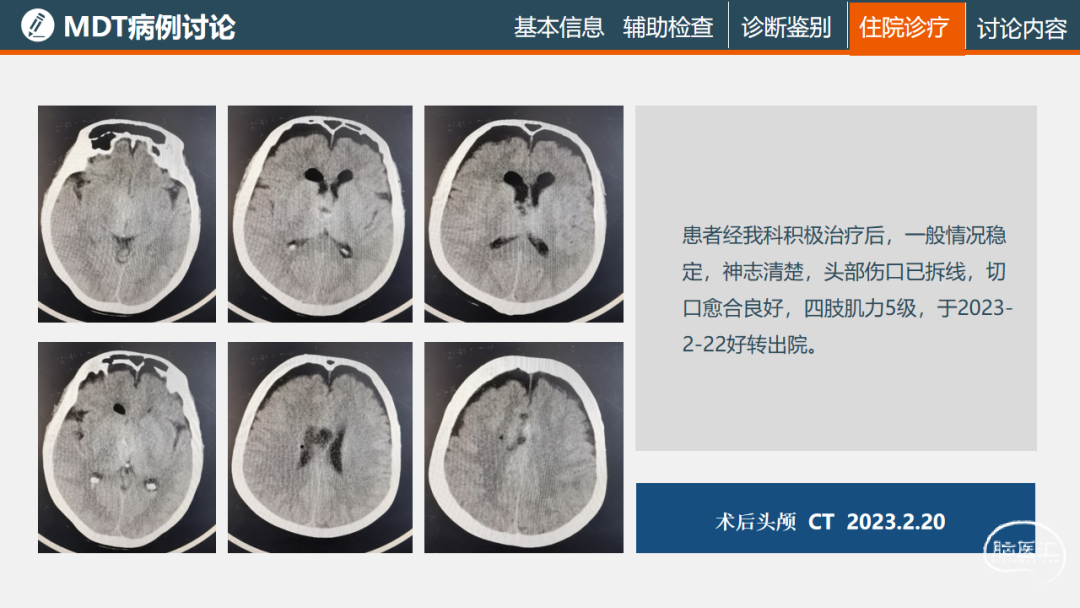
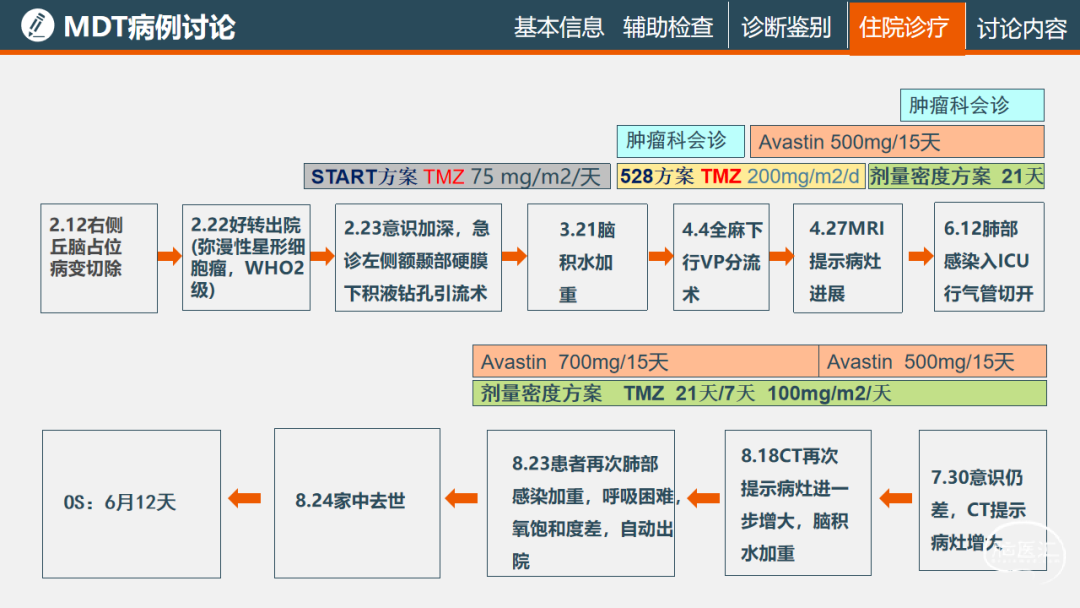
华西医院神经外科:该病例病变位于双侧丘脑及胼胝体,不能完全切除,乐山市人民医院老师通过手术切除取到病理样本,后续患者状态差,又出现脑积水,脑室系统以及脑室系统周围的基底节、丘脑的病变切除手术会对脑脊液循环造成影响和干扰,导致术后发生硬膜下积液或者脑积水,手术应该遵循最大范围内安全切除原则,病变切除越多,术后发生的肿胀可能会少一些。该病例术后的硬膜下积液推测可能与中脑导水管的压迫有关,脑积液循环不是很通畅,术中将胼胝体切开,胼胝体漏口又较大,就导致硬膜下积液,个人经验胼胝体切开程度可以小一些,切除肿瘤后将开放的脑室尽量封闭,减小硬膜下积液的可能性。另外双侧丘脑及累及下丘脑的病变预后较差,可以考虑穿刺活检获取病理诊断,或者分流处理脑积水。
华西医院肿瘤科:因生殖细胞瘤对放疗敏感,曾有少数生殖细胞瘤昏迷患者进行过放疗,但是放疗风险大,患者意识差,放疗期间产生的放射性脑水肿会加重意识障碍,因此不建议对放疗不敏感的胶质母细胞瘤昏迷患者行放疗。
![]()
临床病例讨论3——华西医院
讨论:
01
![]()
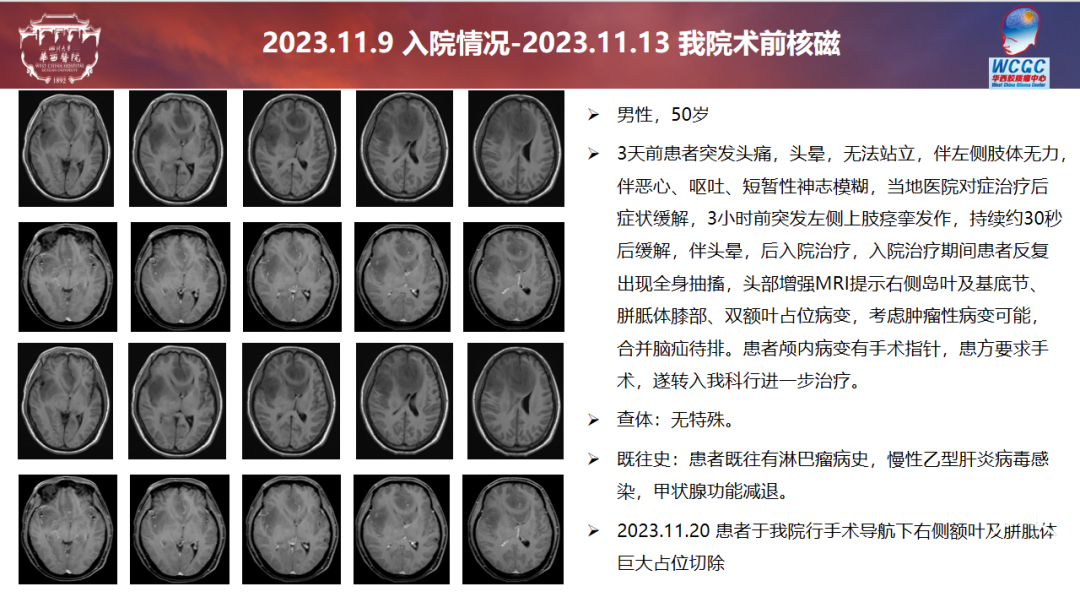
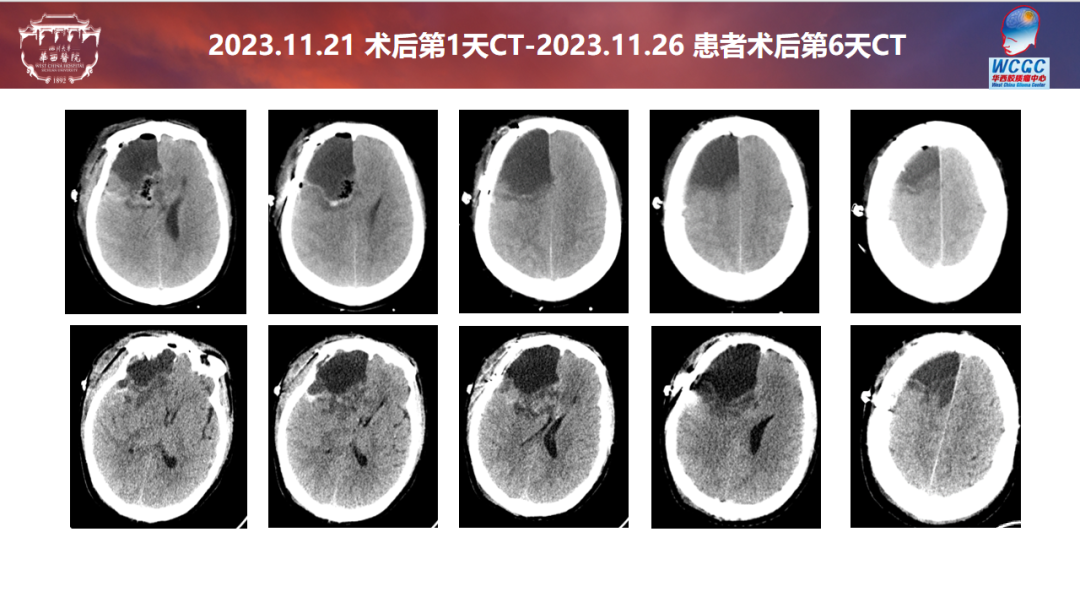
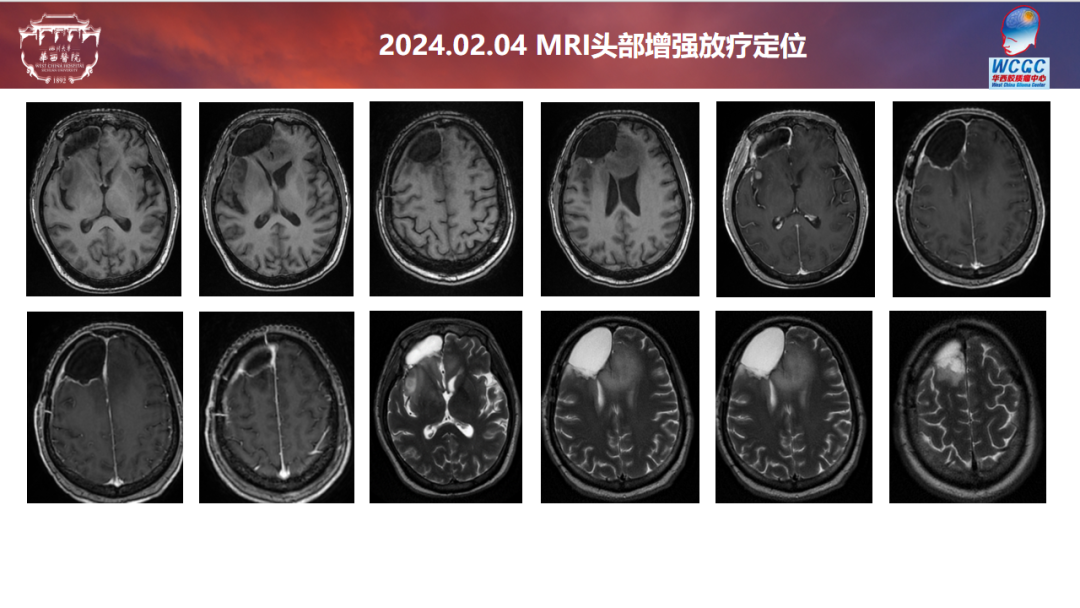
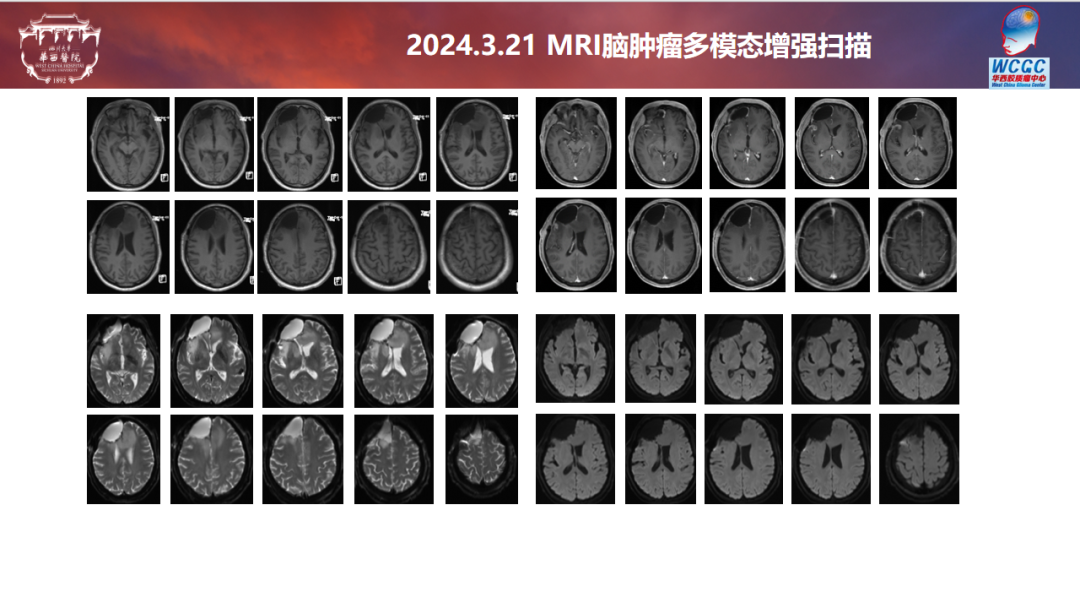
华西医院影像科:该病例有淋巴瘤病史,出现颅内占位病变,会先考虑胶质瘤和淋巴瘤,术前CT病灶不明显,但是中线向左侧移位,右侧额叶稍低密度影,术前核磁病灶明显,胼胝体前方、右侧额岛叶区域弥漫性病灶,T1增强强化不明显,岛叶片状强化,T2项呈现病变位于右侧大脑半球、丘脑区域延着胼胝体达到对侧额叶区域,T2flair显示与T2类似,T2高信号不像淋巴瘤的水肿,淋巴瘤的水肿是肿瘤引起周围血管通透性增高,出现水肿,延着白质分布,不太会累及皮层,该病例病变额叶岛叶皮层受累,T2与flair信号一致,故淋巴瘤不作为第一诊断,首先考虑弥漫性胶质瘤(星形细胞瘤或胶质母细胞瘤、大脑半球胶质瘤、儿童型胶质瘤)。
华西医院病理科:该例虽然有外周淋巴瘤病史,但颅内病变形态学不考虑淋巴瘤。病变部位较为表浅,送检组织中可见较多神经元,胶质细胞密度不大,异型性也不大。增生的细胞GFAP、Oligo2阳性,为胶质细胞;CD20和CD3均阴性,排除淋巴瘤;Ki-67指数非常低,组织学诊断为2级,结合TERT启动子突变,综合诊断为胶质母细胞瘤,IDH野生型,WHO 4级。
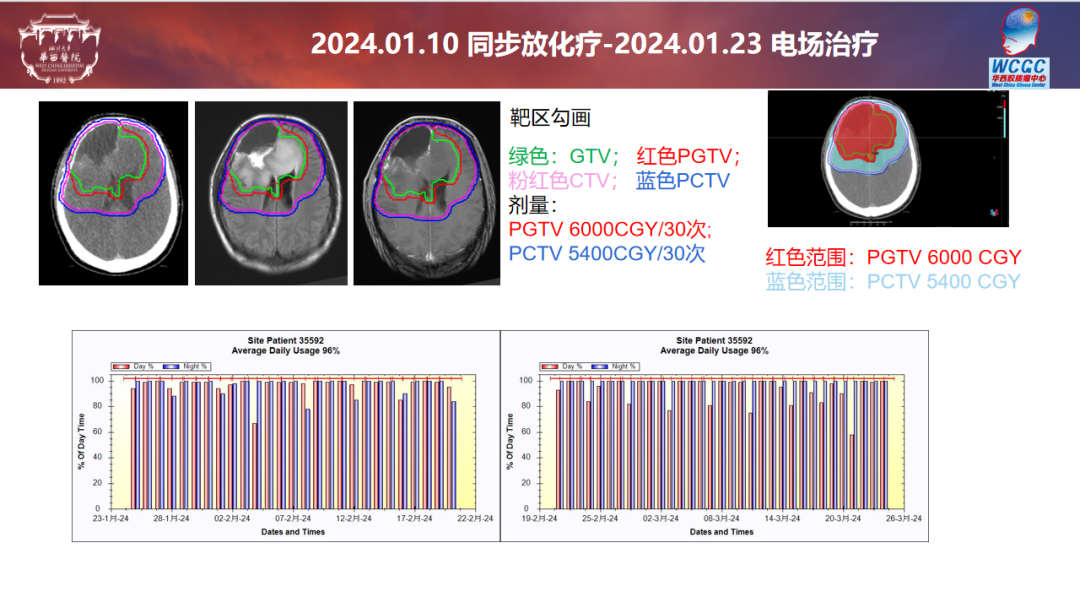
华西医院肿瘤科:该病例的放疗靶区GTV包括T1增强病灶、瘤床腔、T2/flair异常信号区,外扩2cm形成CTV(遇解剖屏障做相应修回),考虑该病例靶区体积大,放疗剂量PGTV60Gy/30次,PCTV54Gy/30次,理论上术后残留区域应同步加量至6450CGy,但残留区域体积大,高剂量范围大,脑坏死的风险大,而患者Ki-67指数低,stupp方案基础上在放疗同时进行了电场治疗,综合考虑不进行局部加量。
华西医院神经外科:该病例在术前已进行淋巴瘤相关治疗,本次病灶进展快,范围宽,手术只能做大部切除,胶质瘤会不会与淋巴瘤的治疗后的环境有关联,可能需要进一步讨论。
华西医院肿瘤科:该病例第一次(2006年)诊断为惰性B细胞淋巴瘤,经过免疫化疗、放疗后PFS达到十年,2018年1月24日复查提示肿瘤复发,再次病理活检诊断为低级别滤泡性淋巴瘤,再行二线化疗、放疗以及利妥昔单抗的维持治疗;2022年12月出现二次复发,后续入组Tazemetostat临床试验。Tazemetostat是一种口服的、选择性的EZH2抑制剂。EZH2负责催化组蛋白H3的第27位赖氨酸(H3K27)的三甲基化(H3K27me3),是一种与基因沉默相关的表观遗传修饰。目前Tazemetostat已被美国食品药品监督管理局(FDA)批准用于治疗转移性或局部晚期的上皮样肉瘤成人患者,以及复发性或难治性滤泡性淋巴瘤患者,该患者在使用该药物期间淋巴瘤病灶明显缩小,但是出现相应的头部症状,后经过手术后病理证实为胶质母细胞瘤,比较可惜的是因为患者在使用Tazemetostat药物之前没有相应的头部症状也未做相应头部检查,因此该药物与脑胶质瘤的关系尚未明确。
![]()
会议照片
![]()
下期预告

![]()
NGMA西南胶质瘤MDT专科联盟
2023年7月1日四川大学华西医院的MDT团队携手西南地区21家医院MDT团队,在国家神经疾病医学中心脑胶质瘤MDT专科联盟(NGMA)支持下,共同组建“西南脑胶质瘤MDT专科联盟”。联盟将致力切实提高西南地区乃至全国患者生活质量与生存获益,引导脑胶质瘤优质集中医疗资源辐射和下沉,赋能区域医学中心、基层医疗机构,切实推动脑胶质瘤及中国神经系统肿瘤疾病医学领域的建设与发展。

NGMA西南胶质瘤MDT专科联盟团队

四川大学华西医院胶质瘤MDT团队
![]()
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。
投稿邮箱:NAOYIHUI@163.com
未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。