
作者:廖长春,吴开华,陈刚(通讯作者)
单位:珠海市人民医院神经外科(暨南大学附属珠海医院)
摘 要
资料与方法
研究资料
1.临床资料
纳入了2021年01月至2021年12月期间在珠海市人民医院神经外科接受枕下乙状窦后入路微血管减压手术治疗的原发性三叉神经痛及面肌痉挛患者共26例。纳入标准:(1)典型的原发性三叉神经痛或原发性面肌痉挛患者,经CT或MR检查排除继发性病变;(2)由课题组进行的微血管减压手术治疗;(3)进行了术前多模态影像融合。排除标准:(1)术前即有面瘫、面部感觉麻木等类似手术并发症的症状者;(2)既往有枕下乙状窦后入路微血管减压手术史者;(3)术后不能完全随访6个月以上的患者。所有研究都得到了患者的书面知情同意。
本课题组纳入的26名患者,包括三叉神经神经痛患者13名,面肌痉挛患者13名,其中11名男性和15名女性,年龄在32-70岁之间,平均52.4±10.6岁,发病时长在0.5~10年之间,平均4.1±3.1年。(表1)

2.设备及数据
(1)MR设备:PhilipsIngenia CX 3.0TMRI,扫描层厚:1.0mm,序列包括T1WI 3D TFE、3D TSE DRIVE、3D TOF MRA、3D-FLAIR-Real-Meniere。(2)CT设备:联影UNITED IMAGING UCT 780,扫描层厚:0.63mm。(3)手术显微镜:ZEISS KV900。(4)术中电生理监测设备:Nicolet PROTEKTOR 32。(5)本课题组所采集的数据均为DICOM数据。
方法
1.术前多模态影像融合及评估
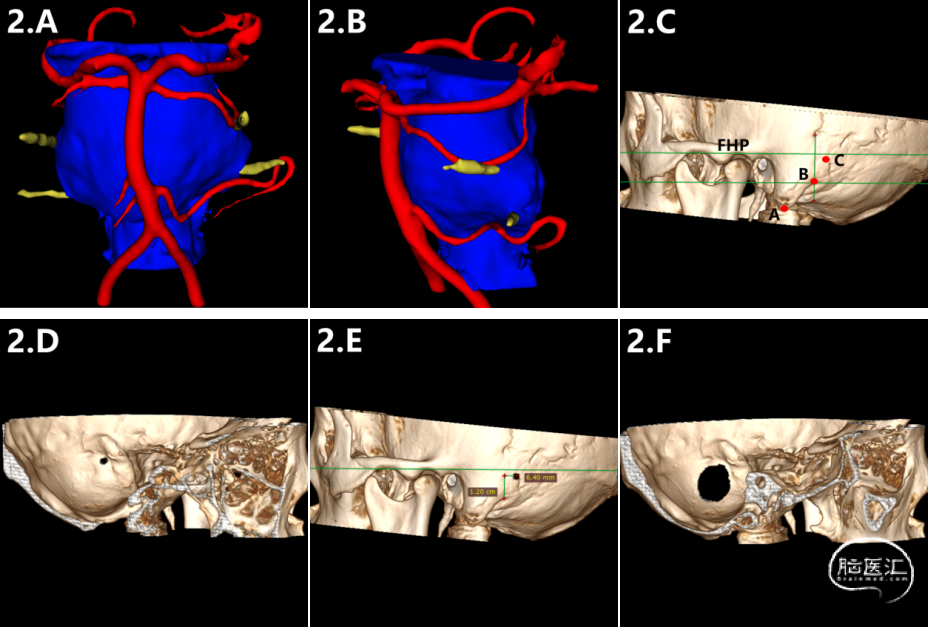
从医院影像科获取26例患者的Dicom图像数据,利用RadiAnt DICOM Viewer或者3D slicer软件对脑干、颅神经、血管、颅骨进行多模态影像融合和三维重建(图1.A、B,图2.A、B),通过多模态影像融合和三维重建,评估:(1)是否存在压迫三叉神经或者面神经的责任血管;(2)神经与血管及周围结构的空间关系;(3)横窦、乙状窦、关键点与颅骨结构(乳突尖、二腹肌沟、导血管孔)的关系(图1.C、2.C)。
术前手术入路模拟设计:(1)关键点定位及骨窗设计:本研究中关键点定义为横窦下缘及乙状窦后缘交界处在颅骨外表面的投影点。课题组利用RadiAnt DICOM Viewer对颅骨进行三维重建后,根据横窦、乙状窦的位置在颅骨模型内侧面上进行关键点模拟钻孔,并根据横窦、乙状窦边缘设计骨窗,从外侧面观察并测量关键点及骨窗的位置(图1.D、E、F、G,图2.D、E、F、G);(2)血管减压模拟:在虚拟骨窗下观察神经血管的空间结构,模拟血管减压操作过程(图1.H、图2.H)。


2.手术过程
(1)麻醉及体位:手术采用气管内插管全身麻醉,患者取标准侧卧位,头部稍下垂,mayfield三钉头架固定头部,面肌痉挛患者给予全程神经电生理监测;
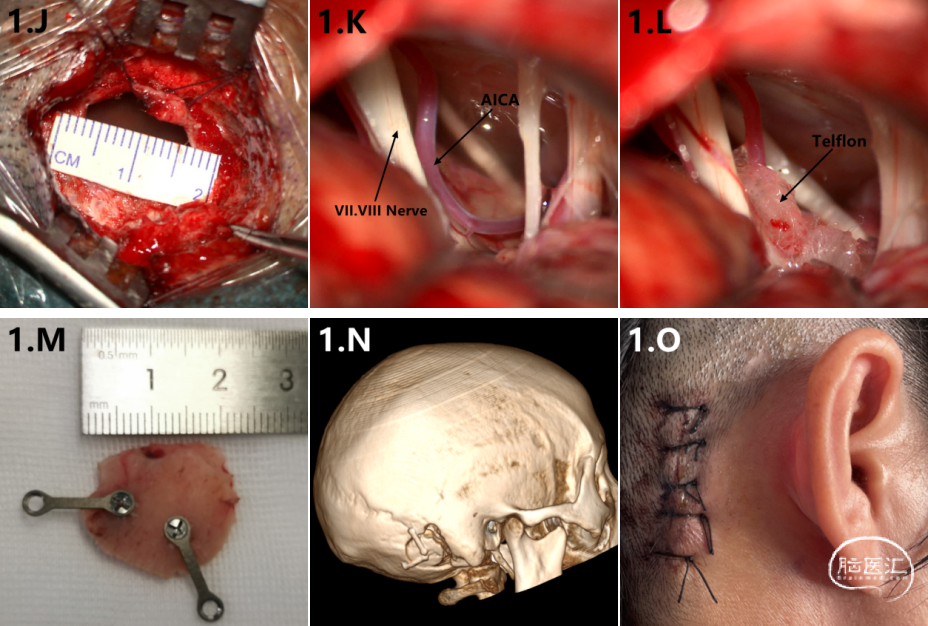
(2)于皮肤表面标记乳突尖、二腹肌沟顶点,标画法兰克福水平面,垂直于法兰克水平面取直切口长约4-5cm(图1.I、1.O,图2.I);
(3)切开头皮、肌肉,完全暴露二腹肌沟、导血管、星点等结构;
(4)按术前多模态重建结果,定位关键点,磨钻钻孔,铣刀游离骨瓣,显露乙状窦后缘及横窦远端下缘;
(5)显微镜下切开硬脑膜(图1.J),释放脑脊液,探查面神经或三叉神经脑池段及出入脑干段,辨认并确定责任血管(图1.K、图2.J),松解蛛网膜后,在责任血管和颅神经出入脑干段垫以Telfon棉(图1.L),使责任血管和和颅神经完全脱离接触至少2mm以上;
(6)严密缝合硬脑膜,连接片固定骨瓣(图1.M、图2.K),缝合肌肉及头皮。术后复查颅脑CT及MR(图1.N、2.L)。
3.评价指标
(4)统计学分析:三维模型中各结构之间的距离使用RadiAnt DICOM Viewer或者3D Slicer软件测量,术中各结构之间的长度使用游离标尺测量,计量资料结果用均数±标准差表示。所有数据使用IBMSPSS 22.0软件包进行统计分析处理。
结 果
术前多模态影像融合结果
(1)责任血管:通过术前多模态影像融合及三维重建,作者发现26例患者均存在责任血管压迫,其中小脑前下动脉12例,小脑上动脉13例,椎动脉1例。(如表2)

(2)关键点位置:作者根据术前多模态影像融合及三维重建中横窦、乙状窦的位置进行关键点模拟钻孔,测算出关键点大致位于二腹肌沟顶点的法兰克福水平面垂直上方12.3±0.46mm及外侧6.3±0.6mm处,与作者在先前关于枕下乙状窦后入路关键点定位的解剖学研究结果相似。
(3)模拟骨窗及手术:通过模拟关键点钻孔及骨窗设计,作者可以设计合理骨窗,设计的骨窗直径大约为2.0cm-3.0cm,在虚拟骨窗下可以顺利观察神经血管的空间关系,模拟整个手术过程。
手术结果
手术效果及并发症
13例原发性三叉神经痛患者中12例(92.3%)疼痛完全缓解,1例明显缓解,手术并发症包括面部感觉麻木1例、眩晕2例、嘴角疱疹1例。13例面肌痉挛患者中12例(92.3%)面部抽搐症状完全缓解,1例患者症状大部分缓解,并发症包括轻度面瘫2例(15.4%),面部感觉麻木2例(15.4%)。
随访
特殊病例展示
52岁男性,左侧面部不自主抽动10年,诊断左侧原发性面肌痉挛,术前多模态影像融合结果提示左侧椎动脉压迫左侧面神经根部,根据术前模拟关键点、开颅及血管减压过程,手术中精确定位关键点,手术过程顺利,术后患者面部抽搐症状完全消失,大致手术过程如图3。

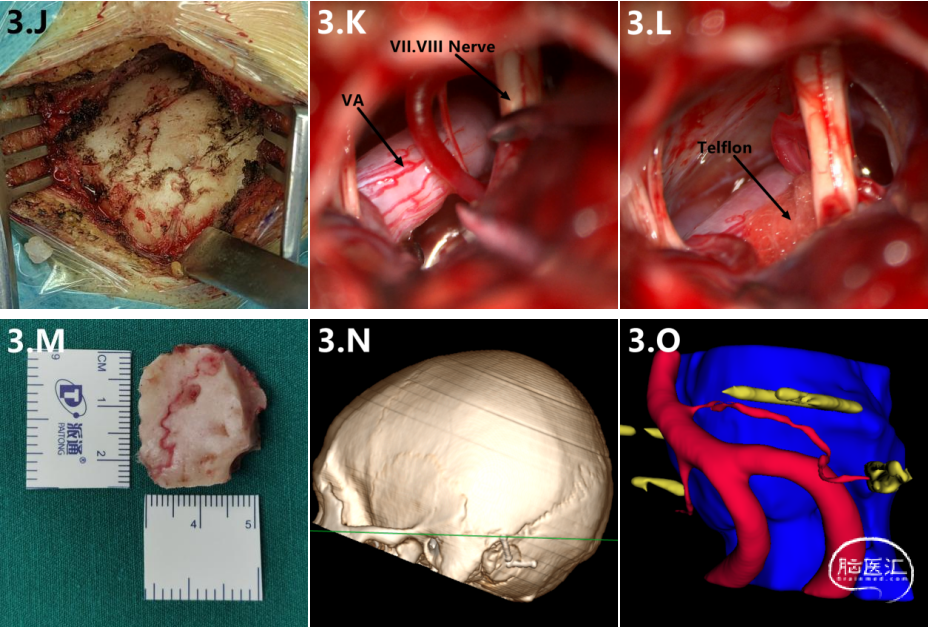
图3.一例特殊的左侧面肌痉挛患者的术前多模态影像融合及手术过程。(3.A)神经、脑干、动脉多模态影像融合重建结果正面观。(3.B)神经、脑干、动脉多模态重建结果侧面观。(3.C)颅骨三维重建及相关解剖标志。(3.D)在颅骨内侧面模拟关键点位置。(3.E)模拟关键点外侧观。(3.F)在颅骨内侧模拟开颅骨窗范围。(3.G)模拟骨窗外侧观。(3.H)模拟开颅后手术视野。(3.I)手术切口大约4.5cm。(1.J)手术中暴露颅骨表面;(1.k)MVD手术中可见椎动脉压迫面神经。(1.L)Telflon垫片垫开椎动脉。(1.M)骨瓣大小。(1.N)术后颅骨三维重建。(1.O)术后神经、脑干、动脉多模态重建结果侧面观。
讨 论
近年来,术前多模态影像融合技术在医学神经外科领域的应用越来越广泛,特别是脑肿瘤、三叉神经痛、面肌痉挛等疾病方面,术前多模态影像融合技术的应用,能更直观地让手术者了解各结构之间的关系,对手术有重要指导意义。本次研究中,课题组通过26例三叉神经痛和面肌痉挛的枕下乙状窦后微血管手术,进一步体现了术前多模态影像融合技术在医学领域的价值。
术前多模态影像融合技术能充分地对枕下乙状窦后入路微血管减压手术进行术前评估。在既往没有术前多模态影像融合技术的情况下,大多数人都是通过经验设计手术皮肤切口,通过星点结构来定位关键点位置,凭经验设计骨窗,这可能会出现切口设计不到位、横窦或者乙状窦损伤、术野暴露不佳等情况,增加手术并发症。截止到目前,仍有很多人把星点作为定位关键点的主要结构[18],认为星点代表横向乙状窦交界处相对应的颅骨外部浅表特征。但是根据研究发现,星点相对于横窦乙状窦的位置存在不确定性,其中一项研究表示,只有23.3%的患者存在这种关系,此外,只有63.3%的患者的星点结构对应者横窦的下缘[19]。因此,在乙状窦后入路开颅手术时如果将星点作为关键点固定依据时,必然有引起静脉窦损伤的风险。在课题组之前的尸头解剖研究中发现,关键点一般位于二腹肌沟顶点上方12mm处[20],但后来的临床手术中课题组发现部分患者关键点位置在二腹肌沟顶点上方12mm再往后0.6cm左右的距离。在本研究中,课题组通过术前影像测量和术中验证,我们发现关键点和二腹肌沟顶点确实存在密切的关系,关键点大致位于二腹肌沟顶点的法兰克福水平面垂直上方12.3±0.46mm及外侧6.3±0.6mm处,这结果与课题组之前的研究结果大致相同,但存在少许差异,课题组将在后续的解剖研究中进一步增加研究例数,争取更准确地测量二腹肌沟及关键点的关系。本研究中,术前多模态影像融合技术的应用为作者提供了可视化3d影像,能让作者全方位地了解颅骨及其骨性结构、横窦乙状窦以及导静脉的走形、神经以及血管之间的空间关系,为手术提供科学的依据。在此基础上,手术者术前通过触摸关键的骨性结构,可以轻松设计手术切口,使手术的皮肤切口尽可能更小。切开皮肤及暴露颅骨后,通过识别乳突、二腹肌沟、星点、导静脉孔等实际骨性结构,结合术前多模态影像融合的测量结果,作者可以更精确地对关键点进行定位,更科学地估计乙状窦横窦的走形,能在减少乙状窦横窦及导静脉损伤以及充分暴露手术视野的同时尽量形成更小的骨窗范围。在术前了解神经、责任血管以及周围重要结构之间的具体空间关系的情况下,术者可以尽可能地减少术中无效的操作,尽最大可能减少手术对神经血管的损伤以及减少手术并发症。
本研究实际手术中发现,有些病例中的病变神经可能存在多根血管压迫,但一般只有压迫面神经或三叉神经根部的血管才是责任血管,三叉神经痛主要的责任血管是小脑上动脉,而面肌痉挛患者则是小脑前下动脉,但其实椎动脉也是面肌痉挛常见的责任血管。另外,静脉也可能是三叉神经痛或者面肌痉挛的责任血管,有一例2020年的三叉神经痛患者,术前课题组通过术前影像评估无法完全确定责任,但术中所见是岩静脉,术中课题组只发现岩静脉与三叉神经存在关系,而且通过松解与垫开岩静脉,患者术后症状完全缓解。

本研究中,多名三叉神经痛及面肌痉挛患者术后出现了面部感觉麻木、眩晕、面瘫等并发症,课题组术后总结分析出现这些并发症的主要原因是应该手术操作对三叉神经及面、听神经的直接骚扰损伤,包括直接的牵拉或者电凝热损伤,其他原因可能是神经滋养血管的损伤,因为一般来说神经的滋养血管非常纤细,松解蛛网膜或者分离血管时很容易造成损伤且术后引起神经功能障碍,但这些损伤一般都可以通过治疗慢慢缓解,这些并发症患者后期主要的康复治疗包括药物营养神经、物理针灸理疗以及星状神经节阻滞治疗。
关于术前多模态影像融合技术的软件方面,本研究主要使用了RadiAnt DICOM Viewer以及3D slicer这两中软件,其中3D slicer软件对对多种DICOM数据进行配准和切割,对脑干、颅神经、血管、颅骨进行多模态影像融合具有很大优势,但也存在一些缺点,包括在颅骨重建的细节上没有RadiAnt DICOM Viewer仔细,RadiAnt DICOM Viewer能更详细地显示颅骨的各种结构,分辨率更高。
此外,课题组发现术前多模态影像融合技术不仅可以为术者提供重要的参考量,它也可以作为术前和患者交流的手段之一。虽然没有经过具体的数据分析,但课题组确实注意到,当课题组有向患者及其家属展示术前多模态影像融合及三维重建结果的时候,患者及其家属很容易便能对疾病及治疗手段产生理解,而且表现得更配合,更容易接受推荐的手术治疗方案。课题组认为,术前多模态影像融合及三维重建技术能为患者及家属更直观更简单得展示疾病的具体情况以及大致的手术过程,让他们更容易接受及理解,增加对手术者的信任。
但是本研究也存在许多缺陷和不足,包括:(1)病例数偏少,可能降低数据的可信度;(2)没有和既往没有进行多模态影像融合技术的微血管减压手术进行对比,无法完全证明多模态影像融合技术的优势。在今后的研究中,课题组将继续增加病例数,多方面具体量化分析,获取更多可靠数据。
结 论
多模态影像融合及三维重建技术对原发性三叉神经痛及面肌痉挛的枕下乙状窦后入路微血管减压手术有重要的指导意义。它能对患者进行充分的术前评估,让手术者能随心所欲地在3D下更直观地观察病变神经与责任血管及周围结构的空间关系,明确责任血管,同时还能辅助设计手术入路,模拟手术过程,尤其是在关键点的定位中具有重要的辅助作用,结果提示关键点可以精准定位在二腹肌沟顶点的法兰克福水平面垂直上方12.3±0.46mm及外侧6.3±0.6mm处。但是本研究也存在许多不足之处,在今后的研究中,我们将加强枕下乙状窦后入路相关解剖结构的基础研究,进一步确认相关结构的固定关系,进一步探讨术前多模态影像融合技术的意义。

作者简介
陈刚 主任医师
珠海市人民医院
主任医师,医学博士,珠海市人民医院神经外科科主任
中国解剖学会神经外科解剖学分会常委
中国卒中学会脑出血微创治疗专业委员会常委
中国医疗保健国际交流促进会神经创伤学分会常委
广东省医学教育协会神经外科专业委员会副主任委员
广东省医院协会神经外科专业委员会副主任委员
广东省医疗行业协会神经外科管理分会副主任委员
珠海市医师协会神经外科分会主任委员
廖长春 主治医师
珠海市人民医院
毕业于南昌大学医学院,神经外科专业硕士,从事神经外科临床工作7年余,拥有良好的临床工作经验,及娴熟的神经外科技术
擅长:1.多模态3D影像技术辅助下微创治疗颅内肿瘤;2.微血管减压手术微创治疗原发性三叉神经痛、面肌痉挛,以及经皮三叉神经半月节球囊压迫术微创原发性三叉神经痛等
![]()
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。







