
Brief Introduce
✦
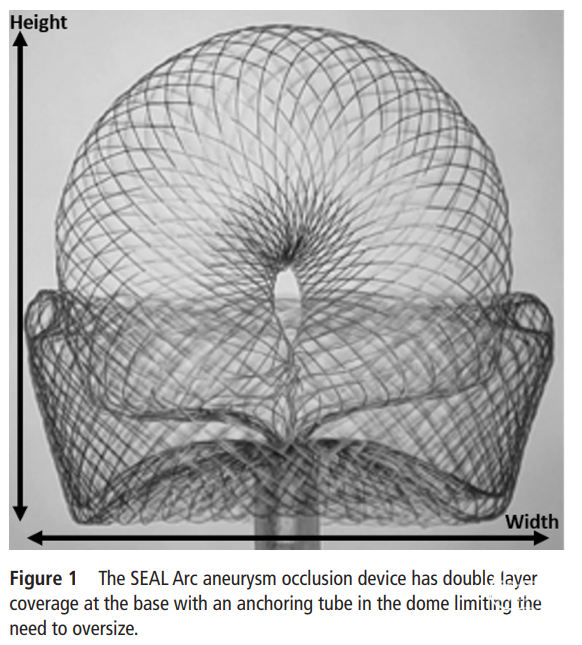
颅内动脉瘤的囊内装置已成为一种被广泛接受的治疗策略。由于其极少暴露于载瘤动脉循环内,囊内装置相对于腔内血流导向装置和支架具有一些优点。主要是,它们不需要双重抗血小板治疗,并且可以释放来减少对小穿支中血流干扰或血小板聚集物脱落的担忧。Woven EndoBridge(WEB, Microvention, Aliso Viejo, CA)装置是最经过深入研究并表现出良好前景的装置,可用于治疗其他方式难以经血管内治疗的宽颈动脉瘤。这些装置旨在干扰动脉瘤囊内的血流,促进血栓形成,并提供跨越动脉瘤颈部的脚手架,以促进新内膜生长,实现永久性从循环血流中排除动脉瘤。WEB目前是唯一获得美国食品和药物管理局(FDA)批准的囊内扰流装置。它表现出良好的安全性;然而,尽管有着有前途的长期结果,但一些研究引发了有关该装置有效性的担忧,强调需要进一步的研究。类似的装置已在其他国家获批,并正在进行FDA批准的临床试验。新型的Saccular Endovascular Aneurysm Lattice Arc configuration(SEAL Arc) (Galaxy Therapeutics, Inc, Milpitas, CA)装置是一种双层、颈部桥接、混合镍钛网状装置,旨在干扰动脉瘤内部的血流。它由类似喇叭环状的结构组成,与动脉瘤颈相接,连接到一个无创锚定管,该管通过径向力使装置接触瘤顶,旨在使装置顺应各种动脉瘤形状(图1)。
高频光学相干断层扫描(HF-OCT)是专门设计用于神经血管的迂曲解剖结构的一种相对较新的技术,用于检查血管内装置。它已经显示出除数字减影血管造影(DSA)外,对于评估血管内装置的解脱放置具有价值。HF-OCT提供了装置支柱上新生内膜生长的独特详细视图,可与组织病理学相媲美。鉴于这些特点,HF-OCT可以代替其他尸检成像技术。
方法
1
实验步骤
我们的大学动物保护和使用委员会批准了所有动物研究试验。我们在新西兰白兔模型(n=11)(性别:任意;体重3.0-4.0kg)中创建了弹性蛋白酶诱导的动脉瘤。在动脉瘤形成的最少3周后,我们给兔子植入了SEAL Arc装置。
所有手术都是在全身麻醉下进行的。动物在皮下注射阿托品(0.01mg/kg)进行术前麻醉,并给予肌内缓释丁丙诺啡(0.03mg/kg)止痛。肌内注射氯胺酮(35mg/kg)和甲苯噻嗪(5mg/kg)麻醉,1-3%异氟醚机械通气维持麻醉。每15分钟监测一次呼吸率、心率、血氧饱和度、末梢呼气二氧化碳水平和体温以评估动物的生理状态。术中使用肝素(100U/kg);但在植入前或植入后未提供抗血小板治疗。
2
影像分析
3
统计分析
使用先前报道的具有相同DSA和OCT输出的相同模型的WEB植入物(植入物和数据分析人员相同)进行比较。使用Kolmogorov-Smirnov检验确定数据是否符合正态分布。使用Student非配对双尾t检验比较连续正态分布数据。使用方差分析比较多组连续数据。由于样本量,离散数据使用Fisher精确检验进行比较。使用GraphPad Prism(Dotmatics,San Diego,CA)和Excel(Microsoft Corporation,Redmond,WA)进行统计测试。使用α 0.05确定统计学意义。由于不同的组织学技术在研究中被应用,因此不对使用不同装置治疗的动脉瘤进行组织学数据比较。
结果
我们的数据分析包括11个用SEAL Arc治疗的兔动脉瘤。SEAL Arc组中的一只兔子在植入后2周因双侧后肢瘫痪而被安乐死。该动物被排除在分析之外。在纳入分析的动物中,有七只为雌性,平均体重为3.5公斤。平均±SD动脉瘤宽度为3.4±0.64毫米,动脉瘤高度为6.8±1.5毫米,动脉瘤颈直径为2.6±0.53毫米。
发现30%(n=3)的SEAL Arc装置疝出,20%(n=2)在HF-OCT上表现出与动脉瘤两侧壁贴壁良好。植入后立即,所有治疗的动脉瘤均未表现出闭塞。在12周时,80%(n=8)的动脉瘤完全闭塞(图2)。
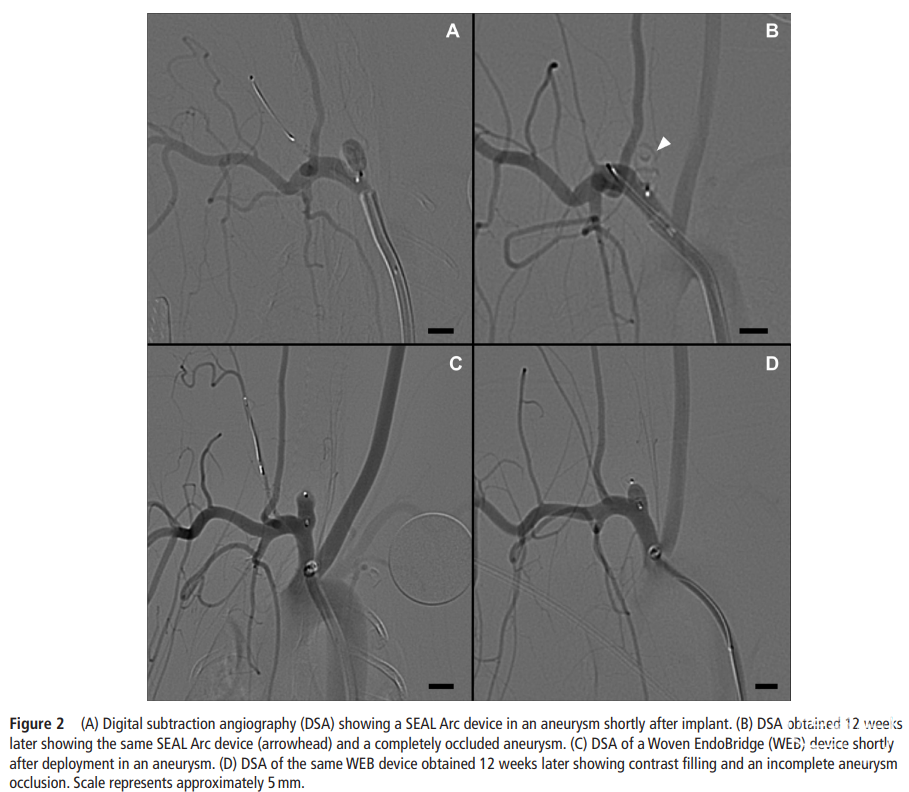
由于图像质量差,一只动物的12周HF-OCT被排除在外。在剩余的九个装置中,平均新内膜覆盖率为86±15%(图3)。在HF-OCT上疝出的装置与未疝出的装置相比,在新内膜生长上没有显著差异(74.3±23% vs 91.4±9%,P=0.135)。良好贴壁的装置和未贴壁的装置之间在新内膜覆盖率上没有统计学差异。完全闭塞的装置与未完全闭塞的装置相比,在新内膜覆盖率上也没有显著差异(89.1±9% vs 73.7±34%,P=0.253)。
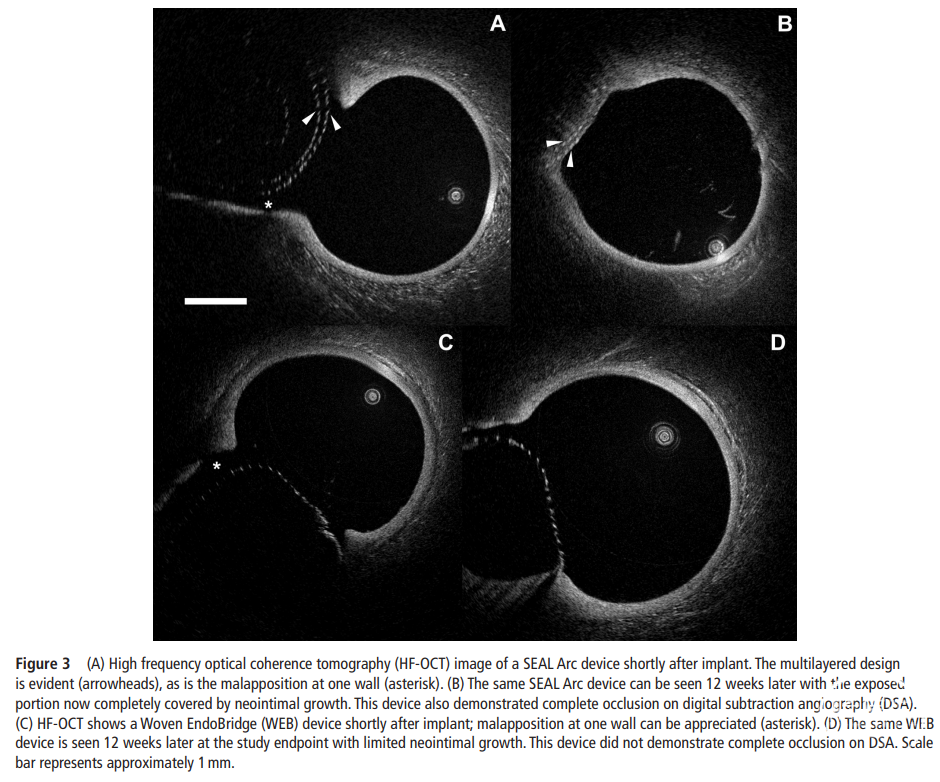
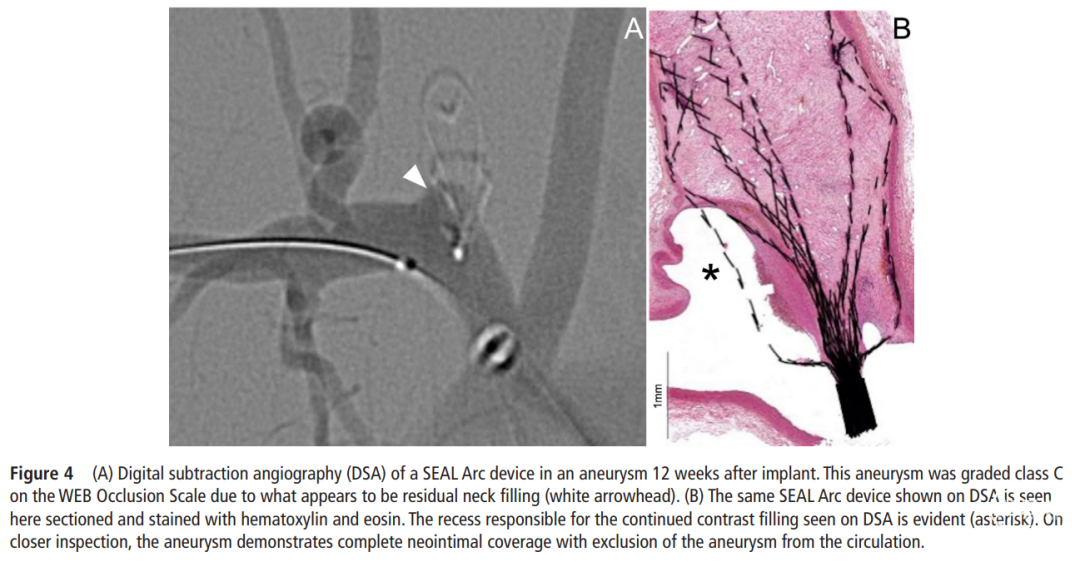
在组织学上,所有治疗的动脉瘤均显示颈部完全闭塞,并被一层薄组织覆盖。在随访DSA中未完全闭塞的两例病例显示了横跨动脉瘤颈部的致密纤维肌性新内膜(图4)。组织学显示,网状材料引起炎症反应极小或没有。
与历史对照的比较
我们将这些结果与先前在我们中心进行的24只动物的历史队列进行比较,这些动物使用WEB装置在相同条件下进行治疗,并且动脉瘤尺寸没有统计学差异。WEB疝出的发生率(63%,n=15)与Arc SEAL装置相比有上升趋势(P=0.057),而WEB良好贴壁率(21%,n=5)几乎相同。在12周DSA上,使用WEB治疗的动脉瘤完全闭塞率(21%,n=5)较Arc SEAL治疗的动脉瘤低(P=0.02)。将两个队列的所有数据综合起来,疝出的装置在研究终点时完全闭塞的可能性显著较低(P=0.001)。对于贴壁不良的装置,未观察到此关系。在HF-OCT上,疝出的装置在未疝出的装置中具有显着较少的新内膜生长(40.7±22% vs 82±21%,P<0.001)。良好贴壁的装置和不良贴壁的装置之间在新内膜覆盖率上没有统计学差异。与WEB相比,SEAL Arc装置在植入后12周具有显着更多的新内膜覆盖(P=0.001)。在此时间点上,SEAL Arc装置的平均新内膜覆盖率为86±15%,而WEB装置为49±27%。即使在控制了较高比例疝出WEB装置的情况下,新内膜生长与SEAL Arc之间的正向关系仍然存在(P=0.001);然而,这个亚组分析的样本量不足。完全闭塞的装置显示出显着更大的新内膜覆盖率(90.9±7% vs 41.3±21%,不完全闭塞装置,P<0.001)。
讨论
先前的研究发现,单层WEB装置产生的闭塞效果与同一模型中其他转化研究的结果基本一致。以往的研究表明,桶形装置的完全闭塞率为29%,单层球形装置为35%,相比之下,我们注意到21%的病例在相同的时间内完全闭塞。WEB装置的双层版本也在该模型中进行了测试,其中33%的装置在1个月内完全闭塞,12周时达到67%。这可以与我们测试的双层SEAL Arc装置进行比较,在此时间点上完全闭塞率为80%。虽然这不是他们文章的主要焦点,但Ding等人还在兔模型中研究了单层和双层装置。他们将单层桶形和球形装置与双层WEB装置进行了比较。双层装置的完全闭塞率为3个月时的67%,而单层仅为41%。这里提出的结果以及先前在文献中发表的结果表明,双层装置与动脉瘤完全闭塞之间存在联系。
SEAL Arc装置的组织病理学结果进一步支持了这一联系。仔细检查DSA上未完全闭塞的两个SEAL Arc,发现动脉瘤已完全愈合,且有密集的新内膜覆盖。
在HF-OCT上,我们还发现12周后SEAL Arc装置上的内膜覆盖率明显高于WEB,这可能解释了DSA闭塞率的差异。已经表明,装置的释放,特别是没有疝出,可能在动脉瘤闭塞中起到作用。疝出可能会对新内膜生长产生负面影响,高剪切力和复杂的流动模式会延迟细胞增殖和附着。
我们对SEAL Arc装置的分析并未发现疝出装置与未疝出装置之间或完全闭塞装置与未闭塞装置之间的新内膜覆盖率差异。虽然可能由于SEAL Arc的独特设计而不适用于先前描述的这些关系,但更有可能是由于样本量过小导致无法检测到这些差异。虽然不显著,但我们的数据趋势显示这些组之间存在差异。此外,在汇总分析中,我们观察到疝出的装置更不可能完全闭塞,并且新内膜生长显著较少,支持在动脉瘤颈部放置装置的重要性。
WEB装置建议使用增大尺寸以减少压缩的风险,从而可能导致疝出。遵循这些建议,我们观察到62%的WEB装置疝出,而SEAL Arc装置仅有30%。虽然这种差异在统计学上并不显著,但考虑到我们和其他人观察到的疝出装置与新内膜生长减少之间的强关系,这一点非常重要。
两种装置都是根据制造商的建议进行尺寸选择的。可能在更大的样本量下,我们会观察到SEAL Arc的疝出率比WEB低。然而,即使在统计控制装置不同疝出率的情况下,SEAL Arc装置与明显更多的新内膜生长之间的关系仍然存在。这表明还有与SEAL Arc装置设计相关的其他因素可以解释观察到的差异。
SEAL Arc的多层设计在动脉瘤内释放后,允许更多的网状结构暴露在颈部并提高闭塞程度,这在HF-OCT上很明显(图4)。这产生了一个更有利于闭塞和新内膜生长的动脉瘤内环境。动脉瘤颈部紧密相邻的镍钛网格层可能会创造出一个有利于细胞生长和增殖的微环境。文献支持这一点,显示金属暴露量与新内膜的发展之间存在相关性。
一些双层设计的缺点可能是导致装置僵硬和不灵活,从而可能阻碍输送。我们在本研究中测试的单层WEB装置是早期双层设计的低剖面替代品。它们是为了改善导航和输送而研发的,并具有更多的尺寸型号。SEAL Arc的设计似乎允许双层网格而不影响装置的整体剖面和导航便利性。正在进行的临床病例系列也证明SEAL Arc可以用于治疗复杂动脉瘤。
除了SEAL Arc装置的设计,还需要考虑可能带来的安全影响。WEB装置的双层版本虽然整体上证明是安全的,并且与单层设计相当,但趋向于增加血栓栓塞并发症。导致更高闭塞和内皮生长的囊内因素也可以促进血栓形成,在没有双重抗血小板治疗的情况下是一个重要考虑因素。最终,暴露部分的SEAL Arc装置被内皮覆盖的速度以及更高的闭塞率可能会导致减少并发症和增加安全性。
总结
我们在一个转化临床前模型中观察到,一个独特的多层设计的囊内扰流装置和一个无创前导锚定管在DSA上显示12周时动脉瘤完全闭塞率非常高(80%)。在所有病例中,证实了动脉瘤的组织学治愈。使用HF-OCT,发现SEAL Arc装置具有更多的新内膜生长,与不同装置之间的疝出率差异无关。这些结果表明,囊内扰流装置设计的进步可能会提高实现动脉瘤完全闭塞的疗效,但这需要临床验证。
点击上方二维码
查看更多“介入”内容
声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。
投稿邮箱:NAOYIHUI@163.com
未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。
投稿/会议发布,请联系400-888-2526转3。





