脑医汇,由外而内,融“汇”贯通
2023年7月11日,复旦大学脑科学研究所那德(Nashat Abumaria)课题组以“TRPM7 kinase activity induces amyloid-β degradation to reverse synaptic and cognitive deficits in mouse models of Alzheimer’s disease”为题在Science Signaling上发表了一项相关的科学研究。来自复旦大学脑科学研究所那德课题组的博士生张诗萌和曹霏霏是该论文的共同第一作者。来自复旦大学脑科学研究所的那德(Nashat Abumaria)研究员和李薇副研究员是该论文的共同通讯作者。来自中国科学院IRCBC的王文元研究员和陈椰林研究员为本课题提供了5XFAD的模型小鼠。
[Zhang S, Cao F, Li W, Abumaria N. TRPM7 kinase activity induces amyloid-β degradation to reverse synaptic and cognitive deficits in mouse models of Alzheimer's disease. Sci Signal. 2023 Jul 11;16(793):eade6325. doi: 10.1126/scisignal.ade6325. Epub 2023 Jul 11. PMID: 37433006.]
该项研究首先证明了阿尔茨海默病患者和两种阿尔茨海默病模型小鼠的海马组织(参与学习和记忆过程的关键大脑区域)中的TRPM7表达量显著降低。随后,作者发现上调TRPM7或者其激酶结构域的表达量可抵消Aβ的病理毒性。并揭示TRPM7激酶结构域是如何减少脑内Aβ的沉积,并保护突触密度,进而修复阿尔茨海默病模型小鼠的记忆缺陷(图1)。
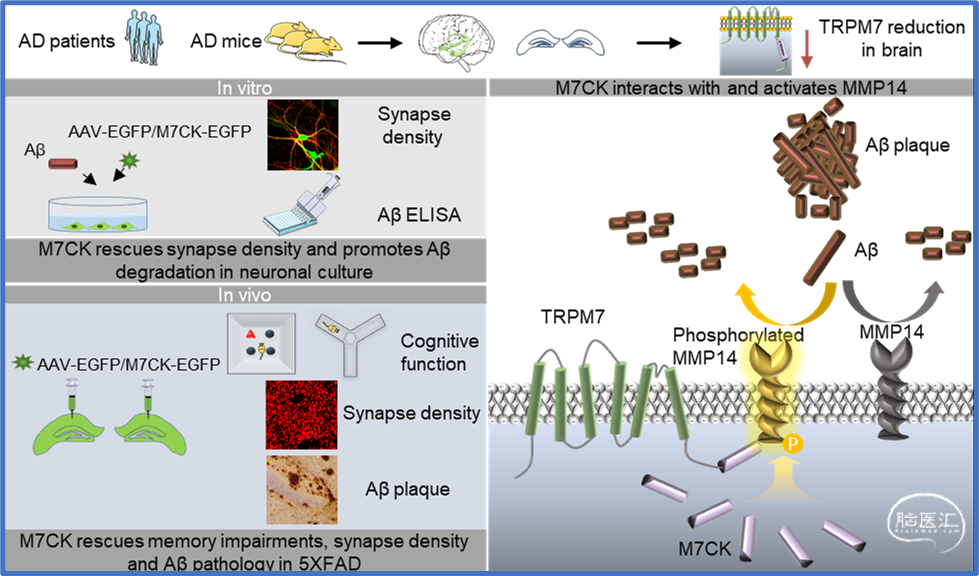
图1. 研究概述(Aβ:淀粉样蛋白-β;AD:阿尔茨海默病;M7CK:TRPM7的激酶结构域)
1
研究背景
2
研究方法&研究结果
3
研究结论
通
讯
作
者
*本文转载自复旦大学新闻网
声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、Ai Brain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。





