现病史:3岁首次发作,发热1天,最高40度,发热当天出现热性发作,表现为:双眼上翻,四肢僵直抖动,持续时间约3-5分钟,发作后无不适。当时诊断“热性惊厥”;3-23岁(1981-1999年)无发作;23岁后再发,表现为中午饮酒后小便前感腰部左侧酸胀,继而倒地,四肢僵直伴意识丧失,持续1-2min后自行缓解,2-3min后缓解自行站立;20天后再发,症状同前,此后在2000年共出现3次发作,表现均同前;34岁(2011年)后再发,表现为腰部左侧发僵抽搐感,继而左侧肢体发僵发硬,双下肢乏力,该过程意识清楚,可自控不跌倒;2011年后3-5天出现1次发作,2019年6月后1-2次/天,晨起剧烈活动及憋小便、饥饿均可诱发;左下肢无力持续时间长时可出现倒地,四肢强直抽搐伴意识丧失:2011年2次,2019年5月、6月各出现1次四肢强直抽搐;2019年10月停药监测发作时出现2次;末次发作:2019年10月18日。母孕出生:G2P2,第二胎,孕期及出生无特殊,否认缺氧窒息史及黄疸史。生长发育:生长发育基本正常,1岁会走路,3岁会讲话;小学成绩中下等;中学成绩中上;中专毕业,目前木材厂就业,车间登记员;药物过敏:无。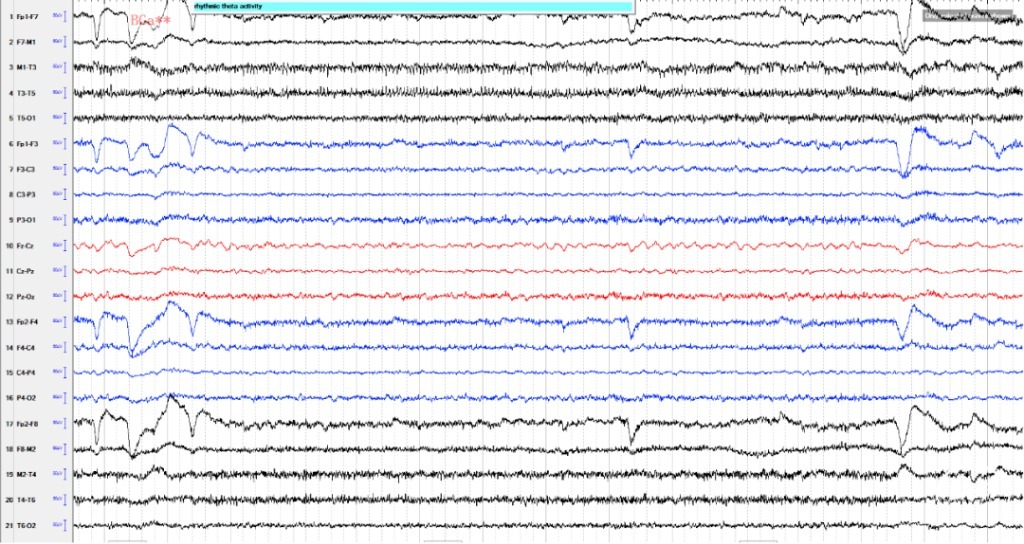
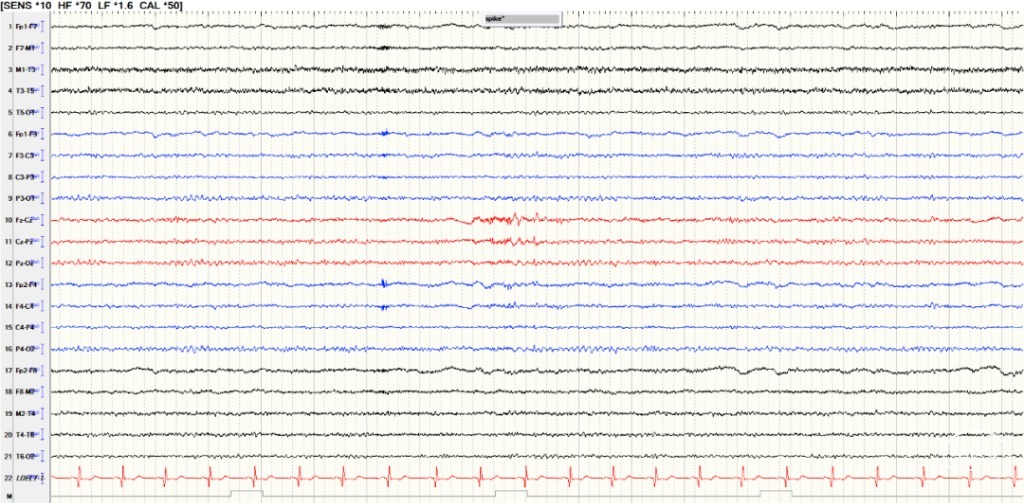
图1.头皮脑电图提示背景活动可见中线区慢波活动,监测到癫痫样放电中线区。
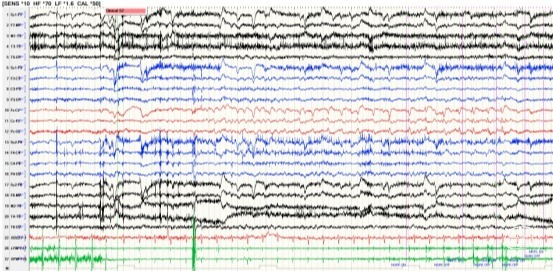
图2.临床发作表现为腰部无力→躯干及左侧下肢阵挛,发作期脑电图中线区为著。
间歇期放电:癫痫样放电,中线-双侧旁中线,中线-右侧旁中线著;
监测到3次癫痫临床发作,表现为腰部无力→躯干及左侧下肢阵挛(惯常发作),发作期脑电图(图2)考虑起始于中线区。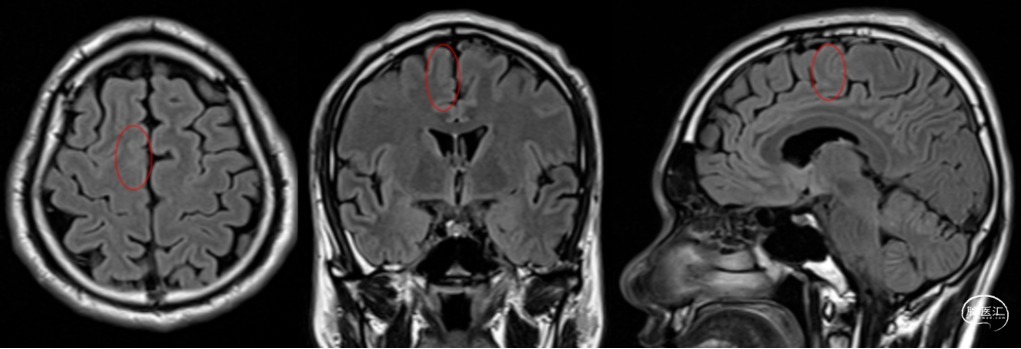
图3.头颅MRI提示右侧旁中央前沟可疑灰白质界限不清。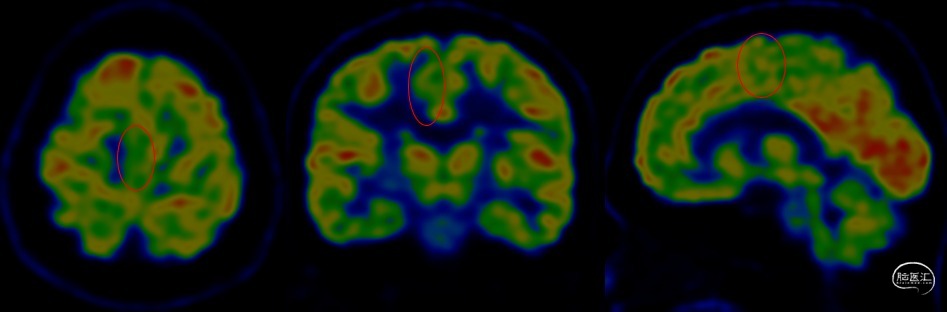
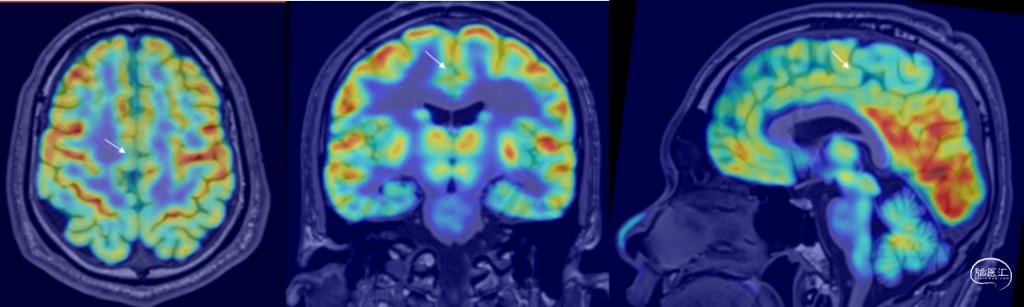
图4.头颅PET提示右侧旁中央前沟、SMA局灶性低代谢。
经过上述术前评估,结合病史,考虑致痫区位于右侧中央区受累为主,左侧中央区需鉴别,需要通过立体定向脑电图确认致痫区及其范围。
在提出工作假设基础上,根据“解剖-电-临床关联”的设计原则,确定SEEG植入方案(图5)。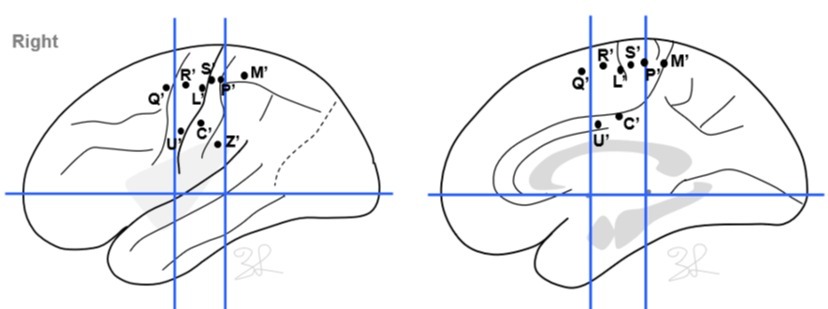
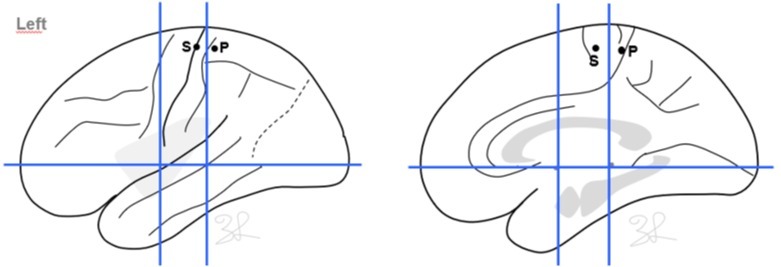
图5.SEEG植入方案及植入计划,以右侧SMA、中央前回、中央后回结构为主,覆盖左侧旁中央小叶相鉴别。发作间期(图6):右侧SMA相关电极可见大量不规则棘慢波,旁中央小叶前部受累;
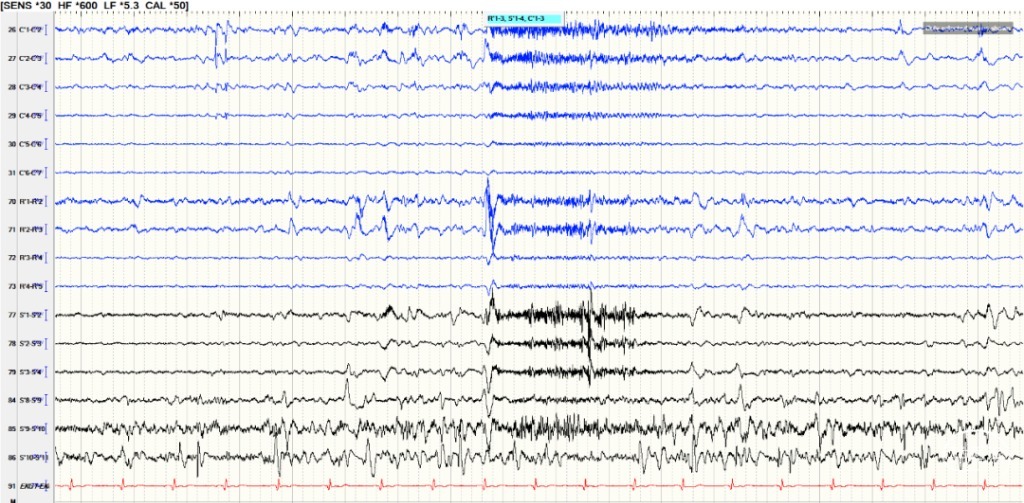
图6.间歇期:右侧中央沟(L’1-4)、右侧中央前回(S’7-10)相关电极可见大量不规则棘慢波,右侧SMA、中央沟电极为著。
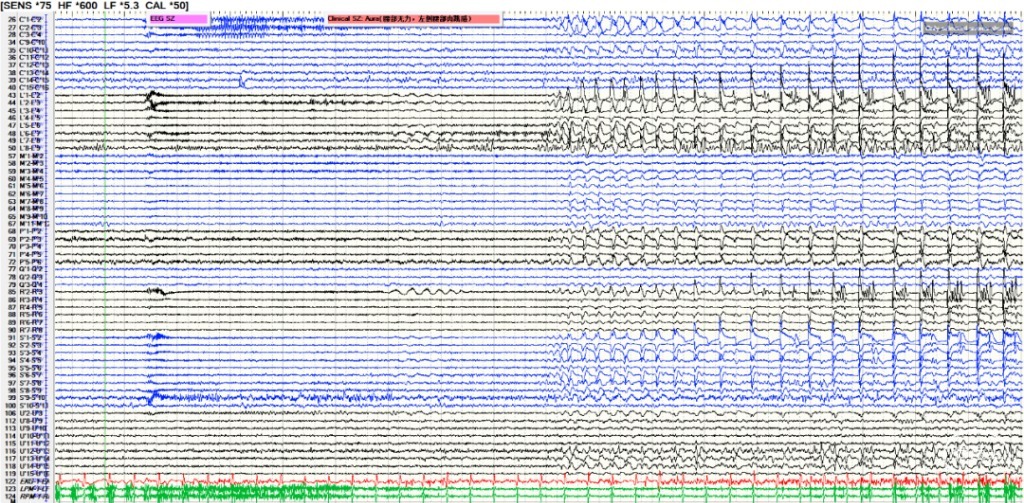
图7.发作期:提示癫痫发作起源于右侧SMA、中央前回。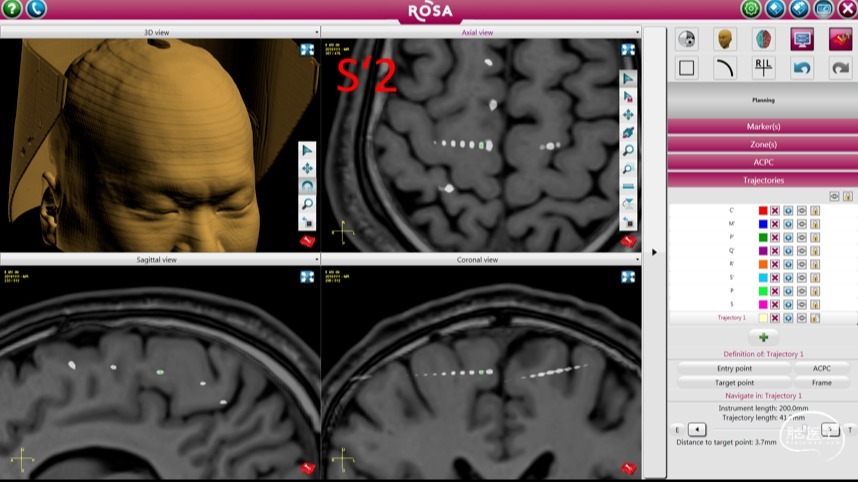
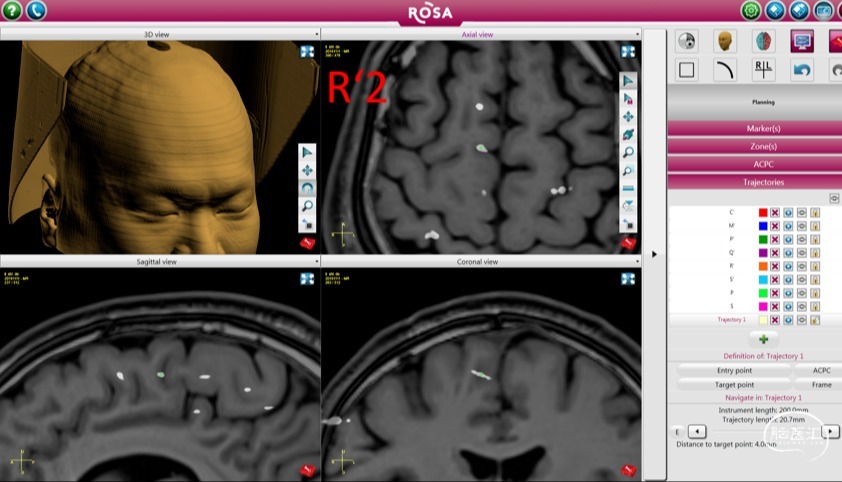
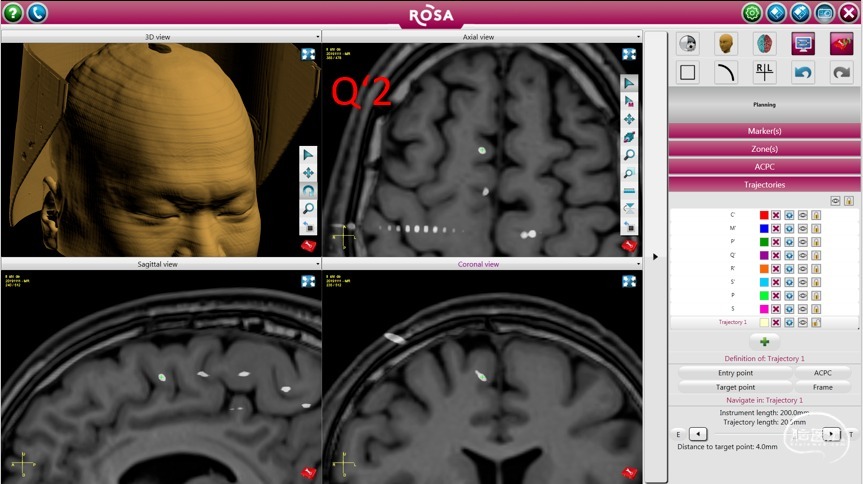
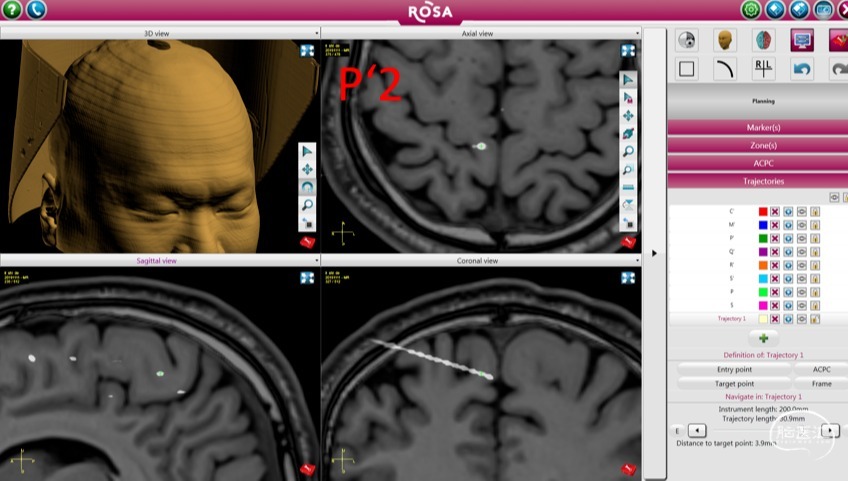
根据对上述资料的综合评估,设计外科切除计划(图8),并实施外科手术。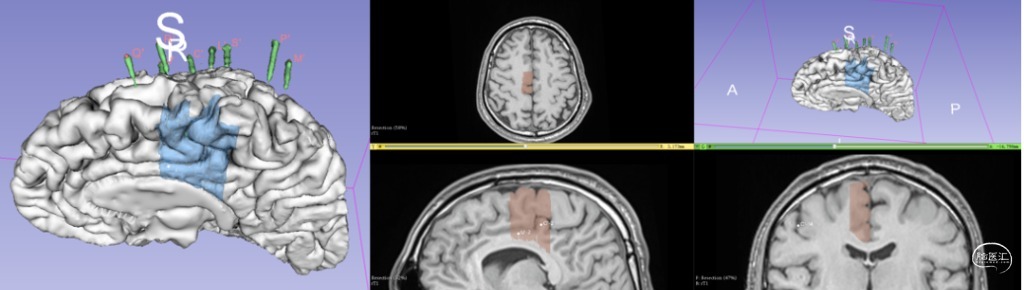
图8.癫痫外科切除计划,切除主体位于右侧旁中央前沟、SMA的皮质及对应的扣带回。
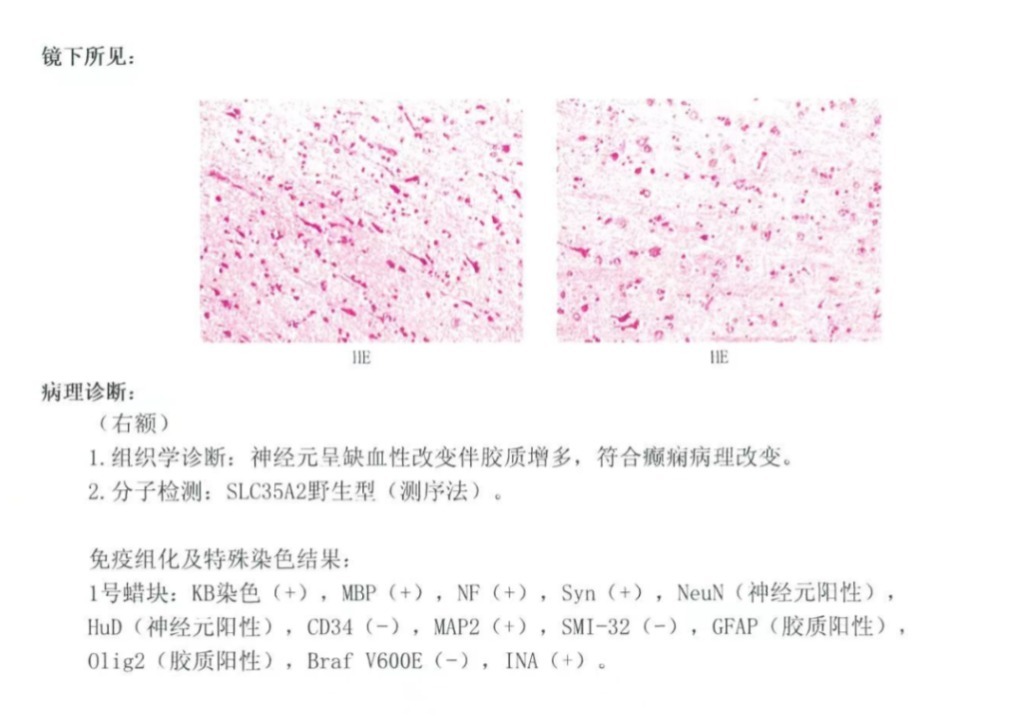
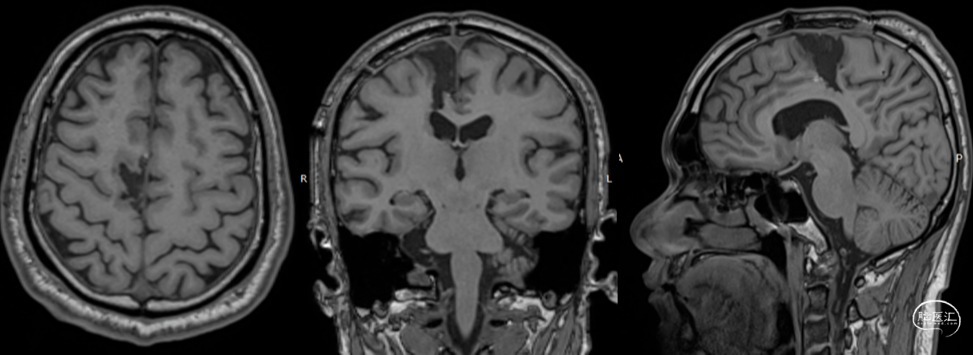
图9.术后MRI:提示右侧SMA、旁中央前沟完整切除。术后左下肢功能短期障碍。术后脑电图复查未见癫痫放电。
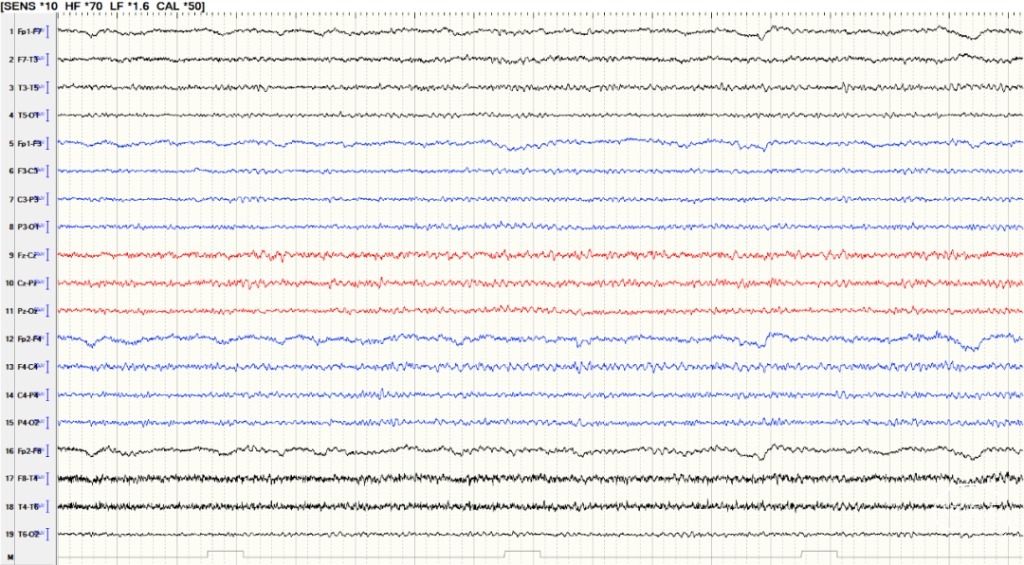
图10.术后复查脑电图:右侧半球中线区缺损节律,未见癫痫样放电。
患者在全麻下完成了右侧SMA及旁中央小叶前部的病灶切除术,术中按照术前计划完成了病灶的切除,术后麻醉清醒后对侧肢体偏瘫,远端肢体肌力0级,术后三周肌力完全恢复,术后一年无癫痫发作。
该患者,男性,45岁,23岁起病,病程二十余年,术前每天活动及憋小便均可诱发1-2次发作,每次均有导致突发性跌倒,惯常发作表现为:腰部无力→躯干及左侧下肢阵挛,持续20秒,发作过程意识清。术前头皮脑电图可见右侧旁中线的癫痫样放电,磁共振为阴性,PET-CT右侧旁中央前沟、SMA低代谢,经过SEEG证实癫痫灶位于右侧SMA。传统的观念认为旁中央小叶为下肢运动皮层,切除后会导致永久性的功能障碍。该区域位于中央区的内侧面,表面有粗大的矢状窦阻挡视野,中央区往往还有粗的引流静脉,手术视野的暴露相当困难。我们术前运用3D脑模型把要切除的范围和中央区、引流静脉的关系搞得清清楚楚,术中我们知道如何翻开硬脑膜、保护引流静脉,在最小的牵拉情况下做到清晰的暴露,手术切除过程中我们按照3D脑沟回的形态逐个脑回切除,术中不会迷失方向,切除的深度严格遵照仅仅切除灰质,不损伤白质纤维的原则切除。SMA切除患者都会有一过性对侧肢体偏瘫,一般不超过4周就可以完全恢复。这个部位如果术中用清醒麻醉也给不了我们太多的帮助,切除到一大部分时候患者对侧肢体已经瘫痪,这个时候我们要切除的区域尚未完全切除,我们停下来病灶未完全切除,术后可能癫痫发作。只有术前做好完备的手术计划,充分暴露、术中严格按照计划执行。
该患者术后病理为术后病理为神经元呈缺血性改变伴胶质增生,可能和我们取材过小有关系,临床上根据患者的代谢特征(沿着一个脑沟的低代谢),考虑FCD的可能性比较大。


























