美国费城德拉克斯勒大学医学院的Sujay Rajkumar等分析nSRS用于BM的最新研究结果以及基本原理。结果发表于2022年11月的《Journal of Neuro-Oncology》在线。
——摘自文章章节
【Ref: Rajkumar S, et al. J Neurooncol. 2022 Dec;160(3):691-705. doi: 10.1007/s11060-022-04190-6. Epub 2022 Nov 14.】
研究背景
约20-40%的癌症发生脑转移(brain metastases,BM)。对颅内转移灶数量少、病灶较大、症状明显或有诊断必要的患者手术切除BM是重要治疗选择。然而,仅通过手术,术后1-2年肿瘤在原转移瘤腔内复发,局部复发率(LR)的可能性高达50%。在最大限度的安全切除后,术后辅助放疗可显著降低LR的风险并改善预后。在过去十几年中,立体定向放射外科(SRS)针对瘤床的照射超过传统的全脑放射治疗(WBRT)或SRS加WBRT联合治疗。2017年的一项随机Ⅲ期试验表明,与单一针对瘤床放疗相比,SRS的局部控制效果更好;另一项试验显示,与WBRT相比,SRS不仅保存认知功能,同时有相似的生存率(OS)。随着神经放射学成像技术的发展和系统性疾病疗效改善,OS得以延长,认知保护尤显重要,因此临床指南推荐SRS而非WBRT。
然而对BM手术切除和SRS治疗的患者,还存在软脑膜播散(LMD)和放射性坏死(RN)等风险。荟萃分析表明,开颅手术(或术后放疗)后LMD发生率的中位风险值为16.1%,辅助SRS后的LMD发生率高达28%和35%。研究认为,LMD继发于切除过程中肿瘤溢出,特别是病灶分块切除患者风险更大,可能带来严重的不良后果。单中心研究显示,结节性LMD确诊后,其死亡率达72%。另外,放射性坏死在脑转移治疗后一年发生率为24%,近半数患者出现神经系统症状。
术前SRS或称新的辅助SRS(neoadjuvant stereotactic radiosurgery,nSRS)已经用于肉瘤、直肠癌、食管癌和胰腺癌的治疗,但nSRS在BM治疗的风险和效果需要评估。美国费城德拉克斯勒大学医学院的Sujay Rajkumar等分析nSRS用于BM的最新研究结果以及基本原理。结果发表于2022年11月的《Journal of Neuro-Oncology》在线。
研究方法
作者使用系统评估和荟萃分析PRISMA报告法,在PubMed检索2017年1月至2022年8月期间与BM及nSRS相关的文献,所用医学术语为“立体定向放射外科”、“伽玛刀”或“分级立体定向放射外科”、“术前”或“新的辅助”和“脑转移瘤”。收集回顾性综述、原始研究、病例报告和临床试验等数据,以提供该主题的系统综述。
研究结果
研究结果有以下几方面:
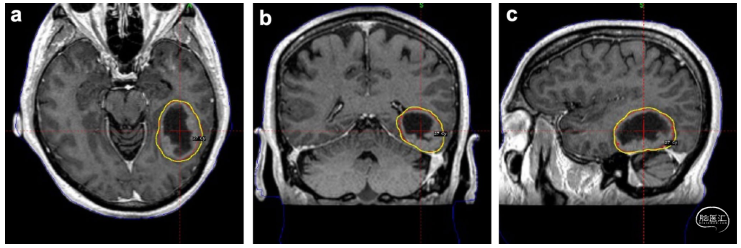
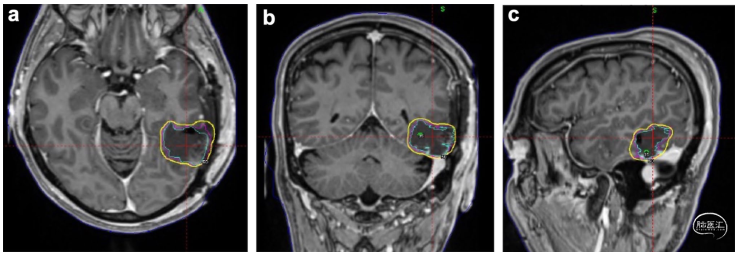
图2. MRI冠状位a、横位b和矢状位c的T1后对比图像。左颞叶术后腔(蓝色),增加1mm边缘(粉红色)和模拟伽玛刀平面(黄色;27Gy/3份)。该患者在肿瘤手术切除前接受nSRS治疗。
研究结论
综上所述,nSRS是一种新兴的放射外科策略,可以降低脑转移术后LMD的发生,也有可能减轻RN。但nSRS仍存在某些局限性,限制在所有需要手术切除的体积大的转移瘤或症状性脑转移患者的应用。作者建议进行前瞻性研究确定nSRS的作用。

声明:脑医汇旗下神外资讯、神介资讯、神内资讯、脑医咨询、AiBrain 所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。






