供稿 | 严贵忠 兰大二院
排版 | AiBrain 编辑团队
与酒精、海洛因和可卡因相比,我们似乎很少看到尼古丁过量服用的现象;而且,尼古丁似乎是唯一一种观察到在啮齿类动物中会引起厌恶的药物,这表明其具有非常独特且强烈的厌恶效应,这也可能解释了为什么我们很少看到过量使用尼古丁的现象。
尼古丁也会引起成瘾,一个主要假设是,尼古丁“劫持”了大脑中的自然奖赏过程。然而,科学家们发现,尼古丁对行为的影响是剂量依赖的:尼古丁在低剂量时是有益的,而在高剂量时才会产生强烈的厌恶感。
此外,尼古丁的厌恶效应可以与愉悦效应同时产生(Sartor等人,2010),对高剂量的耐受性也会随着时间的推移而发展(Heishman和Henningfield, 2000),这表明对尼古丁的厌恶可能与尼古丁奖励不同。
最近的研究指出,缰核-脚间轴及其向脑干背侧被盖的投射在尼古丁的反感行为中起着关键作用;相反,尼古丁和其他滥用药物的奖励及强化作用涉及腹侧被盖区(VTA)的多巴胺能(DA)神经元,后者在伏隔核(NAc)释放DA。
然而,VTA-DA神经元并不是一个单一的整体。由解剖位置和投射靶点确定的亚群具有不同的特性和功能:典型的奖赏预测错误编码DA神经元位于外侧VTA (lVTA),并将投射于NAc的外侧,而内侧VTA-DA神经元会投射至NAc的腹内侧核,并在预测厌恶刺激的线索和遇到厌恶刺激时释放DA。
那么,调节奖赏和厌恶情绪的多巴胺环路是否构成尼古丁剂量依赖效应的基础?
加州大学分子与细胞生物学系和海伦威尔斯神经科学研究所Stephan Lammel团队对尼古丁剂量依赖性的神经环路进行了研究,结果在2022年8月2日发表在了《Neuron》杂志上。
尼古丁通过尼古丁乙酰胆碱受体(nAChRs)作用于DA神经元;实验和建模研究表明,含β2和α7亚基的nAChRs的激活可介导该过程,其中β2主要表达于VTA-DA神经元,从而增加放电率,而α7则参与兴奋性输入,负责爆发放电和突触可塑性。
然而,尼古丁也会使nAChRs脱敏,使它们暂时失去活性,从而阻止乙酰胆碱受体的进一步激活。
重要的是,VTA α7和β2亚基的破坏可以改变对VTA内注入低浓度尼古丁的厌恶和奖励相关行为的反应。
然而,研究nAChRs和尼古丁相关行为的大部分工作都集中在低剂量的增强作用上,因此对高剂量的系统性尼古丁作用于nAChRs以调节DA细胞活性和释放知之甚少。
首先研究人员通过静脉置管的方式给药,避免因皮下或腹腔注射对尼古丁急性厌恶反应的干扰;给药不同剂量后观察小鼠对条件位置的偏好;结果发现,接受低剂量尼古丁的小鼠确实更偏好停留在与尼古丁配对的房间,而接受高剂量尼古丁的小鼠确实在尼古丁配对的房间停留的时间更短,表明对该环境的厌恶。
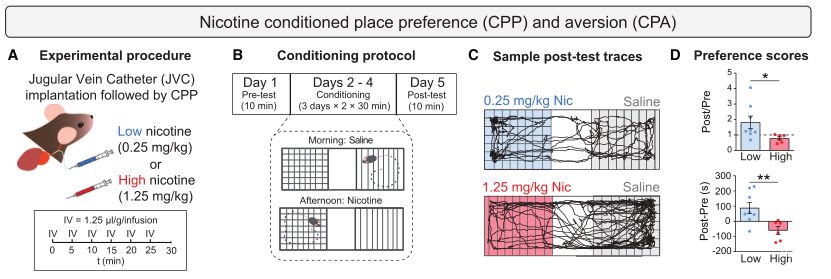
为了解释这种剂量依赖性的不同行为过程,研究人员借助光纤技术,记录不同剂量尼古丁对VTA-DA细胞活动的影响。
结果发现,每次注射奖赏剂量的尼古丁都能持续激活VTA-DA细胞;而首次注射高剂量的尼古丁会激活VTA-DA细胞,而随后的注射会抑制细胞活性。
通过计算VTA-DA细胞活性的平均反应来揭示奖赏或厌恶尼古丁的净效应。结果显示,奖励剂量的尼古丁显著能够激活VTA-DA细胞,但注射厌恶剂量的尼古丁可引起双相反应:其中抑制性早期成分(Early component, EC)持续15s,兴奋性晚期成分(Late Component, LC)会持续15-60s。
研究人员提出假说,认为尼古丁可能是通过a4b2Rs对VTA-DA细胞的作用呈现出低剂量奖赏激活和高剂量首次输注后脱敏。
通过使用对含β2亚基的nAChRs具有选择性的受体拮抗剂(DHBE)进行验证,该团队发现DHBE降低了VTA-DA细胞对厌恶剂量尼古丁的反应,显著降低了首次注射引起的激活;支持了在尼古丁暴露过程中,α4β2Rs的持续脱敏状态可能是抑制VTA-DA细胞对厌恶尼古丁反应的关键。
随后,该团队将检测DA释放的dLight1.2注入NAcMed和NAcLat中,考察注射厌恶剂量尼古丁后DA的释放。结果表明,抑制EC出现在NAcLat中,而在LC期间NAcMed中可以观察到DA释放的显著增加,这证实了VTA-DA细胞体信号的双相活性可以通过投射不同的靶点分离。
值得注意的是,DA在NAcMed中释放的增加主要发生在a4b2Rs脱敏之前,首次注射厌恶剂量尼古丁后;而DA在NAcLat中释放的减少则发生在首次注射a4b2R脱敏之后。在另一个实验中,证实了NAcLat减少DA释放的行为相关性;光遗传沉默NAcLat中VTA-DA末端足以促进实时位置厌恶,这表明抑制DA在NAcLat中的释放是促进高剂量尼古丁厌恶的重要因素。
接下来,作者发现EC期间,α7介导的VTA-DA神经元在尼古丁厌恶过程中抑制DA的释放是必需的。
虽然a4b2和a7受体都参与尼古丁的奖赏和强化,但它们在药效学和解剖学表达上具有独特的特征,每次注射厌恶剂量的尼古丁都能激活a7Rs,并在首次注射中迅速脱敏大部分a4b2Rs。
结果表明,厌恶剂量的尼古丁剂量,显著激活了VTA-GABA神经元。脑干背外侧被盖核(LDT)是VTA-DA神经元的主要兴奋性输入,同时还包含GABA能细胞群。
利用荧光原位杂交、膜片钳及在体光遗传学技术,作者发现LDT-GABA神经元通过a7R介导,抑制VTA-DA神经元从而编码尼古丁厌恶。
总的来说,厌恶剂量的尼古丁对不同NAc亚区DA释放模式具有不同的作用;尼古丁的剂量依赖效应与a4b2和a7 nAChRs有关;厌恶剂量的尼古丁通过a7受体减少外侧NAc中DA的释放;LDT-GABA细胞介导了厌恶剂量尼古丁对DA释放和行为的影响。
加州大学伯克利分校分子与细胞生物学系和海伦威尔斯神经科学研究所Christine Liu和Amanda J. Tose为共同第一作者,Stephan Lammel为通讯作者。
该研究得到美国国立卫生研究院(1R01DA042889),烟草相关疾病研究计划(26IP-0035),One Mind基金会(047483),NARSAD青年研究者奖(23543),大脑研究基金会(BRFSG2015-7)的资助。
文章链接:
https://linkinghub.elsevier.com/retrieve/pii/S0896-6273(22)00608-0
参考文献(上下滑动查看):
✦往期精彩回顾✦


声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、AiBrain所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。