
撰稿 | Mancy 复旦大学
排版 | AiBrain 编辑团队
人类的大脑具有区别于其他物种的独特特征。尽管近年来许多研究对小鼠和人类发育中的大脑细胞组成进行了详细的描述,但由于难以获得大脑区域化最早期阶段的组织,以及缺乏可以系统地操纵基因功能的方法,研究控制人类大脑发育的机制一直是一个难题。
来自于瑞士巴塞尔联邦理工学院的Barbara Treutlein教授团队通过对人脑类器官进行单细胞转录组、染色质可及性分析,阐述了大脑区域特异性的调控机制。
随后,通过对多组学数据和转录因子结合位点的预测,推测人脑类器官发育的全基因调控网络。
文中以转录因子GLI3为例,阐释了GLI3在端脑的背腹侧分化命运决定中的作用。
本研究为利用人脑类器官模型和单细胞技术重建人类发育生物学提供新方向。相关研究成果以Inferring and perturbing cell fate regulomes in human brain organoids为题,于近日发表于Nature。


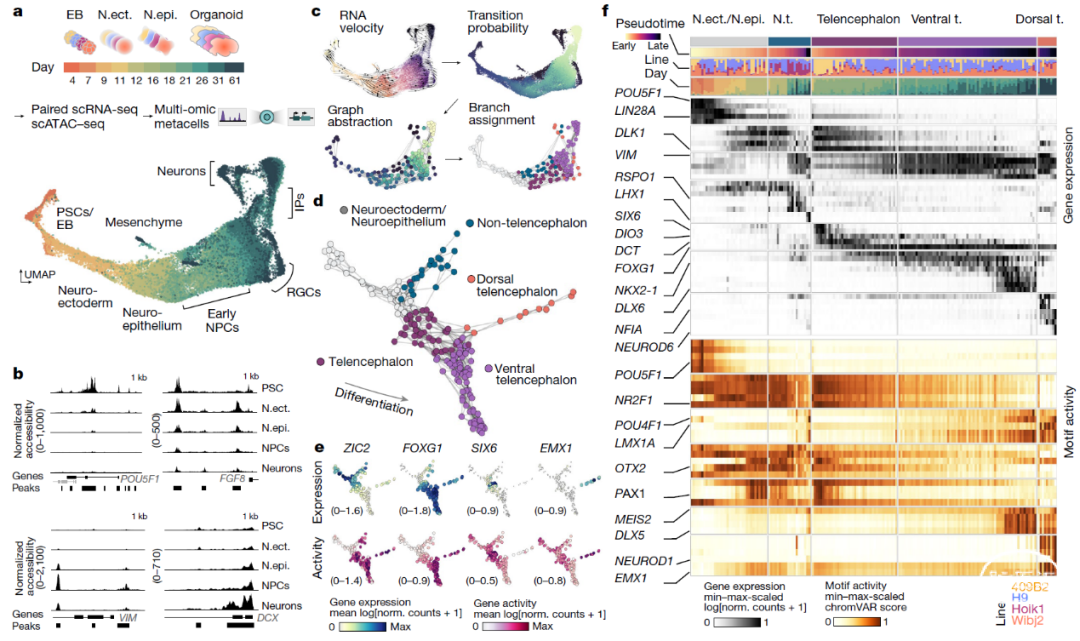
为了研究人类大脑发育的机制,作者将不同的多能干细胞(3种iPS和2种ES细胞系)诱导分化形成人脑类器官,收集整个诱导分化过程中11个不同时间点的样品进行单细胞转录组(scRNA-seq)和单细胞可及染色质(scATAC-seq)分析(Fig.1a),识别出处于不同细胞状态的标记基因以及基因调控区域(Fig.1b)。
基于转录和调控的动态信息检测神经发生、分化轨迹,揭示了大脑发育过程中基因表达的区域特异性、染色质可及性和阶段特异性的结合转录因子(Fig.1c-f)。

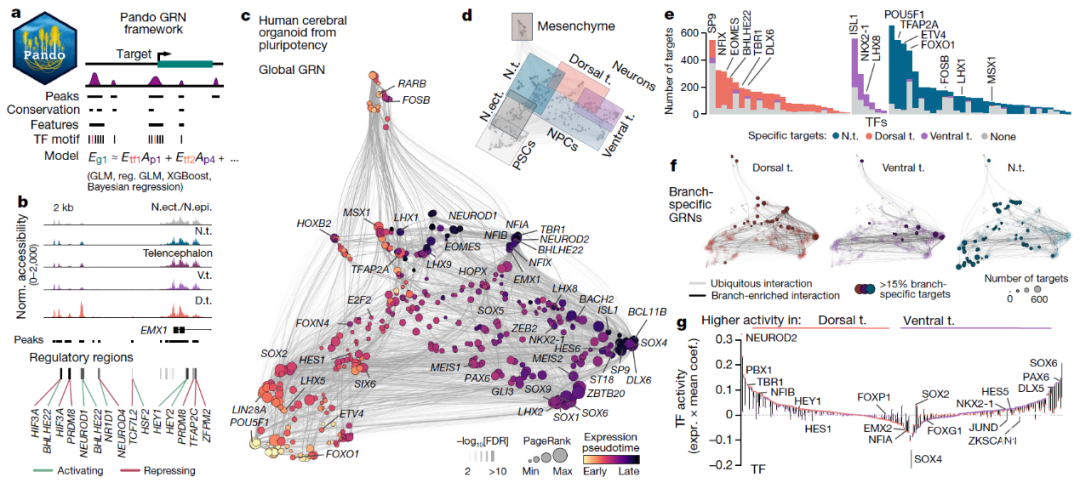
为了进一步预测人脑类器官发育的基因调控网络(GRN),作者开发了一种名为“Pando”的算法(Fig.2a),该算法利用回归模型来推断出每个转录因子(TF)的正向调控或负向调控靶基因(基因模块)以及调控基因组区域(调控模块)(Fig.2b)。
通过UMAP分析对GRN进行可视化,揭示了大脑器官发育的不同阶段(多能干细胞→神经上皮细胞→神经前体细胞→神经元)中细胞状态转变的时间顺序(Fig.2c-d)。
同时GRN结果表明调控区域可及性和TF表达随着类器官发育阶段而变化,并在大脑区域化过程中分离(Fig.2e-g)。

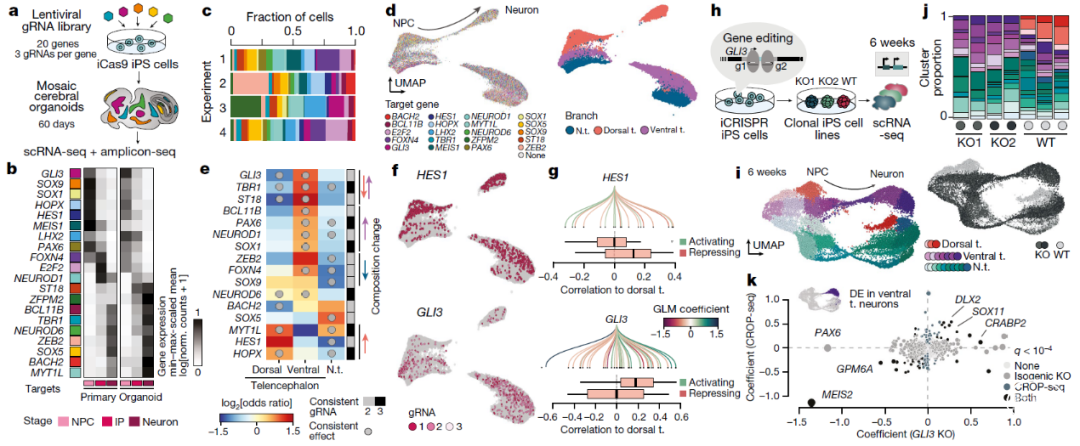
为了探讨在人类大脑发育过程中调节细胞命运和状态的机制,作者利用靶向20个IF的gRNA慢病毒库,在类脑器官不同发育阶段敲除转录因子(Fig.3a-c),检测gRNA与细胞类型丰度和细胞类型内差异基因表达的关联。
研究发现靶向8种TF的gRNAs在腹侧端脑表现出一致的富集,而在包括皮层在内的其他区域则表现出相应的缺失,例如GLI3基因;另一组TF干扰出现相反的效果,TF靶向gRNAs在皮层中富集,而在腹侧端脑或非端脑中缺失,如HES1基因(Fig.3e-f)。
为进一步探究GLI3参与决定细胞命运及其潜在机制,作者使用CRISPR-Cas9技术构建GLI3敲除(KO)iPS细胞(Fig.3h)。
发现GLI3 KO细胞在端脑背侧减少,而在端脑腹侧富集增加(Fig.3j),差异基因表达分析显示GLI3 KO影响端脑腹侧细胞状态(Fig.3k)。
这些数据证明转录因子GLI3在人类皮层神经元命运决定中极其重要,GLI3缺失影响腹侧端脑的发育。
综上,作者通过整合单细胞转录组、染色质可及性和遗传学干扰手段,揭示调控人类大脑区域特异性的相关机制。并提出转录因子GLI3在调控啮齿动物端脑的背腹侧命运中的作用。
本研究亦证明多区域特异化的人脑类器官可以作为探究人类大脑发育的预测模型系统。

PMID: 36198796
DOI: 10.1038/s41586-022-05279-8
AiBrain内容团队为大家整理了文章的pdf,如有需要,请公众号后台留言“pdf”或扫码添加AiBrain助手微信获取。

✦往期精彩回顾✦


声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、AiBrain所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。