| AiBrain内容团队编辑

古人“辟谷”,就是希望通过间歇性禁食的方式恢复身体机能,达到养生的效果。以往研究发现,间歇性禁食确实有诸多好处:激活代谢相关的基因转录、蛋白质合成、线粒体代谢及神经营养因子的释放;这些过程也可能参与轴突再生,但其中的神经机制目前还不清楚。
一
研究概述
2022年6月22日,《Nature》在线发表了伦敦帝国理工学院Simone Di Giovanni研究团队的一项研究成果,他们发现间歇性禁食能够促进肠道菌群产生吲哚-3-丙酸(IPA),并通过产生免疫反应,促进轴突再生和功能恢复。

研究人员首先通过粉碎小鼠的坐骨神经(从脊柱向下延伸到腿部的最长神经),建立了轴突损伤模型。随后,将小鼠分为两组,间歇性禁食组(尽可能地吃东西,然后隔天不吃东西)和自由饮食组(可以不受限制地自由进食)。研究人员发现,仅仅10天的间歇性断食就能够有效促进轴突再生。
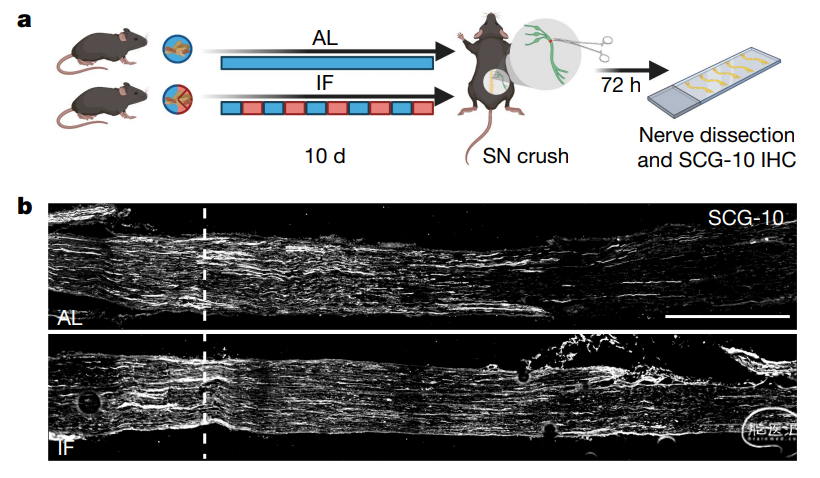
图1 间歇性禁食(IF)促进轴突再生
由于间隙性禁食可能会影响到细胞代谢,研究人员对间歇性禁食小鼠的代谢物进行了分析,发现饮食限制会导致小鼠的血液中富集更高水平的吲哚类代谢物。
随后通过粪便微生物群移植实验,发现单纯将间歇性禁食小鼠的菌群移植于自由进食组的小鼠,也能显著促进自由进食组小鼠的神经再生;后续又进一步通过抗生素干预,清除肠道细菌,发现梭状芽孢杆菌及其产生的IPA是促进轴突再生的重要因素。
更重要的是,当给坐骨神经损伤后的小鼠灌胃服用IPA10天后,即可观察到受损神经再生和恢复的增加;而在轴突损伤后给予2-3周的IPA干预,能够显著改善表皮神经支配,从而促进感觉功能恢复。这些结果共同表明,肠道细菌产生IPA具有促进神经再生和功能恢复的能力。
那么,代谢产物是如何促进神经再生的呢?
研究人员通过RNA测序发现,IPA不直接增加受损轴突部位的中性粒细胞,而是选择性地增加了背根神经节中的中性粒细胞数量;并通过CXCR2趋化因子被激活和吸引,随后募集下游信号通路释放干扰素γ,产生免疫反应,从而促进轴突的再生和功能恢复。
综上,这项研究结果再次证明了肠—脑轴的重要作用及作用机制:肠道微生物分泌的代谢物如IPA,能够通过免疫介导的机制促进感觉轴突的再生和功能恢复。
二
作者自述
Professor
Simone Di Giovanni
就职于英国伦敦帝国理工学院医学院脑科学系,是再生修复神经科学学会主席、英国NHS(国家医疗服务体系)神经病学顾问
专注于控制轴突出芽和再生的分子信号传导
研究小组指出,产生IPA的细菌——梭状芽孢杆菌,在人类和小鼠的肠道中都自然存在,而IPA也存在于人类的血液中。因此在小鼠中发现的这一机制,可能也会适用于将来的临床试验。
Simone Di Giovanni教授说:“目前,除了手术修复之外,没有任何治疗神经损伤的方法。而手术修复只在一小部分病例中有效,这促使我们探索是否能够通过改变生活方式促进恢复。此前有研究组将间歇性禁食与伤口修复以及神经元的新生联系在一起,但我们的研究首次解释了禁食如何有助于轴突再生及功能恢复。我认为它的意义在于打开了一个全新的领域,我们不得不思考:这只是冰山一角吗?是否其他细菌或细菌代谢物也可以促进修复?”
“我们现在的目标之一是系统地研究细菌代谢物治疗的作用。目前,尚未充分探索的一个问题是,由于IPA在血液中以高浓度持续四到六个小时,因此全天反复给药或将其添加到正常饮食中,是否有助于将治疗效果最优化?总之,我们还需要开展更多研究,以考察人在禁食后IPA 是否增加,以及IPA和间歇性禁食作为临床潜在治疗方法的疗效。”
三
同行评述
注:以下内容根据peer review file整理而成
Referee #1:
总而言之,这是一项非常有趣的研究。并且作为原创研究,发现微生物来源的IPA是一种促进DRG轴突再生的代谢产物,同时揭示了一种新的机制——即肠道-神经系统相互作用可以改善创伤性PNS损伤后的神经再生,这是令人兴奋的。此外,研究提供的数据质量高,令人信服。
Referee #2:
Serger等人假设了一个非常新颖有趣的机制,即间歇性禁食改变小鼠的微生物群,从而增加肠道细菌产生的代谢物吲哚-3-丙酸(IPA)。本研究为轴突的驱动机制提供了证据。
在行为学测试中,周围神经损伤和功能恢复后的增强再生效应大小让我怀疑这项工作是否能够向临床推广。此外,有大量关于脊髓损伤后禁食的影响的文献,这些文献确定了该方法在促进轴突生长和功能恢复方面的局限性(Plunet et al. Exp Neurol 2008)。
事实上,在目前的研究中,禁食对再生的影响程度也有显著的限制:每隔一天禁食一次,在损伤部位3500微米或4000微米处,或在相对较小的损伤模型(横切轴突但基底板完整,不能反映人类损伤类型)中,轴突再生的程度没有显著差异。这意味着作者发现的机制虽然有趣,但却是定义初级感觉神经元再生能力的一个次要过程。这也意味着,如前所述,这项研究的临床转化潜能恐怕是有限的。
Referee #3:
虽然这项研究的结果可能很有趣,但关于这些发现的机制和医学转化还有一些主要问题。所有的实验都涉及伤前治疗方案,这使得临床转化的可能性不明确。此外,本文报道的轴突再生和功能恢复的程度相当有限。因此,当受伤后使用这些治疗方法时,测试它们是否仍然有用是至关重要的。
并且特别需要注意的是,如果潜在的机制真的是作者声称的提高DRG中性粒细胞浸润的机制,这可能是任何类型的临床治疗的主要担忧。
Referee #4:
这项研究是全面的,令人印象深刻,有很多值得喜欢的地方。作者提供了许多证据来支持IPA在间歇性禁食诱导的轴突再生中的作用。此外,目前微生物组学在分子机制研究方面的应用明显不足,而这里所采取的方法将引起广泛的关注,其应用成果将代表着一个重要的进步,并有可能带动更多的这方面研究。
AiBrain内容团队为大家整理了文章及审稿意见的pdf,如有需要,请公众号后台留言“pdf”或扫码添加AiBrain助手微信获取。
参考资料:
1.https://doi.org/10.1038/s41586-022-04884-x
2.https://static-content.springer.com/esm/art%3A10.1038%2Fs41586-022-04884-x/MediaObjects/41586_2022_4884_MOESM2_ESM.pdf
✦往期精彩回顾✦


声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、AiBrain所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。








