[REF: Li Z, Qin Z, Kong X, et al. CCL14 exacerbates intraplaque vulnerability by promoting neovascularization in the human carotid plaque [published online ahead of print, 2022 Aug 13]. J Stroke Cerebrovasc Dis. 2022;31(10):106670. doi:10.1016/j.jstrokecerebrovasdis.2022.106670] PMID: 35973397
摘 要
介 绍
材料和方法
实验人体组织
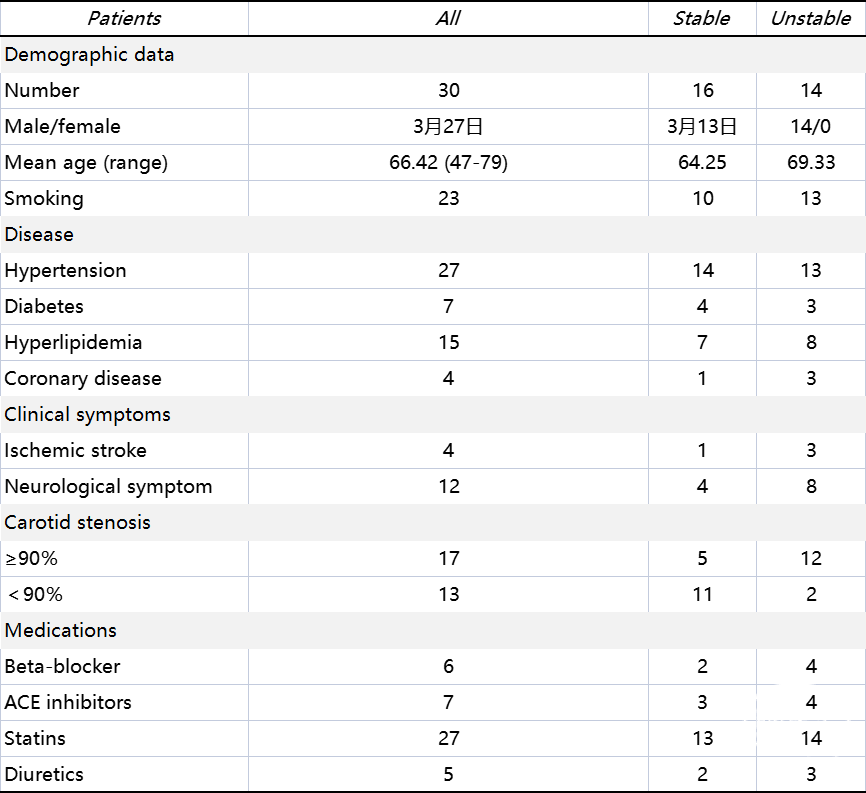
Table 1. Patients’ demographics and clinicopathological data
免疫组织化学(IHC)
细胞培养
CCL14和VEGF-A的调控
HUVEC成小管实验
Western blot(WB)
两组收集于临床的人体斑块组织,添加RIPA细胞裂解缓冲液提取总蛋白,用bicinchoninic acid(BCA)试剂盒对比标准浓度进行蛋白浓度测定,用12% SDS-PAGE对蛋白质进行分离,使蛋白转移到PVDF膜上,随后用5%的脱脂牛奶封闭一小时,然后孵一抗摇床上一小时后-4℃过夜,第二天室温复温后用酶标二抗孵育2小时,随后采用化学发光法显影,采用Image J对图像进行灰度分析。内参蛋白为GAPDH。
统计学分析
结 果
颈动脉斑块的易损指数计算
获得各组分图像后,用Image J软件计算平均光密度值的方法测算出两组颈动脉斑块中脂质、巨噬细胞、胶原纤维、平滑肌细胞的面积百分比,并根据公式:

Table 2. Vulnerability index for the vulnerable and stable groups

Vulnerability index presented as mean±SD
人颈动脉斑块中CCL14、JAK2、STAT3和VEGF-A的表达增加
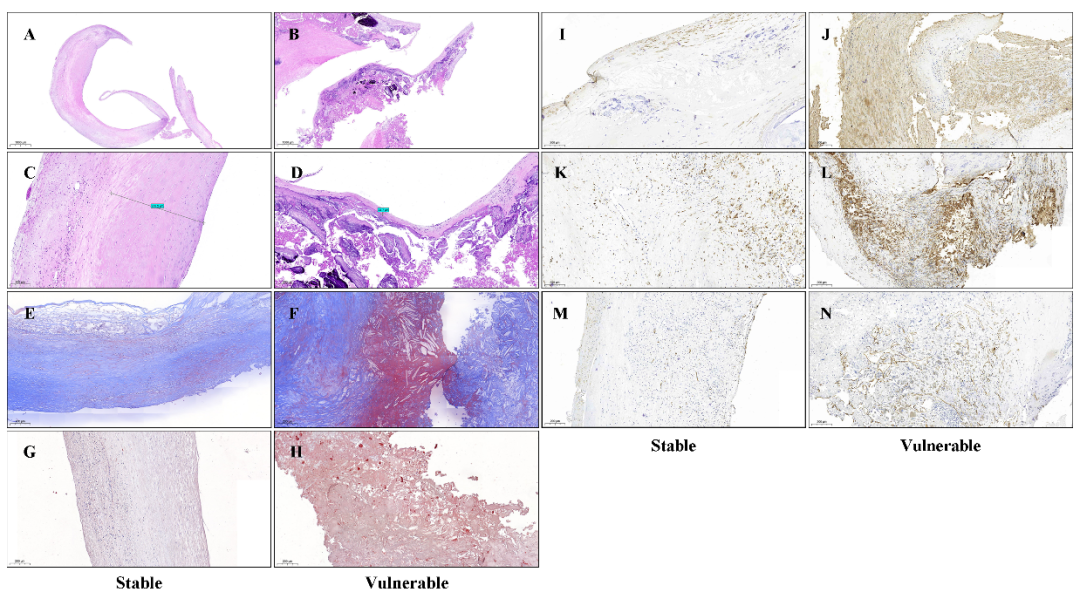
我们首先对两组人颈动脉动脉标本进行了切片分析,免疫组织化学染色(IHC)显示易损斑块组中的CCL14、JAK2、STAT3、VEGF-A蛋白水平较之稳定斑块组有明显增高(Fig.2A)。随后,为了验证颈动脉斑块组织中的相关蛋白表达量,我们又进行了Western blot(WB)实验分析,结果显示易损组的JAK2/STAT3,P-JAK2/P-STAT3的蛋白水平明显高于稳定组,同样的CCL14与VEGF-A的蛋白表达量也较稳定组升高(Fig.2B-C),与IHC结果大抵相同。值得注意的是,这些蛋白表达水平的差异与两组颈动脉斑块组织的狭窄程度并没有直接联系。根据以上的蛋白变化,我们猜测,CCL14可能通过JAK2/STAT3通路调控VEGF-A的表达,本阶段实验只是为了验证斑块组织中的蛋白表达差异,为之后的体外模型的构建做出了论据。

Fig 2. Differential expression of each protein in stable and vulnerable carotid plaques.Under IHC, the expression of CCL14, JAK2/STAT3, P-JAK2/P-STAT3, and VEGF-A was higher in vulnerable plaques than in stable plaques (A). These proteins were detected by Western blotting, and the expression levels were higher in the carotid vulnerable plaque group than in the stable plaque group (B), and the internal reference protein was GAPDH, followed by statistical comparison using Image J to calculate the grayscale values of each protein (C). These measures are expressed as mean ± SD, and P < 0.05 is statistically significant. Two-tailed 's t-test was used to compare the data between the two groups. * P<0.05,**P<0.01,***P<0.001,S: Stable;V:Vulnerable.
CCL14促进了HUVEC的成管效应
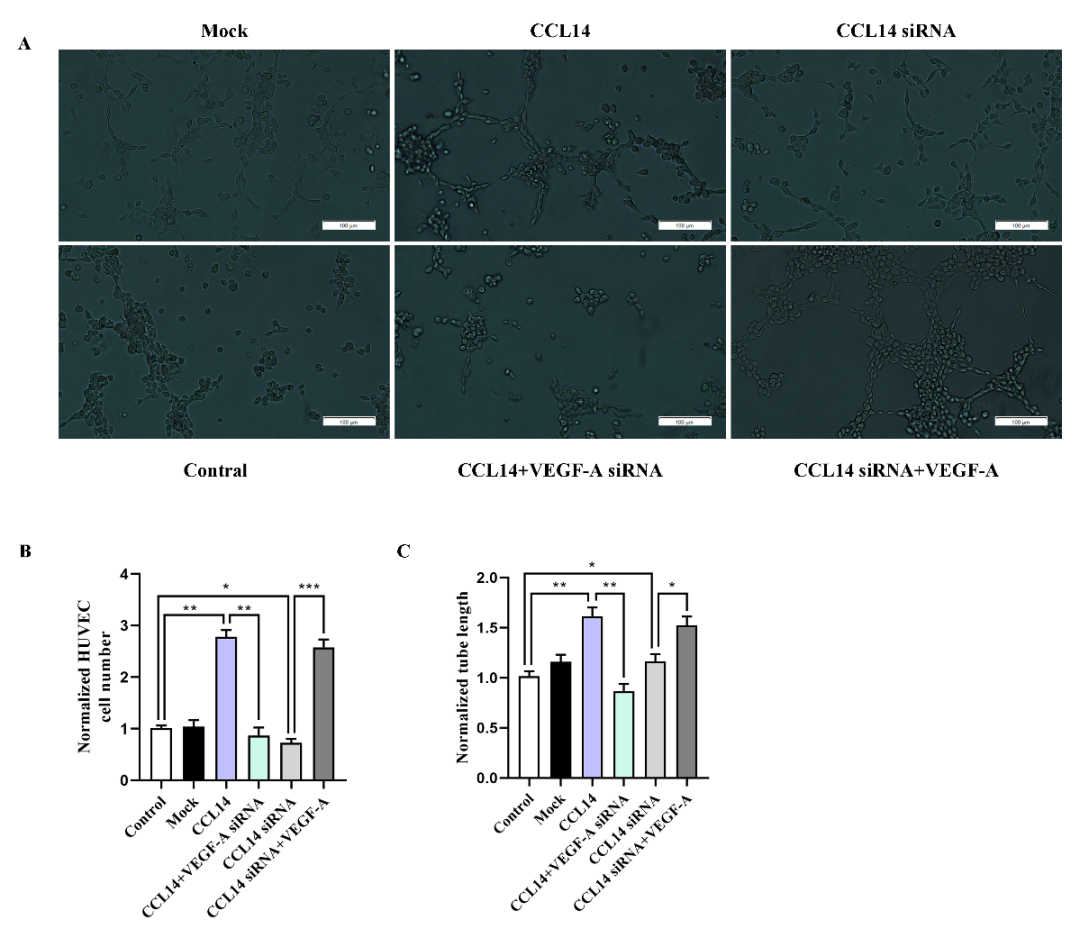
我们首先进行了脐静脉内皮细胞(HUVEC)的成管实验,以此探讨CCL14能否促进血管内皮细胞的血管生成,并和VEGF-A产生一定的关联。HUVEC的成管实验是为了研究HUVEC在细胞外基质凝胶培养基上形成类似毛细血管样的微血管管状结构的能力。我们使用携带CCL14和CCL14 siRNA的慢病毒去感染HUVEC,在培养基(CM)孵育完成后,在光学显微镜下观测脐静脉内皮细胞的成管情况(Fig.3A),并且统计所形成小管的数量(Fig.3B)和长度(Fig.3C)。以前的研究已经证实VEGF-A对HUVEC有较强的成管实验作用,所以我们又创建了CCL14+VEGF-A siRNA培养基和CCL14 siRNA+VEGF-A培养基,同时,为了进行对照,我们加入了空白组对照(Control)和空载慢病毒组(MOCK)。结果显示,过表达CCL14组的HUVEC的成管数量和长度明显高于Control组和Mock组。相反CCL14敲除组的HUVEC相比Control组和Mock组,生成的小管数量更少,长度更短。对于VEGF-A对CCL14的影响而言,我们发现,VEGF-A siRNA可以在一定程度上抵消掉CCL14的促进HUVEC的成管实验的作用,而在CCL14 siRNA 培养基中加入VEGF-A则会抵消掉CCL14 siRNA的抑制血管成管实验的作用,我们猜测,VEGF-A可能作为CCL14的下游蛋白而存在。
CCL14通过JAK2/STAT3信号通路轴调控VEGF-A的表达
既往研究表明JAK2/STAT3通路可以通过调控VEGF-A在血管生成中发挥重要作用。为了进一步研究JAK2/STAT3在CCL14促进HUVEC血管生成过程中所扮演的角色,我们检测了JAK2和磷酸化JAK2、STAT3和磷酸化STAT3、VEGF-A的蛋白水平。我们单独提取了CCL14组和CCL14 siRNA组培养基的蛋白,通过Western blot分析各蛋白的表达。我们发现,与CCL14组相比,敲除CCL14后可以显著降低CCL14蛋白的表达水平和JAK2蛋白的磷酸化水平,进而降低STAT3蛋白的磷酸化水平,最终使VEGF-A的表达水平降低(Fig.4A、C)。接下来我们又把CCL14组分为两个实验组,分别加入VEGF-A和VEGF-A siRNA,通过Western blotting实验分析,VEGF-A siRNA处理仅仅降低了VEGF-A的表达,但并没有影响信号通路上游的CCL14、JAK2和STAT3的表达(Fig.4B、D)。值得注意的是,虽然敲除CCL14可以降低JAK2和STAT3蛋白的磷酸化水平,但我们并没有发现总蛋白水平的表达变化。这些结果表明,CCL14可以通过激活JAK2的磷酸化从而调控VEGF-A的表达。

Fig 4. CCL14 down-regulates VEGF-A protein expression through the JAK2/STAT3 signaling pathway. Total proteins were extracted by transfection of HUVEC with CCL14 and CCL14 siRNA lentivirus, respectively, and the expression of each protein was analyzed using Western blotting technique. CCL14 knockdown significantly decreased the phosphorylation of JAK2 and STAT3 proteins and the protein expression of VEGF-A (A, C). In the medium of CCL14 group, VEGF-A and VEGF-A siRNA lentivirus were transfected separately, and total protein was extracted to detect the expression of each protein, and it was found that knockdown of VEGF-A did not affect the regulation of JAK2/STAT pathway axis by CCL14 (B, D). Two-tailed 's t-test was used to compare the data of the two groups, * P<0.05, **P<0.01.
讨 论
颈动脉粥样硬化是一种复杂的、长期的病理过程,是老年男性常见的血管疾病。而作为中国最高致死疾病脑血管病的关键病因,颈动脉斑块治疗显得尤为重要。在临床对颈动脉斑块的传统的可行治疗只有手术一种方式,对于手术指征也是根据影像学检查来判断颈动脉血管的狭窄度来制定的。然而,手术治疗并不适用于那些并没有临床症状的病人,并且也没有特效药去及早的治疗,所以寻找一种创新性的,有效的治疗方式显得尤为重要。
我们首先比较了Gene Expression Omnibus数据库(GSE125771),通过全基因组芯片技术筛选出在颈动脉易损斑块中显著上调的CCL14,以了解颈动脉易损斑块样本的差异性基因表达。随后,我们在KEGG通路分析中发现,CCL14作为一个上游蛋白,可以对JAK2发挥一些调节作用。以前的研究表明,JAK2-STAT3信号通路在心血管疾病(如动脉粥样硬化)中也起着重要作用。多种生理和病理过程中,VEGF-A都是关键的促进血管生成的因子之一,而VEGF-A在动脉粥样硬化疾病的产生和进展中,都扮演着促进内皮细胞再生,血管生成等重要角色,并且在多种疾病中,VEGF-A都作为JAK2/STAT3信号通路的下游调控信号发挥着作用。但令人惊讶的是,尚未有CCL14与JAK2/STAT3之间联系的详细报道。
在本研究中,我们首先用临床颈动脉斑块标本通过计算各组斑块的易损指数进行了易损性分组,并通过IHC在显微镜下直观观测了各组分含量对比,并通过Western blot技术验证了CCL14,P-JAK2、P-STAT3和VEGF在颈动脉易损斑块组中高表达,证实了CCL14在颈动脉斑块易损性进展中的作用,对我们的猜测奠定了理论基础。为了验证CCL14对JAK2/STAT3的调控作用,随后我们进行了HUVEC培养这一体外实验,通过对HUVEC的培养,观测它的细胞间的成管的长度和数量来验证CCL14对其产生的一系列作用。在之前的研究证实了,JAK2/STAT3通过VEGF-A对HUVEC的成管实验的起到明显的促进作用。我们通过慢病毒转染的方式对CCL14和VEGF-A进行过表达或者敲除,以此进行分组,我们发现CCL14可以激活JAK2的磷酸化,进而通过JAK2/STAT3信号通路轴正性调控VEGF-A的表达,而CCL14敲除后可以明显抑制VEGF-A的表达。值得注意的是,在添加CCL14后,单独敲除VEGF-A虽然会使HUVEC的成管效应被抑制,但并不影响CCL14对JAK2/STAT3的调控。与以前的研究一致,CCL14可以显著促进JAK2的磷酸化,从而通过JAK2/STAT3信号通路调控VEGF-A的表达。
结
论
斑块内出血(IPH)被认为是可能改变动脉粥样硬化生物学和自然史的重要特征,是脑血管事件的有力预测因素,许多研究表明,斑块内新生血管与IPH和斑块的易损性密切相关。如果在临床实践中正确实施IPH的早期识别和预防,预计将对缺血性卒中的一级和二级预防更加有效。我们的实验可能通过深入研究IPH的潜在机制,为IPH的病理生理学提供新的见解,并为后续IPH的发生机制提供线索。随着对颈动脉易损斑块研究的逐步深入,CCL14对新生血管这一调控机制或许会对颈动脉斑块的非手术治疗提供一种新的思路。
通讯作者简介
栗世方 教授
青岛大学附属医院
医学博士,主任医师,教授,硕士研究生导师
青岛大学附属医院神经外科副主任、市南院区神经外科病区主任
山东省医学会神经外科分会委员、山东省医师协会脊髓脊柱分会副主任委员、山东省脑血管病防治委员会常务委员,青岛市医学会神经外科分会副主任委员,国家自然科学基金委员会评审专家
从事神经外科临床工作20余年,擅长颈动脉狭窄、颅内动脉瘤等脑血管病的外科治疗,迄今完成颈动脉内膜切除术近400例;对脑膜瘤、胶质瘤、垂体腺瘤等颅内肿瘤具有丰富的治疗经验
作为第一作者或通讯作者,在国际期刊和中华医学杂志、中华神经外科杂志等学术期刊发表论文40余篇;先后主持国家自然科学基金、国家863计划子课题、山东省自然科学基金及青岛市重大研究攻关课题等多项;2013年被评为青岛市优秀青年临床专家,2015、2019年度青岛市专业技术拔尖人才
万芪 教授
青岛大学神经再生与康复研究院
首席教授,博士生导师,国家海外杰青
青岛大学神经再生与康复研究院院长,青岛大学医学部常务副部长
长期从事脑疾病(如:脑卒中)发生机制及治疗的研究,在脑损伤保护、干细胞再生与修复、神经递质受体功能、学习与记忆分子机制等研究方向上做出了一系列贡献。在Nature、Nature Medicine、Nature Neuroscience、Trends in Neuroscience、PNAS、Stem Cells、Stroke等期刊发表SCI论文80余篇,单篇论文引用率高达400余次
首创干细胞仪器治疗新策略,研制了一种促内源性神经干细胞脑卒中治疗仪,并形成可穿戴治疗+预警+物联网一体化产品。基于团队原创发现进行脑卒中创新药物设计,合成了全新脑卒中治疗先导化合物和脑保护小肽。申请并获得多项国家发明专利
担任国家自然科学基金会“优青”医学组二审组长、国家自然科学基金会“神经科学组”二审组长。担任“国家重点研发计划干细胞及转化研究专项”“教育部科技奖”“工信部人工智能产业创新重点任务揭榜项目”“华夏医学科技奖”终审评委专家。担任“中国医疗保健国际交流促进会”常务理事、“中国国际神经外科协会”学术委员、“中国研究型医院学会”生物治疗专业委员会委员。应邀作为多个国际期刊及基金会的评审专家







