
32.1 引言
关于多发性脑转移瘤患者的现代治疗有很多争议。大多数脑转移瘤患者会有多发肿瘤。在标准的磁共振成像(MRI)扫描中,估计80%的转移瘤患者会有一个以上的肿瘤,一半会有三个或三个以上的肿瘤。关于多发性脑转移瘤的治疗,最受争议的问题之一是,是否可以或应该对立体定向放射外科(SRS)治疗转移瘤的数目作出限制。十年前,一项对放射肿瘤科医生的调查显示,只有不到5%的放射肿瘤科医生会选择将5个以上的转移瘤作为他们初始放射外科治疗的最大脑转移瘤数量目。在一次国际放射外科会议上,一项类似的调查显示,尽管超过一半的人将SRS作为≥5个脑转移瘤的初始治疗,但没有明确的共识。从那时起,放射外科临床医生越来越愿意单独使用SRS治疗数目多的脑转移瘤。
多年来,脑转移瘤的治疗均采用全脑放疗(WBRT)。近100年前,WBRT被认为能够缓解有症状的脑转移瘤。1931年,《外科年鉴(Annals of Surgery)》刊登了一系列尸检报告,报告对因各种广泛转移性癌症接受治疗的患者的发现,其中包括3例脑转移瘤患者的描述,他们在WBRT后存活了1-1.5年。到1954年,纪念斯隆-凯特琳癌症中心发表了一篇文章,描述了全脑放疗的剂量分割方案是如何通过确定治疗方案来改善症状,同时避免由于千伏电压放射治疗提供的非常高的表面剂量导致的头皮湿脱皮(the moist desquamation of the scalp )。
在过去的50年里,WBRT从早期放疗肿瘤组(RTOG)分割研究中使用的平行对映入口,发展到现在被许多人认为是标准的回避海马技术。NRG肿瘤学NRG CC001是一项III期前瞻性随机研究,显示回避海马全脑放疗(HA-WBRT)比标准WBRT更有利于神经认知,显示治疗后不同时间点执行功能、学习和记忆的恶化更少。然而,即使试验中使用的调强放疗(IMRT)使海马保留程度有所提高,但仍存在一定程度的功能退化,而SRS治疗增加了海马保留程度,有可能改善这一结果。然而,SRS治疗多少个病变是合适的,这个问题仍然没有答案。
数十年来,SRS一直用于脑转移瘤的治疗,可向肿瘤提供靶向治疗剂量的照射,同时避免对正常组织进行不必要的照射。肿瘤临床试验联盟NCCTG 0574和欧洲癌症研究和治疗组织(EORTC) 22952-26001试验均显示,在有≦3个脑转移瘤的患者中,单独SRS比SRS联合WBRT的认知退化更少,生活质量更好。在伽玛刀SRS治疗早期,由于多种原因,使用SRS治疗转移瘤的上限为3或4个肿瘤。从实际的角度来看,计划病例和提供治疗所需的时间是一个主要障碍。此外,尚不清楚治疗超过4个转移瘤的毒性,不使用WBRT会对生存产生不利影响。此外,该地区的第一个随机试验随机选择了2-4个肿瘤作为纳入标准。
在20世纪90年代,Yamamoto等人提出了一个独特的经验,用伽玛刀SRS分别治疗了36个和37个肺癌脑转移瘤的患者。在SRS治疗后,患者有临床和影像学反应,生存时间分别为4.5和5.5个月。随后发表的针对4个以上转移瘤的机构经验表明,没有发现明显的毒性,经验表明使用SRS不会影响生存率(见表32.1)。匹兹堡大学的一项研究通过对中位5个转移瘤患者的脑转移瘤分级RTOG递归分区分析(RPA)进行评估,表明在选择SRS治疗的患者中,生存率比历史上使用WBRT缩获得的生存率更好。重要的是,影响生存率的不是转移瘤的数目,而是肿瘤的总体积。来自日本的一项大型病例匹配分析显示,虽然有5个或5个以上转移瘤的患者的总体生存期比有1-4个转移瘤的患者稍差(7个月vs . 7个月),但与SRS治疗相关毒性在两组中是相同的。
表32.1选择的SRS治疗数目较多的转移瘤患者的系列。
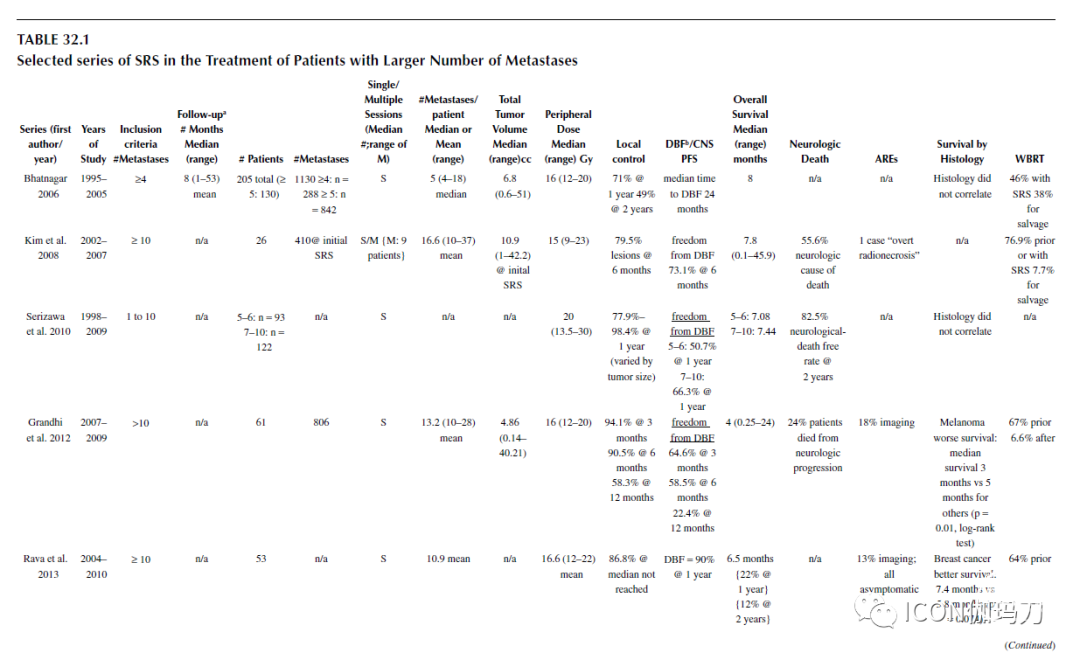
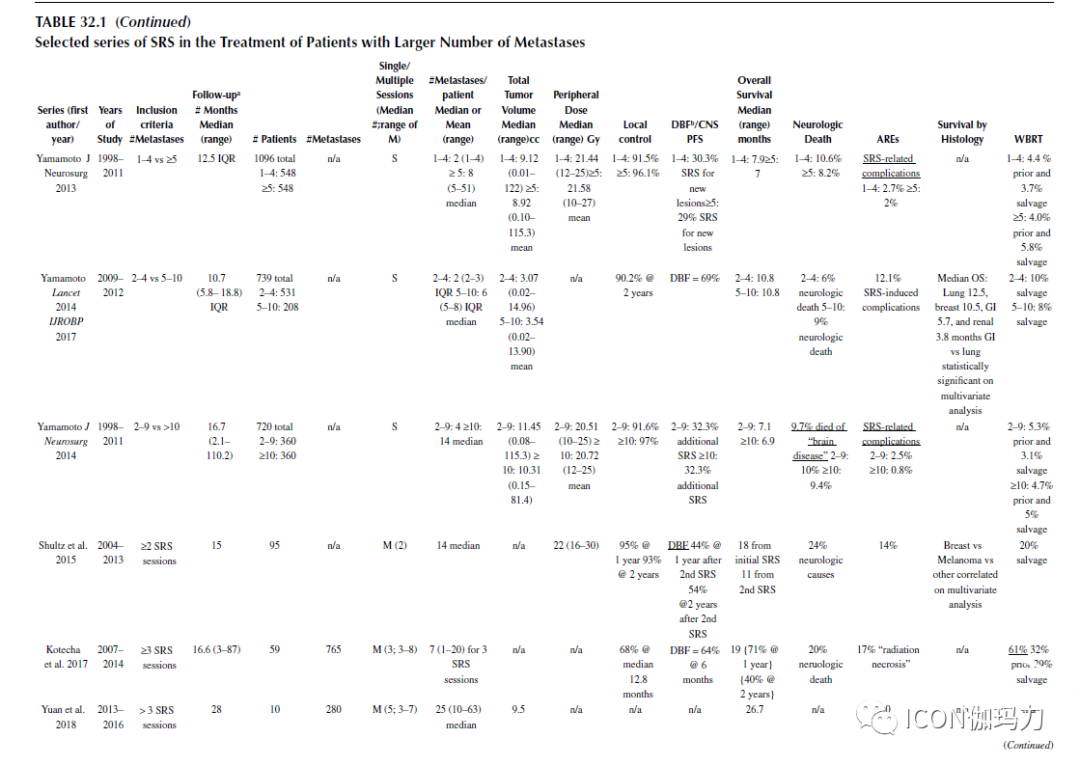
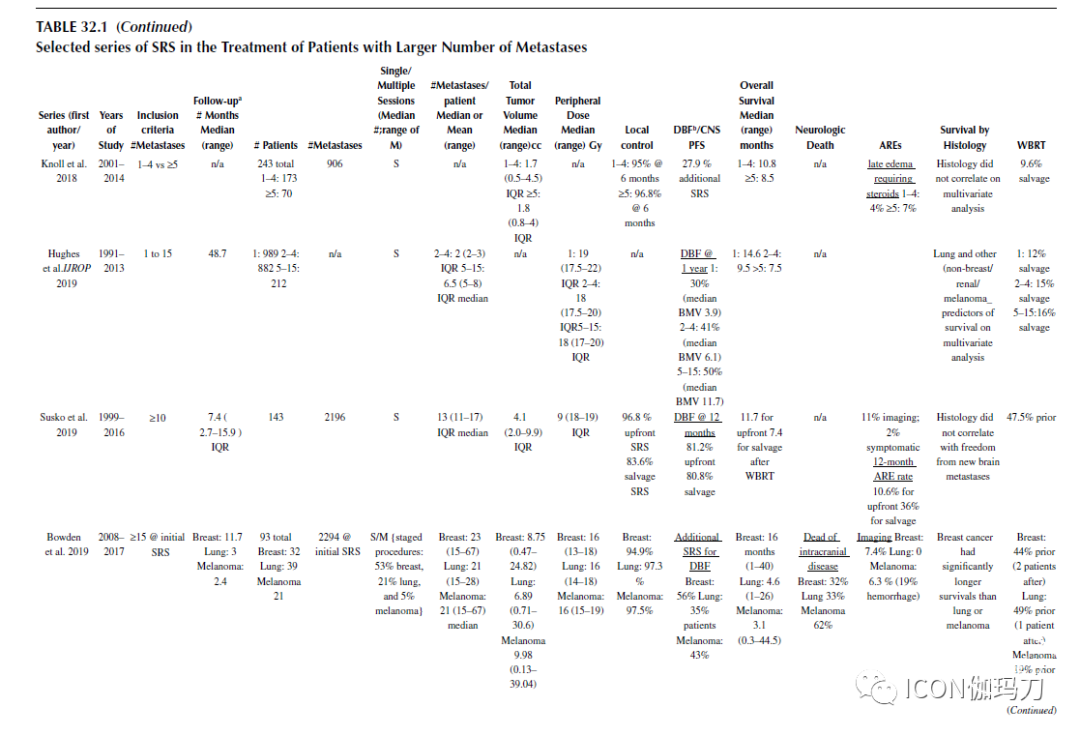
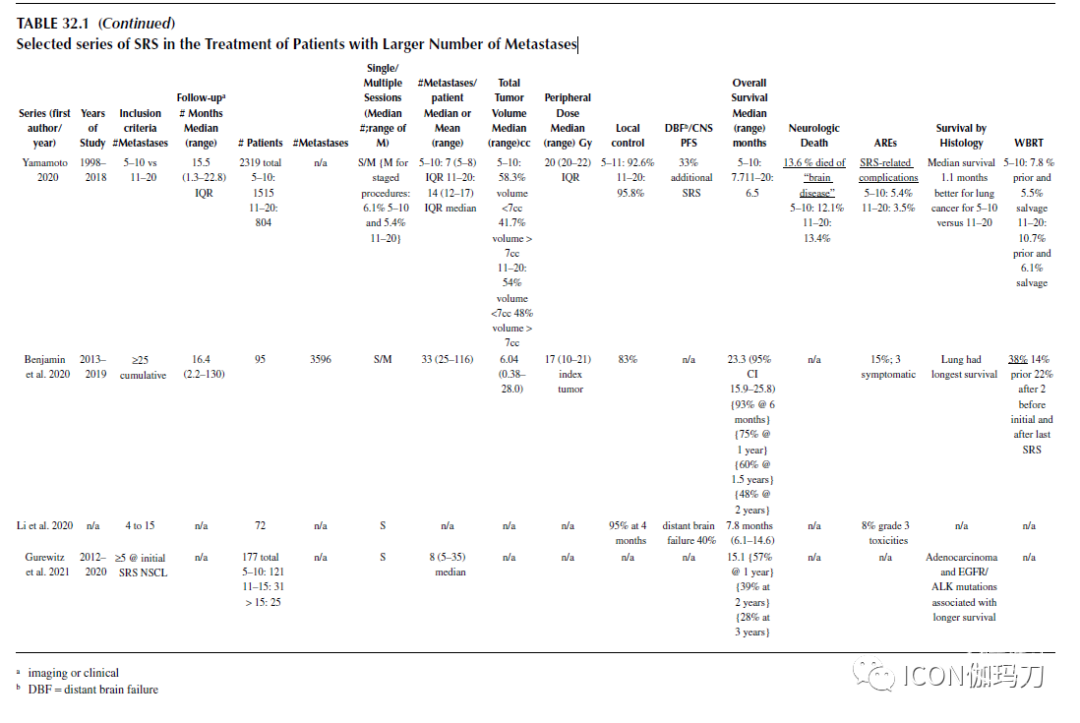
两个大型的多中心经验,一个来自日本,一个来自美国,进一步帮助解决了与治疗超过四个转移瘤相关的担忧。在这方面最有帮助的出版物是JLGK0901 (Yamamoto Lancet Oncol, 2014)的报告。这项前瞻性观察研究纳入了1000多例接受SRS治疗的患者,检查接受单独SRS治疗的有5-10个肿瘤的患者的生存期是否不低于有1-4个肿瘤患者的生存期。每组的中位生存期为10.8个月,重要的是,两组神经系统死亡的风险分别为6%和9%,没有统计学差异。根据2017年公布的数据,病变数目较多组的晚期并发症发生率为12%,与病变数目较少组的晚期并发症发生率相同。此外,转移瘤较多的患者在神经认知结果或脑白质改变的发展方面并没有更差的表现。事实上,12名在MRI上有脑白质病变证据的患者中有11人接受过WBRT。
在一项对美国大型多中心SRS患者数据库的回顾性研究中,有1-4个肿瘤组与有5个或5个以上肿瘤组之间没有生存差异。1-4个转移的患者中位生存期为10.8个月,而≥5个转移的患者中位生存期为8.5个月(p = 0.143)。与日本的经验相似,与SRS治疗相关的毒性分别为4%和7%,是可接受的。在匹兹堡的经验中,肿瘤的数目并不能预测生存;结果主要由运动状态和全身性疾病状态决定。
几年来,治疗多达10个转移性肿瘤的经验增加,包括来自国家综合癌症网络(NCCN)的指南都作出修改,以反映在这种情况下使用SRS的选择(NCCN 2020)。尽管缺乏随机数据,神经外科医生和放射肿瘤科医生越来越愿意单独使用SRS治疗有10个以上肿瘤的患者。几个因素的共同作用导致了这一结果,包括使治疗大量病变更有效的技术变化,以及上述III期试验的结果,该试验证实了WBRT与单独SRS相比的不良神经认知和生活质量(QOL)影响。这些进展与系统性治疗的重大进展相吻合,这些进展使患者活得更长,因此,人们对WBRT的晚期影响的担忧加剧了,这些影响可能在延长的生存期中表现出来。
32.2 生存
使用SRS治疗>10个肿瘤的数据来自单中心和多年前的小型研究系列。匹兹堡的一项回顾性研究观察了61例接受过单次伽玛刀放射外科治疗的患者,中位13个病灶。整个组的中位生存期为4个月,但在选定的亚组中,生存期较长。对于有<14个脑转移瘤,非黑色素瘤性原发灶,全身性疾病得到控制,中位生存期21.0个月。在另一个系列中,56例有≥10个转移瘤患者接受SRS治疗的中位生存期为6.5个月,与其他原发肿瘤患者生存期5.8个月相比,乳腺癌患者较好的生存期为7.4个月(p = 0.074) 。后来,来自日本的大量经验分析有10个或10个以上转移瘤的患者与有2 - 9个转移瘤的患者的生存期,两组之间的生存期没有差异,每组的中位生存期约为7个月。与转移瘤数目较少的患者相同,有≥10个转移瘤的患者神经系统死亡率(9.4%)和毒性(<1%)仍然处于可接受的低水平。
关于使用初始SRS治疗较大数目转移瘤的最大报告之一是一项对来自美国和加拿大8个大型学术性医学中心的2000多名患者的回顾性研究。Hughes等人报告了他们在Wake-Forest医院使用先期SRS治疗68例有5-15个转移瘤的经验(Hughes 2019)。在该患者队列中,中位生存期仅为4.7个月,神经系统死亡率高于病变较少的患者。在更大的多中心经验中,包括了212例有5-15个转移瘤的患者,与有2-4个转移瘤的患者相比,有5-15个转移瘤患者的死亡风险没有增加(p = 0.25),中位生存期分别为7.5个月和9.5个月。神经系统死亡率和毒性未见报道;分析了远处脑失效时的脑转移速度(BMV)。这显示了中位BMV的差异,6.1个相比11.7个新的转移瘤/年(p <0.01),但补救性WBRT率差异无统计学意义。有趣的是,在5-15个肿瘤队列中,有22例患者有11-15个病灶,在这个小群体中,中位生存期为10.5个月。
在治疗较大数目转移性肿瘤的最初报道中,原发性肿瘤的组织学并不一定与预后相关。然而,在过去的几年中,有更令人信服的证据表明组织学与生存率的关系。考虑到颅外疾病的状况对预后的影响以及新的全身疗法对颅外疾病的影响,这并不令人惊讶。匹兹堡大学的一项回顾性分析报告初始SRS治疗有≥15例脑转移瘤的患者根据肿瘤组织学的中位生存期。乳腺癌患者的中位生存期为16个月,肺癌患者的中位生存期为4.6个月,黑色素瘤患者的中位生存期为3.1个月。
根据我们在纽约大学的经验,生存率因组织而异。在我们的队列中,接受SRS治疗的累计转移灶数目≥25个的95例患者中,三分之二患有活动性颅外疾病。
肺、乳腺和黑色素瘤患者的中位生存期分别为33.3、23.3和15.9个月。此外,在原发性恶性肿瘤的类别中,与特定分子谱系相关的组织学亚型和可靶向突变已成为预后的重要决定因素。在过去的8年里,我们治疗了177例有≥5个脑转移并采用初始SRS治疗的非小细胞肺癌(NSCLC)患者。腺癌患者的中位总生存期明显长于非腺癌患者,分别为17.1个月和5.7个月(p<0.001)。表皮生长因子受体(EGFR)或间变性淋巴瘤激酶(ALK)突变患者的生存期分别为26.3个月和10.4个月,较未突变患者有统计学意义和临床意义上的延长(p = 0.008)。
32.3 剂量学
早期建模研究表明,SRS治疗25个脑转移瘤,保持每个转移瘤的最大点剂量<40Gy,会导致全脑剂量达到脑体积的50% (D50) <5Gy 。此外,模型显示,与肿瘤的实际数目相比,肿瘤总体积更能预测平均全脑剂量和全脑累积剂量。然而,平均全脑剂量与肿瘤总体积的确切关系可能并不总是可预测的,因为在肿瘤数目和/或肿瘤体积较大的情况下,处方边际剂量可能会减少,以试图降低放射副作用的风险。图32.1显示,当对多个治疗疗程的剂量进行汇总时,12Gy等剂量线可在较大比例的大脑区域重叠,潜在地增加副反应发生的可能性;在本例中,处方边缘剂量在随后的SRS疗程中减少。
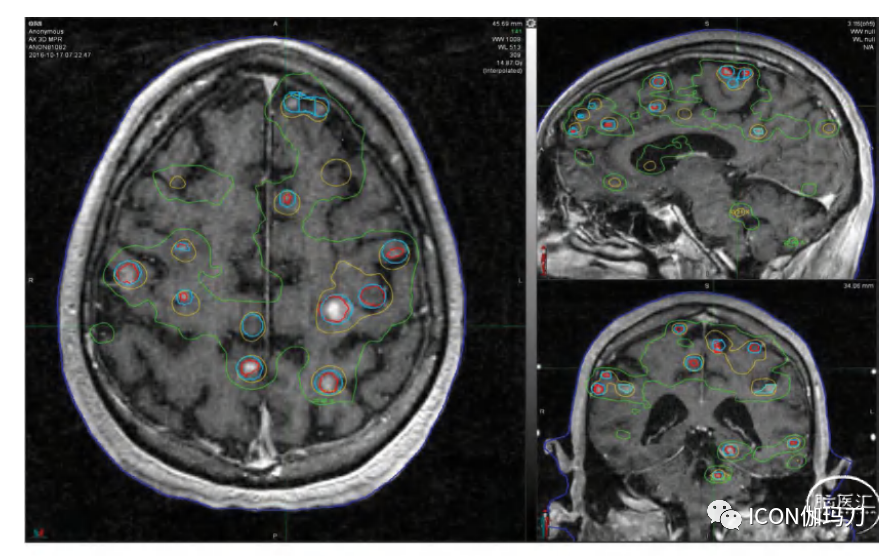
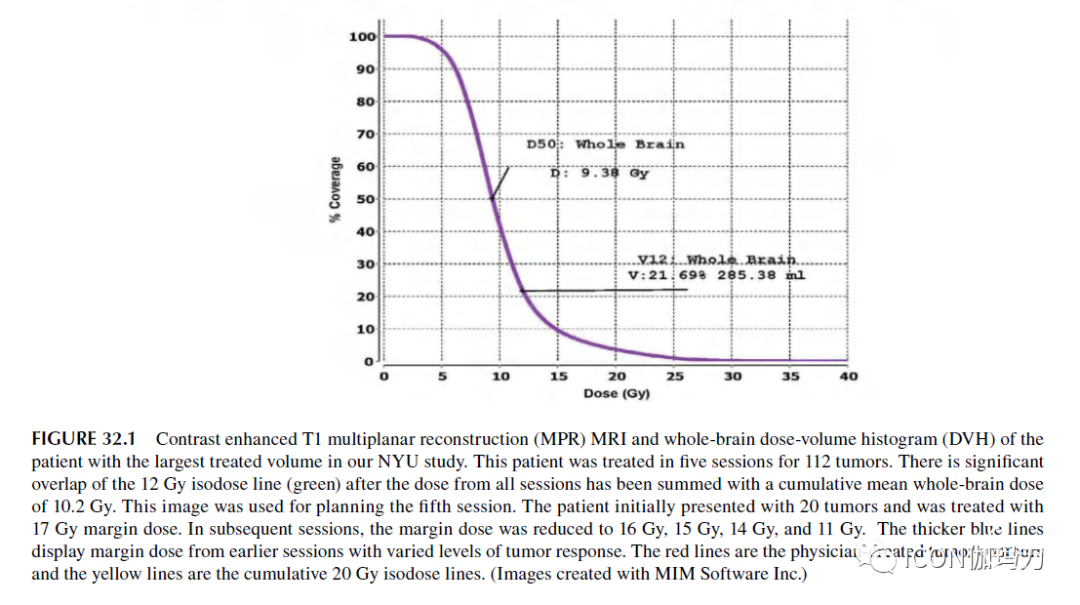
图32.1我们纽约大学(NYU)研究中治疗体积最大的患者的T1多平面重建(MPR) MRI和全脑剂量体积直方图(DVH)。该患者共接受了5次治疗,共治疗112个肿瘤。在将所有疗程的剂量与10.2Gy的累积平均全脑剂量相加后,12Gy等剂量线(绿色)有显著重叠。这个图像用于计划第五个疗程。患者最初出现20个肿瘤,并接受了17Gy边缘剂量的治疗。在随后的治疗中,边缘剂量降低到16Gy、15Gy、14Gy和11Gy。较粗的蓝线显示早期不同程度的肿瘤反应的边缘剂量。红线是医生绘制的肿瘤轮廓线,黄线是累积20 Gy等剂量线。
对接受大数目肿瘤治疗的患者的脑部剂量学进行评估的系列研究显示,相对较低的平均全脑剂量和相对较低的正常结构的受照剂量,尽管这些研究之间的比较有些困难,因为一些研究报告了在一个SRS疗程中治疗较大数目的肿瘤,而其他研究报告了随着时间的推移,连续SRS治疗的累积肿瘤数目和正常结构受照的累积剂量。然而,即使在转移瘤数目最多的研究系列中,平均全脑剂量通常也较低,如图32.2所示。NYU系列治疗的112个肿瘤的最大平均全脑剂量为10Gy。
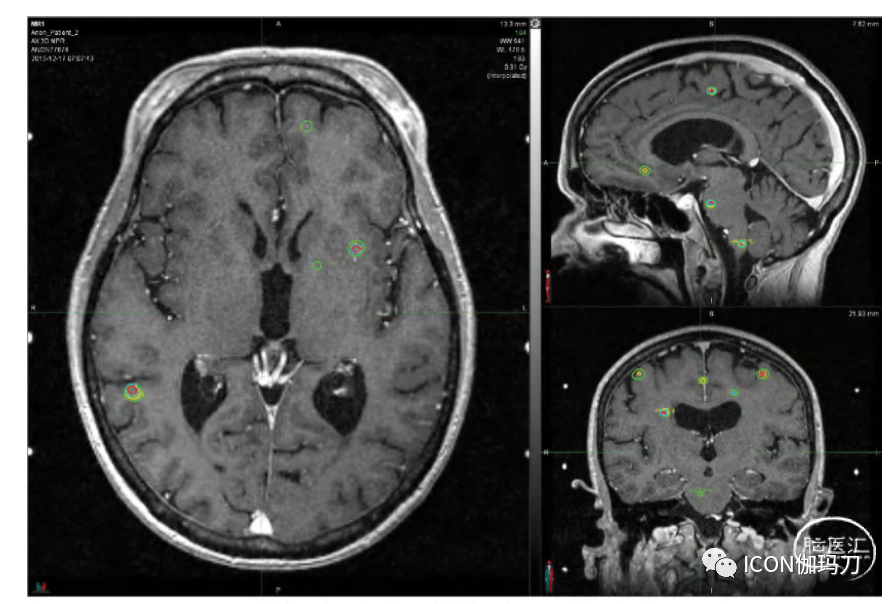
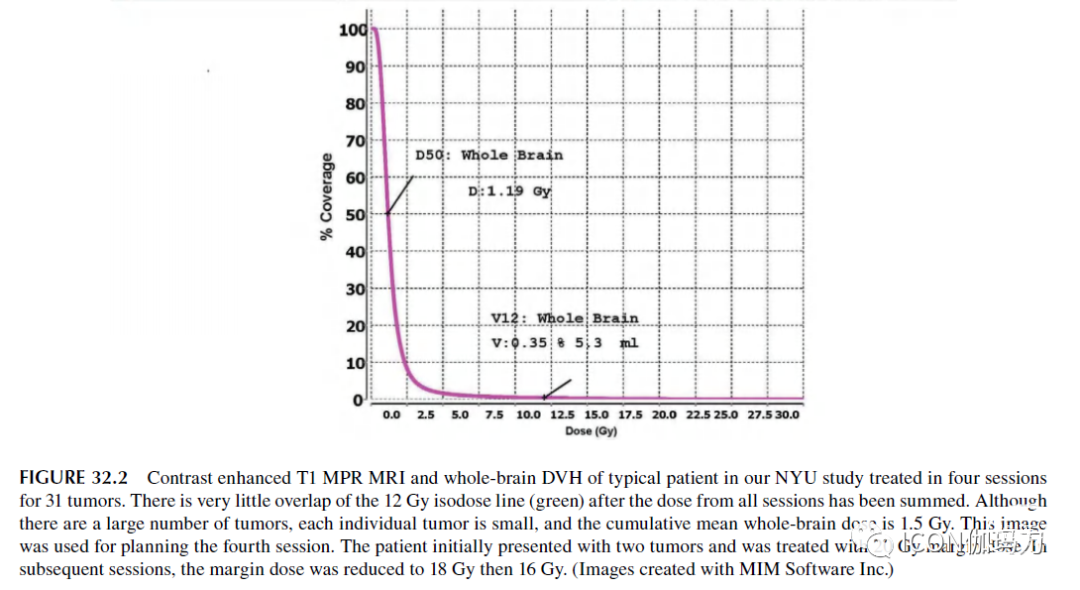
图32.2我们纽约大学(NYU)研究中典型患者的T1 MPR增强MRI和全脑DVH,4次疗程共治疗了31个肿瘤。在所有疗程的剂量相加后,12Gy等剂量线(绿色)的重叠很小。虽然肿瘤数目众多,但单个肿瘤体积较小,累积平均全脑剂量为1.5 Gy。该影像用于计划第四次疗程。患者最初出现两个肿瘤,接受20Gy边缘剂量的治疗。
Yamamato等人报道了对较大数目转移瘤患者进行的一些最早的剂量分析。80例有≥10个及10个以上脑转移瘤的患者,中位全脑累积剂量为4.71 Gy 。耶鲁大学对接受伽玛刀SRS治疗8个肿瘤(范围1-41)的患者进行的一系列剂量学评估显示,中位平均全脑剂量为1.4 Gy,作者报道称,有<25个肿瘤的患者接受治疗剂量没有>4Gy。转移瘤的总体数目和肿瘤的总体积与受照的平均全脑剂量相关。Bowden等人报告了42例接受单疗程伽玛刀SRS治疗≥15个转移瘤(中位20个)的患者的剂量。中位平均脑受照剂量为2.58 Gy,近80%的患者受照剂量<3Gy,是标准10次分割WBRT的每次分割通常所受照的剂量。值得注意的是,这与平均脑受照剂量和肿瘤体积有关,但与转移灶的数目无关。在16例继续接受额外SRS治疗的患者中,额外的照射脑部的平均剂量为1.4 Gy(范围为0.2-3.8 Gy)。
在照射全脑剂量方面,最具挑战性的问题之一是如何将非均匀分布的SRS剂量与标准分割全脑放疗过程中更均匀的剂量等同起来。用单次分割SRS治疗5例有>10个转移瘤的患者,评估正常结构受照的剂量,并与模式化的WBRT治疗的剂量进行比较,10次分割的剂量为30 Gy,并比较了生物效应剂量(BED)。在所有5例患者中,SRS治疗中的正常脑组织的平均BED为1.3%-34.3%,与其他系列病例一样,正常脑组织的平均受照剂量与肿瘤的总体积有关,而与治疗的肿瘤数目无关。
长期以来,12Gy受照体积一直是放射外科治疗动静脉畸形的重要体积参数。一些作者声称其与颅内肿瘤背景下,与SRS治疗后放射性坏死的相关性,注意到12gy体积>10 cm3 有症状性坏死的增加。在接受单次分割基于直线加速器放射外科治疗的≥4个转移瘤的小研究系列的患者中,较低的正常大脑受照>12 Gy的体积与生存增加相关。然而,在治疗较大数目转移瘤中,关于12Gy受照体积的重要性的数据不如AVM文献中的可靠,而且尚不清楚它与不同时间阶段多次SRS治疗的患者的累计12Gy受照体积之间的关系。在一研究系列>5个接受SRS治疗的转移瘤中,12 Gy的体积已被报道,Grandhi是第一个测量中位12 Gy体积为16.9 cm3的作者之一(Grandhi等2012)。一般来说,报告的12Gy容积在整个脑容积中所占比例很低。Bowden系列中,中位12 Gy体积为12.45 cm3,相当于<1%的脑容积 。然而,几乎没有相关数据表明该环境中12Gy剂量与毒性或神经认知结果之间的关系,对这种关系的描述有待进一步分析。
除了全脑剂量外,研究者还报道了其他关键颅内结构的受照剂量学(见表32.2)。在明尼苏达大学(University of Minnesota)的一系列研究中,Yuan等人确定了10例有中位25个转移瘤的患者,并计算了脑干、视神经结构、和海马以及大脑的累积剂量。脑干中位最大剂量(Dmax)为6.1 Gy,视交叉中位Dmax为3.9 Gy,左和右侧视神经中位Dmax分别为2.9 Gy和2.6 Gy。与其他研究系列一致,中位累积全脑平均剂量为4.1 Gy。在我们对纽约大学所治疗的有≥25个累积脑转移瘤的患者的剂量-体积分析中,受照≥12 Gy (V12)治疗的患者的中位累积全脑平均剂量和体积分别为4.07 Gy和37.46 cm3 。脑干的中位累积Dmax为22.19 Gy(1.79-58.83),视神经交叉的中位累积Dmax为4.85 Gy(1.38- 32.49),右侧视神经的中位累积Dmax为3.62 Gy(1.08 - 20.02),左侧视神经的中位累积Dmax为3.33 Gy(1.39-16.43)。这些剂量优于对相同结构进行10次分割30Gy姑息性WBRT治疗的剂量,中位随访期为19.4个月(2.2-79.4),未出现累及脑干或视神经结构的不良辐射事件。
表32.2SRS治疗数目多的脑转移瘤的剂量学数据。
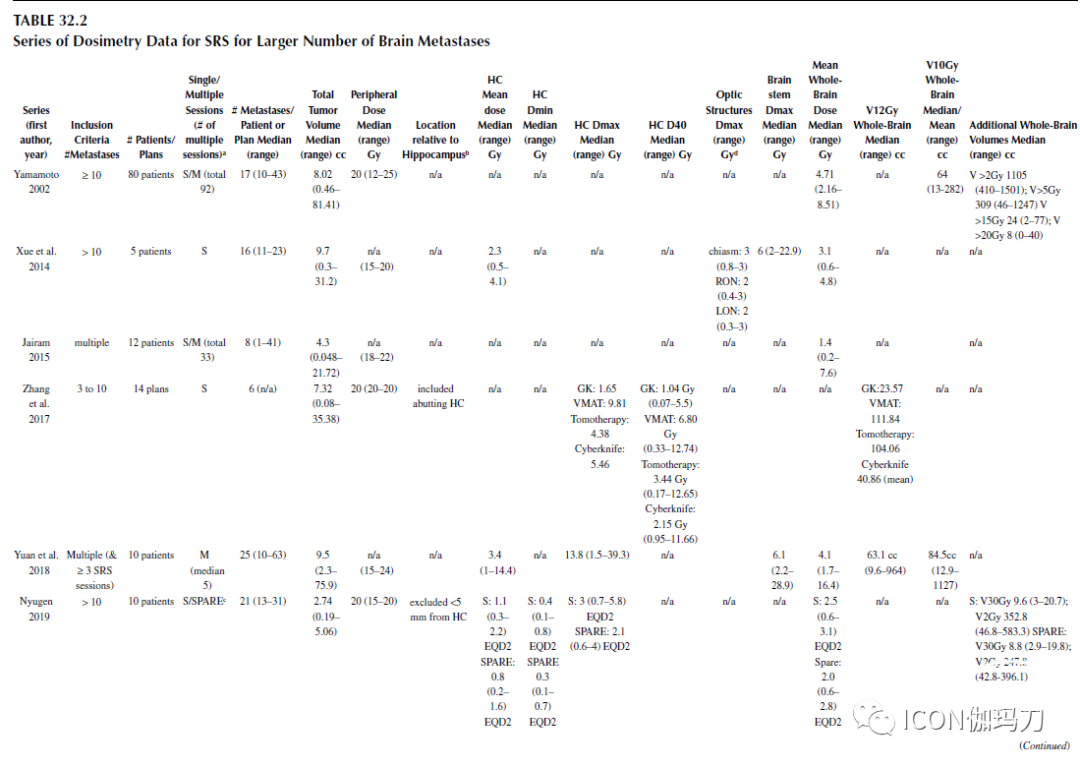
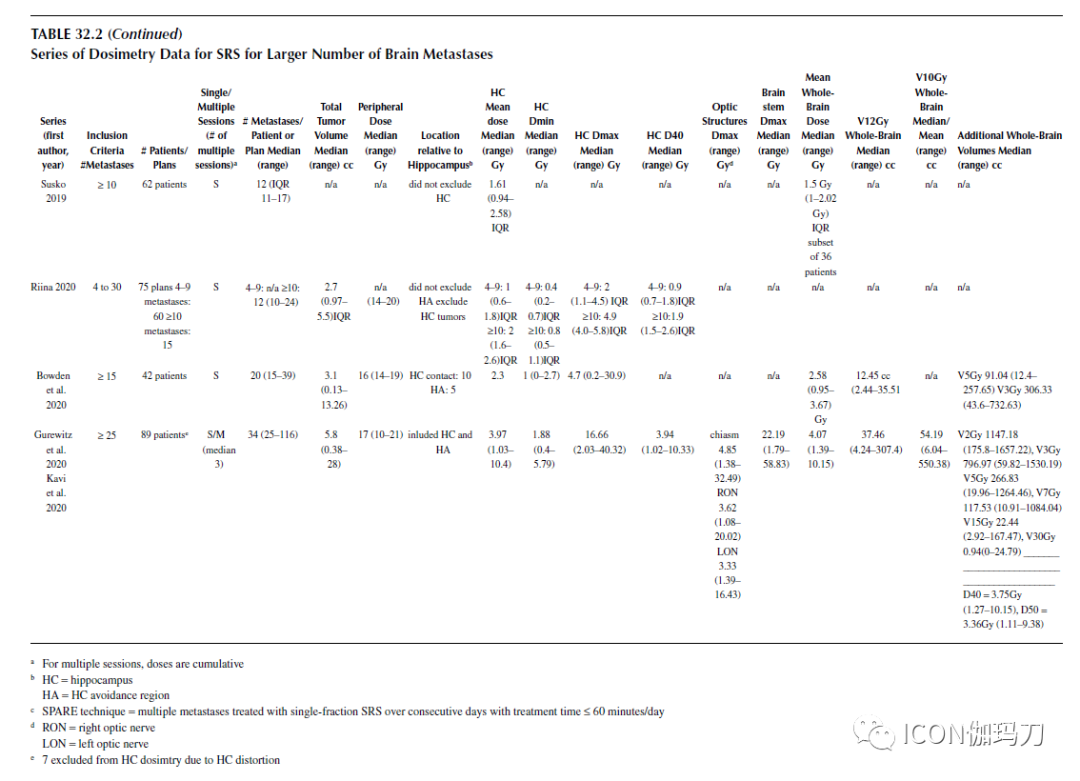
海马的受照剂量已被证明是辐射诱导的神经认知能力下降的一个因素,而回避海马是一种减轻全脑放疗的辐射诱导的神经认知影响的策略。回避海马可以通过多种照射技术实现,包括HA-WBRT和SRS。考虑到这些类型的照射在剂量分割、时间和对alpha-beta(α/β)比值假设(即,每次分割剂量对短期和长期毒性的影响)的敏感性方面存在较大差异,因此对HA-WBRT与SRS治疗广泛脑转移瘤患者的剂量学比较是有问题的。然而,在SRS建模研究和已发表的报告中获得的海马受照剂量比HA-WBRT更为有利。在Bowden剂量学测定中,中位双侧海马受照平均剂量为2.3 Gy 。在来自纽约大学的我们的系列中,中位转移瘤数目高于Bowden系列的(33对20),所有患者的中位双侧海马平均受照剂量为3.97 Gy,治疗位于海马回避区外的患者受照剂量为3.07 Gy。
尽管治疗了较多数目的肿瘤,我们的中位最小剂量(Dmin)仅为1.88 Gy。在我们的研究系列和大多数其他系列中,就Dmin和平均剂量(Dmean)而言,SRS的剂量都低于HA-WBRT。我们的高Dmax剂量至少部分原因是使用SRS治疗海马或HA区(一般定义为海马外5毫米)内的病变。同样,在Riina的系列中,海马和靶区之间距离的缩短与计划超出海马的约束有关(reduced dis-tance between the hippocampus and the target was associ-ated with plans exceeding hippocampal constraints )。这些较高的Dmax剂量尚未被证明与有害结果相关。需要进一步分析SRS治疗较多数目转移性肿瘤的脑剂量学与神经认知结果之间的相关性。
32.4 毒性
已发表的治疗4个以上转移瘤的医疗机构经验表明,对显著毒性的恐惧并没有随着放射外科治疗的应用而得到认识理解(the fear of marked toxicity was not realized with the use of radiosurgery)(见表32.1)。JLGK0901 (Yamamoto Lancet Oncol, 2014)的初始报告显示,放射副反应的风险为12%,可被接受;然而,中位生存期在10个月左右,长期毒性发生率的问题没有得到解答。幸运的是,与原始文章相比,JLGK0901研究的存活患者观察期延长了近2年,更新后的分析结果显示,仅新增44例患者出现与放疗相关并发症,导致粗算发病率仅增加3.7% 。此外,通过该患者队列的连续测试,在神经认知功能的长期维持方面,接受SRS治疗的有2-4个肿瘤的患者与有5-10个肿瘤的患者之间没有显著差异。
32.5影像监测
在美国,MRI通常被认为是脑转移患者治疗后随访的最合适的成像方式。然而,这种成像的最佳频率仍然存在争议。在诊断为脑转移瘤时接受SRS治疗的患者中,Sheehan报告了初始伽玛刀放射外科治疗后新发转移的中位时间为8.8个月,并发现除NSCLC外组织学和有3个病灶的患者早期远处脑部失效的风险增加。作者假设这些患者可能会从密切的监测中受益,并建议间隔3个月进行MRI监测。然而,监测脑部磁共振成像会产生成本,而且这种监测对患者的好处可能需要证明。Lester等表明,与常规监测成像检测出的无症状脑部复发患者相比,出现有症状脑部复发的患者可能有更糟糕的临床结果,并需要花费更多的药物费用。我们在SRS治疗后8周进行脑部MRI检查,之后每3个月进行一次,根据SRS发生的时间、脑转移的速度、全身疾病状态和个别治疗目标,决定将监测扫描间隔增加到4或6个月。
32.6 SRS与 HA-WBRT
对转移瘤数目较多的患者的回顾性和前瞻性观察数据表明,保留WBRT不会影响该人群的总体生存率;然而,在这种情况下使用SRS仍然令人担忧,不仅是总体生存,而且是患者和社会随后补救远处脑部衰竭的成本。最近,一项MD Anderson III期随机对照试验的结果显示,在患有415例非黑色素瘤脑转移的患者中,SRS与WBRT的比较显示,接受SRS治疗的患者在4个月时神经认知能力下降的风险显著降低,生存率没有受到影响。本研究提供了前瞻性随机数据,支持在4个以上转移瘤患者中使用SRS治疗而不是WBRT治疗。即将对现代WBRT(即HA-WBRT)与SRS进行随机数据测试,以完全解决与治疗与较多数目脑转移瘤相关的所有问题。这种假设不应该是一种方法总是比另一种好;我们希望,通过严格收集和分析前瞻性数据,可以为哪些患者最适合每种治疗方法提供一些指导。
加拿大癌症试验组CE.7于2018年开放,将515例脑转移患者随机分至HA-WBRT(含美金胺)组或SRS 组(ClinicalTrials.gov https://clinicaltrials.gov/ct2/show/NCT03550391)。测量的主要结果是总体生存期和神经认知无进展生存期。有15个次要结果,包括成本分析、多重生命质量评估、生物学问题、MRI评估和先前发表的预测无远处脑生存诺模图(nomogram)的前瞻性验证。在CE.7中,HA-WBRT的中位总体生存期可以预期与NRG肿瘤学- cc001中HA-WBRT报告的6.3个月相同。尽管针对数目较多的转移瘤的CCTG试验正在进行,但对“数目多的(larger number)”转移瘤的定义正在改变。日本最近的一份报告对1515例有5-10个转移瘤患者SRS治疗结果和804例有11-20个转移瘤患者的SRS治疗结果进行比较(Yamamoto等,2020年)。两组之间的存活率差别很小,毒性仍然很低。在纽约大学,“数目多”的定义随着时间的推移而改变。在20世纪90年代末,几乎所有有1-3个肿瘤的都接受了转移瘤治疗,,人数非常少的有4个肿瘤的接受了转移瘤治疗,无有5个或5个以上肿瘤的患者接受转移瘤的治疗。在2013年至2019年期间的2074次SRS治疗的转移瘤中,三分之一为有4-10个肿瘤,近15%有10个以上的肿瘤。在此期间,我们治疗了50例初次SRS时有超过15个肿瘤的患者。我们有6例患者在初始SRS治疗时有25个或更多的转移瘤;然而,已经有越来越多的患者接受了多次放射外科治疗,累计数目超过25个。
32.7全身系统治疗的作用
在当今时代,系统治疗在较多数目脑转移瘤患者的治疗中所发挥的作用必须得到检验,包括其延长总体生存期的效果,以及直接治疗颅内转移性疾病的效果。用于治疗脑转移瘤的系统治疗手段,包括靶向药物和免疫疗法,已经迅速扩充,具有中枢神经系统活性的药物现在在包括乳腺癌、肺癌和黑色素瘤等一些最常见的恶性肿瘤的治疗中发挥着重要作用。
酪氨酸激酶抑制剂(TKIs)如奥希替尼(osimertinib)延长了晚期EGFR突变NSCLC患者的中位总生存期3年。劳拉替尼(Lorlatinib)是治疗ALK突变型肺癌的第三代TKI,除了产生脑转移的放射影像学上的退缩外,研究表明可以预防约80%已经有脑转移瘤的患者的CNS进展。HER2CLIMB III期试验显示,图卡替尼(tucatinib)[口服的人表皮生长因子受体2 (Her2)小分子抑制剂]与曲妥珠单抗和卡培他滨一起,在大力度预处理(heavily pretreated)的脑转移瘤患者中,1年无进展生存期为25%,而没有图卡替尼(tucatinib)的患者为0% 。快速加速纤维肉瘤同源物B (rapidly accelerated fibrosarcoma homolog B, BRAF)和丝裂原激活激酶(mitogen activated kinase ,MEK)抑制剂已被证明在BRAFv600突变型黑色素瘤患者中具有CNS活性,免疫检查点抑制剂伊匹单抗(ipilimumab)和纳武单抗(nivolumab)已被用于治疗无症状的黑色素瘤脑转移患者的CNS疾病。
虽然全身疗法对中枢神经系统的疗效是很明显的,但除非结合适当的局部治疗,单独的全身疗法可能会导致生存率下降。据报道,EGFR突变的NSCLC脑转移瘤患者的最佳生存期是使用先期SRS,而不是单独使用TKI 。正在进行的奥希替尼(osimertinib)联合SRS与单独使用奥希替尼治疗EGFR突变的NSCLC的II期随机Trans-Tasman放射肿瘤组(TROG) OUTRUN试验将有助于明确这些患者的最佳治疗方法(ClinicalTrials.gov,https://www.clinicaltrials.gov/ct2/show/NCT03497767)。也可能是全身靶向治疗结合SRS的使用改变了中枢神经系统疾病的模式并影响了死亡原因。在新的系统治疗的背景下,长期随访将是必要的,以明确神经死亡的风险。此外,到目前为止,系统试验主要集中在包括联合SRS治疗的影像学结果,已将神经认知纳入其结果分析。系统方法和局部方法之间的比较需要使用一个共同的结果,以便真正了解组合使用的获益。
32.8未来的发展方向
治疗>5个脑转移瘤的技术和经验不断增加;已经突破了SRS治疗的脑转移数目的界限,但在未来,什么将是越来越有效的系统性治疗,问题将不是数目多少上限的病变应该用SRS治疗,而是什么是最好的方法来整合不断发展的系统性治疗与SRS。
点击或扫描上方二维码,查看更多“脑肿瘤”内容





