来自美国伊利诺大学芝加哥分校神经外科的McGuire LS等使用定量磁共振血管造影术(QMRA)比较了接受药物治疗和血管内治疗的颈部动脉夹层患者随时间的脑血流变化,结果发表在2022年6月3日的《Interventional neuroradiology》杂志上。
——摘自文章章节
【REF:McGuire LS, et al. Interv Neuroradiol. 2022 Jun 3. doi: 10.1177/15910199221106040.】
颈动脉或椎动脉的颈部动脉夹层(cervical arterial dissections,CAD)引起所有缺血性卒中的2-3%、45岁以下缺血性卒中的5-22%,通常归因于原发病变处的血栓形成和随后的远端栓子。然而,夹层部位和远端的血流量减少也可能是一个重要的影响因素。了解CAD患者脑血流量的数量差异及其与血管内治疗的关系可以帮助指导管理决策,如考虑血管内治疗。虽然抗血小板和抗凝血药物广泛应用于CAD患者以降低卒中的风险,血管内治疗的作用仍不清楚。血管内介入支架置入术或血管成形术是存在抗血栓禁忌症或抗血栓治疗失败伴进展性临床症状或影像提示卒中高风险时的选择。来自美国伊利诺大学芝加哥分校神经外科McGuire LS等使用定量磁共振血管造影术(quantitative magnetic resonance angiography,QMRA)选择脑血流量低的患者进行血管内治疗,通过分析序贯QMRA及其与卒中临床和影像学进展之间的关系,比较了接受药物治疗和血管内治疗的CAD患者随时间的脑血流变化,结果发表在2022年6月3日的《Interventional neuroradiology》杂志上。
利用回顾性图表对CAD患者进行回顾。纳入标准为成年人(> 18岁)、诊断为颈内动脉或椎动脉夹层,并接受QMRA检查。对病例进行临床表现、诊断、治疗和影像学审查,特别是对接受血管内治疗的患者进行评估。使用商业上可用的NOVA软件(Noninvasive Optimal Vessel Analysis; VasSol, Inc.;River Forest, IL USA),可对MRA的时间飞跃(TOF)和相位对比(PC)技术图像进行血流定量分析。
研究纳入41名患者,其中女性占46.3% ,平均年龄46.0 +/-11.9岁。21名(51.2%)患者存在对侧ICA夹层,19名(46.3%)患者为椎动脉VA夹层,1名患者两者都有。5名患者接受了支架置入术、血管成形术或两者兼而有之。尽管接受支架/血管成形术的患者患有糖尿病(p = 0.015)和既往抗凝治疗(p = 0.007)的比例更高,接受内科与血管内治疗的患者之间的基线特征相似。所有血管内治疗的病人在MRI上都表现出缺血,而接受内科治疗的病人中有53.1%表现出缺血(p = 0.047)。比较这两个患者组的同侧血管流量随时间的变化,结果显示那些接受支架或血管成形术的患者基线脑血流量较低,虽然不具显著性(p = 0.629)。与药物保守组相比,接受血管内治疗的患者远端脑血流量更低。
表1. 接受和不接受支架置入/血管成形患者的特征比较

表2. 病人表现特征


图1. 颈内动脉夹层患者血管内治疗前后同侧血管和同侧大脑中动脉血流测量结果的箱形图

图2. 椎动脉夹层患者血管内治疗前后通过同侧血管和同侧基底动脉血流测量结果的箱形图

图3. 随访过程中支架置入/血管成形术后同侧血管血流的意大利面图

图. 4(双向重复测量ANOVA比较支架置入/血管成形术患者和无支架置入/血管成形术患者(受试者内和受试者间设计,Greenhouse-Geisser球形度校正,受试者内效应 p = 0.130,受试者间效应 p = 0.629)的感兴趣血管中的流量。排除双侧或多个夹层部位的患者。)
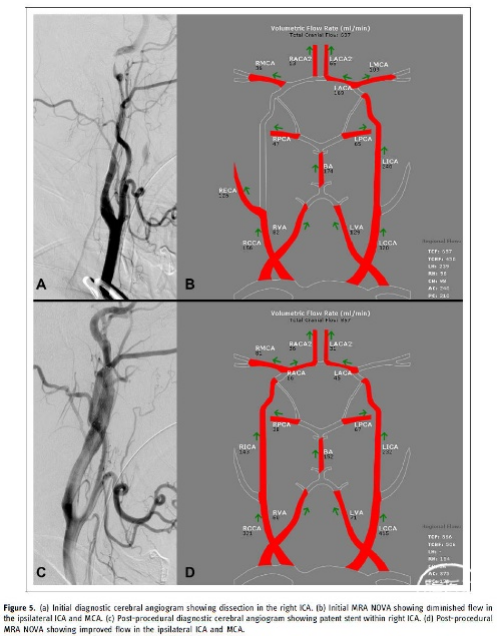
图5. (a)初始诊断性脑血管造影显示右颈内动脉夹层。(b)初始MRA NOVA显示同侧ICA和MCA血流减少。(c)术后诊断性脑血管造影显示右ICA内通畅的支架。(d)术后MRA NOVA显示同侧ICA和MCA血流改善。
这项研究是第一个使用QMRA评估颈动脉夹层血管内治疗患者血管流量的研究。结合进行性症状,QMRA可能作为选择动脉夹层行血管内介入治疗患者的辅助手段,但需要更大规模的前瞻性研究进行验证。虽然接受支架或血管成形术的患者与药物保守治疗患者相比,最初的血流量较低,但随着时间的推移,所有组的同侧血流量都会增加。






