01
基本信息
患者男,36岁,帕金森病史7年。
02
主诉
右侧肢体抖动7年,左侧肢体抖动5年。
03
现病史
患者7年前无明显诱因出现右上肢不自主抖动,安静时出现,紧张或激动时加重,随意运动时不消失,后逐渐加重至右下肢,无动作迟缓、僵直,服用美多芭250mg一天三次、普拉克索0.25mg每天一次治疗仍无明显好转后停药,5年前出现左侧肢体抖动,2年前自觉四肢抖动加重,影响进食饮水等日常活动,睡眠中抖动消失,伴活动变慢、不灵活。
04
神经系统查体
右利手,高级皮层功能、颅神经未见明显异常,眼球各项活动可,感觉查体正常,四肢均可见静止性震颤、姿势性震颤、动作性震颤,四肢肌力正常,肌张力稍高,腱反射(++),共济运动可,病理征(-)。
05
辅助检查
DAT显像支持帕金森病诊断。患者因经济原因未行基因检查。
06
术前评估
UPDRS-III“关期”48分(图1),服用美多芭437.5mg(1.75片)1小时后“开期”评分43分(图2),最大改善率10%,H-Y分期2期,TUG关期12s,开期11s,MMSE26分,MoCA23分,HAMD2分,HAMA1分,PDQ39量表26分。

图1:美多芭负荷试验服药前(关期)螺旋画圈实验。
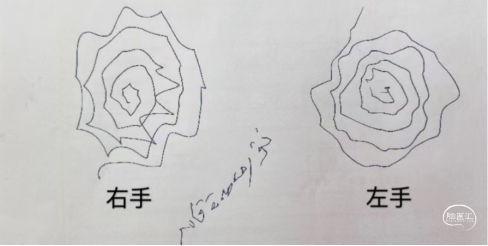
图2:美多芭负荷试验服药后1小时(开期)螺旋画圈实验。
07
诊断与治疗
经我院多学科讨论后考虑诊断原发性帕金森病,为左旋多巴冲击试验改善率低特殊类型,选择最经典的STN靶点。手术顺利,经术后CT验证双侧靶点位置准确。

08
术后结果
术后因微损毁效应,双侧肢体抖动均较前减轻,左侧明显。术后3天试开机,刺激参数:RC+1-60us 130Hz 1.0V,LC+8-60us 130Hz 1.2V,患者双侧静止性震颤及四肢轻度肌张力增高均完全消失。1周后四肢震颤逐渐加强,调整刺激参数为:RC+1-70us 160Hz 1.2V,LC+8-70us 160Hz 1.8V,患者四肢震颤均改善。


09
出院后随访
术后1月复诊时,患者左侧上下肢及右下肢未见震颤,右上肢仍有静止性、姿势性、动作性震颤,UPDRS-III评分15分。将刺激参数调整为:RC+1-90us 180Hz 2.1V,LC+10-11-90us 180Hz 2.2V,患者四肢静止性震颤均消失,仍存在右上肢姿势性、动作性震颤,患者无不适(图3),UPDRS-III评分11分。将刺激参数调整为:RC+1-80us 230Hz 2.3V,LC+10-11-90us 230Hz 2.5V,患者右上肢静止性、姿势性、动作性震颤均消失,患者有说话费力感(图4),UPDRS-III评分2分,改善率95%。

图3:刺激参数调整为:RC+1-90us 180Hz 2.1V,LC+10-11-90us 180Hz 2.2V,患者右上肢静止性震颤消失,仍存在姿势性、动作性震颤,螺旋画圈实验如图。


图4:刺激参数调整为:RC+1-80us 230Hz 2.3V,LC+10-11-90us 230Hz 2.5V,患者右上肢静止性、姿势性、动作性震颤均消失。螺旋画圈实验如图。

讨论
本例患者是以四肢震颤为主的帕金森病,其特点为左旋多巴冲击试验改善率低(<30%),行STN-DBS治疗后症状明显改善,改善率(95%)明显高于左旋多巴负荷试验最大改善率。震颤表现为静止性、姿势性、动作性震颤,其震颤症状采用超高频刺激(180-230Hz)治疗效果明显。本单位采用STN-DBS治疗的该帕金森病患者通过短期随访发现频率130-160Hz刺激时震颤部分改善,轻度肌张力增高缓解。将刺激频率调整为高频(180~230Hz)刺激时,患者震颤完全消失,但出现说话费力症状。
左旋多巴负荷试验经常作为PD患者DBS手术首要的一线筛选方法,尤其对于一些具有帕金森综合征症状但不符合帕金森病诊断标准的患者进行确诊和DBS手术效果预估有所帮助[1,2]。我们可能普遍都认为术前左旋多巴反应性与STN-DBS疗效的具有非常重要的相关性,因此对于左旋多巴负荷试验改善率低的患者应谨慎选择手术。但也有一些研究认为,手术前PD患者的左旋多巴反应性并不能准确预测STN-DBS的预后[3,4]。国内一项回顾性分析提出STN-DBS对LCT改善率<30%的原发性PD患者的运动症状改善有效,尤其对震颤为主型的原发性PD患者的短期疗效更佳[5]。本病例为震颤为主的原发性PD,结果表明患者术后运动症状改善率较术前药物改善率明显提高。因此,笔者认为术前LCT改善率<30%的患者经过严格筛选,排除认知障碍、精神异常等症状的患者,应用STN-DBS可改善患者的运动症状。
PD是神经系统退行性病变,患者中脑黑质致密部多巴胺能神经元进行性减少,服用左旋多巴治疗是直接补充脑内缺失的左旋多巴,使其在体内转化为多巴胺而发挥用。但该过程受吸收效率、人体对外源性左旋多巴的耐药性以及纹状体对左旋多巴的储备功能等多种因素的影响,因此即使诊断为原发性PD的患者,其对左旋多巴的药物反应也各不相同。目前认为DBS产生调控作用的基本机制离不开高频刺激的脉冲对于细胞膜的兴奋作用,这种兴奋可能诱导胞体和轴突细胞膜的间歇性去极化阻滞,进而使得病理性神经信息传导被阻断,电信号恢复正常,症状改善[6,7]。DBS的刺激是以一定频率持续存在的,且其作用机制与药物不同,因此,对于左旋多巴冲击试验改善率低的PD患者也可能产生很好的改善效果。
另外,患者低频震颤改善不佳,高频(180~230Hz)刺激时,震颤改善明显,但出现说话费力症状。该患者情况与文献报道一致。一项双盲长期随访研究显示高频电刺激丘脑可有效抑制PD的严重震颤达6年以上[8]。
本例虽然说明左旋多巴负荷试验与STN-DBS术后效果不具有必然相关性,但也存在病例数太少,随访时间较短的不足。其关系尚需进一步研究。笔者正在进行大样本随访对照研究,以验证左旋多巴反应性与STN-DBS效果的关系,为DBS术前筛查提供新思路及可推广的实施依据。另外,患者是否为原发性PD合并特发性震颤,STN是否为其最佳靶点等问题都需要进一步探讨和随访观察。
新医大一附院
神经外科中心神经外四科
新疆医科大学第一附属医院神经外四科主要收治功能性神经精神疾病患者,主要收治病种包括:难治性癫痫、继发性癫痫、疼痛(三叉神经痛、舌咽神经痛、癌痛等),面肌痉挛、帕金森病、肌张力障碍(特发性震颤,书写痉挛,痉挛性斜颈)、冻结步态、脑卒中后遗症、强迫症等功能性神经精神类疾病。近年来,熟练应用并开展DBS手术治疗运动障碍性疾病患者百余例,并开展包括强迫症在内的精神疾病的DBS外科治疗。此外,熟练开展各种类型的癫痫手术,包括颞前叶及海马-杏仁核切除术、症状性癫痫病灶切除术,迷走神经电刺激(VNS),立体定向脑电图(SEEG)等。
新医大一附院运动障碍性疾病团队由神经外科、神经内科、影像科、康复科医师联合组成,针对帕金森病,肌张力障碍,特发性震颤,书写痉挛,痉挛性斜颈,冻结步态等疾病对患者制定精准的诊疗方案。专家团队成员根据运动障碍性疾病患者的临床表现、基因型及影像学等辅助检查,明确患者的症状学诊断、病因学诊断及分类,在此基础上结合个体差异制定治疗策略。由于运动障碍性疾病诊断和治疗的复杂性及特殊性,必须经过多学科MDT讨论,并共同制定治疗方案,由神经外科进行DBS手术并进行术后程控管理,为广大运动障碍性疾病患者提供一站式多学科多位一体的协作式诊疗方案。
专家介绍

郝玉军
教授/主任医师
新疆医科大学第一附属医院神经外科中心副主任、功能神经外科病区主任
世界华人神经外科学会功能学组常委
中国医师协会神经外科分会委员
中华医学会神经外科学分分会功能学组委员
中国医师协会神经外科学分会功能学组委员
中国抗癫痫协会理事
中国医师协会神经调控专业委员会委员
中国医师协会神经修复专业委员会委员
新疆医师协会神经外科学分会副主任委员

姜磊
主任医师
中国神经修复专业委员会青年委员
中国研究型医院学会神经再生与修复专业委员会脑认知与神经调控学组委员
中国医师协会神经调控专业委员会西北区域工作委员会委员
中国抗癫痫协会会员
中国医师协会神经外科分会会员
中华医学会神经外科分会会员
1
参考文献
1. Lang, A., et al., Deep brain stimulation: preoperative issues. Movement disorders : official journal of the Movement Disorder Society, 2006: p. S171-96.
2. Rodriguez, R., et al., Pearls in patient selection for deep brain stimulation. The neurologist, 2007. 13(5): p. 253-60.
3. Piboolnurak, P., et al., Levodopa response in long-term bilateral subthalamic stimulation for Parkinson's disease. Movement disorders : official journal of the Movement Disorder Society, 2007. 22(7): p. 990-7.
4. Zaidel, A., et al., Levodopa and subthalamic deep brain stimulation responses are not congruent. Movement disorders : official journal of the Movement Disorder Society, 2010. 25(14): p. 2379-86.
5. 杨春晖, et al., STN-DBS治疗左旋多巴冲击试验改善率较低的原发性帕金森病患者的短期疗效. Vol. 2019年12月28日. 2019.
6. Al-Fatly, B., Coherence: a unifying mechanism of deep brain stimulation. Journal of neurophysiology, 2019. 121(1): p. 1-3.
7. Chiken, S. and A. Nambu, Mechanism of Deep Brain Stimulation: Inhibition, Excitation, or Disruption? The Neuroscientist : a review journal bringing neurobiology, neurology and psychiatry, 2016. 22(3): p. 313-22.
8. Rehncrona, S., et al., Long-term efficacy of thalamic deep brain stimulation for tremor: double-blind assessments. Movement disorders : official journal of the Movement Disorder Society, 2003. 18(2): p. 163-70.






