近期,德克萨斯大学安德森肿瘤中心的Wajd N. Al-Holou等比较沿脑沟整块切除和瘤内分块切除低级别胶质瘤的疗效,发现沿脑沟整块切除低级别胶质瘤的全切除率更高,患者预后更好,结果发表在2022年1月的《J Neurosurg》在线。
——摘自文章章节
【Ref: AI-Holou WN, et al. J Neurosurg. 2022 Jan 7;1-11. doi: 10.3171/2021.9.JNS21718. [Epub ahead of print]】
低级别胶质瘤(LGG)具有侵袭性,但很少跨脑沟回生长。神经外科医生在保留神经功能前提下,沿MRI图像上T2像和FLAIR像高信号的切除范围越多,患者预后往往越好。目前,大多数神经外科医生仍采用瘤内分块切除以保护正常脑组织。近期,德克萨斯大学安德森肿瘤中心的Wajd N. Al-Holou等比较沿脑沟整块切除(sulcus-guided resection,SGR)和瘤内分块切除(piecemeal resection,PMR)低级别胶质瘤的疗效,发现沿脑沟整块切除低级别胶质瘤的全切除率更高,患者预后更好,结果发表在2022年1月的《J Neurosurg》在线。研究者回顾性研究1993年6月至2015年12月在安德森肿瘤中心收治的519例脑胶质瘤患者。纳入研究的标准为位于大脑半球的非增强型WHO II和III级胶质瘤,包括星形胶质细胞瘤和少突胶质细胞瘤患者;在MRI-T2像和FLAIR像高信号,在T1像无或少量增强信号。排除位于深部、后颅窝或者不利于实施沿脑沟切除的肿瘤,如脑室、丘脑或岛叶的LGG。完整切除定义为MRI-T2像上高信号区完全消失。
沿脑沟切除肿瘤技术是依据低级别胶质瘤生长一般不跨过脑沟,即使侵犯邻近脑回也是沿着短U联络纤维生长的客观事实。LGG的边界可由MRI-T2/FLAIR像上高信号边缘的脑沟界定。手术第一步是在空间上判定肿瘤边界:在完成开颅和剪开硬膜后,通过术中导航、超声或者肉眼观察确定肿瘤所侵犯的脑回和脑沟,以及肿瘤边界的脑沟。在某些情况下,肿瘤膨胀到附近脑回的下方,会造成肿瘤似乎侵犯附近脑回的假象,其实附近脑回未被侵袭。注意确认并保留皮质的重要血管。第二步是确定功能区:通过术中监测技术辨认功能区与肿瘤。第三步是沿脑沟切除肿瘤:确定肿瘤边界后,可以沿肿瘤边界锐性打开脑沟的蛛网膜。保留供应周边脑组织的动脉和静脉。向脑沟底部分离时,遇到大的过路血管予以保护,小穿支电凝切断;原则上,脑沟基底部的静脉可以电凝。遇到功能区脑回,可在脑沟软膜下分离,借助周围软脑膜和脑脊液保护脑回。也可利用导航指引沿脑沟分离肿瘤边界。第四步分离白质;采用吸引器和双极轻轻分离肿瘤周缘脑沟深部的白质,边分离边铺脑棉作标记;直至沿肿瘤的四边和深部将肿瘤完整剥离。分离过程中,采用皮质下电刺激引导可减轻脑组织的神经损伤(图1、2、3)。
图1. A. 黑框代表开颅部位,此处肿瘤位于运动前回前方的额中回。B. 在MRI导航引导下找到肿瘤周围脑沟。黑色虚线表示肿瘤位于中央前沟、额上沟和额中沟。红星代表位于额中回的肿瘤前界。C. 栅电极刺激仪的双极在刺激肿瘤表面时无阳性反应,刺激运动前回可定位手运动区(标记H)和脸部运动区(标记F)。D. 为图A的局部,表示肿瘤膨胀凸向周围正常脑回的下方,似乎肿瘤侵犯至周围脑回,但事实上并无侵犯;肿瘤边界仍可由脑沟界定。图中星号代表刺激运动前回,沿其下方被推移的脑沟(井号、箭头和虚线表示)分离肿瘤边界,可不影响运动前回。用相同方法沿脑沟分离肿瘤的另一侧边缘。
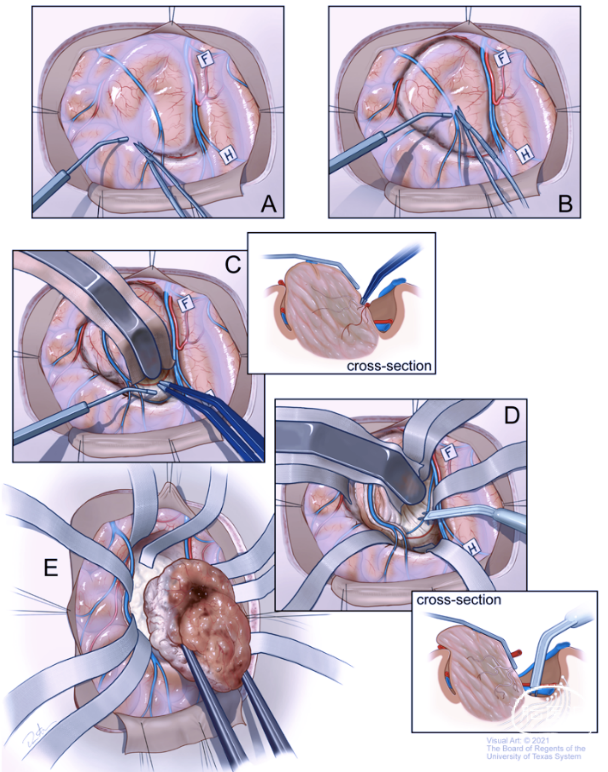
图2. A. 锐性打开脑沟上的蛛网膜并分入脑沟。B. 必要时保留浅表静脉。C. 分离脑沟至底部,保留大动脉,电凝切开小的穿支。D. 脑沟底部分离后,导航定位肿瘤边界并沿边界切开白质,直接皮质下电刺激可以避免损伤重要下行运动纤维。E. 肿瘤最终完整切除。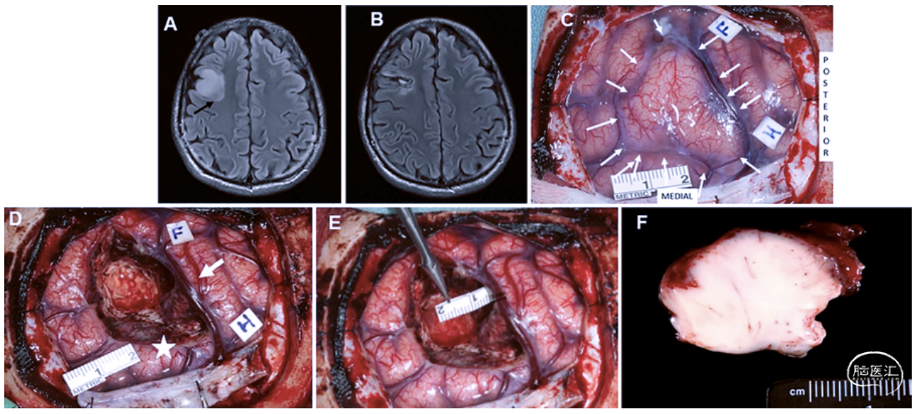
图3. A. 术前MRI-FLAIR像显示,位于额中回靠近中央前回的无强化肿瘤。B. 术后MRI-FLAIR像显示肿瘤完整切除。C. 术中图片示,唤醒刺激手术前的肿瘤。F为面部运动区,H为手运动区。肿瘤边界由白色小箭头表示。D. 切除术后的肿瘤残腔,边缘额上回软脑膜完整(星号),中央前沟的静脉保留(箭头)。E. 中央前回保留,测量中央前回至肿瘤腔对侧边界的距离。F. 用福尔马林固定的完整切除的肿瘤标本。
519例患者中,208例沿脑沟切除LGG;311例瘤内分块切除术。64%临床表现癫痫,沿脑沟切除术和瘤内切除术时,分别26%和29%采用术中唤醒技术(p=0.5)。沿脑沟切除术部分切除率和完整切除率均比瘤内切除术高,分别p=0.019和p=0.016。体积越小的肿瘤切除率越高(p=0.002),WHO II级的肿瘤切除率更高(p=0.012)。多变量分析显示,与肿瘤切除率高相关的变量为沿脑沟切除(OR=1.7;95%CI,1.1-2.6;p=0.03)和肿瘤体积小(OR=0.97;95%CI,0.96-0.98;p<0.001)。术后19%患者有语言障碍,14%出现新的神经系统并发症或并发症短期加重。单变量分析显示,肿瘤位于功能区(18%)比非功能区(11%)更易出现术后并发症(p=0.03)。沿脑沟切除术的患者术后并发症发生率(11%)比瘤内分块切除组(16%)明显地低(p=0.09)。肿瘤位于功能区,沿脑沟切除术后并发症发生率(12%)比瘤内切除(21%)更低(p=0.16)。根据COX回归模型的生存分析,与生存期长相关的变量有切除率>75%(HR=0.6;95%CI,0.4-0.8;p=0.003)、MRI-T2像上肿瘤初始体积小(HR=1.004;95% CI,1.001-1.008;p=0.015)、少突胶质细胞瘤(HR=0.53;95%CI,0.4-0.8;p=0.003);而肿瘤WHO分级和沿脑沟切除或瘤内切除不影响生存期。
该研究是首项比较沿脑沟切除与瘤内分块切除低级别胶质瘤治疗效果的研究,文章详细描述沿脑沟切除技术。沿脑沟切除技术的优点,①因为肿瘤边界由脑沟界定,术中全程掌握肿瘤和周边脑组织的解剖结构;②因为最后完整切除肿瘤,脑沟位置在术中无变化,导航系统可以一直保持准确;③看似肿瘤侵犯功能区,其实只是肿瘤将脑沟推到功能区下方,沿脑沟切除可完整切除肿瘤而不损伤功能区;④脑沟底部可帮助确定肿瘤深度;⑤打开脑沟可早期暴露过路血管,从而保护周围脑组织的血供;⑥因为低级别胶质瘤血供来自于脑沟内动脉发出的小穿支,可早期电凝切断,减少肿瘤出血。研究结果显示,与瘤内分块切除相比,沿脑沟切除显著提高低级别胶质瘤的全切率,并未增加神经系统并发症,值得推荐。

声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、AiBrain所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。









