第12期“诺华ACRO之声--肢端肥大症文献速递与专家点评”,精选了5篇近期发表的文献,包括Daniel F. Kelly教授发表的垂体腺瘤内镜手术不同阶段并发症的规避方案;浙江大学第二附属医院吴群教授和张建民教授团队发表的垂体大腺瘤和巨大腺瘤肿瘤预后预测模型的研究;生长激素释放激素拮抗剂抑制垂体腺瘤细胞生长的分子机制研究;发现早期使用替莫唑胺可能改善侵袭性垂体腺瘤应答的研究;ACRO患者肌肉和脂肪的可逆性胰岛素抵抗与代谢综合征并无相关性的研究。本期文献点评,我们邀请了山东大学齐鲁医院的倪石磊教授、江西医科大学附属第一医院的徐积兄教授,对其中两篇文献进行深度点评分析,欢迎大家阅读交流!

1
垂体腺瘤内镜手术并发症的规避:一项514例患者的回顾性队列研究
Pituitary. 2021 Dec;24(6):930-942. doi: 10.1007/s11102-021-01167-y.
IF=3.954
本研究发表在《Pituitary》杂志上,论文的通讯作者Daniel F. Kelly教授是美国著名神经内镜专家,该研究介绍了单中心垂体腺瘤内镜手术的并发症预防方案的技术细节,并评估了该标准化方案在降低包括嗅觉丧失、鼻出血、颈内动脉损伤、垂体功能减退、脑脊液漏和脑膜炎等术后并发症的发生率方面发挥的作用。
研究纳入了2010年至2020年期间在Saint John’s医学中心接受神经内镜治疗的所有垂体腺瘤患者。初级评价指标包括90天内的并发症发生率、内分泌功能、再手术率、再入院率及住院日。次级评价指标包括肿瘤切除程度、短期的内分泌功能缓解及视力恢复情况。共有514例患者(549次手术)纳入研究,平均年龄为51岁,78%为垂体大腺瘤,19%有既往垂体手术史。18例患者出现手术相关的严重并发症,脑脊液漏(9例,1.7%)和脑膜炎(4例,0.8%)最为常见,其中14例患者术后并发症被认为是可预防的。4例(0.8%)出现永久性后遗症(2016年前3例):1例不明原因死亡,1例中风,1例动眼神经麻痹,1例眼麻痹。所有患者均未出现颈内动脉损伤、永久性的视力视野恶化或永久性的嗅觉丧失情况,新发垂体功能减退的比例为4.7%(23/485)。平均住院日为2天,出现严重并发症患者的平均住院日为7天。6%(31/535)的患者再次入院治疗,其中大多数原因为低钠血症(18/31)。无功能型垂体腺瘤的全切率为69%(214/312),功能型垂体腺瘤术后生化缓解率为71%(148/209)。视野或视敏度术后改善的患者比例为91.3%(126/138)。综上,严格遵循垂体瘤内镜手术并发症预防的标准化方案可降低并发症发生率、再入院率并缩短平均住院日,并能增加保留垂体正常功能的可能性。
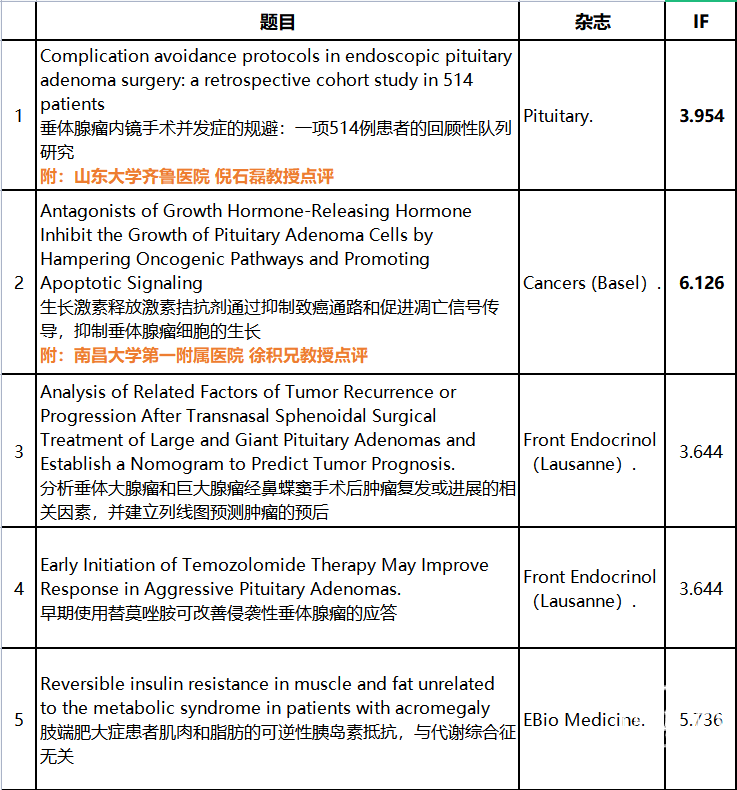
图1. 神经外科和耳鼻喉科联合进行垂体腺瘤内镜手术的并发症规避方案及手术室设置。关键的手术步骤包括(1)鼻腔鼻窦阶段制备补救黏膜瓣,旨在预防术后嗅觉丧失和延迟性术后鼻出血,(2)鞍底暴露及多普勒定位动脉走行,避免颈内动脉损伤,(3)切除肿瘤时遵循假包膜分离技术和垂体切开保留技术,将切除率/缓解率最大化并防止新发垂体损伤,(4)按照分级修补标准化方案进行鞍区及颅底重建,避免脑脊液漏及脑膜炎。
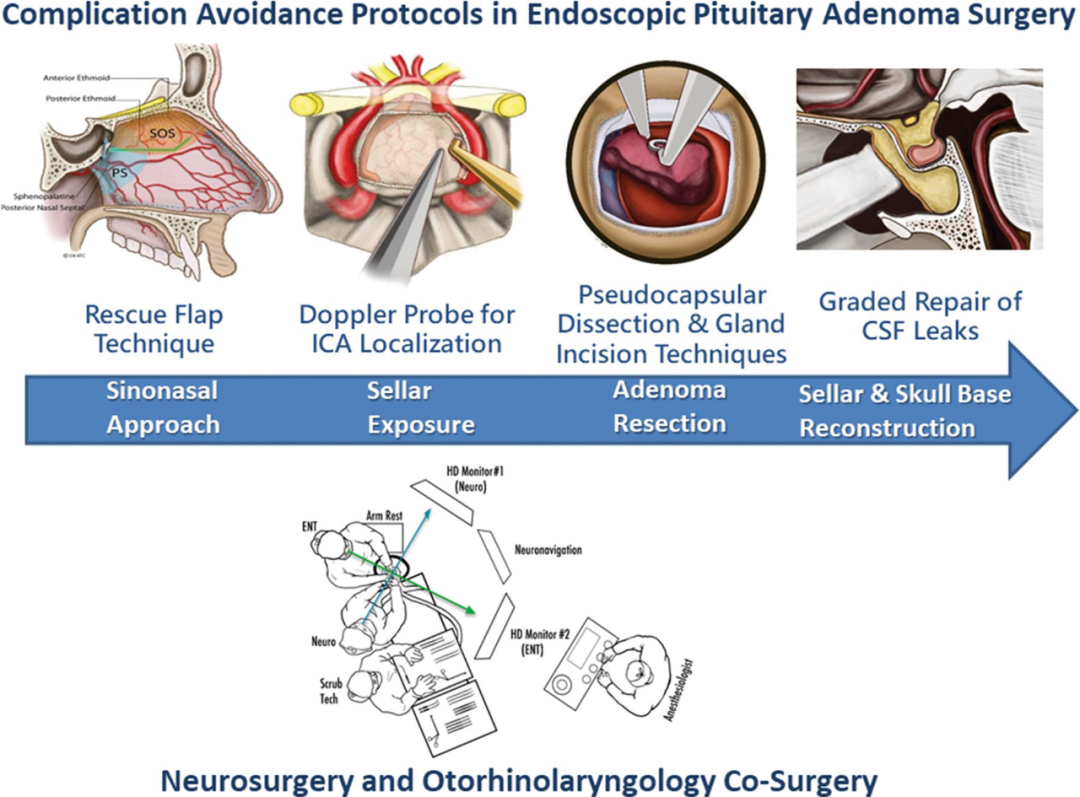
表2. 初级评价指标:并发症、住院日、患者处置、30天内再住院及再手术
内镜经鼻入路目前已成为治疗垂体瘤的首选手术方式,近年来我们中心超过97%的垂体腺瘤患者采用该入路进行手术切除。内镜手术具有微创、光照好、视野清晰等特点,但同时存在学习曲线,初学者往往伴随相对高的并发症发生率,认真学习并严格遵守并发症规避方案可更好地提高手术安全性和临床疗效。
Kelly教授从内镜垂体瘤手术的不同阶段详细阐述了并发症规避方案的多个关键技术细节,包括耳鼻喉科医师制备补救黏膜瓣,多普勒定位颈内动脉位置,对于颈内动脉损伤风险较高的患者执行“战术暂停”,肿瘤假包膜分离,垂体切开和保护技术等。为减少脑脊液漏及脑膜炎发生率,Kelly教授团队结合多年诊疗经验,建立了术中脑脊液漏分级体系,并制定了针对不同程度脑脊液漏的标准化多层颅底修补策略[1,2],上述技术流程和细节具有很好的可执行性,已成为包括我们中心在内的众多垂体瘤诊疗中心开展相关工作的重要参考。《中国肢端肥大症诊治共识(2021版)》强化了多学科合作诊疗(MDT)模式和个体化诊治的理念,并提倡将一部分有丰富诊疗经验的垂体腺瘤MDT团队进一步建设为垂体瘤卓越诊疗中心(PTCOE)。其实,Kelly教授早在2012年即联合几位垂体瘤资深专家提出了建立PTCOE的初步建议[3]并应用于临床实践之中;他在本研究中指出,PTCOE可更好地促进神经外科医生、内分泌科医生、耳鼻喉科医生、神经眼科医生和放射肿瘤学家之间的协作。尤其是文中最后提出的快速康复和术后预防迟发低钠方案,可实现部分患者术后一天出院,该优秀的治疗效果即得益于上述具体技术流程制定和多学科协作模式,值得我们学习借鉴。[1] Conger A., Zhao F., Wang X, et al. Evolution of the graded repair of CSF leaks and skull base defects in endonasal endoscopic tumor surgery: trends in repair failure and meningitis rates in 509 patients[J]. J Neurosurg. 2018 May 11;130(3):861-875. [2] Esposito F., Dusick J.R., Fatemi N., et al. Graded repair of cranial base defects and cerebrospinal fluid leaks in transsphenoidal surgery[J]. Oper Neurosurg (Hagerstown). 2007 Apr;60(4 Suppl 2):295-303.[3] McLaughlin N., Laws E.R., Oyesiku N.M., et al. Pituitary centers of excellence[J]. Neurosurgery. 2012 Nov;71(5):916-24.

倪石磊 教授
山东大学齐鲁医院神经外科副主任,主任医师,教授,博士生导师美国康奈尔大学及匹兹堡大学、挪威卑尔根大学访问学者山东省齐鲁卫生与健康领军人才,山东省优秀科技工作者《中华神经外科杂志英文版》《中华神经医学杂志》等多家杂志的通讯编委;先后主持国家自然基金5项,中国博士后课题2项及省级课题3项,发表论文30余篇,SCI论文20余篇。编著及译著《临床神经外科学》《神经外科手术核心技术》

2
生长激素释放激素拮抗剂通过抑制致癌通路和促进凋亡信号传导,抑制垂体腺瘤细胞的生长Cancers (Basel). 2021 Aug 5;13(16):3950. doi: 10.3390/cancers13163950.
IF=6.126
垂体腺瘤(PAs)是一种颅内肿瘤,常伴有过度的激素分泌和严重的合并症。有部分患者药物治疗疗效不佳时,需要更多的治疗方案。生长激素释放激素(GHRH)拮抗剂具有较强的抗肿瘤作用,早期GHRH拮抗剂在体内和体外均能抑制GHRH诱导的垂体GH分泌。然而,GHRH拮抗剂在PAs中的抗肿瘤作用尚不清楚。本研究发表在《Cancers(Basel)》杂志上,发现MIAMI类GHRH拮抗剂MIA-602和MIA-690,在转染人GHRH受体并分泌GH/泌乳素的GH3 PA细胞(GH3-GHRHR)和分泌促肾上腺皮质激素ACTH的AtT20 PAs细胞中,可抑制细胞活力和生长,并促进细胞凋亡。GHRH拮抗剂还可降低肿瘤发生和癌症进展相关蛋白的表达,上调促凋亡分子,降低GHRH受体水平。MIA-690与替莫唑胺联用可协同降低GH3-GHRHR和AtT20的细胞活力。此外,MIA-690可降低基础和GHRH诱导的GH分泌和细胞内cAMP水平。最后,GHRH拮抗剂可抑制人原代GH-和ACTH-PA细胞培养中的细胞活力。综上所述,无论是GHRH拮抗剂单药治疗还是与其他药物联用,均可考虑作为PAs的进一步治疗方法。
垂体腺瘤(PAs)通常是一种良性的颅内肿瘤,但其具有异质性和复杂性,表现出多种增殖和激素行为,可以快速生长出现因导占位导致的不良效应,或者因过量产生激素而引起严重综合征,从而增加发病率和死亡率。尽管现有药物通常能有效减少激素分泌过多和促进肿瘤缩小,但一些患者常出现耐药性,同时也有多种不良反应的报道。因此,研究开发PAs新的治疗药已成为一个热点问题。该研究发现,MIA-602和MIA-690,最近MIAMI类别的GHRH拮抗剂,在生长激素和促肾上腺皮质激素PAs细胞系,以及人原代PAs细胞培养物中表现出抗肿瘤活性。同时,该研究也是首次证明GHRH拮抗剂在促肾上腺皮质激素腺瘤细胞中的抑制活性。与以前的研究结果不同的是,该研究主要集中在GH分泌的抑制上,首次证明了GHRH拮抗剂在体外降低PAs细胞活力和生长、促进细胞凋亡和调节参与垂体瘤发生和发展的关键信号通路的能力。而且,GHRH拮抗剂与奥曲肽、帕瑞肽和兰瑞肽相比,在降低细胞活力和生长方面表现出更大的能力。因此,该研究结果显示,GHRH拮抗剂有望成为PAs的新治疗选择,可能与标准药物治疗联合使用提高疗效。期待未来会出现疗效好副作用少的药物让PAs患者有更多的药物选择。

徐积兄 教授
先后承担国家自然科学基金3项等15项科研课题;曾获省科技进步奖1项。发表论文50余篇(第一或通信作者),其中SCI收录26篇(1区2篇)
3
分析垂体大腺瘤和巨大腺瘤经鼻蝶窦手术后肿瘤复发或进展的相关因素,并建立列线图预测肿瘤的预后
Front Endocrinol (Lausanne). 2021 Dec 14;12:793337. doi: 10.3389/fendo.2021.793337.IF=3.644
垂体腺瘤是由腺垂体细胞引起的良性神经内分泌肿瘤,占所有原发性颅内肿瘤的10%-20%。对于直径≥3cm的巨大型垂体腺瘤,由于肿瘤形态、浸润部位、病理特征等多种因素的影响,其手术结局和预后存在显著差异。由浙江大学第二附属医院吴群教授和张建民教授团队发表在《Front Endocrinol(Lausanne》杂志上的本研究,旨在探讨垂体大腺瘤和巨大腺瘤经鼻蝶窦手术后肿瘤复发或进展的相关危险因素,并建立肿瘤预后的预测模型。本研究回顾性分析浙江大学第二附属医院2011年1月-2017年12月期间172例经蝶窦手术的大腺瘤和巨大腺瘤患者的临床和随访资料。检索基本临床信息(年龄、性别、既往病史等)、影像学特征(肿瘤大小、浸润特征、切除范围等)和组织病理学特征(病理结果、Ki-67、P53等)。采用SPSS 21.0软件进行统计学分析,采用R软件建立预测的列线图。研究结果发现,172例检查病例中有70例(40.7%)肿瘤复发或进展。术后1年、3年和5年的总体无进展生存(PFS)患者比例分别为90.70%、79.65%和59.30%。Log-rank检验显示,BMI(P<0.001)、Knosp分级(P<0.001)、切除范围(P<0.001)、Ki-67(P<0.001)、蝶窦浸润(P=0.001)、Hardy分级(P=0.003)、吸烟史(P=0.018)与术后复发或进展显著相关。Cox回归分析进一步提示吸烟史、BMI≥25kg/m²、Knosp分级4级、部分切除、Ki-67阳性率≥3%是肿瘤复发或进展的独立危险因素(P<0.05)。此外,基于上述结果的列线图、ROC曲线显示有显著的临床价值。因此,大腺瘤和巨大腺瘤术后复发或进展与多种因素有关,基于BMI(≥25kg/m²)、Knosp分级(4级)、切除范围(部分切除)和Ki-67(≥3%)的预后列线图,可以预测大腺瘤和巨大腺瘤术经鼻蝶手术后的复发或进展。
图2. 根据患者Knosp分级、Hardy分级、蝶窦浸润、Ki-67、切除范围、BMI和吸烟史分层的生存曲线。
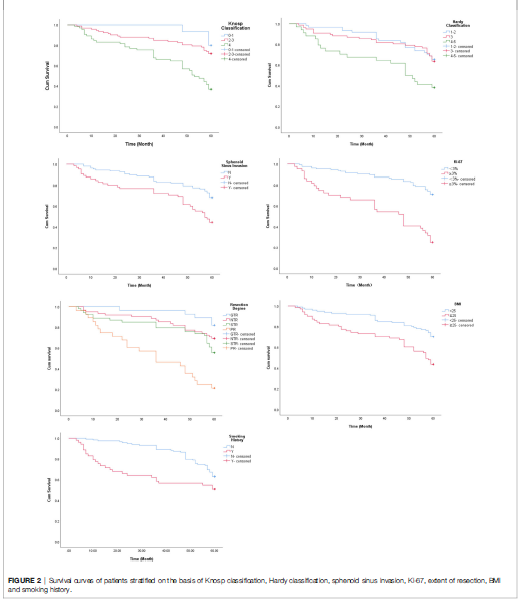
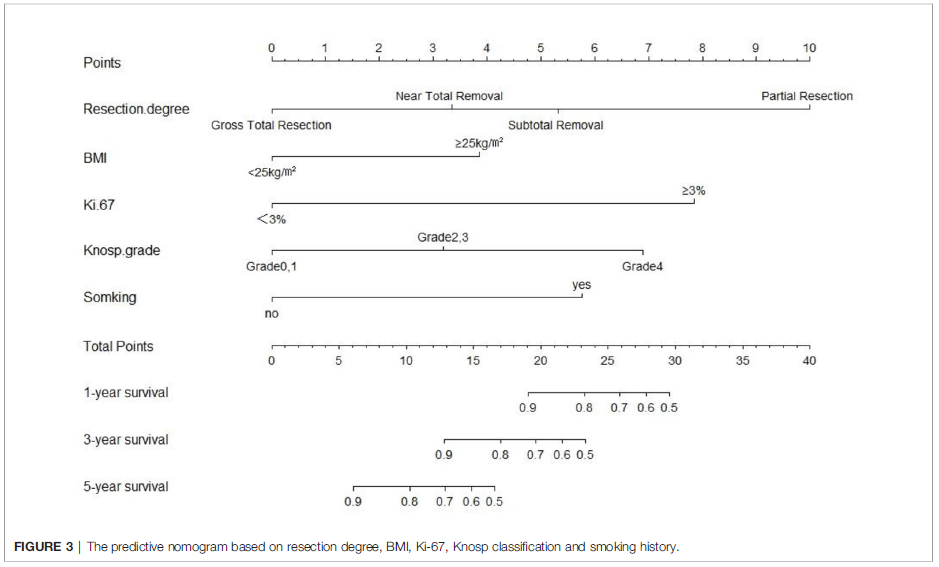
图3. 基于切除程度、BMI、Ki-67、Knosp分级和吸烟史的预测列线图。

4
Front Endocrinol (Lausanne). 2021 Dec 17;12:774686. doi: 10.3389/fendo.2021.774686.
IF=3.644
侵袭性垂体腺瘤(APAs)对多模式治疗方法应答不佳,替莫唑胺已越来越多地被用于APAs患者,但缺乏证据支持其早期使用。本研究发表在《Front Endocrinol(Lausanne)》杂志上,是一项单中心研究,纳入所有接受至少3个周期替莫唑胺(150–200mg/m²)治疗的APAs患者。记录患者基线临床生化和放射学特征。对细胞周期标志物O6-甲基鸟嘌呤DNA甲基转移酶(MGMT)、MutS同源物2(MSH2)、MutS同源物6(MSH6)、MutL同源物1(MLH1)和减数分裂后分离时增加2(PMS2)进行免疫组化评估,并计算h评分(阳性细胞数和染色强度的乘积)。采用RECIST标准对影响学反应进行评估。疾病控制的患者(肿瘤体积缩小≥30%)被归类为应答者。研究发现,共纳入的35例患者(肢端肥大症48.6%、泌乳素腺瘤37.1%和无功能垂体腺瘤14.3%)中,应答者占队列的68.6%,更有可能为功能性肿瘤,MGMT阳性染色细胞比例较低,MGMTh评分较低。与应答者相比,无应答者起始TMZ治疗的时间明显更长(中位数36个月vs.15个月,p=0.01)。低至中等MGMT阳性(40%的肿瘤细胞),MGMT h评分为80,对预测应答的灵敏度超过80%,特异性超过70%。总之,早期开始TMZ治疗,对功能性肿瘤和MGMT h评分较低的APAs,可预测APAs患者对TMZ的良好应答。
5
肢端肥大症患者肌肉和脂肪的可逆性胰岛素抵抗,与代谢综合征无相关性
EBioMedicine. 2022 Jan;75:103763. doi: 10.1016/j.ebiom.2021.103763.
IF=5.736
活动性肢端肥大症患者会表现出胰岛素抵抗,而控制疾病可提高胰岛素敏感性,并增加脂肪重量。这一看似矛盾的结果其背后的机制尚不清楚,但生长激素诱导脂肪分解在其中发挥了主要作用。本研究发表在《EBioMedicine》杂志上,目的是探讨肢端肥大症患者胰岛素抵抗的分子机制与肥胖无关。这是一项前瞻性研究,纳入21例肢端肥大症新确诊患者,通过手术(n=10)或生长抑素类似物(SA)治疗(n=11)获得疾病控制后,评估患者的身体成分(DXA扫描)、全身和组织特异性胰岛素敏感性、以及脂肪组织和骨骼肌中的GH和胰岛素信号。研究结果发现,肢端肥大症的疾病控制显著降低了瘦体重(p<0.001),增加了脂肪重量(p<0.001)。确诊时,在肌肉和脂肪中检测到生长激素调节基因(CISH和IGF-I)的表达增强。而无论采用何种治疗方式使疾病控制后,骨骼肌、肝脏和脂肪组织中的胰岛素敏感性均增加,这与肌肉和脂肪中胰岛素信号增强有关,包括磷酸酶和张力蛋白同系物(PTEN)的下调,同时,脂肪中GH和脂解激活剂的信号降低。因此,该研究支持过度的脂肪分解是活动性肢端肥大症胰岛素抵抗的一个主要特征,其特点是PTEN上调、和肌肉和脂肪中胰岛素信号的抑制。
有效期:2023-02-22,资料过期,视同作废。
声明:脑医汇旗下神外资讯、神介资讯、脑医咨询所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。

![]()



![]()

![]()


![]()
![]()




