病例
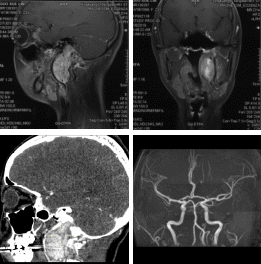
患者,女性,23岁,因“发现颈部包块7年,头痛两周”入院。7年前因左侧腮腺炎对症治疗,好转后仍有左侧颈部包块,误认为肿大淋巴结故未予重视。两周前因头痛行CT检查,提示颈静脉孔区占位。为求手术治疗转入我院。查体:左侧上颈部可触及一直径4cm质韧肿块,边界清,活动度尚可,伸舌左偏,可见左侧舌肌萎缩和纤颤,余NS(-)。我院MRI提示:左侧颈静脉孔区沟通性病变,增强后明显强化,颈静脉孔区骨质破坏明显,颈内动脉和颈外动脉呈高脚杯样改变。
治疗经过和随访
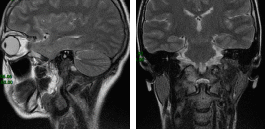
考虑到肿瘤颅内外沟通,遂采用颅颈联合入路,首先暴露颈部肿瘤全程,见肿瘤起源于颈总动脉分叉处,和颈总动脉及颈内动脉粘连紧密,沿颈动脉鞘向上扩展,经颈静脉孔突入颅内。术中严着肿瘤包膜仔细分离肿瘤和血管界面,但肿瘤和颈总动脉分叉部粘连紧密,少许残留。舌下神经被肿瘤包裹难以分离,遂予以离断。切除颈部肿瘤后打开颈静脉孔切除颈静脉孔内及颅内部分。手术顺利,术后有轻微声音嘶哑,三个月随访时症状明显改善。术后病理证实为颈动脉体瘤,截至随访时未见肿瘤进展。
讨论
颈动脉体瘤(carotid body tumor, CBT)是一种临床罕见的高度血管化、缓慢扩张的化学感受器肿瘤,起源于颈动脉分叉处的神经节旁组织,属于副神经节瘤,约占头颈部副神经节瘤发病率的65%,占全身肿瘤的0.03%。该病好发年龄40~50岁,女性多见,多为单侧发病,良性病变居多,约5%的病变可发生恶变。
CBT患者多以无意中发现颈部无痛性肿块就诊,肿块多数生长缓慢,可扪及搏动感,轻压肿块可以引起心率加快。因肿瘤下方有颈动脉鞘限制其生长,所以多向上及两侧发展,肿瘤不断生长侵犯迷走神经或交感神经时可引起声带麻痹或Horner综合征,累及颈静脉孔区可表现为颈静脉孔综合征。多数CBT都是无功能性的,功能性肿瘤患者偶尔出现阵发性的高血压、心悸、头痛和多汗等儿茶酚胺水平升高的表现。
CBT的术前诊断主要依赖影像学,严禁穿刺活检或组织活检。CT平扫呈软组织密度肿块,密度均匀,增强扫描明显强化,可见动脉壁骨质侵蚀性破坏。MRI平扫T1WI上肿瘤呈等、稍高信号,T2WI呈不均匀高信号,其内可见血管流空,肿瘤边缘清晰,增强后明显强化。CTA或MRA对CBT的诊断具有重要的价值,三维重建后可以发现病变起源于颈动脉分叉处多数呈纵向长梭形生长,颈动脉分叉角度开大,颈内外动脉受压推移形成特征性的“高脚杯征”。李树玲等提出了CBT具有独特的三主征:①颈前三角区肿瘤;②颈动脉向浅侧移位;③颈内与颈外动脉分离。
手术是CBT唯一公认有效的治疗方法,但因其解剖结构复杂,血供丰富,手术难度大,术后并发症多。
Shamblin等将CBT分为三级:I级瘤体局限于颈动脉分叉处,与动脉壁无粘连;Ⅱ级瘤体部分包绕颈动脉分叉处血管,与颈动脉壁部分粘连;III级瘤体完全包绕颈动脉分叉周围的颈动脉,并与颈动脉粘连紧密。II级和III级患者术后并发症明显高于I级。此外,CBT瘤体距颅底距离每缩短1.0cm,术中出血量增加1.8倍,颅神经损伤的风险增加1.5倍。因此,累及颈静脉孔区的颈动脉体瘤尤其富于挑战。手术难点主要在于术中出血的控制,颈动脉血管的保护或重建,颈部及颅底神经的保护。术前DSA和BOT评估对于手术规划有着重要的价,术前供血动脉栓塞可以显著减少手术中出血,降低风险。ShamblinI级的病变多可以完整从颈内动脉上分离下来。ShamblinII级和III级颈内动脉损伤的风险则相对较高,如术前DSA提示患侧颈内动脉闭塞或者BOT试验代偿良好,术中可以直接结扎颈内动脉;否则则需考虑自体或人工血管重建。术中严格按照肿瘤包膜锐性分离有助于避免神经损伤。





