
德国癌症研究中心的Stefan Gröschel等通过全外显子组和基因组测序发现11例晚期脊索瘤可能存在缺陷性同源重组DNA修复和影响HR相关基因变化的基因组模式,例如BRCA2、NBN、CHEK2缺失和病原种系变异。在72.7%的标本中出现HR缺陷相关的突变特征,与基因组不稳定性共发展,文章发表在2019年4月的《Nature Communications》在线。
——摘自文章章节
【Ref: Gröschel S, et al. Nat Commun. 2019 Apr 9;10(1):1635. doi: 10.1038/s41467-019-09633-9.】
研究背景
结论
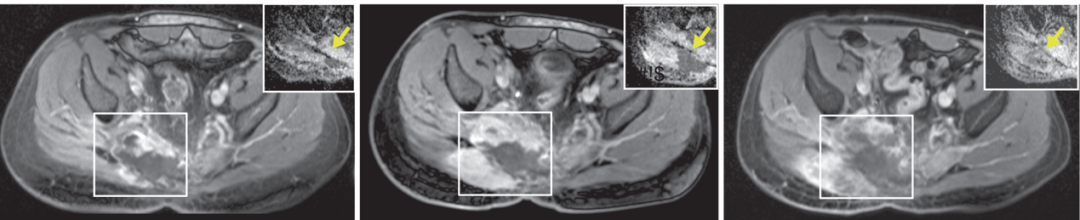
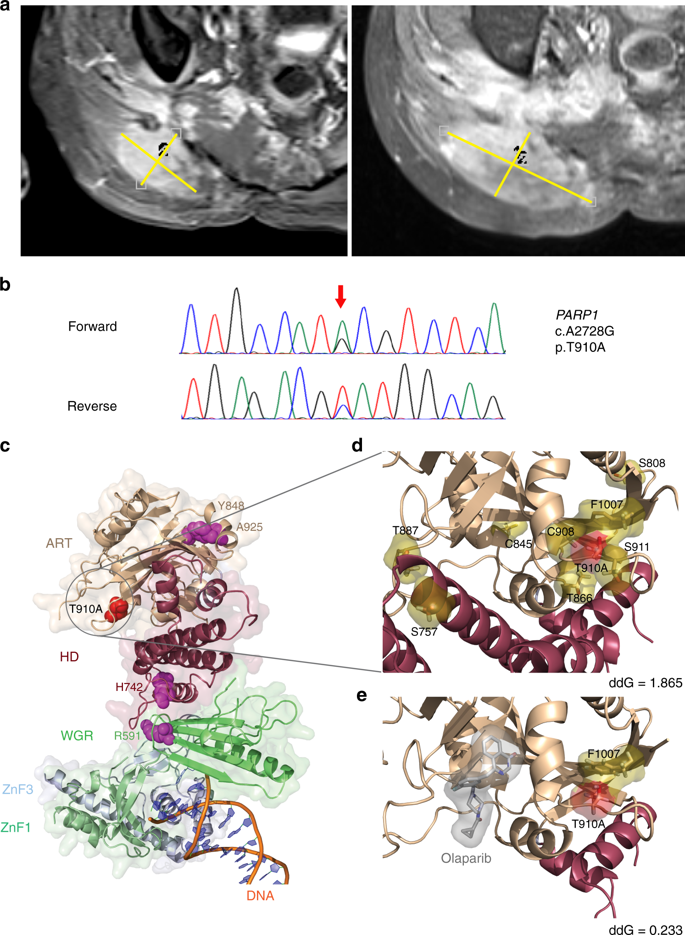
图2. 应用Olaparib治疗脊索瘤发生耐药性。a.Olaparib治疗7个月(疾病稳定;左图)和10个月(疾病进展;右图)后的MRI成像。b.在进展时活检取样,行全基因组测序。通过Sanger测序发现PARP1外显子20中的错义突变。c、d、e.与DNA结合的p.T910A突变PARP1的结构图。






