美国德克萨斯大学休斯顿健康科学中心McGovern医学院Vivian L. Smith神经外科部的Eun S. Park等在小鼠实验模型研究过度激活的内皮细胞KRAS基因引发脑动静脉畸形,结果发表在2021年3月的《Annals of Neurology》在线。
——摘自文章章节
【Ref: Park ES, et al. Ann Neurol. 2021 May;89(5):926-941. doi: 10. 1002/ana.26059. Epub 2021 Mar 22.】
脑动静脉畸形(bAVM)是儿童和年轻人发生出血性卒中和神经功能障碍的主要原因。95%以上的bAVM呈散发性,无家族史,发病机制未知;目前无有效的药物治疗,因此给治愈带来困难。在癌症研究中,经常观察到KRAS基因突变;KRAS基因属调节细胞功能的RAS蛋白亚家族;KRAS的突变、过度激活下游信号可导致细胞生长和分裂异常。最近,有报道称60%的散发性bAVM患者手术切除的畸形血管团中发现体细胞激活KRAS突变,包括KRAS p.Gly12Val(KRASG12V)。也有研究报告在部分散发的bAVM患者内皮细胞上检测到KRAS突变。由此认为,KRAS突变可能与bAVM的发生相关。美国德克萨斯大学休斯顿健康科学中心McGovern医学院Vivian L. Smith神经外科部的Eun S. Park等在小鼠实验模型研究过度激活的内皮细胞KRAS基因引发脑动静脉畸形,结果发表在2021年3月的《Annals of Neurology》在线。研究者给5周龄小鼠静脉注射新的靶向脑血管内皮的腺相关病毒(AAV-BR1);8周后,通过组织学和分子学观察bAVM的形成及其特征。同时,采用曲马替尼抑制KRAS下游信号表达,进一步分析AAV-BR1对bAVM发生的诱导过程。实验结果发现,病毒介导的KRAS过表达参与bAVM的形成,这一现象在大动脉瘤的发生中尤其明显(图1)。
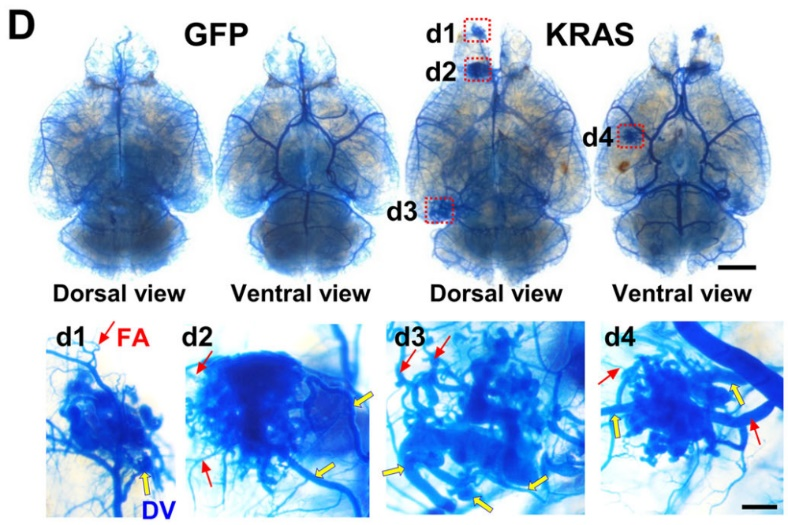
图1. 注射AAV-BR1-KRASG12V 9周后的大脑图像,显示缠结和扩大的脉管系统、供血动脉(FA;红色细箭头)或引流静脉(DV;黄色粗箭头)。从不同方向(背侧、腹侧、背侧和侧向)进行观察,并与小鼠血管图谱中正常血管解剖结构相比。实验动物bAVM形成模型中,伴有局灶性血管生成、脑出血、血管成分改变、神经炎症和感觉/认知/运动功能受损等现象,同临床接近。临床取得的病理标本,其KRAS过表达也跟动物实验基本一致。研究者利用曲马替尼阻断KRAS下游的MEK/ERK途径可以有效抑制bAVM的生长。作者最后指出:KRAS突变可能通过MEK/ERK途径促进bAVM的发生和发展。该研究提供的新bAVM小鼠模型,也有助于为bAVM患者制定治疗策略。

声明:脑医汇旗下神外资讯、神介资讯、脑医咨询所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。









