

不知小伙伴们发现没有,美国漫威的超级英雄美国队长、绿巨人、蜘蛛侠、蚁人、金刚狼、神奇四侠等等,他们的超能力并不是与生俱来,也不是勤学苦练而成,而是靠基因变异获得的。比如被视为美国精神象征的美国队长,原本是一名身体瘦弱的年轻人,在接受“改造”后,成为各项体能都远超常人的“超级战士”;再比如蜘蛛侠,原为美国的一名普通学生,由于意外被一只受过放射性感染的蜘蛛咬到,因此获得了和蜘蛛一样的超能力、超人般的耐力、反应、敏捷和速度……

这些超级英雄的形象塑造于上世纪五六十年代,那时候没有太多人去追究超能力获得的科学依据。不过近两年的剧中加入了CRISPR 基因编辑技术的科学背景。

《X档案》中对 CRISPR 基因编辑的涉及
获得超能力显然不能当真,但 CRISPR 基因编辑技术是真实存在的,而且也确实将一些科幻情节变成了现实。
让我们先来简单介绍一下这个神奇的CRISPR-Cas基因编辑技术吧。
CRISPR-Cas原本是细菌的免疫系统,能够提取外来入侵病毒等病原的特征,从而当病原二次入侵时能及时识别消灭。具体来说,细菌的DNA序列中有一段叫做CRISPR的基因序列,其中包含着很多历代祖辈曾经遇到过的坏蛋病毒的基因片段,附近住着“剪刀手”Cas9蛋白的基因,该蛋白可将识别的DNA切掉,发挥它们“卫士”的作用。经过科学家们的改造,CRISPR-Cas便成为我们编辑基因的工具了。比如,这套工具中,有一段能够识别DNA链中“错别字”的序列——sgRNA,在它的引导下,Cas9蛋白便会切断这个位置,断裂的DNA在体内是不稳定的,于是机体启动修复机制,根据提供的“模板”,将“错别字”更正过来。
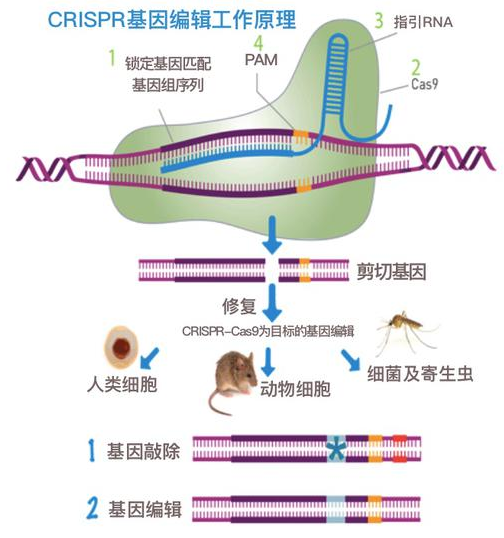
以往CRISPR-Cas9工具存在编辑效率不足、安全性低下等问题,而新型单碱基编辑器ABE和CBE的出现,克服了以上弊端,使得基因编辑更加高效、精准。科学家们已将这一利器应用于小鼠模型中并获得了振奋人心的效果,但在非人灵长类动物模型中,对如何将这一工具递送进去,以及它的治疗效果仍然知之甚少,严重限制了单碱基编辑技术在临床治疗中的应用。

2021年5月19日,美国Verve Therapeutics公司的Sekar Kathiresan团队在《Nature》发表题为“In vivo CRISPR base editing of PCSK9 durably lowers cholesterol in primates”的论文。文章成功的利用脂质纳米颗粒(LNPs)将单碱基编辑工具ABE导入了非人灵长类模型中,并利用这种方法实现了PCSK9基因剪接位点的单碱基精准编辑并有效降低了低密度脂蛋白的水平,这为单碱基编辑在临床中的应用奠定了基础。

PCSK9是降血脂和预防心血管疾病的重要靶点。研究者的思路是,用单碱基编辑工具ABE精准编辑PCSK9的基因剪接位点,最终持久抑制PCSK9的表达。为此,研究者首先根据ABE的活性窗口和PCSK9剪接受体/供体位点的序列特征,设计出20条gRNAs。随后研究者通过脂质纳米颗粒转染ABE的 mRNA/gRNA的方式在人原代肝细胞、食蟹猴原代肝细胞及小鼠肝脏中筛选出了最优gRNA——靶向PCSK9基因1号外显子剪接供体的PCSK9-1 gRNA,编辑效率达到了60%(图1)。
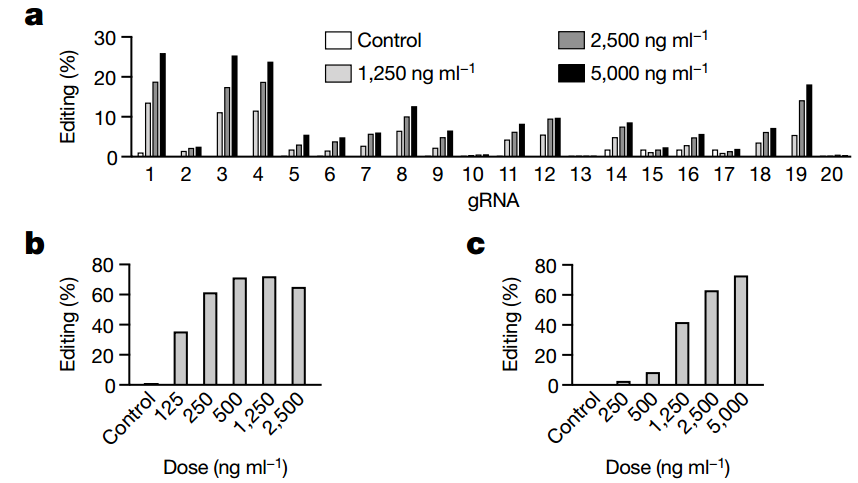
图1. 在人原代肝细胞、食蟹猴原代肝细胞及小鼠肝脏中筛选出最优gRNA
插一句,这里用到的脂质纳米颗粒(LNPs)是可以保护RNA,并帮助它们进入机体细胞的“好帮手”,它可是目前能将大名鼎鼎的mRNA新冠疫苗递送到体内发挥保护作用的“大功臣”(图2)[1]
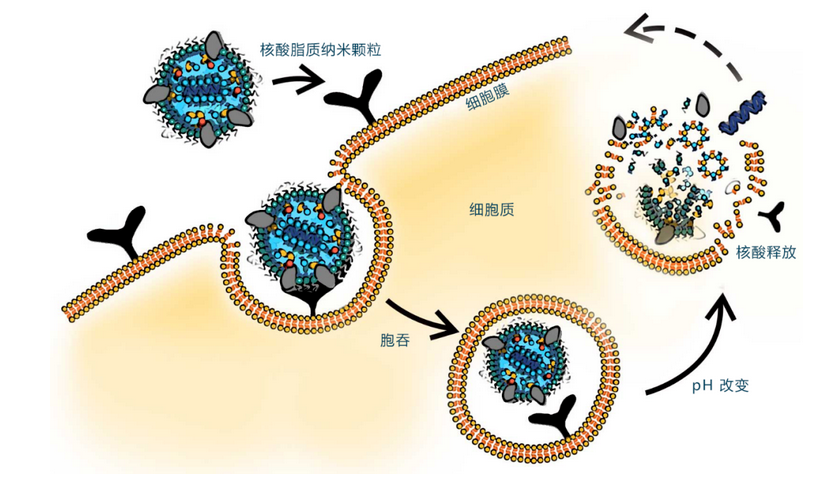
图2. LNP携带的RNA进入细胞,并且释放的过程
筛选好了sgRNA,研究者便开始开展非人灵长类模型的研究,用食蟹猴对其效果进行检测。结果显示,治疗后食蟹猴肝脏中PCSK9靶位点的编辑效率可达63%,血液中PCSK9蛋白降低81%,低密度脂蛋白(LDL)胆固醇水平降低65%,这表明脂质纳米颗粒介导的单碱基编辑技术可实现食蟹猴肝脏中PCSK9靶位点的高效精准编辑并具有潜在的治疗意义(图3)。
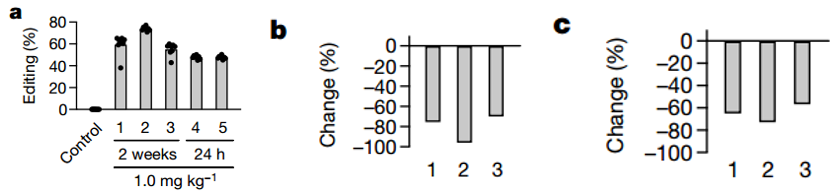
图3. 食蟹猴中对PCSK9的短期编辑效果、PCSK9表达及LDL胆固醇水平
之后,文章还分析了PCSK9基因编辑后PCSK9和LDL胆固醇水平降低的持久性。结果显示,治疗一周后血液中PCSK9水平、LDL胆固醇和脂蛋白的水平会显著降低,且可持续至少8个月(图4)。文章还开展了一项持续至今的长期研究根据LNPs剂量检验食蟹猴对单碱基编辑的药物耐受性。结果显示,治疗后,肝脏指标AST和ALT会有瞬时中度上升,但两周后恢复正常。此外食蟹猴并无其它异常。
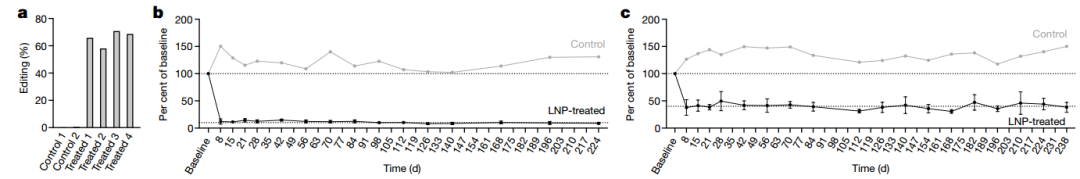
图4. PCSK9基因编辑后PCSK9和LDL胆固醇水平降低的持久性
目前单碱基编辑工具在DNA水平和RNA水平可能存在不同程度的脱靶风险。脱靶效应也就是,在识别错别字的时候,可能会误伤其他正常的DNA序列(图5)。

图5. 脱靶效应(转自科普中国)
为此,研究者对ABE在DNA水平的脱靶效应进行分析。借助于新的脱靶分析方法ONE-seq和定向PCR扩增测序,文章发现肝细胞和肝脏组织中仅1处位点有较明显的脱靶效应但脱靶位点的编辑效率<1%(图6-7)。RNA水平的脱靶效应发现,其在RNA水平并无明显的脱靶效应(图8)。以上结果表明,非人灵长类动物中,通过LNPs递送的ABE单碱基编辑有较高的安全性。
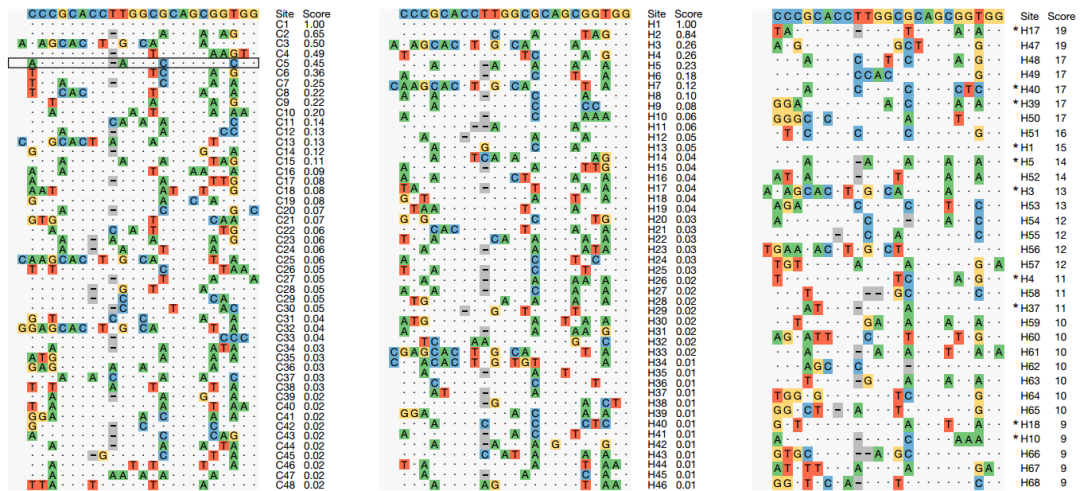
图6.分析食蟹猴原代肝细胞、肝组织及人原代肝细胞的脱靶位点
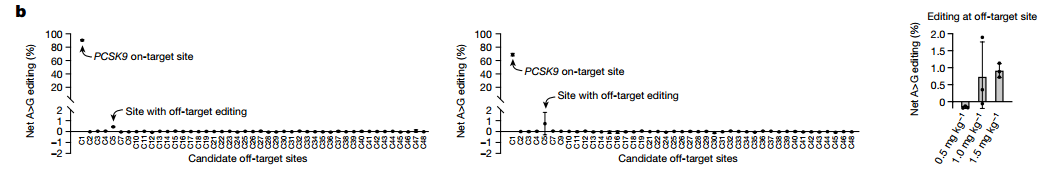
图7.DNA水平脱靶分析
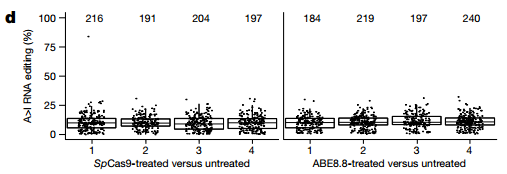
图8. RNA水平脱靶分析
此外,《Nature Biotechnology》杂志还发表“In vivo adenine base editing of PCSK9 in macaques reduces LDL cholesterol levels”的文章,该研究也是借助于LNP递送ABE系统,在小鼠和非人灵长类动物中成功实现了肝脏组织中PCSK9基因的精准编辑,最终有效降低了血液中PCSK9和LDL蛋白的含量[2]。
总的来说,利用脂质纳米颗粒LNPs递送单碱基编辑工具ABE在非人灵长类动物中的编辑效果非常好,这也是研究者首次在非人灵长类动物体内开展单碱基编辑治疗的研究,对推动单碱基编辑技术在疾病治疗中的应用有重要意义。
所以,人类的超级英雄梦还会远么?

原文链接:
https://doi.org/10.1038/s41586-021-03534-y

参考文献:
[1] Aldosari, B.N., I.M. Alfagih, and A.S. Almurshedi, Lipid Nanoparticles as Delivery Systems for RNA-Based Vaccines. Pharmaceutics, 2021. 13(2).
[2] Rothgangl, T., et al., In vivo adenine base editing of PCSK9 in macaques reduces LDL cholesterol levels. Nat Biotechnol, 2021.
复旦大学脑科学转化研究院

官网:itbr.fudan.edu.cn
邮箱:itbr@fudan.edu.cn
扫码关注我们
1

声明:脑医汇旗下神外资讯、神介资讯、脑医咨询、AiBrain所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。






