
本次Grand Round聚焦于癫痫的相关研究。Theodore H. Schwartz教授首先提出目前癫痫治疗面临的问题是如何准确定位并切除引起癫痫的病变神经元,同时尽量减轻对正常脑功能的影响。接着他介绍了基于立体三维脑电图(SEEG)的癫痫网络模型。癫痫网络为参与癫痫活动产生和传播的大脑区域,其中节点代表电极位置,边代表联系强度。癫痫网络模型能够更好地描述癫痫发作动力学的复杂性,并真实地描述大脑中致痫病变的分布。我们可以在皮层和皮层下脑区癫痫发生和传播的过程中,依据SEEG分析得到大脑连接的显著变化。这对于癫痫手术治疗意义重大。
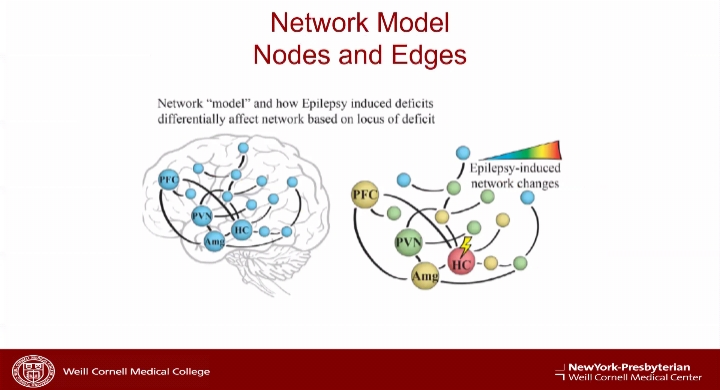
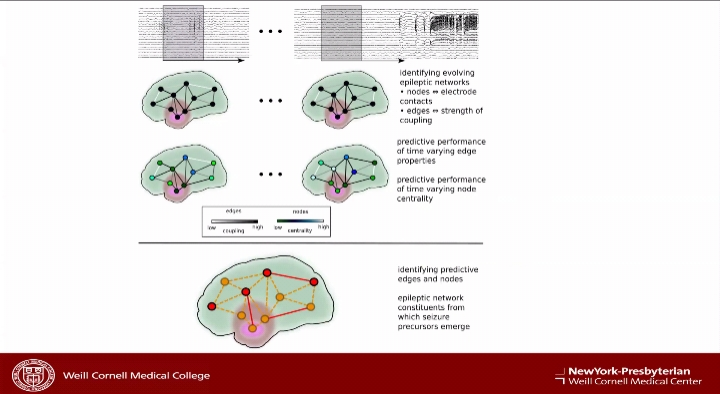
之后,Theodore H. Schwartz教授指出目前癫痫研究中的焦点,包括创建慢性局灶性新皮质癫痫小鼠模型,利用钙成像技术在单细胞和小群体水平上绘制兴奋性和抑制性中间神经元图谱,绘制癫痫病灶发展过程中的多节点图谱,确定节点上下游可能对癫痫发作发挥作用的细胞类型,以及如何调控节点以改变癫痫发作的起始和传播等前沿问题。
接下来Theodore H. Schwartz教授分享了本次Grand Round的主要内容,即多学科合作在癫痫研究中的重要作用,其领域涉及生物医学工程学、生理和生物物理学以及神经病学等学科。
多处软脑膜下横切术是一种治疗癫痫的外科手术,康奈尔大学生物医学工程学博士Chris Shaffer拓展了这一手术概念,他所从事的研究工作为双光子激光软膜下横切以阻断癫痫的传播。基于双光子聚焦原理,于皮层下第2-3细胞层利用激光在显微尺度下平行或垂直于皮层切割,其切割宽度随着皮层下的深度呈指数减少,而最大切割深度随激光能量呈对数增加。
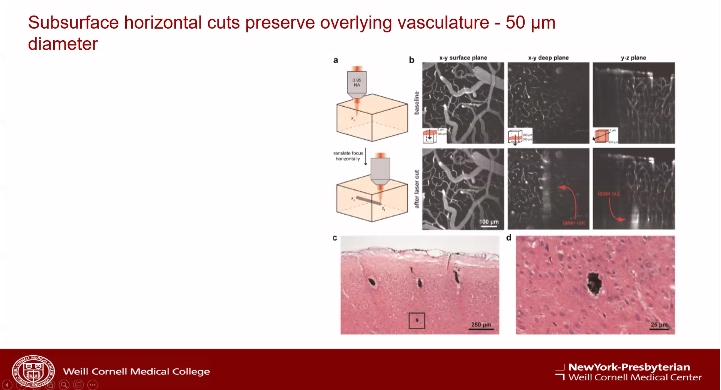
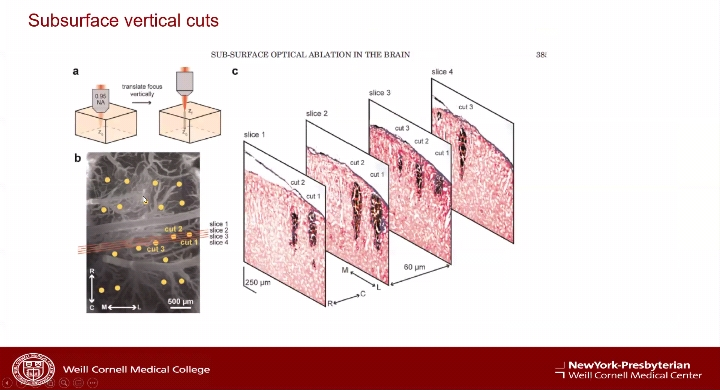
康奈尔大学生理和生物物理学博士Emre Aksay的研究侧重于全脑单细胞兴奋性和抑制性细胞成像。哥伦比亚大学神经病学博士Cathy Schevon则进行了急性和慢性小鼠癫痫模型癫痫发作和传播的多单元记录和成像,在4-氨基吡啶(4-AP)癫痫模型中,使用多电极阵列和双光子钙成像来研究癫痫的发作及传播。
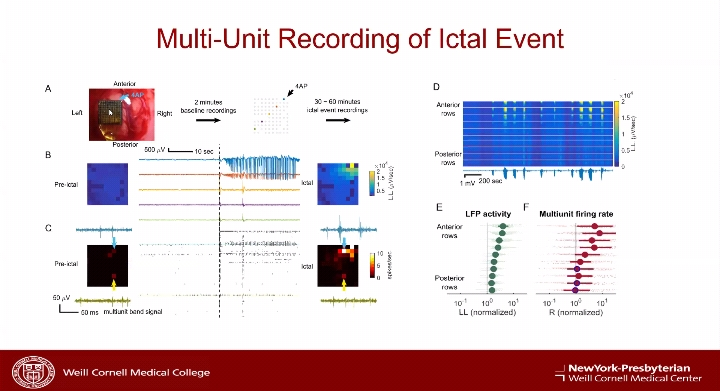
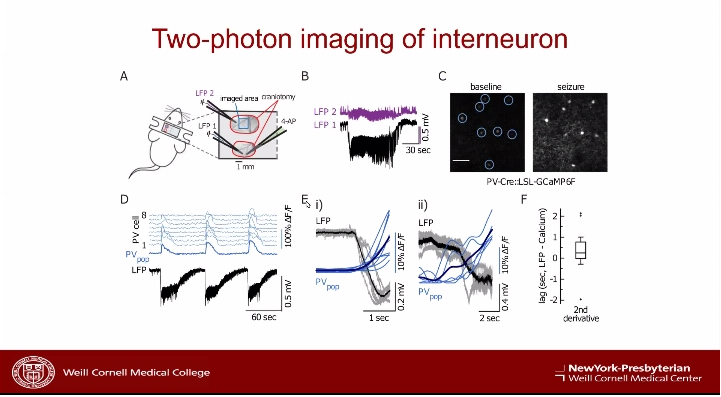
研究发现,虽然发作性神经元爆发传播不超过2-3mm区域,但它们与半球宽场电位波动和病灶外的中间神经元活动有关。在离病灶较远的部位使用药物抑制抑制性神经元活动可导致癫痫网络的形成,证明痫性网络传播可由局部抑制神经元缺陷引起,并且癫痫网络可以在正常大脑结构的背景下出现,而不需要病变位点之间的病理联系。
结合Chris Shaffer博士的研究,激光软脑膜下横切后,癫痫起始和传播分数均明显下降,癫痫的波幅和持续时间下降,证明显微横切显著减弱了癫痫的传播,体感功能基本保存。研究进一步分析了激光切割强度对正常脑功能的影响。结果提示重度烧灼及局部毁损会严重影响正常脑功能,且远期恢复不理想。而常规切割强度对远期脑功能无严重损害。
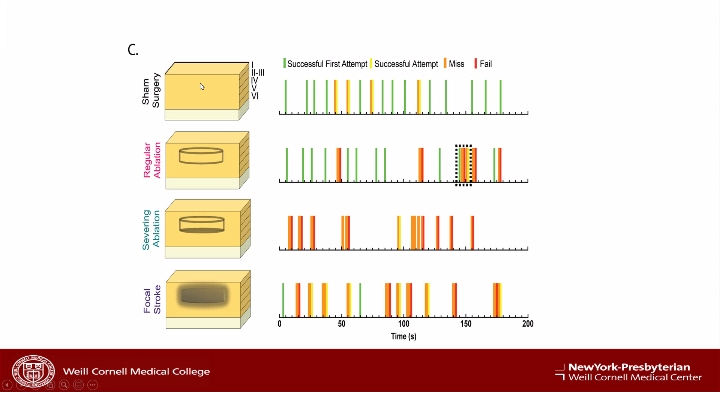
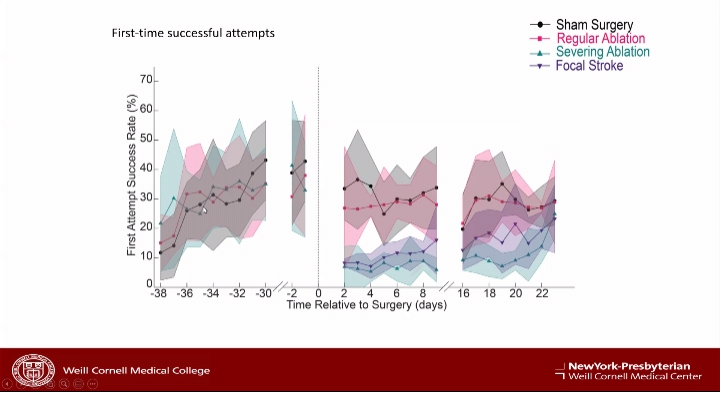
最后Theodore H. Schwartz教授做出总结,癫痫通过局部回路以及连接节点的长距离通路在大脑中传播,涉及兴奋性和抑制性神经元之间复杂的相互作用。通过皮层下第2-3层细胞层的精确横切可以降低急性和慢性小鼠癫痫模型中痫性发作的发生和传播,同时最大限度地减少对垂直方向神经连接的损害。未来有可能开发一种设备来进行有限的皮层下第2-3层细胞层横切,以帮助治疗源于大脑功能区的难治性癫痫。
(本文由高连升主治医师整理,洪远主任医师审校,张建民主任终审)





