![]()
《Experimental and Clinical Endocrinology & Diabetes》杂志2021年3月刊载[ Mar;129(3):146-156.] 德国Wolfgang Saeger,和 Arend Koch撰写的综述《垂体瘤2017年WHO新分类的临床意义。Clinical Implications of the New WHO Classification 2017 for Pituitary Tumors 》(doi: 10.1055/a-1310-7900. )。

根据垂体瘤WHO2017年分类,腺瘤不仅根据垂体激素的结构和免疫染色进行分类,还根据垂体转录因子Pit-1、T-pit和SF-1的表达进行分类。通过这些因素,我们可以确定三种细胞谱系:Pit-1代表生长激素、泌乳素和TSH细胞谱系,T-pit代表ACTH细胞谱系,SF-1代表促性腺激素细胞谱系。
根据这一原则,所有分泌生长激素和/或泌乳素的腺瘤和所有分泌TSH的腺瘤必须为Pit-1阳性,所有促肾上腺皮质激素细胞性腺瘤,T-pit为阳性,所有促性腺激素细胞腺瘤SF-1为阳性。
在没有垂体激素表达的腺瘤中,必须进行转录因子免疫染色检查。如果这些结果也是阴性,则符合内分泌不活跃零细胞腺瘤的标准。如果一项转录因子是阳性的,相应的细胞谱系表明腺瘤有潜在的激素活性。因此,有Pit-1表达的激素阴性的腺瘤可以解释肢端肥大症、高泌乳素血症或TSH功能亢进。T-pit阳性的激素阴性的腺瘤可诱发库欣病,SF-1阳性的激素阴性的腺瘤提示促性腺激素细胞腺瘤。
与WHO 2004年分类中删除的不典型(atypical)腺瘤不同,现在(WHO 2017年分类)的标准是确定预后较差的进袭性(aggressive)腺瘤。一些腺瘤亚型被描述为“本身(per se)”是进袭性的,而不需要增加增殖性的形态学标志。如果其他腺瘤亚型表现出增殖性增加(有丝分裂,Ki-67指数>3-5%,肿瘤临床快速生长)和侵袭性,也必须被认定具有进袭性。根据这些标准,约有三分之一的垂体腺瘤属于进袭性腺瘤,预后可能较差。
只在有转移出现时,非常罕见的垂体癌(占垂体瘤的0.1%)才被定义。其中许多是在分泌泌乳素或促肾上腺皮质激素的腺瘤多次复发后发生的。
垂体腺瘤的临床表现和组织学分类之间的相关性是非常重要的,因为每一个差异都必须在临床医生和病理学专家之间进行讨论。根据德国垂体肿瘤登记处的数据,本综述给出了一个相关性肿瘤检查列表。
流行病学
垂体腺瘤是常见的肿瘤,约占一般人群的17。居于脑膜瘤和胶质瘤之后,是神经外科门诊中第三位常见的颅内肿瘤。在成人中,大多数垂体腺瘤是分泌泌乳素的(45-65%),其次是无功能腺瘤(15-37%)。对尸检垂体的未作选择的多个系列研究的调查显示占8-26%。这些主要是分泌泌乳的素腺瘤,其次是促性腺激素细胞腺瘤。临床上显著的垂体腺瘤很少发生,只发生在0.1%左右的一般人群中。每个年龄都可受累,而在40到50岁之间出现高峰,但是垂体腺瘤在儿科人群中比较罕见,占接受脑部成像的儿童的0.2%。在儿童,分泌促肾上腺皮质激素的和泌乳素的腺瘤是最常见的亚型。性别分布非常类似,但在年龄较大的男中(in higher ages men)性占多数(over-respansented),而女性在45岁之前更为常见。
分类
正常垂体腺的发育依赖于谱系限制性( lineage- restricted)转录因子(PIT-1, T-PIT, SF-1),这些转录因子将腺垂体祖细胞(progenitor)分化为嗜酸性( acidophilic)、促肾上腺皮质激素细胞和促性腺激素细胞谱系。其中,垂体特异性的POU类同源结构域转录因子( the pituitary-specific POU-class homedomain transcription factor,PIT-1)驱动生长激素细胞、泌乳素细胞和促甲状腺激素细胞的分化,而T-box家族成员TBX19 (T-PIT)转录因子负责促肾上腺皮质激素细胞的分化。促性腺激素细胞由类固醇因子1 (SF-1)控制。由于这些谱系限制性转录因子在垂体腺瘤中的表达具有诊断和预后意义,转录因子表达已被纳入更新的WHO内分泌肿瘤分类(2017)的正式分类标准。免疫组织学识别不同腺瘤中的转录因子被添加与垂体激素免疫染色一起,但不能取代它。从三年前的新分类开始,随着引入转录因子免疫染色法,存在许多问题。与以前Ki-67和p53免疫染色的问题类似,现在的这些方法似乎是最可靠的和可重复的( be mostly reliable and reproducible)。在病理组织学日常工作中,大多数垂体腺瘤可不检查转录因子就可作出分类,但对识别零细胞腺瘤和不寻常的或复杂的肿瘤或相关临床状态不足或缺乏的患者( in cases with insufficient or lacking correlation to the clinical status ,)检查转录因子是必不可少的。由于WHO肿瘤分类包含了病理学家的指南,因此要求他们使用最新版本中的WHO分类。以下形态学亚群来自于当前有效的2017年WHO分类。
分泌生长激素的(生长激素细胞)腺瘤(PIT-1阳性)
分泌GH的垂体腺瘤,呈致密或稀疏颗粒性,占垂体腺瘤的15.8%(表1)。生长激素细胞腺瘤的共同特征是核表达PIT-1转录因子,且有最初用电子显微镜识别到的大的分泌颗粒。使用低分子细胞角蛋白(CAM5.2, CK18),它们无疑被区分成致密颗粒性GH细胞腺瘤和稀疏颗粒性GH细胞腺瘤。这两种腺瘤亚型不仅能表达GH,还能表达泌乳素(混合性生长激素细胞亚型或双激素单细胞GH腺瘤),但雌激素受体阴性,而这是泌乳素细胞分化的特征。稀疏颗粒性和致密颗粒性生长激素细胞腺瘤的生长抑素受体2和5 (SSTR2, SSTR5)的膜表达水平不同。虽然已知这些腺瘤对生长抑素类似物有反应,但生长抑素受体(SSTR)表达和治疗反应之间的明确相关性尚不明显。大量研究表明,伴有GNAS突变的分泌GH的腺瘤表现出明显的临床特征,主要为致密颗粒性形态表现,年龄较大,肿瘤体积较小,较少侵袭性生长。此外,还没有明确的证据表明GNAS突变状态是否影响生长激素细胞腺瘤患者对生长抑素的反应。
致密颗粒性分泌GH的腺瘤(8.5%)(表1)呈弥漫性模式,轻度多形性,中等大小或偏大,部分为角状细胞(partly angular cells)。细胞质呈强烈的嗜酸性,且PAS阴性。小到中等大小的核可以是单型的,卵形的,染色质较差,或轻微多形性,染色质丰富。有丝分裂非常罕见或缺乏。GH的免疫染色通常非常强(图1)。与稀疏颗粒性GH腺瘤相比,强烈表达α亚基,而肿瘤细胞的雌激素受体阴性。
表1、转录因子(TF)的细胞谱系和腺瘤类型的频率。
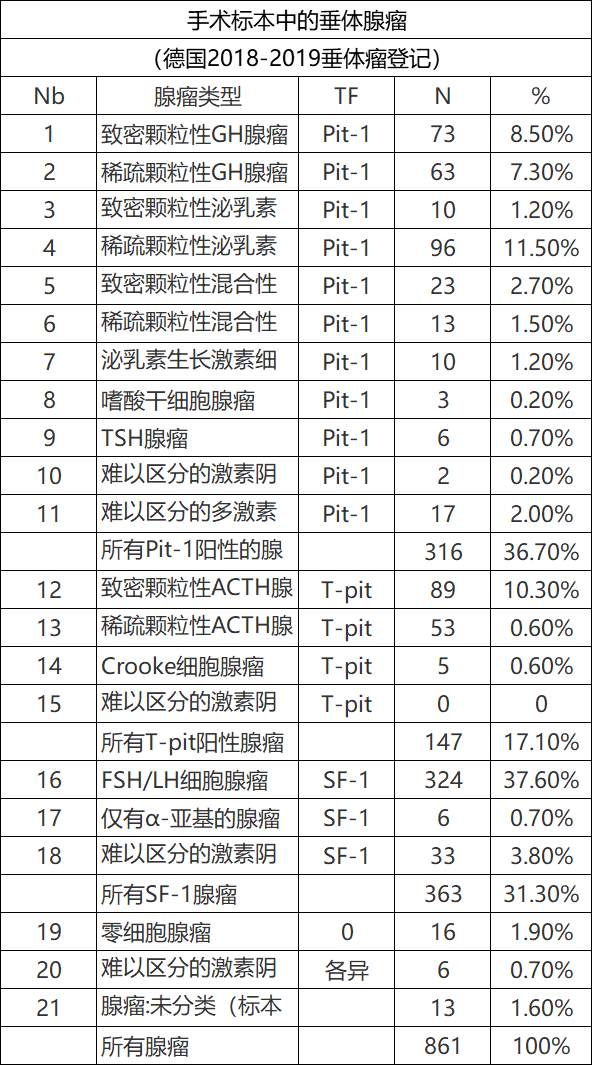
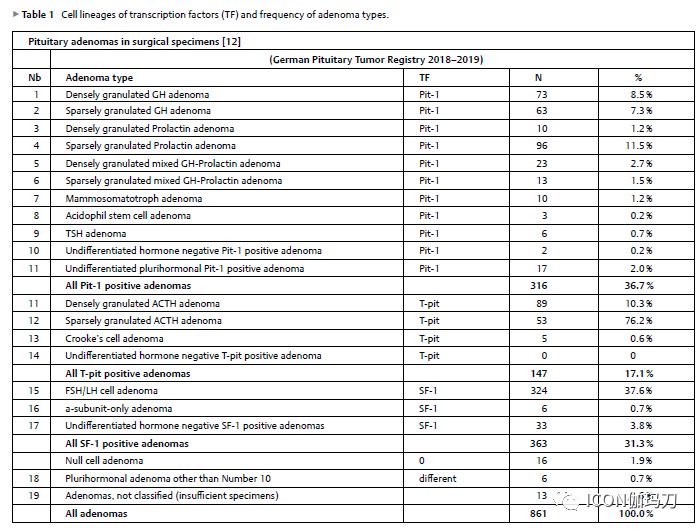
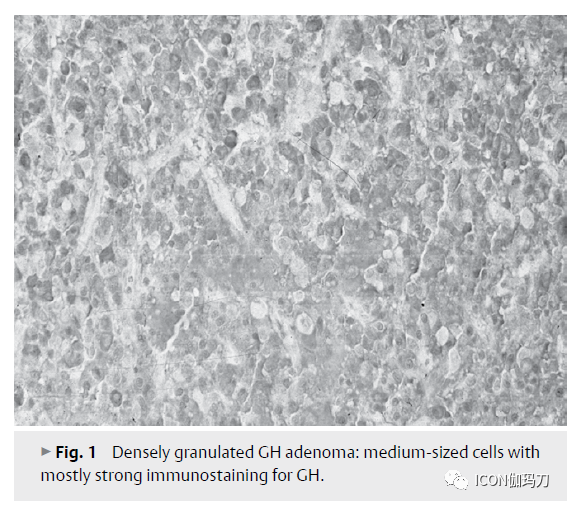
图1、致密颗粒性GH腺瘤:细胞中等大小,GH免疫染色最强。
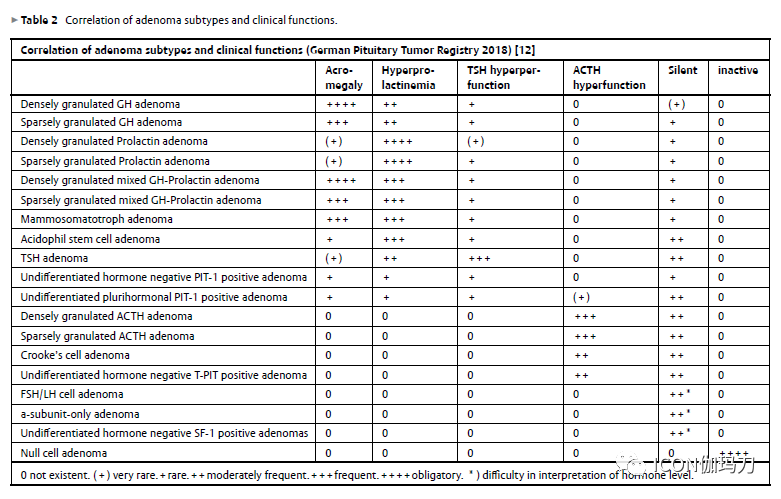
几乎所有有致密颗粒性分泌生长激素的腺瘤的患者都患有肢端肥大症(表2),但根据细胞谱系,可以想象会有TSH或泌乳素的过度分泌。
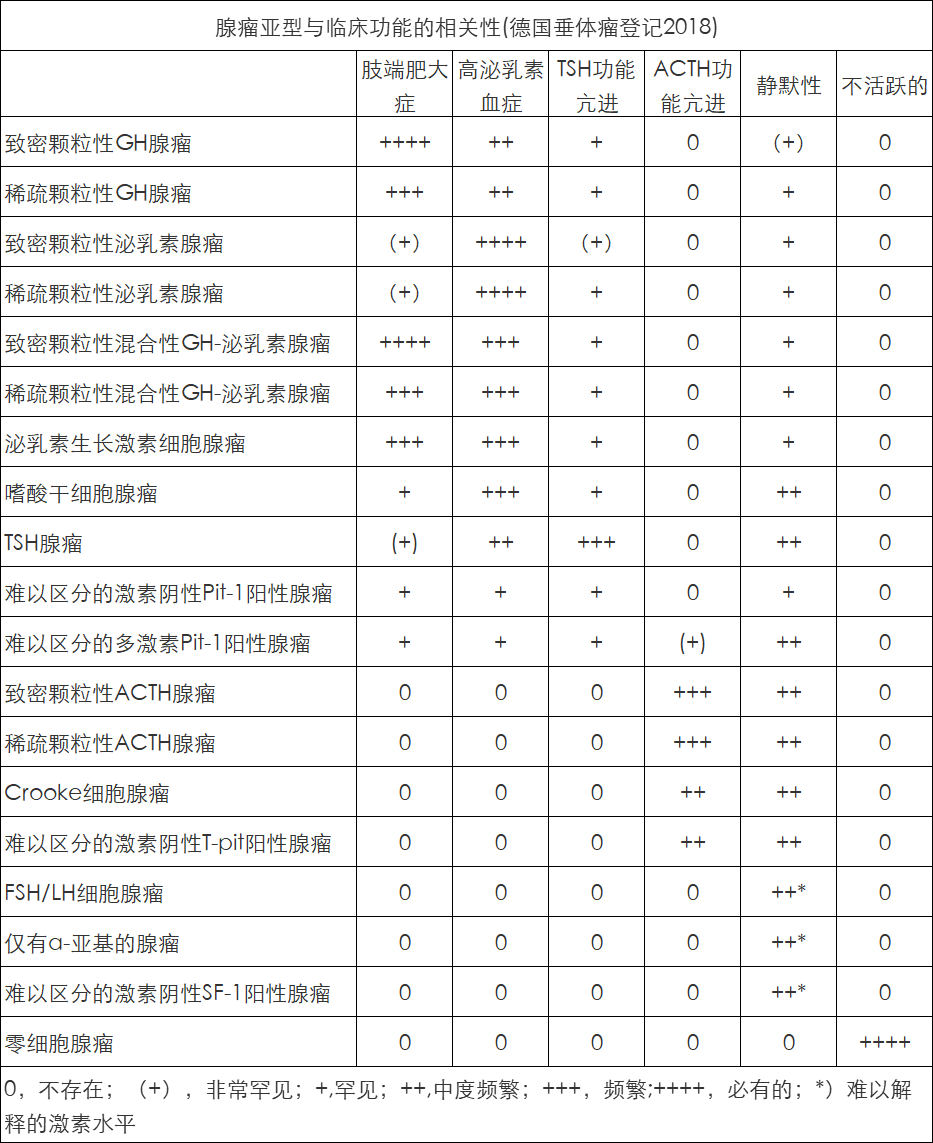
表2、腺瘤亚型与临床功能的相关性。
稀疏颗粒性分泌GH的腺瘤(7.3%)(表1)是由轻微嗜酸性或嫌色性(chromophobic)以及PAS阴性的细胞以弥散模式组成(图2)。稀疏颗粒性GH腺瘤的特征是对应于致密排列的细胞细丝)(cytofilaments)组成的超微结构纤维小体的核旁球形嫌色性小体(图3)。泛角蛋白免疫染色可以证明这一点,尤以细胞角蛋白Cam5.2染色最能证明。70%以上的腺瘤细胞必须含有这些小体,否则不能识别稀疏颗粒性GH腺瘤。稀疏颗粒性生长激素细胞瘤是最常见的“本身”具有进袭性行为的腺瘤(表3)。偏大的肿瘤大小和较显著的侵袭性生长得到描述。
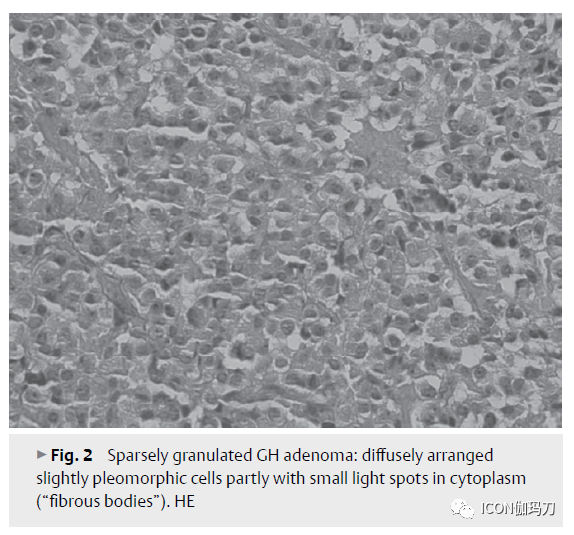
图2、稀疏颗粒性GH腺瘤:细胞呈弥漫性排列,轻微多形性细胞,部分的胞浆中可见小亮点(纤维小体)。HE染色
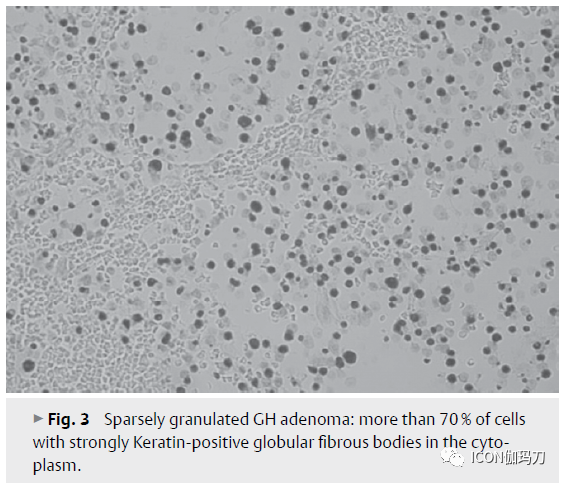
图3、稀疏颗粒性GH腺瘤:70%以上的细胞的胞浆中有角蛋白阳性的球形纤维小体。
大多数稀疏颗粒粒性分泌生长激素的腺瘤可导致肢端肥大症,但少数没有功能亢进或激素水平升高的征象(静默性腺瘤)(表2)。
分泌生长激素和泌乳素的(混合性生长激素-泌乳素细胞)腺瘤(PIT-1阳性)
总比例占5.4%(表1),有三种不同类型分泌GH和泌乳素的腺瘤。都是以核表达PIT-1和雌激素受体(混合性双激素腺瘤)为特征。可以由不同数目的腺瘤细胞集中产生泌乳素和生长激素。双细胞性分泌GH和泌乳素的腺瘤比单细胞腺瘤更具进袭性。在大多数双激素性腺瘤的患者中,肢端肥大症是主要的功能亢进,但许多患者也有高泌乳素血症或TSH分泌超量。
双细胞性分泌生长激素和泌乳素的腺瘤(混合性生长激素泌乳素细胞)由致密颗粒性(2.7%)(图4)或稀疏颗粒性(1.5%)生长激素细胞细胞和稀疏颗粒性泌乳素细胞组成。表达泌乳素的细胞较少,通常雌激素受体阳性,不与对抗α亚基的抗体起反应,而GH阳性细胞较多见。这些腺瘤细胞类型的显微和超微结构特征与单细胞腺瘤类型没有区别。双细胞性生长激素/泌乳素腺瘤的稀疏颗粒性变体属于进袭性腺瘤组(表3)。
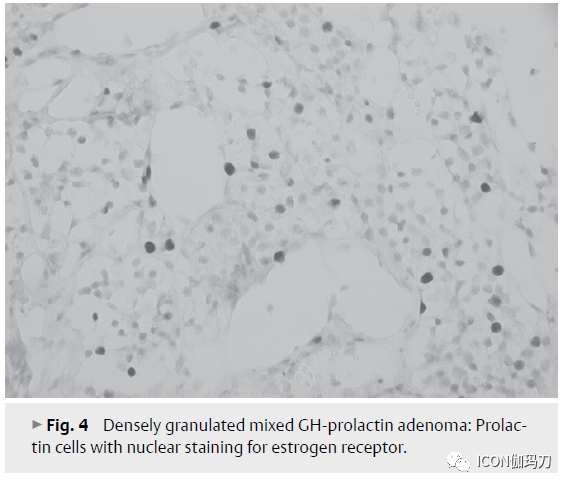
图4、致密颗粒性混合性GH-泌乳素腺瘤:泌乳素细胞具有雌激素受体的核染色。
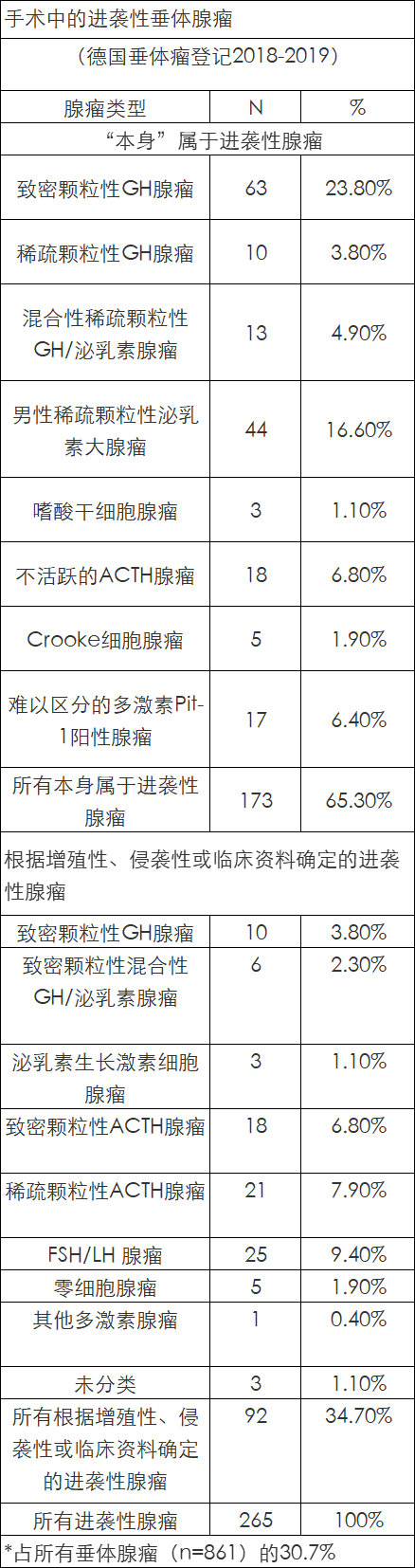
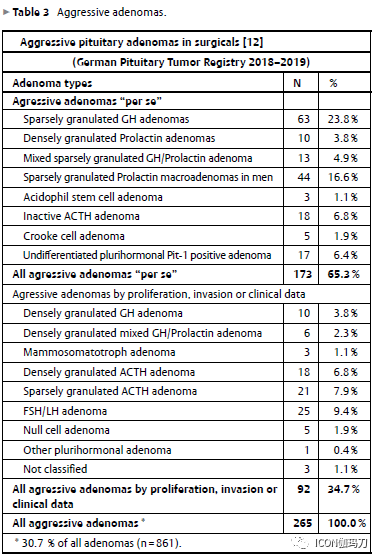
表3、进袭性腺瘤
泌乳素生长激素腺瘤(1.2%)(表1)是以致密颗粒性细胞为特征,它们共同表达生长激素、泌乳素、PIT-1、雌激素受体和α亚基。
![]()




