《Clinical Neurology and Neurosurgery》 2016 年10月刊载[149:122-35.]瑞士University Hospital of Lausanne的 Giulia Cossu , Roy Thomas Daniel, Mahmoud Messerer等撰写的系统综述《鞍区神经节细胞瘤:具有挑战性的诊断。Gangliocytomas of the sellar region: A challenging diagnosis》(doi: 10.1016/j.clineuro.2016.08.002. )。

鞍区神经节细胞瘤极为罕见,常与垂体腺瘤共存。这篇综述的目的旨在收集文献中报道的所有病例,并总结关于这一主题的最新文献证据。通过PubMed检索,系统地回顾了截至2015年9月为止,描述成年人口鞍区神经节细胞瘤的文章。对流行病学资料、临床表现、组织化学和放射影像学特征以及随访资料进行了分析。我们的分析包括55篇文献,报告了129例鞍区神经节细胞瘤。我们的医院也包括一例确诊病例。85%的患者合并垂体腺瘤。女性的流行是明显的。分离鞍区神经节细胞瘤时,患者最常表现为高泌乳素血症(44%)或视觉障碍(47%),或神经节细胞瘤合并垂体腺瘤时表现为肢端肥大症(67%)。免疫组化显示高发病率的混合GH-PRL腺瘤与鞍神经节细胞瘤,其次是GH腺瘤。25%的患者发现单纯位于鞍内,30%的病例发现鞍上伸展。约40%的患者有更广泛的浸润。有56%的碰撞病灶可获得完整切除。随访时间是可变的,但报告81%的相关神经节细胞瘤和垂体腺瘤的内分泌缓解。鞍区神经节细胞瘤是一种罕见的病变,与垂体腺瘤应经常搜索。混合性GH PRL腺瘤最常分离。碰撞病变似乎有孤立腺瘤的类似的行为,但更重要的进袭性应排除在分子水平。进一步的研究将有助于进一步阐明这种关联的发病机制。
1.引言
垂体腺瘤是生长在蝶鞍的最常见的肿瘤,占颅内肿瘤(intracranial neoplasms )的10-15%。然而,在同样的情况下,也可能发现其他肿瘤。神经节细胞瘤(Gangliocytomas )是一种罕见的肿瘤,占脑瘤的不到2%。它们是由大的多极性神经元(large mul-tipolar neurons )的不规则群形成的分化良好、生长缓慢的神经上皮肿瘤(well-differentiated slow-growing neuroepithelial tumors ),通常具有起源于神经节细胞的(arising from ganglion cells )发育不良的特征(dysplastic characteristics )。它们是WHO I级肿瘤,完全切除肿瘤被认为是可治愈的。颞叶和小脑难求是最常见的位置,而它们在鞍区被发现是极其罕见的。神经节细胞瘤可能表现为孤立的鞍区肿块,或更常见的与扁平腺瘤相关。在过去十年中,发表了越来越多的孤立的病例报告或病例系列。
我们对所有鞍区神经节细胞瘤的病例进行文献系统分析,以总结到目前为止已有的资料。
2.方法
GC和MM使用PubMed平台独立进行系统的文献检索,检索词为“神经节细胞瘤和垂体(gangliocytoma AND pituitary)”作为自由词( free text)。检寻工作一直进行到2015年9月。包括所有报道的成人鞍神经节细胞瘤病例的文章。通过使用PubMed中的“相关文章(related articles)”工具,还可以在已确定研究的参考文献列表中手动检索其他相关研究。考察了英语、法语、意大利语和德语的文章。未考虑未公布的数据或国会报告。分析病史、内分泌情况、术前影像、病理结果及随访资料。
3.结果
通过文献检索和标题和摘要筛选得到91篇文章,其中43篇文章被认为适合我们的分析。另有12篇文章被发现为相关文章。因此,我们的分析包括55篇文章,报告129例垂体神经节细胞瘤。然后通过筛选我们的一系列垂体病变发现了一例。在111例(包括本文报告的病例)中,(85%的患者为)神经节细胞瘤伴有垂体腺瘤,而19例(15%的患者)包含在孤立性鞍区神经节细胞瘤中( isolated sellar gangliocytomas)。(图1)
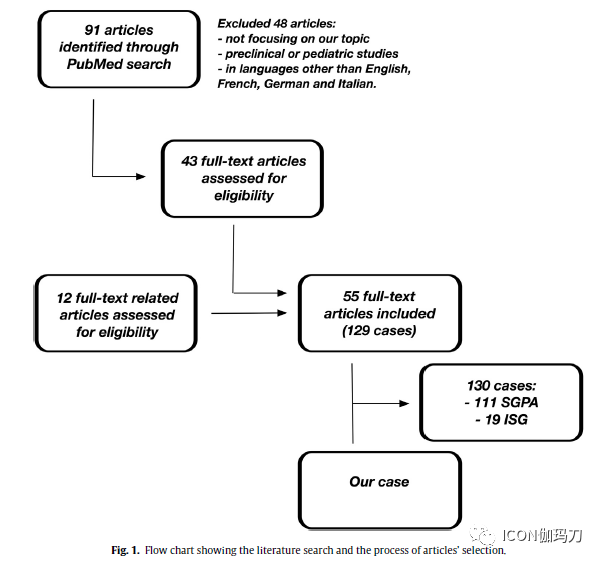
图1.文献检索和文章选择过程的流程图。
一例48岁女性入院,有2年的头痛病史。她报告说她的四肢变大,她被检查发现有睡眠阻塞性呼吸暂停综合征。此外,她主诉沿右侧的v2区三叉神经痛。脑部MRI发现Knosp 2级, Hardy A级垂体大腺瘤,侵袭右侧海绵窦(图2A和B)。内分泌内分泌评估显示IGF-1升高,为178mcg/l,口服葡萄糖耐量试验(OGTT)下GH抑制缺失。PRL水平是正常的。经由资深作者(MM和RTD)的鼻内镜下经蝶窦入路切除肿瘤,手术证实右侧海绵窦侵袭。在组织病理学上,该肿瘤由两个不同的细胞群组成。第一个成分是神经元的(neuronal ),特征是在纤丝(fibrillary )的背景下有大量神经节细胞。神经节细胞显示卵圆形核,罕见的双核(binucleations ),核仁突出(prominent nucleolus and )和丰富的嗜酸性细胞质(abundant eosinophiliccytoplasm )。血管周围有淋巴细胞浸润(Perivascular lymphocytic infiltrates )。第二种成分是典型的稀疏颗粒性生长激素细胞腺瘤(sparsely granulated soma-totroph adenoma )。腺瘤细胞小,与肾状核不紧密结合(poorlycohesive with kidney-shaped nuclei )。核的周围被一个大的球状低分子细胞角蛋白免疫阳性包涵体所取代(The nuclei were peripherallydisplaced by a large globular inclusion immunopositive for low-molecular-weight cytokeratins )。局部有丝分裂计数高,在一个高倍视野中有4个有丝分裂。Ki67标记指数高(5%),P53免疫表达阳性。大部分腺瘤细胞对生长激素(90%)呈免疫反应,少数对PRL呈免疫反应。生长抑素受体2 (SSTR2)在10%的细胞中弱表达。神经元组分呈MAP2阳性,部分细胞呈PRL阳性。两种成分的突触素(synaptophysin )染色均呈阳性。病理和组织化学特征符合稀疏颗粒性生长激素细胞腺瘤的诊断,伴部分细胞对PRL 反应。未发现嗜酸干细胞腺瘤的组织学(acidophil stem celladenoma were )特征。
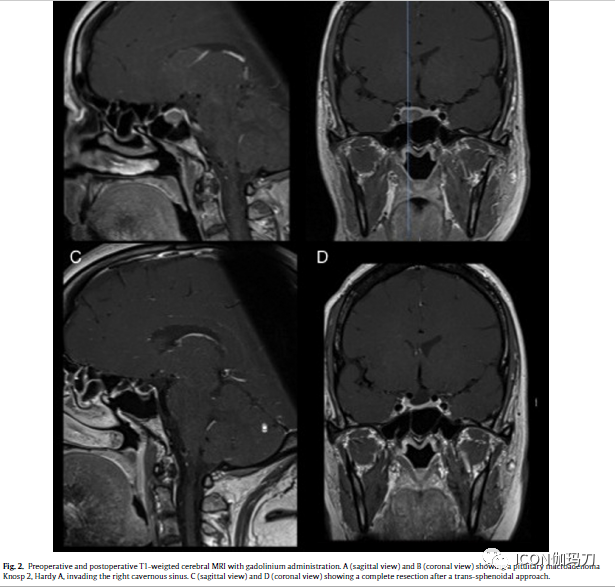
图2.术前和术后T1加权钆剂给药的脑部MRI。A(矢状面)和B(冠状面)显示Knosp2级,HardyA级垂体大腺瘤,侵袭右侧海绵窦。C(矢状面)和D(冠状面)显示经蝶窦入路完全切除。
术后无并发症发生,患者右侧三叉神经痛完全消退。她经历了生物学的缓解:OGTT期间GH<0.05 mcg/l,在整个(20个月)随访期间观察到与年龄相关的IGF-1水平正常化。术后MRI观察到完整切除(图2c和D)。
3.2.1.流行病学
孤立性鞍区神经节细胞瘤(ISG)患者平均年龄43岁,其中女性占70%(13例),男女比例为2.2:1。对于鞍区神经节细胞瘤合并垂体腺瘤(SGPA),我们提供了95例流行病学资料。发病时总平均年龄44.5岁,女性占80%(76例),男女比例为4:1。同时根据垂体腺瘤的组织化学亚型分析诊断时的平均值(图3)。
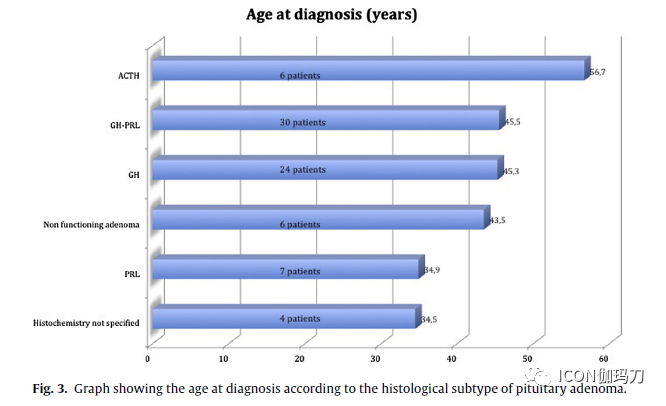
图3.根据垂体腺瘤的组织学亚型显示诊断年龄的图表。
3.2.2.临床表现
对于孤立性鞍区神经节细胞瘤(isolated sellar gangliocytomas ,ISG),尽管缺乏对垂体腺瘤组织学分析,16/19例(84%)有内分泌表现(表1),临床表现实际上6例(37.5%)是基于肢端肥大症的、7例(43.8%)是基于高泌乳素血症的、和3例(18.7%)是基于库欣综合征的临床症状和体征 。9/19(47%)的患者存在视觉障碍,表现为双颞侧偏盲或视力下降(bitem-poral hemianopia or decreased visual acuity.)。
表1.孤立性鞍神经节细胞瘤(ISG)患者的流行病学特征、临床表现、影像学表现及免疫组化分析。
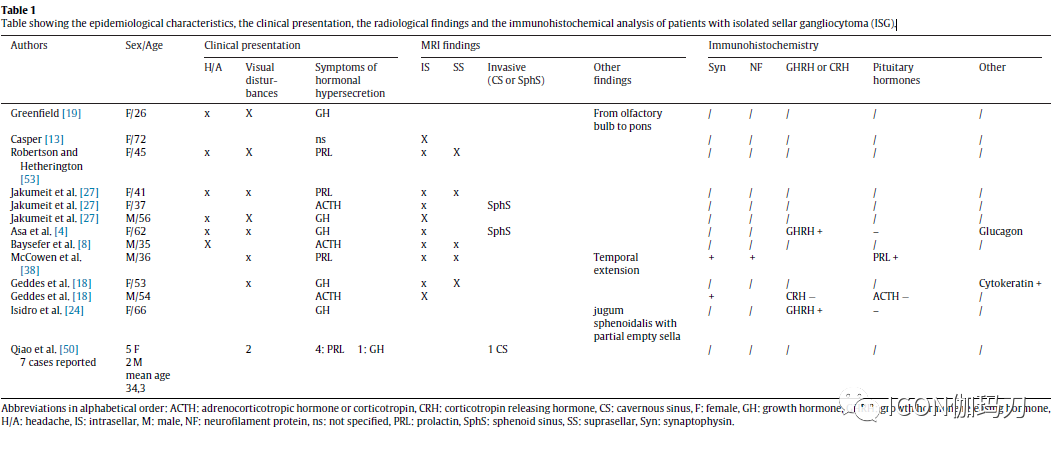
鞍区神经节细胞瘤合并垂体瘤(sellar gangliocytoma coupled with pituitary adenoma,SGPA)在大多数病例中表现为一项或多项垂体激素分泌过量。108例的临床表现是有特点的(表2)且在超过一半的病例(72例/ 108人,67%)中最经常与肢端肥大症的临床表现相关,其次是如视力下降或双颞侧偏盲等视觉障碍(29例,29%)、头痛(29例,29%)和月经紊乱(原文为dysmenorrhea )(或男性溢乳,28例,26%)。7例(6.5%)出现库欣病症状。
表2.鞍区神经节细胞瘤合并垂体腺瘤患者的流行病学特征、临床表现、影像学表现及免疫组化分析。
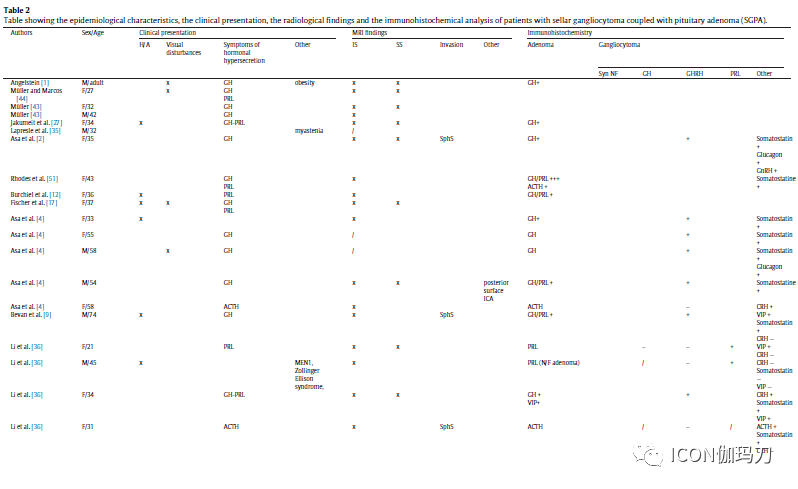
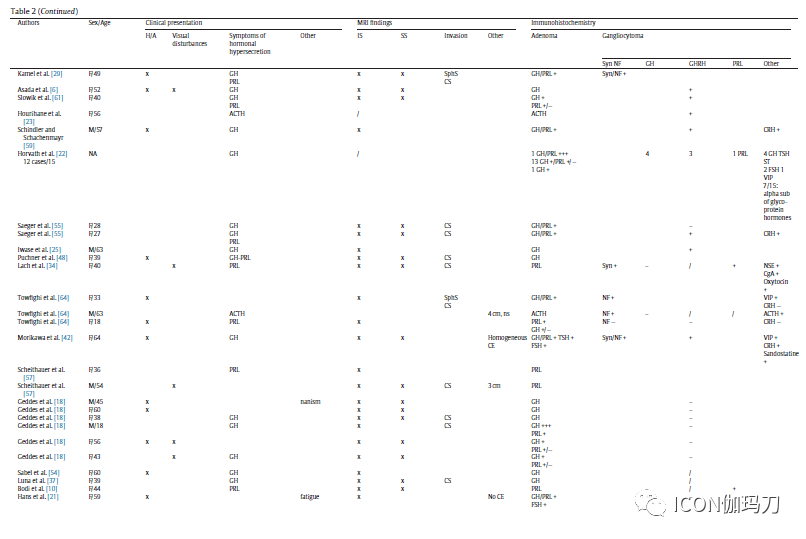
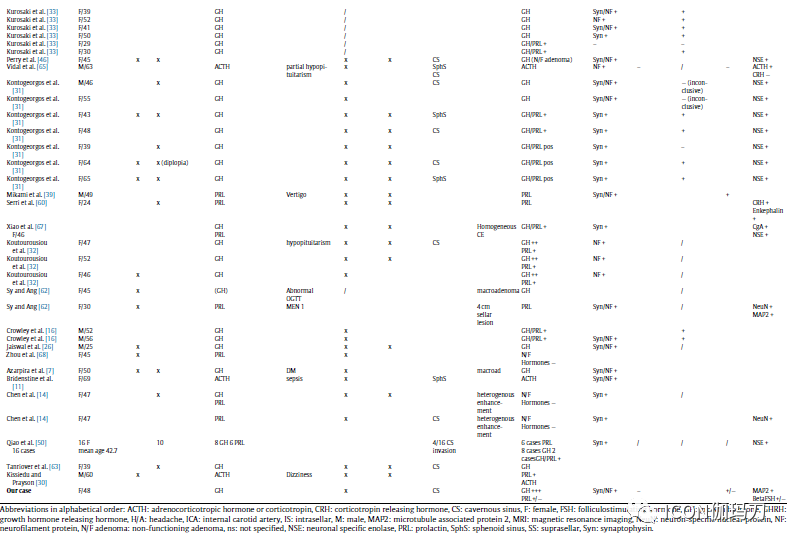
3.2.3免疫组化
只对少数(5/19,26%)的孤立性鞍区神经节细胞瘤(ISG)患者,进行免疫组化分析。结果非常异质性,并且依赖于所执行的检索(表1)。
对111例鞍区神经节细胞瘤合并垂体瘤(SGPA)中的106例进行了免疫组化检查(表2)。46例(43%)分离出混合GH-PRL腺瘤,35例(33%)分离出GH -腺瘤,15例(14%)分离出泌乳素腺瘤。106例中6例(6%)为分泌ACTH的腺瘤,1例(1%)为ACTH-PRL混合性腺瘤(图4)。4例NFPA(无功能性垂体瘤)免疫抗血清(antisera)都呈阴性。
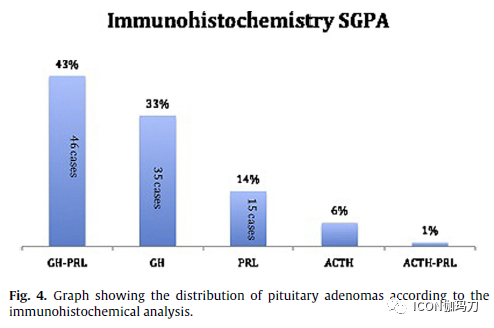
图4.垂体腺瘤免疫组化分析分布图。
对神经节细胞瘤的成分进行分析,多数患者GH、GHRH(生长激素释放激素)、PRL或 CRH(促肾上腺激素释放激素)阳性(表1)。28例GHRH阳性,17例GHRH阴性,未确诊11例。5例GH和PRL阳性,6例PRL阳性。3例为ATCH阳性,6例为CRH阳性。在一些病例中也发现VIP、生长抑素和胰高血糖素(somatostatine and glucagone)阳性。
3.2.4.放射影像学特点
关于孤立性鞍区神经节细胞瘤(ISG),有13例影像学特征明确(表1),其中3例(23%)ISG局限于蝶鞍,4例(31%)表现有单纯的鞍上伸展。5例患(38%)者表现为进袭性(aggressive)较强,2例侵袭蝶窦,1例海绵窦浸润,病灶延伸至颞叶,和广泛延伸(病灶从颅前窝延伸至桥脑)各1例。在一个病例中,病灶定位于蝶轭(the sphenoid jugum ),并与空蝶鞍相关。
关于鞍区神经节细胞瘤合并垂体瘤(SGPA),71例患者的影像学表现见表2。18例(25%)单纯出现鞍内病变,23例(32%)伴鞍上伸展,30例(42%)SGPA侵袭海绵窦或蝶窦,1例广泛延伸。1例PRL垂体癌伴脑转移被报道。
3.2.5.手术
关于孤立性鞍区神经节细胞瘤(ISG), 12例中4例经蝶窦入路,6例经鼻入路,1例经蝶窦入路多年后经颅入路。在一例患者中,未明确具体入路方法,而在(华山医院)Qiao等人的论文中,无法确定哪些患者接受了经蝶窦入路或经颅入路。全部切除10例(67%),部分切除5例(33%)。4例手术切除范围未见报道(表3)。
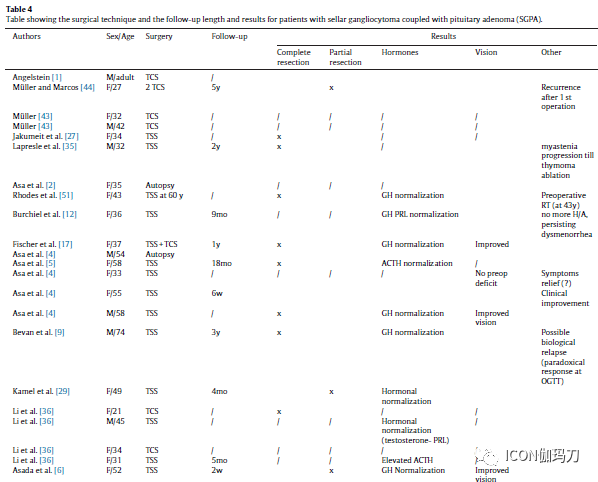
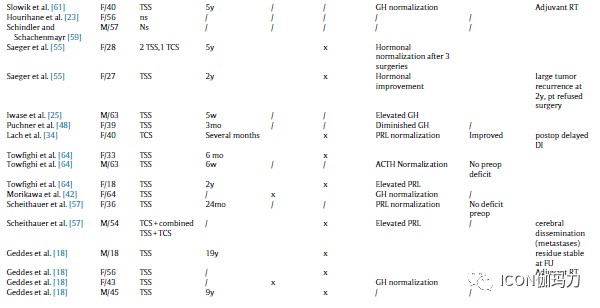
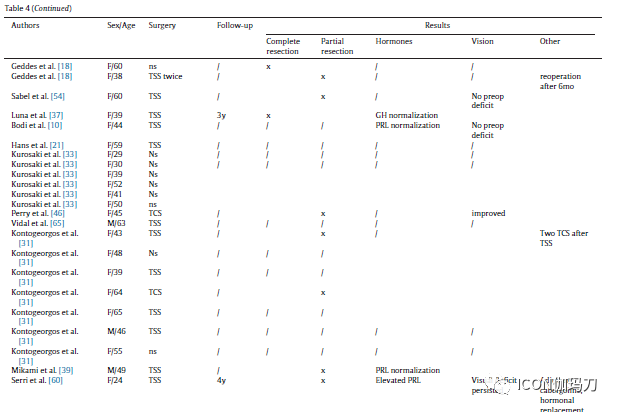
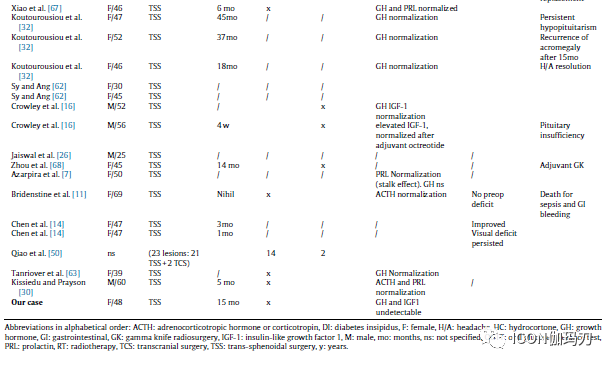
表4报告鞍区神经节细胞瘤合并垂体瘤(SGPA)的手术入路及结果:55例经蝶入路手术,9例经颅入路手术,3例联合入路手术。其中26例未明确外科入路,2例在尸检中诊断有垂体病变。同样,在Qiao等的论文中,也未确定哪些患者接受了经蝶窦入路或经颅入路。其中31/55例(56%)患者获得完全切除。
表4.鞍区神经节细胞瘤合并垂体腺瘤(SGPA)患者的手术入路、随访时间及结果。
3.2.6.术后随访
术后效果一般良好,术后无主要并发症(major complications )的报告。
对于孤立性鞍区神经节细胞瘤(ISG),如果详细来看,随访时间从术后即刻至最长的9年不等。有两例报告在术后期间激素正常化,而在其他3例,GH和ACTH仍然升高,患者需要进行辅助药物治疗。2例术前有视力减退的恢复正常。不幸的是并不是所有的作者详细说明术后结果(表3)。
表3.孤立性鞍神经节细胞瘤(ISG)患者的手术入路、随访时间和结果。
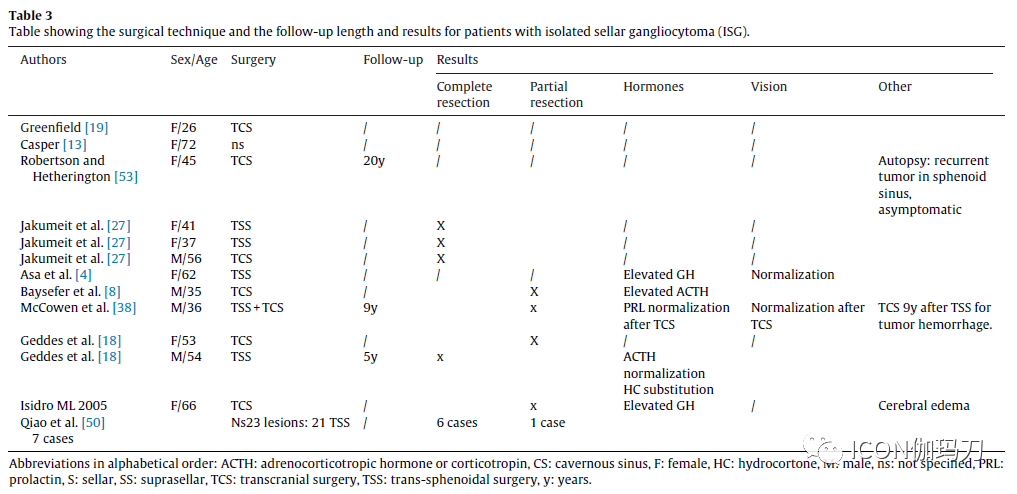
37例鞍区神经节细胞瘤合并垂体瘤(SGPA)内分泌的结果报道:30例(81%)术后激素得到正常化,30例中13例得到完整的切除(报道6例部分切除,11例未详细说明)。7例接受部分切除术的患者中5例术后未能有生物学的缓解(其他2例未说明切除范围)。进一步随访数据见表4。
4.讨论
根据我们的分析,85%的患者与鞍区神经节细胞瘤合并垂体腺瘤有关,87%的患者由腺瘤成分决定激素分泌过量。只有13%的腺瘤无功能或不明确。
最常见的发现是神经组织和分泌GH的垂体腺瘤共存,而组织学上最常(43%)分离到混合性GH - PRL 腺瘤。泌乳素瘤是功能性腺瘤中最常见的亚型。相反,分泌GH的腺瘤是鞍区碰撞性病变(collision sellar lesions )中最常见的病变,大多数病例伴有神经元成分,伴有稀疏颗粒性生长激素细胞腺瘤。一个可能的偏差可能取决于患者的选择:事实上,高泌乳素血症患者使用多巴胺能激动剂作为一线治疗,而肢端肥大症患者则选择手术作为一线治疗。因此,因为药物治疗的疗效较好,神经节细胞瘤合并分泌的 PRL腺瘤的病例可能会被低估。
诊断为鞍区神经节细胞瘤合并或不合并有垂体腺瘤的患者多为女性(70%为孤立的鞍区神经节细胞瘤,80%为碰撞性病灶)。这种联系的性质尚未得到进一步的研究,但女性可能比男性有更明显的临床表现(例如闭经)。据我们所知,从未研究过神经节肿瘤的激素依赖性。
垂体腺瘤的平均年龄为44岁,但如果将不同亚型的垂体腺瘤分开分析,泌乳素瘤碰撞性病变患者的平均年龄为35岁,而分泌ACTH腺瘤碰撞性病变患者的平均年龄为57岁。
临床表现方面,孤立性鞍区神经节细胞瘤(ISG)患者最常表现有高泌乳素血症(44%)或视觉障碍(47%),而鞍区神经节细胞瘤合并垂体腺瘤(SGPA)患者较常表现为肢端肥大症(67%),只有29%的患者出现视觉障碍。这可能是由于事实上分泌生长激素的腺瘤成分在发展到压迫视交叉之前就引起症状。
即使是孤立性鞍区神经节细胞瘤(ISG), 84%的患者也会表现出内分泌失调,最常见的是肢端肥大症和高泌乳素血症。在其他部位有神经节细胞瘤的患者中没有发现神经内分泌失调的临床症状,因此研究这种差异存在的原因是很有趣的。在我们看来,这种差异可能归因于孤立性鞍区神经节细胞瘤(ISG)的“孤立性(isolated)”一词是不合适的,而且在某些情况下,显微镜和免疫组化分析可能无法识别腺瘤成分。另一方面,胶质细胞可分泌垂体或下丘脑激素,直接决定临床表现。然而,这一理论的证据是有限的,而且仅来自少数孤立的研究。
要解决的主要问题是澄清鞍神经节细胞瘤的组织发生及其与垂体腺瘤的联系:许多假说已经阐明,但未得到证实。
神经肿瘤与垂体腺瘤的巧合性发现(coincidental finding )假说已经被搁置,许多作者试图找到两者之间的因果关系。由于与垂体前叶的异常相互作用,垂体中下丘脑神经元的异常迁移可能发生在胚胎发生期间,随后是肿瘤转化。神经节细胞可产生一些垂体激素释放下丘脑激素(pituitary hormone-releasinghypothalamic hormones ),从而刺激垂体前叶细胞的异常增殖。在一些神经节细胞中,免疫组化显示有生长激素释放激素(GHRH),支持这一假设。然而,人们对这种假说存有强烈的争议,在某些情况下,我们观察到下丘脑激素的释放与腺瘤细胞的分泌之间缺乏相关性。Horvath等人认为,神经节细胞瘤显示的免疫组化特征不一致,最常见的是对垂体激素α-亚基、促甲状腺激素和生长激素的反应。只有少数病例对GH-RH呈分散阳性。
Puchner等人认为,一种未知的同时启动事件(unknown simultaneousinitiating event )可能影响异位下丘脑神经节细胞(the heterotopic hypothalamic ganglion cells )和垂体细胞两者的生长。然而神经节细胞释放的下丘脑释放激素似乎只是促进垂体腺瘤的增殖而不是启动肿瘤的形成。
一些作者进一步提出了神经节细胞可能源自于已存在的垂体腺瘤的神经元分化的假设。神经生长因子(NGF)可能是诱导神经细胞分化的关键中介。事实上,NGF(神经生长因子)和NGFR(神经生长因子受体)存在于多种腺瘤亚型中。神经丝蛋白(NFP)在神经节细胞和腺瘤细胞中均呈阳性。这可能支持垂体细胞中神经元分化的理论,根据Nguyen等人所述,术语“具有神经元分化的垂体腺瘤(pituitary adenomawith neuronal differentiation )”将更好地定义这些碰撞性病变。
另一种理论认为,正常垂体细胞中存在的神经元标志物(突触素和NSE[神经元特异性烯醇化酶)以及腺瘤细胞中的神经元样过程可以用由于存在与(具有中间特征的细胞)胚胎垂体休眠(embryonic pituitary rest)相同的前体(same spancursor )来解释。然而,这些“中级体(intermediate )”细胞在正常垂体中未被发现。也有假设神经元和腺瘤细胞有来自不确定的干细胞的共同来源。
许多作者认为,存在垂体腺神经节细胞瘤并不能改变患者的整体预后或手术切除后复发的风险。然而,未完全切除的肿瘤对激素靶向治疗或放疗的反应有限。我们可以认为,缺乏这方面的反应可能归因于碰撞性病变中孤立性垂体腺瘤最常见的组织类型是稀疏颗粒性腺瘤或嗜酸干细胞腺瘤,根据定义,它们对生长抑素类似物反应较弱。但是,在大多数患者中,垂体腺瘤的亚型没有明确说明。叠加的作用(An additive contribution )可能是由于残留病变持续分泌的刺激激素或旁分泌物质(continuous secretion of stimulating hormones or paracrinesubstances by the residual lesion )。对这些方面需要进一步研究。
本研究的一个局限性是,由于每个作者使用的技术具有异质性,且可用的数据很少,因此无法根据免疫组化方法对随访数据进行分析。
考虑到在我们的综述中包括的鞍区神经节细胞瘤合并垂体腺瘤(SGAP)的患者,30例患者在部分切除术后有6例术后激素正常。然而,这些患者的随访时间很短或没有具体说明,因此我们认为不应低估全切除术的重要性。
5.结论
仅根据临床和放射影像学诊断鞍区神经节细胞瘤是非常困难的,常被排除诊断为垂体腺瘤(are commonly dismissed for pituitary adenomas)。如果术前怀疑神经节细胞瘤,应寻找相关的垂体腺瘤,对于术前没有激素过量证据的患者也是如此。
在混合性神经节细胞瘤-垂体腺瘤肿瘤中,腺瘤成分应被彻底分析以确定进袭性的标准,并应尝试完全切除,且进行长期随访。
进一步的分子和免疫组织化学研究是必要的,以阐明这种罕见相关联的组织学发生及其意义。




