
脑膜瘤是成人颅内最常见的原发性中枢神经系统肿瘤之一。针对伴随症状的脑膜瘤患者,目前临床治疗方案主要限于手术切除和/或辅以放射治疗。大部分低级别脑膜瘤治疗效果良好,然而,难治性脑膜瘤仍面临着手术全切率低,复发率高,致残率高等问题,严重影响患者临床预后和生存质量。影响脑膜瘤治疗及预后的因素较为复杂,肿瘤切除程度(Extent of resection,EOR)以及组织病理学分级等变量被认为能够较为准确地预测肿瘤复发和患者预后[1-3]。然而,随着对脑膜瘤病理发展过程的遗传学基础逐步阐明,过去以脑膜瘤形态学概念作为定义标准的诊断、分级及分型已经受到严峻挑战。本次将简单的向大家介绍脑膜瘤分子生物学特征及最新研究进展。

脑膜瘤基因组变异(Genomic Alterations in Meningiomas)
随着近年来多组学技术的蓬勃发展,高通量高效能研究技术的应用,脑膜瘤病理过程中分子特征正不断被揭示(图1)。
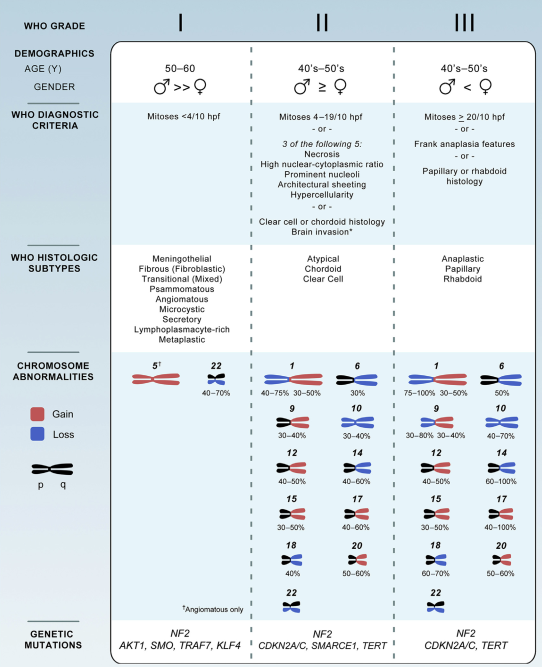
图1.WHO I-III脑膜瘤病理分型与遗传学背景。(引自图Bi W L, Abedalthagafi M, Horowitz P, et al. Genomic landscape of intracranial meningiomas[J]. Journal of neurosurgery, 2016, 125(3): 525-535.)
1.1. 染色体拷贝数异常(Copy Number Alterations,CNAs)
1967年,研究人员发现大部分脑膜瘤中存在G显带染色体畸变,表现为21号或22号染色体缺失[4]。随后又不断有研究证实半数以上脑膜瘤中存在22号单倍染色体[5]。这些现象表明,22号染色体丢失在脑膜瘤的病理过程中起着关键作用。除22号染色体异常外,1号染色体长臂缺失(Chromosome 1p)在高级别脑膜瘤中也较为常见[6]。此外,脑膜瘤中还存在其他CNA类型,如4p、6q、7p、9p、10q、11p、14q和18q缺失[7]。上述遗传学研究为进一步发现脑膜瘤中特异性基因突变奠定了基础。
1.2. 基因突变(Gene Mutation Signature)
在过去数十年中,研究人员致力于寻找与脑膜瘤进展、侵袭等生物学行为相关的致病基因,其中一部分靶点有望在不久的将来实现临床转化(图2)。
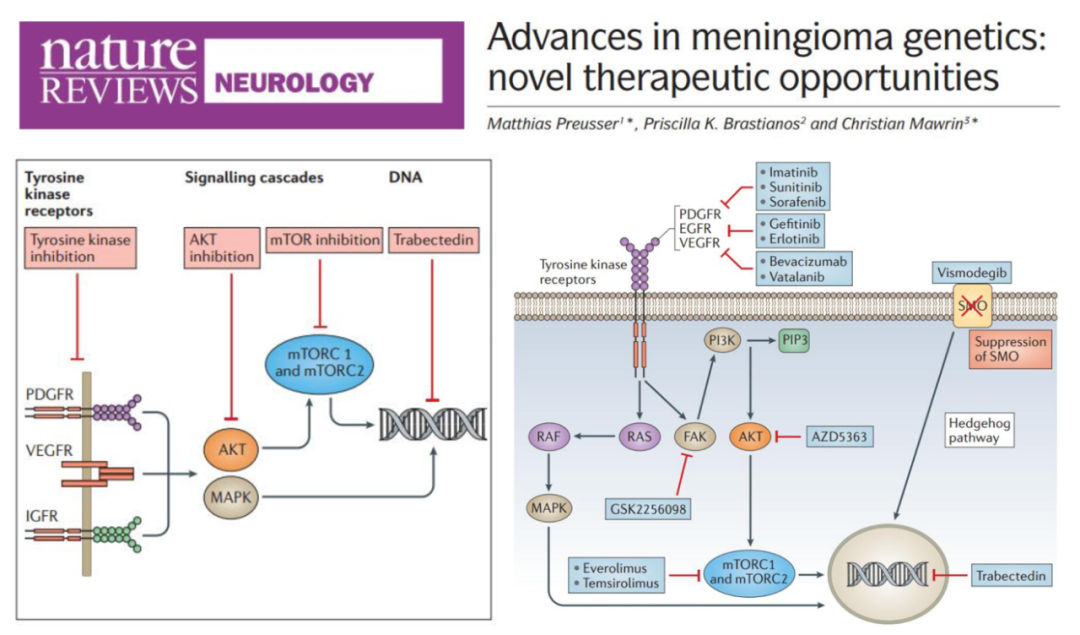
图2.脑膜瘤潜在治疗靶点及对应小分子药物。(引自Preusser M, Brastianos P K, Mawrin C. Advances in meningioma genetics: novel therapeutic opportunities[J]. Nature Reviews Neurology, 2018, 14(2): 106-115.)
NF2突变或丢失是脑膜瘤最常见的分子病因,约30-50%散发性脑膜瘤患者中存在该基因突变[8]。除NF2突变外,约五分之一脑膜瘤中存在TRAF7(Tumor necrosis factor [TNF] receptor associated factor 7)基因突变[9],它与NF-kappaB转录因子的调节、细胞应激途径激活、多细胞靶点泛素化和凋亡诱导相关。此外,约10%散发性脑膜瘤中存在AKT1突变[10]。还有研究报道,脑膜瘤中AKT1或KLF4突变常与TRAF7突变同时发生,但AKT1和KLF4基因突变往往不同时发生。Hedgehog(Hh)信号通路异常也参与脑膜瘤的病理过程,其中SMO和SUFU基因易受累及 [11]。另有4-7%的脑膜瘤中存在PIK3CA突变[11]。PORR2A(RNA polymerase II)编码真核生物细胞中催化核糖核酸转录的酶,其突变率在WHO I级脑膜瘤中占6%。PORR2A点突变类型常见于G403K以及Leu438,His439框内缺失。
SWI/SNF(Switch/sucrose non-fermentable)染色质重塑复合物在脑膜瘤形成和侵袭性中起重要作用。SMARCB1为构成SWI/SNF复合体的的核心组份,有研究发现,多发性脑膜瘤和神经鞘瘤中存在SMARCB1突变[12],部分散发性WHO I级和II级脑膜瘤中还观察到SMARCB1突变与NF2突变同时发生[13]。横纹肌型脑膜瘤中存在BAP1(BRCA associated protein 1)抑癌基因突变,该基因编码产物可通过抵抗组蛋白H2A泛素化来调节基因表达[14]。EZH2(Enhancer of zeste homolog 2)抑制剂对伴随BAP1突变的恶性间皮瘤有一定治疗效果,这为发生BAP1突变脑膜瘤提供了系统性药物治疗的机会。近期还有研究团队报道乳头型脑膜瘤中存在抑癌基因PBRM1失活突变(图3),并强调了后续评估PBRM1突变与患者临床预后关系的必要性[15]。
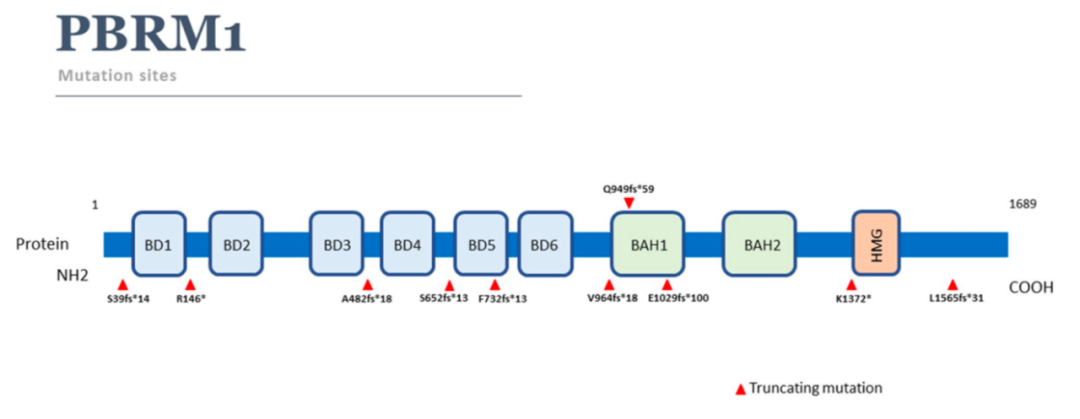
图3.乳头型脑膜瘤病例中PBRM1基因失活突变示意图。(引自Williams, E.A., Wakimoto, H., Shankar, G.M. Frequent inactivating mutations of the PBAF complex gene PBRM1 in meningioma with papillary features. Acta Neuropathol. 2020; 140, 89-93.)
除上述编码区基因异常外,脑膜瘤中非编码区基因突变也越来越受到重视。端粒酶逆转录酶(Telomerase reverse transcriptase,TERT)能够通过在染色体末端加入高度保守的TTAGGG序列来维持端粒末端长度。体细胞中TERT基因处于抑制状态,从而导致细胞衰老。TERT启动子区突变增加了Ets转录因子(E-twenty-six transcription factor)的结合从而降低TERT表达,导致细胞永生化。脑膜瘤中TERT启动子突变约占6.5-11%,常发生于C228T和C250T位点[16]。事实上,TERT启动子突变在大部分恶性肿瘤中均较常见,这也提示了该突变类型可能在恶性复发脑膜瘤中起关键作用。TERT启动子突变在NF2突变型和NF2野生型脑膜瘤中均可发生,但它与其他类型基因突变的关系尚不明确[16]。
表观遗传学异常 (Epigenomic Alterations in Meningioma)
2.1. DNA甲基化 (DNA Methylation)与组蛋白修饰(Histone modification)
DNA甲基化是最早被发现、也是研究最深入的表观遗传调控机制之一。DNA甲基化能引起染色质结构、DNA构象、DNA稳定性及DNA与蛋白质相互作用方式的改变,从而控制基因表达(图4)。约10%脑膜瘤病例中TIMP3(Tissue inhibitor of metalloproteinase 3),CDKN2A(Cyclin-dependent kinase inhibitor 2A)以及TP73(Tumor protein 73)存在高度甲基化[17]。TIMP3高度甲基化将导致其转录产物下调而丧失抑癌活性[18]。40-60%高级别脑膜瘤中TIMP3存在高度甲基化,这部分患者常在接受治疗后短期内快速复发[17,18]。由于TIMP3位于22号染色体(22q12),几乎所有TIMP3高度甲基化的脑膜瘤病例均伴随22q等位基因丢失[18]。此外,约70%到80%的高级别脑膜瘤中存在TP73启动子甲基化,但这一现象在WHO I级脑膜瘤中并不常见,说明TP73启动子甲基化在高级别脑膜瘤中具有一定特异性。同时,部分研究人员认为H3K27me3缺失可能增加脑膜瘤临床复发风险[19]。
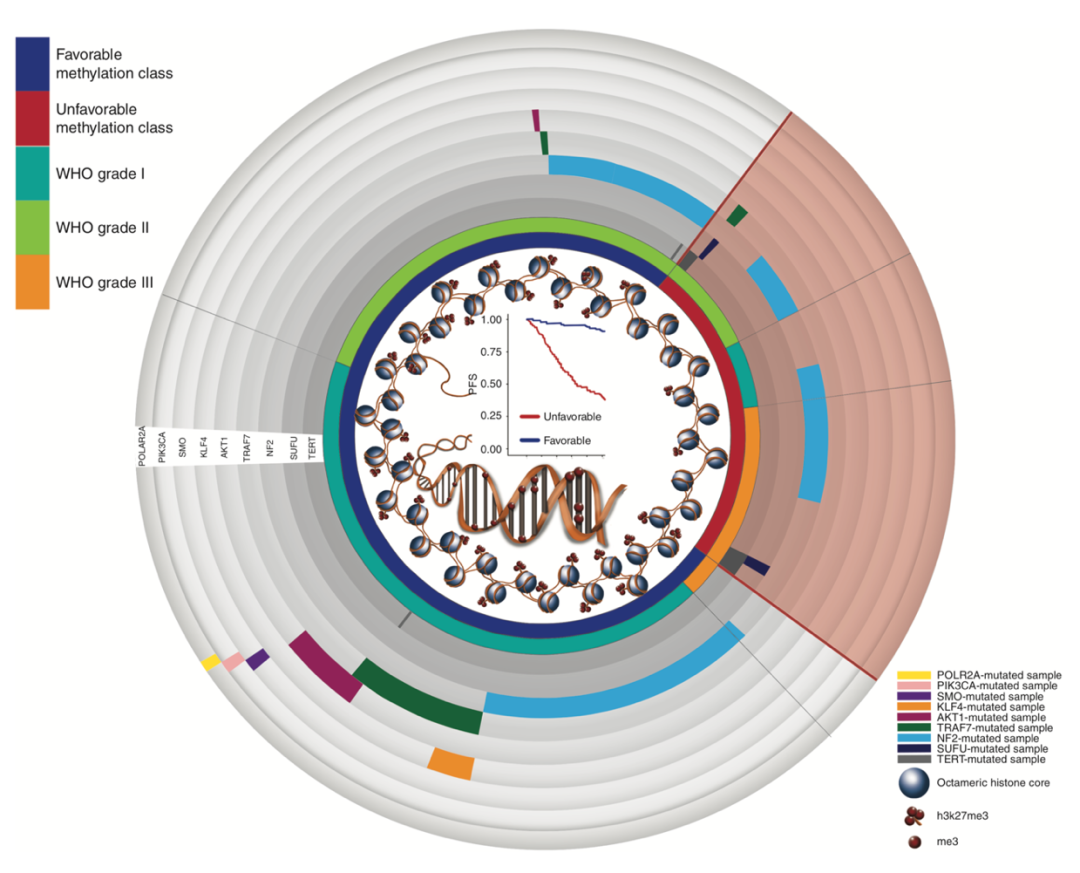
图4.脑膜瘤表观遗传学背景。[引自图Suppiah S, Nassiri F, Bi W L, et al. Molecular and translational advances in meningiomas[J]. Neuro-oncology, 2019, 21(Supplement_1): i4-i17.]
2.2. 非编码RNA调控(non-coding RNA regulation)
非编码RNA是指能被转录但不能翻译为蛋白质的功能性RNA,主要包括miRNA、LncRNA、circRNA等。MicroRNA(miRNA)是一类由内源基因编码的长度约为22个核苷酸的非编码单链RNA分子,它们在动植物中参与转录后基因表达调控。目前只有少部分研究对miRNA在脑膜瘤中的作用进行探讨。其中,有研究发现miRNA-200a在脑膜瘤中表达下调,由于与β-catenin的相互作用减少从而导致Wnt/β-catenin信号通路异常[20]。此外,不同病理级别和不同基因背景(NF2突变型和NF2野生型)的脑膜瘤之间也存在不同miRNA表达模式。例如,miRNA-145在高级别脑膜瘤中表达明显减少,而细胞系中过度表达miRNA-145则表现为细胞增殖缓慢[21]。还有研究人员还发现脑膜瘤中miRNA-109a高表达,miRNA-29c-3p和miR-219-5p低表达也与肿瘤复发相关[22]。还有研究认为,与miRNAs类似,长非编码RNA(long-noncoding RNAs,lncRNAs)也参与调控脑膜瘤的生物学行为。尽管这些研究结果离真正的临床应用还存在一定距离,但这增加了我们对表观遗传调节的潜力和局限性的理解,将来有望成为难治性脑膜瘤的有效手段。
脑膜瘤的转录组学特征 (Transcriptomic Signatures in Meningioma)
中心法则表明遗传信息在精确的调控下通过RNA(mRNA)从DNA传递至蛋白质。转录组则是指在一定的时间和环境条件下,细胞内的全部转录产物及其数量。除DNA甲基化等表观遗传学研究外,基因表达分析(microarray gene expression analysis)也被用于相关领域研究,试图对脑膜瘤生物学行为进行区分。研究人员发现,TGM2基因转录产物在高级别脑膜瘤中表达增加。此外,DCC基因转录产物netrin-1跨膜受体缺失,也被认为是脑膜瘤进展的高危因素[23,24]。然而,大部分转录组研究由于样本量有限,需要进一步扩大样本量以证实其潜在临床转化价值。
脑膜瘤的蛋白质组学特征 (Proteomic Signatures in Meningiomas)
目前,脑膜瘤相关的蛋白质组学研究仍然很有限,少数研究团队在前期工作中分析了不同病理级别脑膜瘤之间的蛋白组学差异。通过凝胶电泳结合质谱分析,Okamoto等人对不同级别脑膜瘤样本进行了比较分析,鉴定出了良恶性脑膜瘤之间的15种差异表达蛋白[25]。Sharma等人利用多肽体外标记定量技术(iTRAQ-based proteomics),在脑膜瘤中鉴定出2000多种差异表达蛋白,这些蛋白参与多种信号通路,包括integrin、Wnt、Ras、EGFR(epidermal growth factor receptor)以及FGR(Gardner-Rasheed feline sarcoma)[26]。另有研究关注WHO I级脑膜瘤及其与肿瘤相邻的蛛网膜组织之间的蛋白差异表达,鉴定出17种显著下调的蛋白以及26种显著上调的蛋白[27]。Saydam等人还采用一例良性脑膜瘤细胞系和原发性蛛网膜细胞进行了蛋白质组学分析,发现MCM(minichromosome maintenance)家族相关蛋白存在明显差异[28]。
以上研究表明,蛋白质组学为阐明脑膜里的分子特征提供了更精准的信息,有助于促进生物标志物的发现和鉴定,同时在制定肿瘤新的治疗策略以及后续阐明耐药机制方面具有重要意义。
结语
尽管目前大部分脑膜瘤患者能够通过外科手术治疗获得良好临床预后,但对于复发、高级别以及颅底脑膜瘤等难治性患者仍面临着手术切除困难,术后辅助治疗手段单一,且缺乏有效化疗及分子靶向药物等困难。随着分子生物学研究技术的不断发展,我们对脑膜瘤的遗传背景和发生、发展机制已有了更深入的理解。与此同时,因测序技术已经逐步应用到脑膜瘤的临床医疗诊断中。通过检测并分析患者脑膜瘤标本中特定的基因的点突变、插入、缺失、融合、拷贝数变异等情况,可帮助病人选择获益最佳的治疗方案,有望实现个体化医疗。随着精准医学进入肿瘤医学,将会使脑膜瘤患者从个性化诊疗中最大程度地获益。
参考文献
1. Adeberg S, Hartmann C, Welzel T, et al. Long-term outcome after radio- therapy in patients with atypical and malignant meningiomas—clinical results in 85 patients treated in a single institution leading to optimized guidelines for early radiation therapy. Int J Radiat Oncol Biol Phys. 2012;83(3):859–864.
2. Simpson D. The recurrence of intracranial meningiomas after surgical treatment. J Neurol Neurosurg Psychiatry. 1957;20(1):22–39.
3. Gousias K, Schramm J, Simon M. The Simpson grading revisited: aggressive surgery and its place in modern meningioma management. J Neurosurg. 2016;125(3):551–560.
4. Zang KD, Singer H. Chromosomal consitution of meningiomas. Nature. 1967;216(5110):84–85.
5. Seizinger BR, de la Monte S, Atkins L, Gusella JF, Martuza RL. Molecular genetic approach to human meningioma: loss of genes on chromosome 22. Proc Natl Acad Sci U S A. 1987;84(15):5419–5423.
6. Lee Y, Liu J, Patel S, et al. Genomic landscape of meningiomas. Brain Pathol. 2010;20(4):751–762.
7. Zang KD. Meningioma: a cytogenetic model of a complex benign human tumor, including data on 394 karyotyped cases. Cytogenet Cell Genet. 2001;93(3-4):207–220.
8. Ruttledge MH, Sarrazin J, Rangaratnam S, et al. Evidence for the complete inactivation of the NF2 gene in the majority of sporadic meningiomas. Nat Genet. 1994;6(2):180–184.
9. Yuzawa S, Nishihara H, Yamaguchi S, et al. Clinical impact of targeted amplicon sequencing for meningioma as a practical clinical-sequencing system. Mod Pathol. 2016;29(7):708–716.
10. Bleeker FE, Felicioni L, Buttitta F, et al. AKT1(E17K) in human solid tumours. Oncogene. 2008;27(42):5648–5650.
11. Abedalthagafi M, Bi WL, Aizer AA, et al. Oncogenic PI3K mutations are as common as AKT1 and SMO mutations in meningioma. Neuro-Oncol. 2016;18(5):649–655.
12. Bacci C, Sestini R, Provenzano A, et al. Schwannomatosis associated with multiple meningiomas due to a familial SMARCB1 mutation. Neurogenetics. 2010;11(1):73–80.
13. Harmancı AS, Youngblood MW, Clark VE, et al. Integrated genomic analyses of de novo pathways underlying atypical meningiomas. Nat Commun. 2017;8:14433.
14. Shankar GM, Santagata S. BAP1 mutations in high-grade meningioma: implications for patient care. Neuro Oncol. 2017;19(11):1447–1456.
15. Williams, E.A., Wakimoto, H., Shankar, G.M. Frequent inactivating mutations of the PBAF complex gene PBRM1 in meningioma with papillary features. Acta Neuropathol. 2020; 140, 89-93.
16. Sahm F, Schrimpf D, Olar A, et al. TERT promoter mutations and risk of recurrence in meningioma. J Natl Cancer Inst. 2016;108(5):djv377.
17. Bello MJ, Amiñoso C, Lopez-Marin I, et al. DNA methylation of multiple promoter-associated CpG islands in meningiomas: relationship with the allelic status at 1p and 22q. Acta Neuropathol. 2004;108(5): 413–421.
18. He S, Pham MH, Pease M, et al. A review of epigenetic and gene expression alterations associated with intracranial meningiomas. Neurosurg Focus. 2013;35(6):E5.
19. Katz LM, Hielscher T, Liechty B, et al. Loss of histone H3K27me3 identifies a subset of meningiomas with increased risk of recurrence. Acta Neuropathol. 2018;135(6):955–963.
20. Saydam O, Shen Y, Würdinger T, et al. Downregulated microRNA-200a in meningiomas promotes tumor growth by reducing E-cadherin and activating the Wnt/beta-catenin signaling pathway. Mol Cell Biol. 2009;29(21):5923–5940.
21. Kliese N, Gobrecht P, Pachow D, et al. miRNA-145 is downregulated in atypical and anaplastic meningiomas and negatively regulates motility and proliferation of meningioma cells. Oncogene. 2013;32(39):4712–4720.
22. Zhi F, Zhou G, Wang S, et al. A microRNA expression signature predicts meningioma recurrence. Int J Cancer. 2013;132(1):128–136.
23. Huang YC, Tsai YH, Lee JD, et al. Hemodynamic factors may play a critical role in neurological deterioration occurring within 72 hrs after lacunar stroke. PLoS One. 2014;9(10):e108395.
24. Schulten HJ, Hussein D, Al-Adwani F, et al. Microarray expression data identify DCC as a candidate gene for early meningioma progression. PLoS One. 2016;11(4):e0153681.
25. Okamoto H, Li J, Vortmeyer AO, et al. Comparative proteomic profiles of meningioma subtypes. Cancer Res. 2006;66(20):10199–10204.
26. Sharma S, Ray S, Mukherjee S, Moiyadi A, Sridhar E, Srivastava S. Multipronged quantitative proteomic analyses indicate modulation of various signal transduction pathways in human meningiomas. Proteomics. 2015;15(2–3):394-407.
27. Cui GQ, Jiao AH, Xiu CM, et al. Proteomic analysis of meningiomas. Acta Neurol Belg. 2014;114(3):187-194.
28. Saydam O, Senol O, Schaaij-Visser TB, et al. Comparative protein profiling reveals minichromosome maintenance (MCM) proteins as novel potential tumor markers for meningiomas. J Proteome Res. 2010;9(1):485–494.
专家简介

邓佼娇,医学博士,复旦大学附属华山医院神经外科住院医师,2018赴美国斯坦福大学联合培养。目前研究方向为难治性脑膜瘤靶向治疗及临床应用。
阔然精准诊疗脑肿瘤产品CaptioX-M是一款以NGS技术为基础的检测产品。CaptioX-M用于脑膜瘤的分子诊断,涵盖了脑膜瘤复发相关的67个基因(NF2、TERTp、CDKN2A/B、ARID1A和BIP1等)、预后相关的染色体(22q、1p、5、10等)拷贝数变异和潜在靶向治疗相关基因的信息,脑膜瘤CaptioX-M可用于脑膜瘤患者分子分型、预后评估和辅助医生制定治疗策略。
“阔然生物医药科技(上海)有限公司(Shanghai KR Pharmtech, Inc. , Ltd.)”简称“阔然基因”,是一家专注于医学研究与转化的企业,专注于脑肿瘤的分子诊断与个体化治疗业务,现已有两家(上海、徐州)国家卫生健康委员会认证的医学检验实验室,在基因检测领域有自主知识产权,拥有完善的全国医疗市场的销售渠道,战略合作的神经外科医生的媒体“神外资讯”,目标成为脑肿瘤分子诊断与个体化治疗领域中国第一品牌。阔然基因重视自有技术开发,目前已建高通量测序平台、单细胞测序平台、多标荧光免疫组化平台,阔然基因在硬件与试剂盒产品端发力,布局术中、术后诊断领域,打造自有技术和行业壁垒,成为并巩固在脑肿瘤领域的领跑者地位。目前阔然基因已布局了术后分子诊断、ddPCR脑脊液检测技术和应用,以及术中实时诊断系统。




