《Annals of Palliative Medicine》 2020 年7月29日在线发表新加坡和美国的 Caryn Wujanto, Balamurugan Vellayappan, Eric L Chang,等撰写的综述《脑部放射疗法:年代悠久的治疗方法的后果是什么?Radiotherapy to the brain: what are the consequences of this age-old treatment? 》(doi: 10.21037/apm-20-856.)。
放射治疗(RT)已被广泛应用于良、恶性脑肿瘤的治疗数十年。然而,由于邻近结构暴露于辐射,可能会出现并发症。因此,谨慎选择患者并决定最合适的放射治疗(RT)方式对减少并发症至关重要。一般来说,并发症可以根据起病时间细分;急性(几天到几周),早期延迟(1-6个月)和迟发性(>6个月)。认知能力下降和放射性坏死等迟发性并发症会使人虚弱,并对生存质量产生负面影响。减少放射治疗(RT)相关并发症的新策略,如海马回避(hippocampal sparing)-全脑放疗(WBRT)、美金刚胺(memantine)和局灶性放疗(RT)(如立体定向放射外科)已经取得了良好的效果,并被应用于临床实践。本综述将重点关注与放疗相关的脑部并发症,重点关注域WBRT或SRS相关的迟发性副反应事件(late adverse events),以及减轻这些并发症的措施。
放射治疗(RT)是脑肿瘤治疗的基石。早在1930年代,就有描述使用放射治疗(RT),当时Lenz和Freid报道“中等剂量的放疗后颅内压增高的征象和局部受累大脑的暂时复原(temporary regression )。”Chao等人1954年报道有三分之二的接受脑部放射的脑转移瘤患者出现症状缓解。从此,放射治疗(RT)已经成为在治愈性的、姑息性的、也可是预防性的(如在小细胞肺癌的情况下减少脑转移瘤的发生率)背景下,确立的脑部肿瘤的治疗。在治愈性的背景下,放射治疗(RT)作为重要的如神经胶质瘤等浸润性的、仅仅通过手术难以完全切除的原发性脑瘤的手术和化疗辅助治疗方式。在脑转移瘤的情况下,早期试验表明,相比单纯糖皮质激素治疗,对整个大脑的放射治疗(RT) (全脑放疗[WBRT])能提高生存。多达30%的癌症患者最终发展出现脑转移瘤,多年来,对这些患者的医疗目标已经扩大到包括保存和提高生存质量。由于脑实质内的系统性化疗的活性有限,放疗仍可发挥主要作用。然而,对预后较差的患者,全脑放疗(WBRT)在生存率和生存质量方面可能没有提供显著的获益。因此,可考虑选择保留(withholding)WBRT。
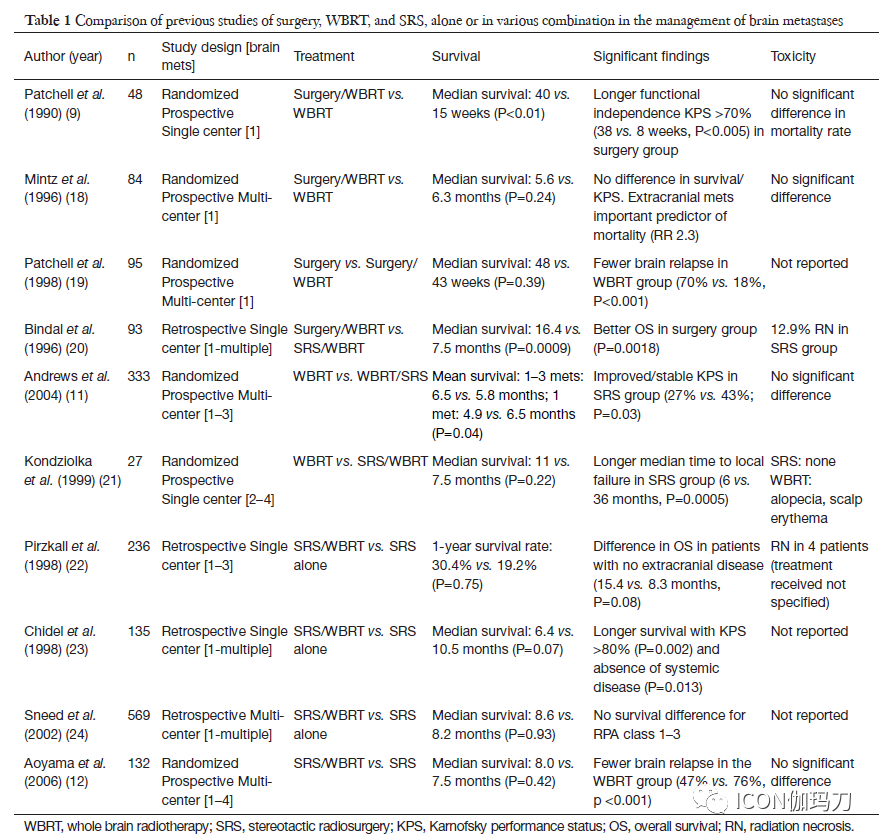
将(手术或立体定向放射外科治疗)局部积极治疗(local aggressive therapy )附加到全脑放疗(WBRT)会带来单个的或有限数目的(1 - 3处)脑转移瘤患者的结果改善,包括改善生存(单个病变的患者),减少复发,有长期的独立功能。对于有1到4处未接受过干预的(intact)脑转移瘤患者,单独使用SRS治疗与先期(upfront)使用WBRT联合SRS治疗进行比较,生存率没有显著差异,但有注意到单独使用SRS治疗远处颅内复发率较高。Chang等人在2009年首次报道一个单中心随机对照试验(RCT) ,以及最近,在一个大规模多中心随机对照试验,在SRS治疗有限数目的脑转移瘤患者后附加WBRT的主要缺点是与治疗相关的神经认知功能的退化。2014年,美国放射肿瘤学会(ASTRO)在Choosing Wisely campaign (明智选择的活动)中,建议在SRS治疗有限数目的脑转移瘤后,不必常规附加WBRT,并建议患者接受仔细监测,且考虑在复发时进行补救性治疗(salvage therapy)。与应用WBRT相比,使用SRS治疗需限制暴露于辐射下的健康脑实质的体积,但邻近结构(如颅神经、脑干)仍有发生并发症的风险。根据国际指南,目前常规推荐仅使用立体定向放射外科治疗有限的脑转移瘤患者,因为它能更好地进行局部控制,同时减少对神经认知的副作用。表1显示了脑转移瘤的不同治疗方式和联合治疗。
然而,谨慎选择患者进行放疗(RT)是重要的。放疗(RT)的迟发毒性可使人衰弱,影响生存质量,有时是不可逆的(at times irreversible )。对于良性疾病(如垂体腺瘤、脑膜瘤)或预防性接受放疗的患者来说,这可能更为重要。即使在姑息性的背景下,由于系统性治疗的改进,患者的寿命也延长了。因此,预后工具是制定临床决策的重要组成部分。在脑转移瘤的背景下,分级预后评估(GPA)为预测患者预期生存期提供了一个组织学特异性评分系统。这是基于年龄、Karnofsky表现状态(KPS)、脑转移瘤数目和颅外转移状态等因素。放射治疗肿瘤组(RTOG)评估了涉及脑转移患者的三个连续试验,并使用递归分区分析(RPA)将预后细分为3类;I类(KPS>70分,<65岁,原发病得到控制,无颅内外转移),III类(KPS <70分),II类(其余的)。利用7个RTOG随机临床试验的去识别数据(de-identified data ),开发出一种脑转移瘤患者的个体化预后诺模图(nomogram),它对咨询患者的预后很有用。
在这篇综述文章中,我们将进一步研究辐射对大脑的影响,重点关注与WBRT或SRS相关的迟发副反应事件。我们将简要介绍其病理生理学、临床表现和缓解策略。
众所周知,脑实质是一种晚反应组织,具有低α/β比和有限的修复能力。此外,脑实质表现出体积效应,即小体积可以耐受较高的辐射剂量。正常组织临床效应的定量分析(QUANTEC)工作组文件是对放疗(RT)的器官特异性组织耐受性重要文献,且得到广泛引用,并将列入以下相关章节。根据临床表现的发病时间,辐射相关并发症可分为急性(放疗期间或放疗后数天至数周发生)、早期迟发(放疗后数周至数月)或迟发的(放疗后数月至数年)。组织学上,Szeifert等人描述了SRS治疗切除的脑转移瘤后出现的3种组织反应;急性、亚急性和慢性型反应。急性型,在SRS治疗后1-17个月观察到,以界限清晰的凝固性坏死(sharply demarcated coagulation necrosis )为特征。而亚急性型,在SRS治疗后5-59个月观察到边界清晰的(well circumscribed )凝固性坏死,而按时间顺序,SRS治疗后9-33个月观察到瘢痕组织和钙化。
脑水肿通常发生在对大脑进行放射治疗的数天至数周内,这是由于辐射引起的血管损伤导致短暂的通透性增加。临床表现为头痛、恶心,甚至原有的神经功能障碍的加重。据报道,SRS治疗后5-43%脑膜瘤患者出现症状性水肿。糖皮质激素通常提供良好的症状缓解,然而,没有皮质类固醇在预防或治疗脑水肿的处方的标准化指南,且实践中医生在很大程度上是依赖3 - 7天使用的4 - 8毫克低剂量地塞米松处方与最常见的质子泵抑制剂。特别是接受SRS治疗的,可在SRS后1-3天发生辐射诱发的癫痫发作,且可能在位于运动皮层的病变中更为常见。然而,在接受SRS治疗患者的癫痫发作的预防实践中仍存在很大的差异。疲劳是WBRT另一个众所周知的急性影响。在接受WBRT治疗的患者中也经常发生可能引起痛苦的脱发(Alopecia )。此前有报道称,低剂量RT可导致可逆脱发,并在2-4个月内完全再生,而高剂量RT可导致不可逆脱发。这引发研究者使用调强放射治疗(IMRT)来评估回避头皮的技术(scalp-sparing technique )。
辐射相关的脱髓鞘发生在放射相关并发症的亚急性期,这些并发症发生在放射治疗后1至6个月。尽管肿瘤本身可以由于压迫和血管紊乱而引起周围组织的脱髓鞘,但辐射和化疗进一步促成了脱髓鞘(42)。有趣的是,剂量依赖性脱髓鞘似乎发生在接受高剂量RT的区域早期,随后的剂量依赖性脱髓鞘发生在RT后4 - 6个月(43)。
SRS后可出现神经麻痹,一般是一过性的。例如,Chopra等报道了4%的听神经鞘瘤患者在SRS后5-48个月出现三叉神经病变。其中约半数患者仅发生一过性麻木,无一例出现面瘫。这与Hansasuta等人对383例SRS治疗的前庭神经鞘瘤患者的回顾性研究结果一致。他们报告了2%的患者在SRS治疗后出现面肌痉挛,其中一半是短暂一过性的,没有人在SRS后出现面部无力。然而,一项对162例因听神经瘤接受SRS治疗的患者进行的研究显示,5年后,分别有79%和73%的患者面部和三叉神经功能正常。最近对49例接受管内段听神经瘤SRS治疗患者的研究报告的常见术语标准报告的不良事件(CTCAE),SRS后3个月出现的面部神经障碍3个月后解决,和一例CTCAE 2级面部肌肉无力12个月后解决。
嗜睡综合征可发生在高达79%对大脑放疗后的患者,其特征是嗜睡(lethargy)、笨拙(clumsiness )、认知功能减退(reduced cognitive function )、困倦(drowsiness )等综合症状,其中一些与癌症患者经历的疲劳症状重叠的症状。在一项前瞻性研究中,19例患者接受了高剂量的RT治疗原发性脑肿瘤,根据Littman量表,所有患者都表现出至少1级疲劳(tiredness ),84%发生>2级嗜睡症状。随后,同一个小组进行了更大规模的研究,在70例接受原发性脑瘤根治性放疗患者中,应用与视觉模拟评分(VAS)评分相关的Littman评分,报告90%的患者为1级嗜睡。在第3周和第12周期间,观察到评分显著增加,并在RT结束时达到峰值,而在第6周后发现有改善。值得注意的是,Littman量表是一个针对嗜睡综合征的特殊评分系统,从0级(没有行为变化)开始到4级(不活动,每天睡18-20小时,发低烧,食欲明显下降,只口服流质)。由于嗜睡综合征可以降低患者的功能能力和打乱他们的日常生活,他们应该充分了解嗜睡综合征影响大多数接受放疗的原发性脑瘤患者的可能性,估计在开始放疗后的6 - 8周达到峰值,并在4到6周后完全消除。
迟发性并发症通常发生在放疗后6个月以上,有不可逆和进行性倾向。迟发性并发症的发病机制通常见于白质,与持续性脱髓鞘、神经发生减少和神经干细胞分化改变、氧化损伤引起的炎症反应以及导致缺血和毒性神经兴奋的微血管破坏有关。
RN通常发生在RT后6 - 24个月之间,但是在再治疗时可以出现得较早。
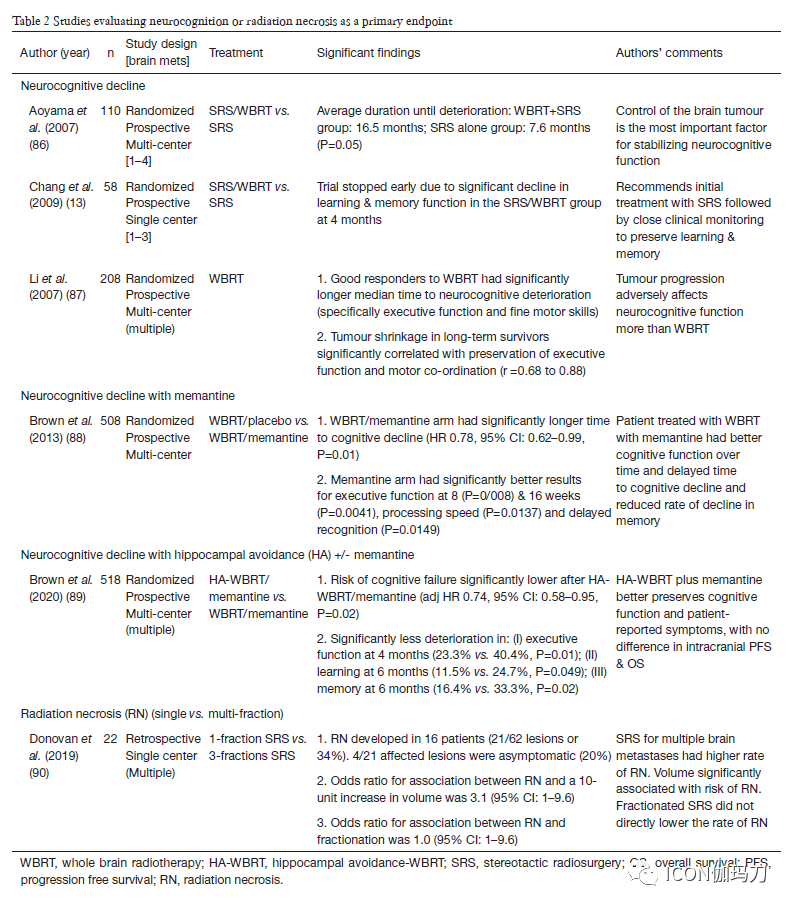
放射性坏死(RN)的危险因素包括再程照射(既往接受过WBRT或SRS)、SRS剂量处方、靶区体积和位置。之前的研究报道了SRS治疗有10%的放射性坏死风险。当使用SRS治疗时,大的病变(直径>4厘米)发展出现放射性坏死(RN)的风险较高。因此,这类患者最好采用先期手术再行瘤腔照射或分割立体定向放射治疗(FSRT)。最近的一项研究比较了1和3次分割SRS治疗出现放射性坏死(RN)作为主要终点,如表2所示。当(以单次分割形式)接受≧12Gy的正常脑实质体积超过10 cc,或当(以5次分割形式)接受≧30Gy受照体积超过10 cc,RN的风险增加。特别是,据报道,重复使用SR治疗一年的RN的风险发生率为20%,既往接受过WBRT或WBRT联合SRS治疗的患者的RN的风险发生率为4-8%。仍不清楚对大脑的再程照射的首选时间间隔,然而,比如最小化计划靶体积(PTV边缘扩展)、优化患者设置,以及使用图像引导则有助于减小暴露于高剂量辐射的正常脑实质的体积。
表2.评价神经认知或放射性坏死作为主要终点的研究。
使用免疫治疗或者靶向治疗进行同步全身系统性治疗可能导致较高的SRS治疗后的放射性坏死的发生率。在Kim等人的一项研究中,使用同步靶向治疗(定义为在五个生物半衰期内给药)增加了12个月放射影像学上放射性坏死(RN)累积发生率(8.8% 相比 5.3%,P<0.01)。使用VEGFR酪氨酸激酶抑制剂(TKI)和EGFR TKIs时,尤其明显。同步化疗增加原发性脑和转移性肿瘤发生RN的风险。然而,没有关于在化疗和实施SRS治疗之间的理想洗脱期标准化的建议,而这通常是根据全身性疾病的负担由具体病例情况决定的。之前的研究也表明在大脑内部的一些地方更倾向于发生RN(如额叶皮层),而其他部位(如脑干)更有抵抗性。Ohtakara和同事们建议认为与较深部的病变相比,浅表病变的RN风险较低,剂量溢漏(dose spillage )发生在非脑实质组织内(如颅骨、皮肤)。
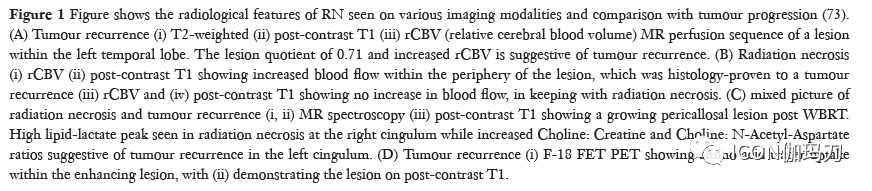
放射性坏死在临床上和影像学上很难与颅内复发区分。临床症状很大程度上取决于其大小/位置,或有时可能保持无症状。(T1序列上)表现为对比增强的病变,伴有周围水肿和脑部MRI上信号强度的变化,这也是复发的常见特征。23例SRS治疗后增大病灶的手术活检或切除术证实22例有放射性坏死。磁共振弥散加权成像被用来鉴别放射性坏死和肿瘤进展。正电子发射断层扫描(PET)中的氨基酸示踪剂(如碳-11蛋氨酸[Carbon-11 methionine,]和氟乙基酪氨酸[Fluoroethyltyrosine ])特别有用,因为正常脑实质的氨基酸摄取相对较低。例如,据报道,在复发胶质瘤的情况下,FET-PET成像的敏感性为100%,特异性为93%。此外,MRI序列,例如化学交换饱和转移(CEST)在鉴别放射性坏死(RN)和肿瘤进展方面显示出前景。图1显示了不同成像方式下放射性坏死(RN)的放射影像学特征以及与肿瘤进展的比较。