美国佛罗里达大学电子与计算工程系的Rene Molina等研究PD患者脚桥核和苍白球内核(GPi)与步态相关的神经电生理功能。研究者对5例FoG的PD患者在服用多巴胺能药物时植入双侧GPi和双侧PPNDBS电极;术后5个月在停药或用药条件下记录执行各种步态任务时的电生理变化;结果发表于2020年6月《Frontiers in Human Neuroscience》在线。
——摘自文章章节
【Ref: Molina R, et al. Front Hum Neurosci. 2020 Jun 4;14:194. doi: 10.3389/fnhum.2020.00194. eCollection 2020.】
人们从动物实验研究中,认识了脚桥核(Pedunculopontine Nucleus,PPN)的生理功能。但尚缺乏人类正常走动的电生理记录。最近,脑深部电刺激(DBS)PPN改善帕金森病(PD)患者的步态和冻结步态(Freezing of Gait,FoG)引起广泛兴趣。美国佛罗里达大学电子与计算工程系的Rene Molina等研究PD患者脚桥核和苍白球内核(GPi)与步态相关的神经电生理功能。研究者对5例FoG的PD患者在服用多巴胺能药物时植入双侧GPi和双侧PPNDBS电极;术后5个月在停药或用药条件下记录执行各种步态任务时的电生理变化;结果发表于2020年6月《Frontiers in Human Neuroscience》在线。
研究结果显示,GPi中低β功率的抑制和PPN中1-8Hz的调制与人类步态相关;同时PPN特征可能反映步行速度。受试者从静息进入走动任务时,GPi核团内β功率去同步化和PPN低频同步化(图1、2、3)。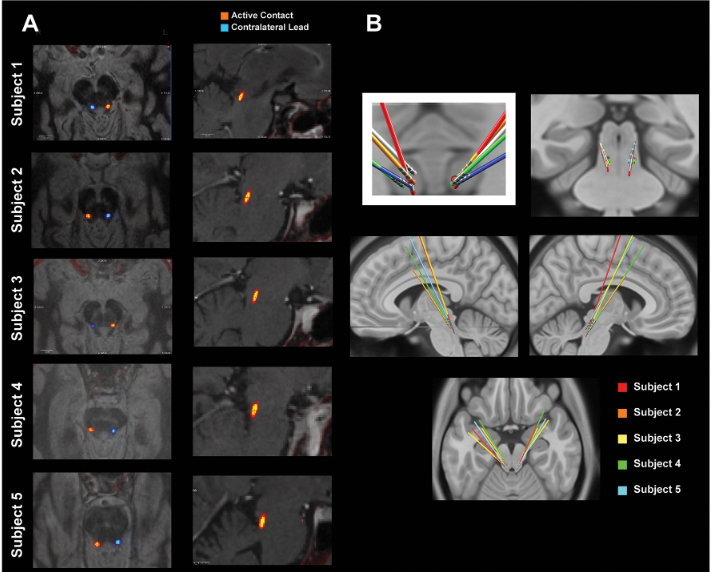
图 1. 脚桥核定位方法。A.每例受试者的MRI-CT配准图像。标记“激活触点”和与步态特征最相关的双极电极配置中心。左图为MRI-T1倒置轴向成像显示激活触点(橙色)和电极导线(蓝色)。右图为MRI-T2矢状位成像显示激活触点。B.在标准化MNI空间内可见DBS及其电极导线。所有导线连接的红点指示PPN的大致位置。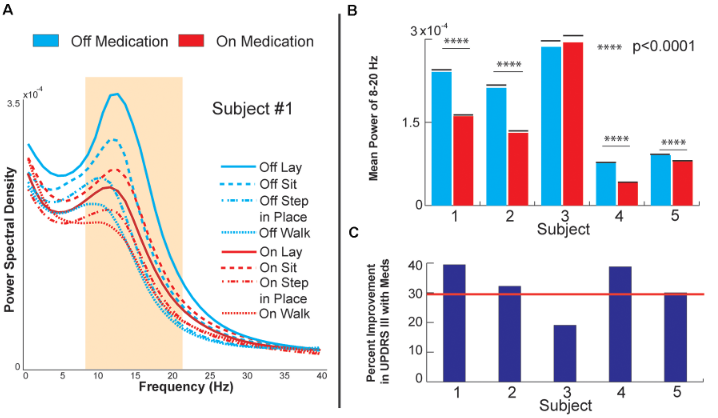
图 2. 苍白球内侧部对药物的反应。A.在各种基线和执行步态任务时,受试者左旋多巴药物治疗关闭和开启时的GPi信号功率谱密度。B.患者坐位时,GPi的β功率降低条形图(8-20 Hz)。C.每例受试者坐位时,从关闭药物至开启药物的UPDRS III评分改善百分比条形图。红线表示改善30%,这是药物反应的常用临床基准。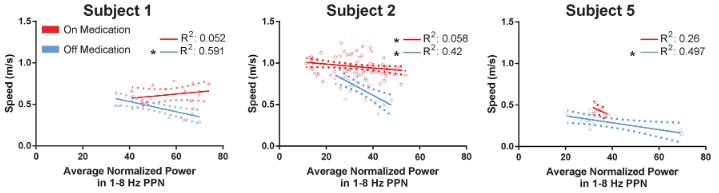
图3. PPN低频特征与步态指标的比较。将受试者1、2和5的平均步行速度与其在1-8Hz PPN特征带中的平均标准化功率作图。每次回归均按受试者在相同的用药条件下进行,共回归6次。每个点代表一次试验。误差线表示趋势线的抛物虚线。*p<0.1。
作者认为,该研究通过检测并发步态障碍或者冻结步态的PD患者脑电生理变化,揭示人类步态与GPi和PPN的神经功能的相关性。实时电生理记录发现对于药物和步态任务,GPi有低β功率抑制,PPN有与走动相关的1–8Hz调制。这些发现增加对步态的神经生理学的理解,并可能有助于开发PD患者异常步态的新疗法。

声明:脑医汇旗下神外资讯、神介资讯、脑医咨询所发表内容之知识产权为脑医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。









