美国孟菲斯市圣犹大儿童医院病理科的Jason Chiang等采用免疫组化、荧光原位杂交、靶向DNA测序、RT-PCR、全外显子测序(WES)和RNA测序(RNA-seq)等技术研究23例TG患者的遗传学变化,通过Infinium甲基化EPIC芯片进行基因学组甲基化分析。结果发表于2019年12月《Acta Neuropathologica》在线。
——摘自文章章节
【Ref: Chiang J, et al. Acta Neuropathol. 2020 Mar;139(3):601-602. doi: 10.1007/s00401-019-02112-x. Epub 2019 Dec 10.】
研究背景
研究结果
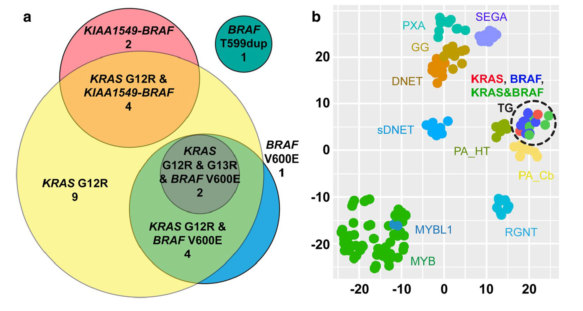
该研究结果显示,19例(82.6%)TG患者的KRASG12R热点突变发生率高;在14例(60.9%)肿瘤中,发现BRAF改变(包括KIAA1549-BRAF、V600E或T599dup)。10例(43.5%)肿瘤内同时包含KRAS和BRAF的变化。根据免疫组化以及与肿瘤细胞相关的KRAS和BRAF改变发生率,研究者认为KRAS和BRAF改变可能发生在同一肿瘤细胞内。所有的TG患者均未出现IDH1、IDH2、TP53、ATRX、组蛋白H3基因、MYB或MYBL1的基因突变。WES或RNA-seq也未发现其它变异或融合。在DNA甲基化层面,TG的KRAS或BRAF任何状态,TG的甲基化表达谱明显区别于下丘脑和小脑的PA表达谱,形成独特的类型(图1)。
结论
作者指出,研究发现在23例TG中,有较高的KRAS G12R突变率以及伴随的KRAS和BRAF改变,显示TG具有独特的临床和形态学特征以及甲基化组谱;建议开展进一步研究TG与cIMPACT‑NOW中描述的其它儿童弥漫性胶质瘤之间的关系。