来自瑞士伯尔尼大学附属医院神经内科的Urs Fischer等人开展了此项观察性队列研究,旨在确定在机械性血栓切除术( MT)失败或脑血管不完全再通的情况下予以动脉内尿激酶的安全性及有效性。
——摘自文章章节
【Ref: Kaesmacher J, et al. JAMA Neurol. 2019 Dec 9. doi: 10.1001/jamaneurol.2019.4192.】
研究背景
实现脑血流完全再灌注(TICI评分3级)是接受机械性血栓切除术(mechanical thrombectomy, MT)治疗患者获得良好结局的关键决定因素。在实际临床工作中,由于栓子自身性质和术者操作方式等多种原因,并非所有患者均能实现脑完全再灌注。此时,动脉内应用组织型纤溶酶原激活剂或尿激酶原/尿激酶可能成为新的选择方式。然而,该方法作为MT辅助治疗方法的安全性和有效性目前尚缺乏相关研究。为此,来自瑞士伯尔尼大学附属医院神经内科的Urs Fischer等人开展了此项观察性队列研究,旨在确定在MT失败或脑血管不完全再通的情况下予以动脉内尿激酶的安全性及有效性,相关结果发表在2019年12月的《JAMA Neurology》上。
研究方法
研究者从三级卒中中心的前瞻性登记研究(Bernese Stroke Registry/Bernese卒中登记研究)中收集数据,Bernese卒中登记研究包括自2010年1月1日至2017年8月4日期间接受第二代取栓装置MT治疗的连续病例。在筛选的1274例患者中,69例患者拒绝参与,在排除了仅接受动脉内尿激酶(有或无静脉tPA治疗)治疗的患者和存在后循环大血管闭塞或前循环远端血管闭塞的患者后,剩余993例患者符合前循环大血管闭塞的观察性研究的入选标准。其中100例患者在MT治疗失败或脑血管不完全再通后接受了额外的动脉内尿激酶治疗。
在该研究中,尿激酶的应用剂量范围为50000至1 000 000 IU(中位剂量为300 000 IU)。正常情况下,尿激酶的应用时间大约为45至60 min,但如果在动脉内尿激酶应用期间连续进行诊断性血管造影显示血管再通则终止尿激酶应用。实验主要安全性结局是根据PROACT-II(Prolyse in Acute Cerebral Thromboembolism II)标准定义的症状性颅内出血(symptomatic intracranial hemorrhage, sICH)。次要终点包括90天死亡率和90天功能独立性(定义为改良Rankin量表[modified Rankin Scale, mRS]评分≤2分)。在给药前后采用TICI分级对患者脑血流进行评估。研究者分析了2017年9月1日至2019年9月20日的患者数据。
研究结果
结果提示,排除后循环卒中患者和仅接受动脉内溶栓治疗的患者后,993例患者被纳入最终分析(中位年龄:74.6[四分位数间距:62.6-82.2]岁;505例[50.9%]女性)(表1)。
表1. 基线和手术特征
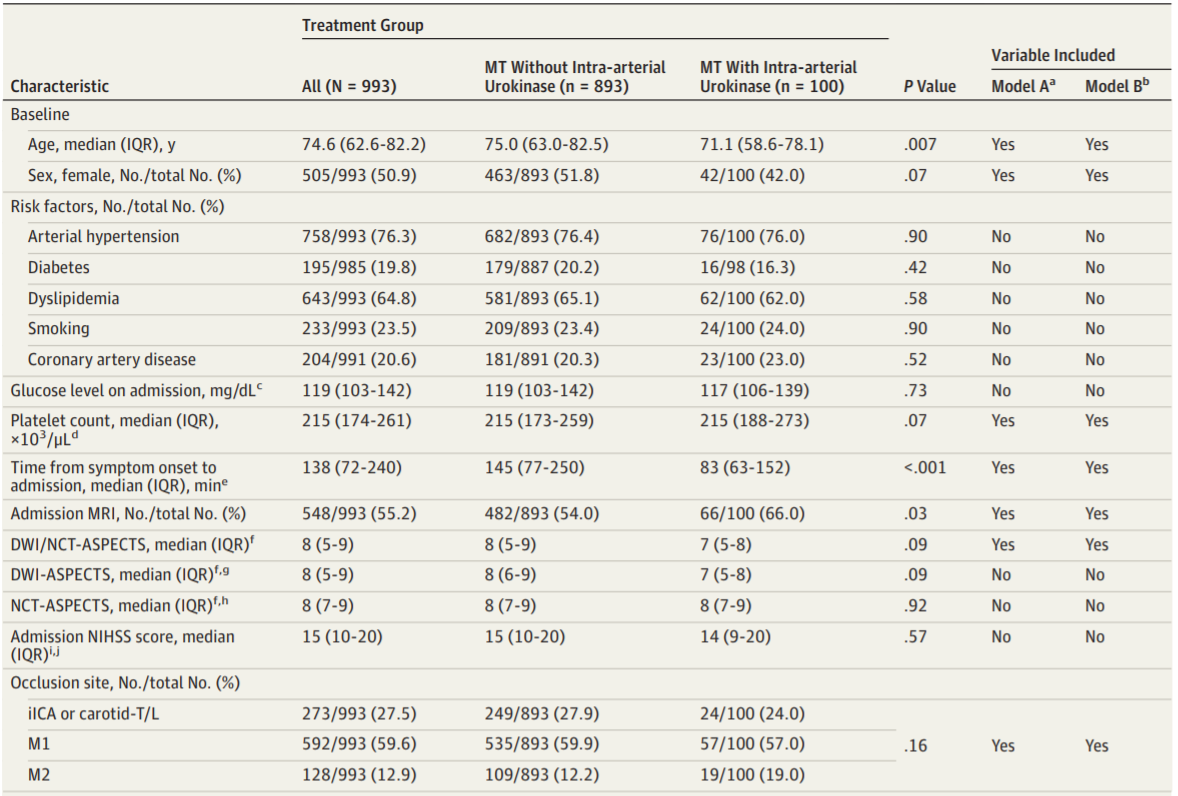
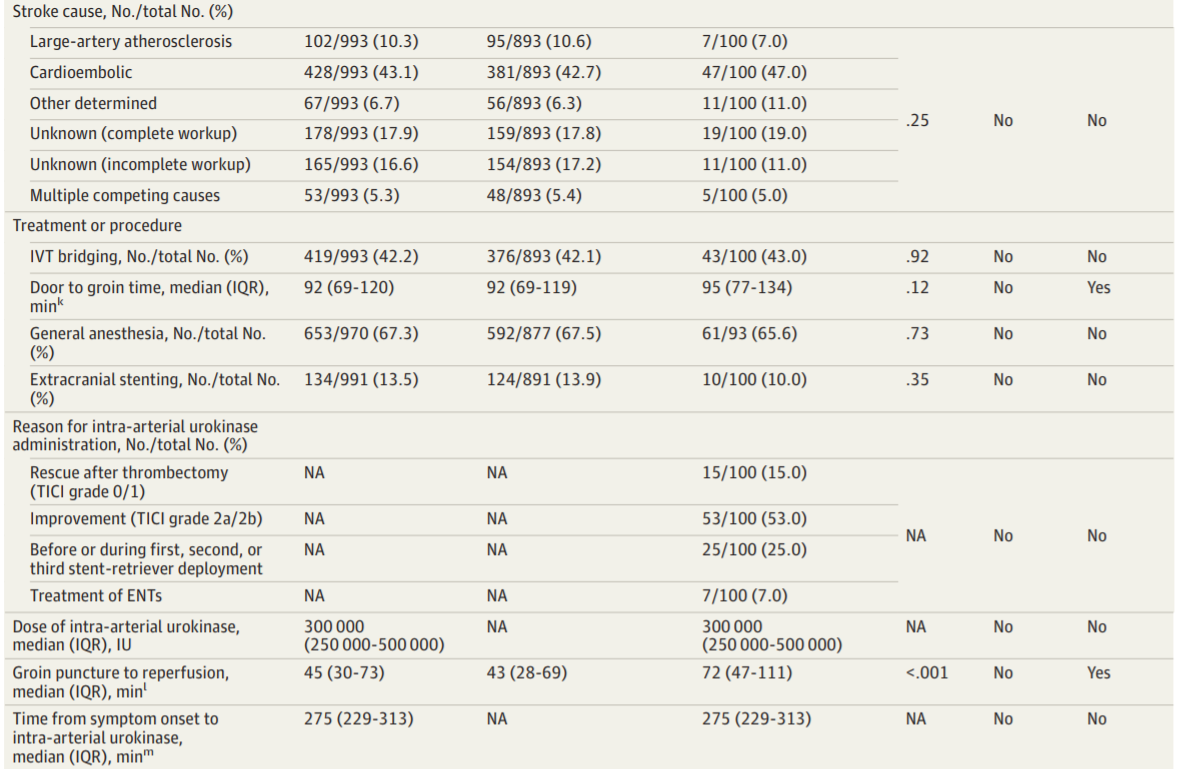
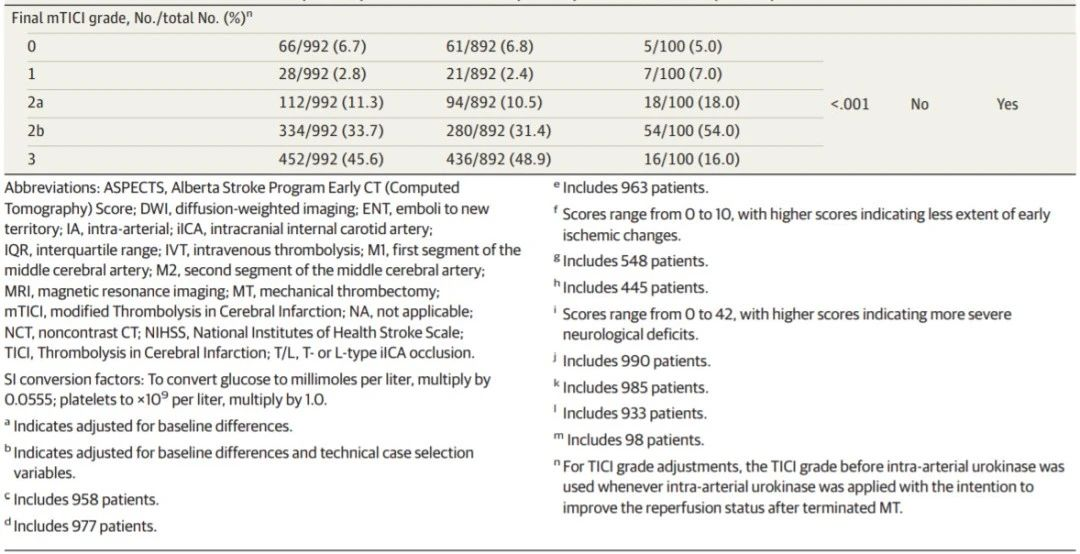
100例患者(10.1%)接受了额外的动脉内尿激酶治疗。给予动脉内尿激酶的最常见原因是MT后未达到完全再灌注(TICI<3)(53.0%),其他原因还包括MT失败(15%)、术者根据各自习惯在取栓前或取栓中运用为促进血栓清除(25%)、治疗异位栓子(7%)。使用和不使用动脉内尿激酶的患者全身出血发生率相当(表2)。
表2. 主要和次要结局
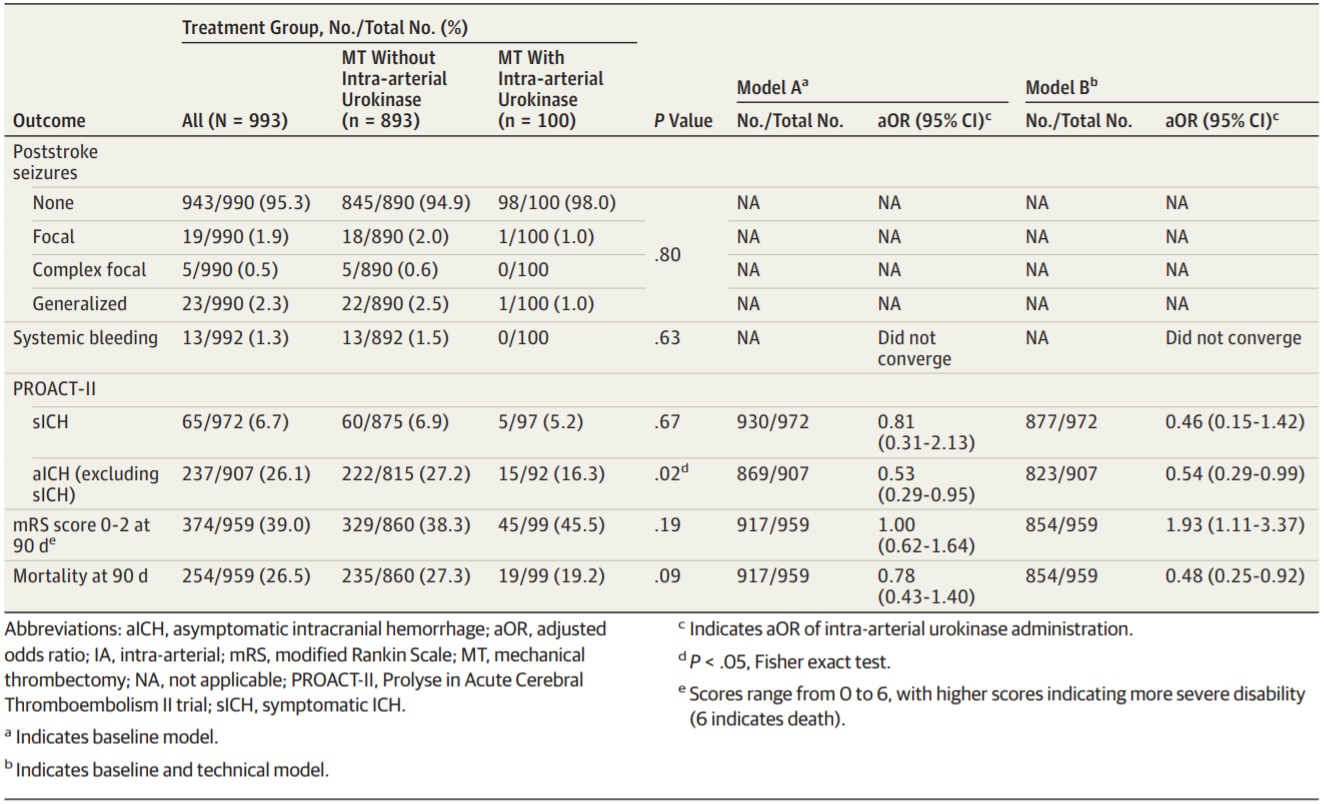
在根据病例选择调整基线特征后,动脉内尿激酶与sICH风险增加(校正比值比[adjusted odds ratio, aOR]:0.81, 95%CI: 0.31-2.13)或90天死亡率(aOR: 0.78, 95%CI: 0.43-1.40)无关(图1)。
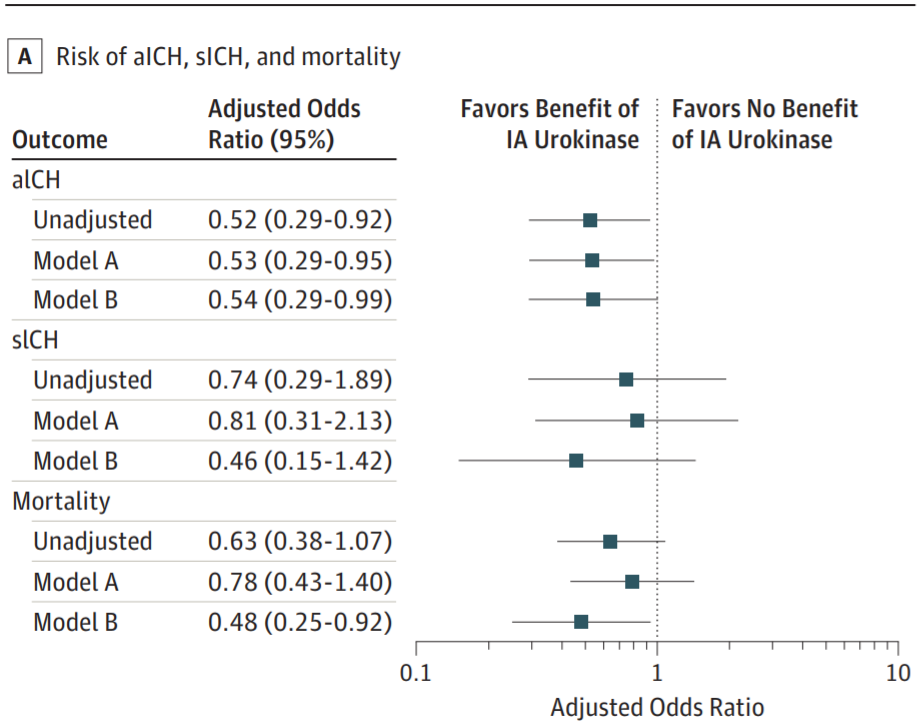
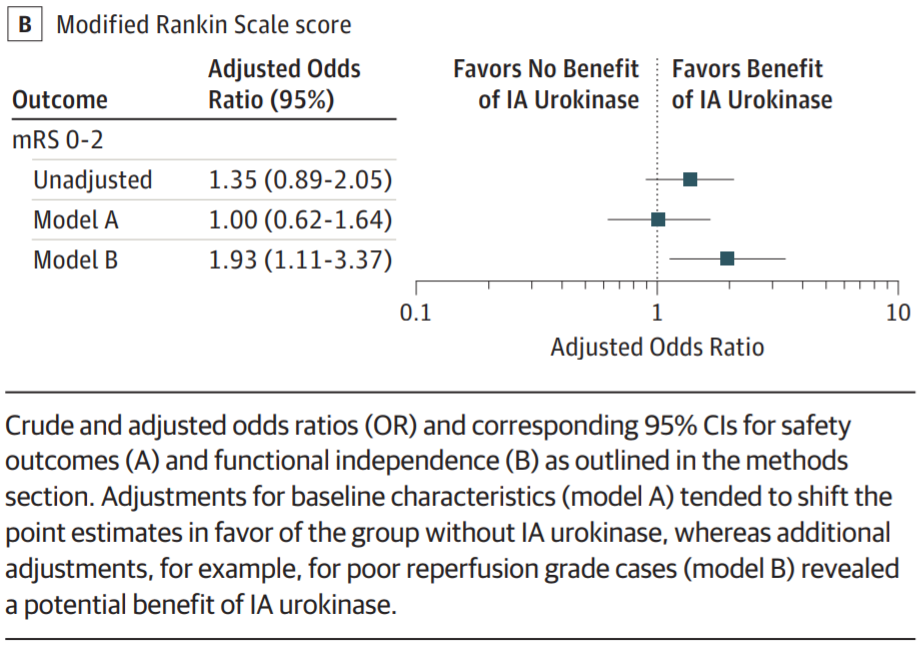
图1. 动脉内(IA)尿激酶和几种结局的粗比值比和校正比值比
在53例部分或接近完全再灌注并接受动脉内尿激酶治疗的患者中,有32例(60.4%)早期再灌注有所改善,53例中18例(34.0%)TICI分级有所改善。相应地,在动脉内尿激酶治疗组中,在调整了先前较差TICI分级的选择偏倚后,接受动脉内尿激酶治疗的患者其功能独立性的比率较高(aOR: 1.93, 95%CI: 1.11-3.37)。
研究结论
最后研究结果表明,作为辅助手段, MT术中或术后给予动脉内尿激酶似乎是安全的,未增加全身、有症状或无症状颅内出血的风险,并且可能改善血管内介入手术患者的再灌注状态,从而可能改善结局。当然,该方法是否安全有效仍需多中心前瞻性注册甚至随机对照研究的验证。
即日起“神经介入资讯”更名为“神介资讯”





