Davidoff-Schechter(ADS)动脉是大脑后动脉仅有的硬膜支,不同于一般的硬膜动脉,它起自硬膜内动脉结构。1965年首先由Wollschlaeger通过尸体钡剂造影显示。
——摘自文章章节【REF: Bhatia KD, et al. American Journal of Neuroradiology February 2020, 41 (2) 300-304; DOI: 10.3174/ajnr.A6380.】
1
研究背景
Davidoff-Schechter动脉(ADS)是大脑后动脉的硬膜支,供应大脑镰-天幕交界处的硬脑膜。常规血管造影上ADS动脉一般不能显示,仅在参与供血硬脑膜动静脉瘘、脑膜瘤或极少数小脑肿瘤时扩张可见。
ADS动脉在其供血的硬脑膜动静脉瘘的治疗中的意义尚不明确。作者回顾了该中心自2006年至2018年治疗的173例硬脑膜动静脉瘘(DAVF),评价ADS动脉相关的局部血管构筑、栓塞策略及临床预后。该组病例中6例(3.5%)存在ADS动脉参与供血。所有病例均采用液体栓塞材料经动脉途径栓塞。其中3例首次栓塞后存在残余瘘口并通过ADS动脉供血,需行二次介入治疗,所有病例最终均得到影像学治愈。
ADS动脉是大脑后动脉仅有的硬膜支,不同于一般的硬膜动脉,它起自硬膜内动脉结构。1965年首先由Wollschlaeger通过尸体钡剂造影显示。ADS动脉可起自大脑后动脉P1-P2段交界处的上表面、或P2段近端,向后外侧延伸穿过环池,于小脑上动脉上方、滑车神经下方走行,最终到达天幕游离缘。供应天幕后内侧约3-4厘米范围硬膜的下表面,并形成对Bernasconi-Cassinari动脉(脑膜垂体干的分支)的补充。ADS动脉在镰-幕交界处与对侧同名动脉吻合,穿过硬膜向后上方沿大脑镰最终到达上矢状窦。
1
材料与方法
研究纳入单中心2006-2018年的DAVF病例,入组标准为DSA证实有ADS参与供血,采用DSA或MRA随访。特征性影像学表现包括:瘘口位置,供血动脉,静脉引流,Borden及Cognard分型,血管内治疗的入路,所用栓塞材料,血管内治疗的次数,首次栓塞后参与瘘口通过ADS动脉供血,最终的影像学转归。
1
研究结果
173例病人共192个DAVF中,6例病人(6个瘘口,3.1%)存在ADS动脉供血(女性3例,男性3例,平均年龄46.5岁):1例表现为蛛网膜下腔出血,4例镰-幕DAVF(均为Cognard IV级),1例为矢状窦旁DAVF(Cognard III级),1例为上矢状窦DAVF(Cognard IIa+b级)。
1
栓塞策略
所有6例患者均采用液体栓塞材料,3例由于存在残余瘘口通过ADS动脉供血需要二次栓塞。2例超选择插管至ADS动脉内,病例2通过ADS动脉栓塞。所有病例在最终的DSA上均获得治愈性栓塞。无手术相关并发症,尤其无返流至大脑后动脉。
1
讨论
回顾文献,作者认为ADS动脉供血不显示可能是由于多支供血动脉的竞争血流所致,故在天幕DAVF病例中容易忽视。天幕DAVF仅占颅脑DAVF不足3%,但出血风险相比其他部位高6倍,可能与其直接向软膜静脉引流相关。本组病例均采用经动脉途径栓塞。
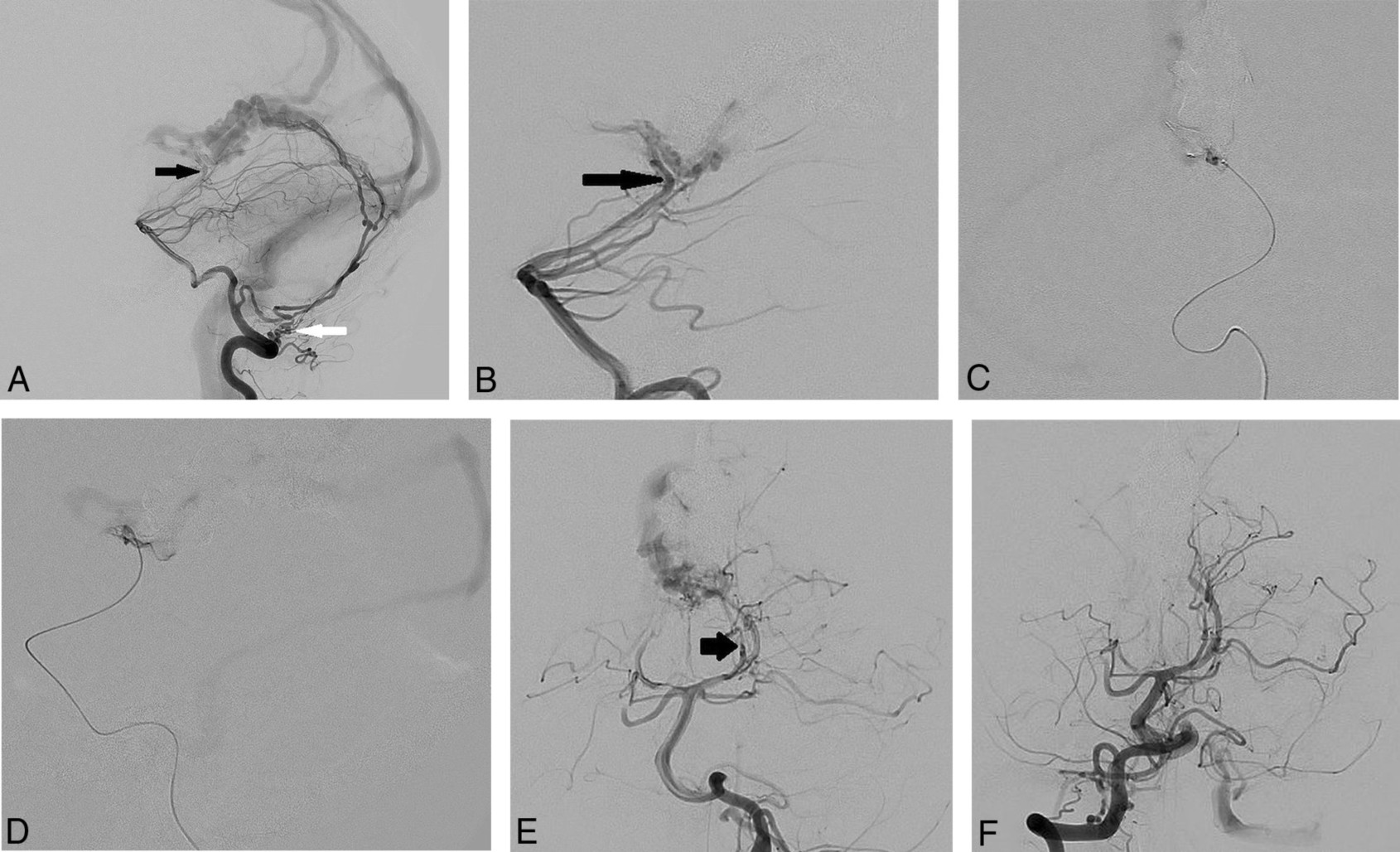
病例2,作者首先闭塞其他脑膜供血动脉后,微导管直接经ADS动脉超选并栓塞。采用改良高压锅技术:先使用弹簧圈减少返流,再通过微导管进一步注入Onyx胶。理解局部动脉解剖是安全有效的治疗关键。(图例1)
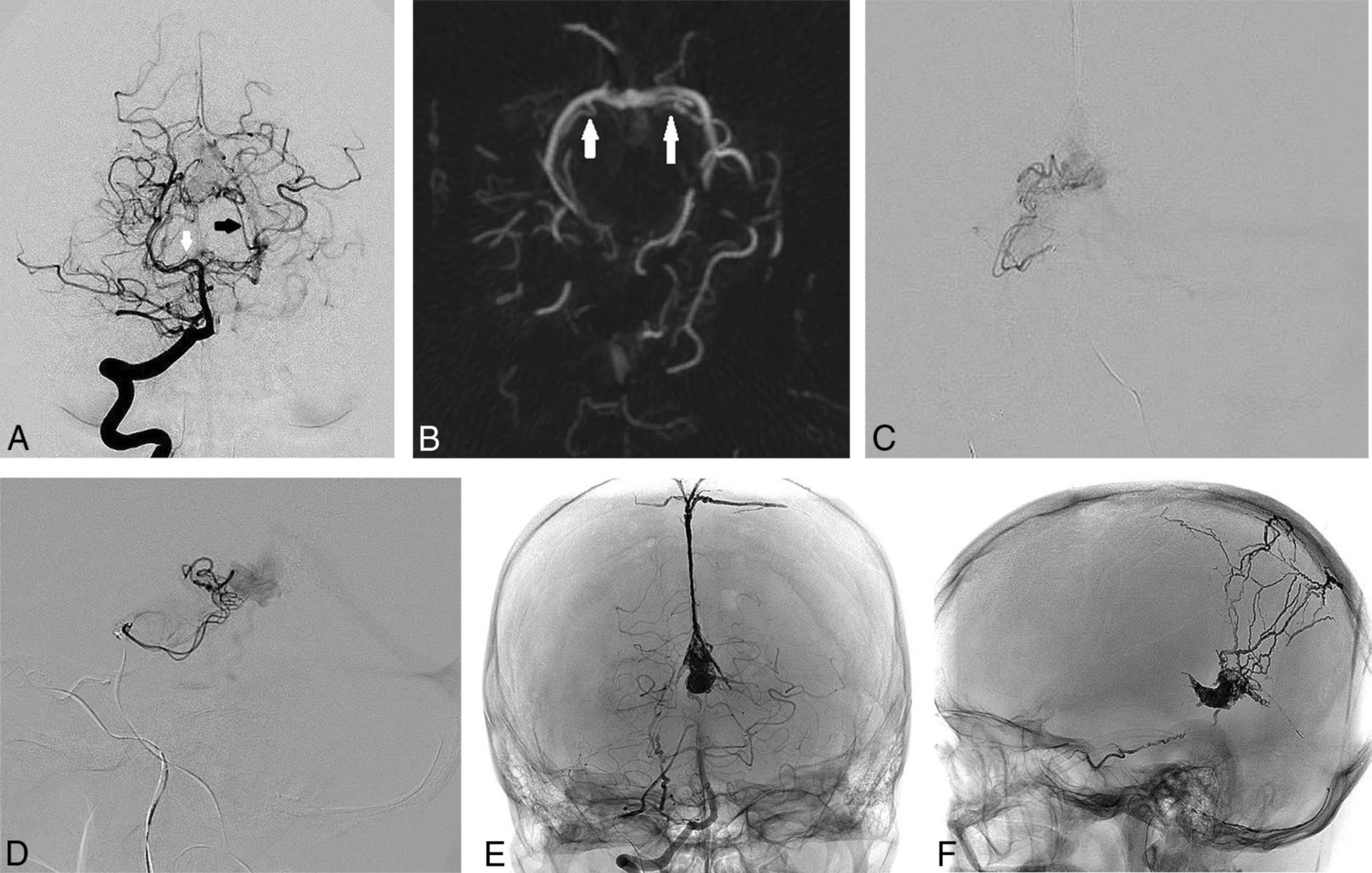
病例1中(图例2),超选进入右侧ADS动脉主干,但无法进一步靠近瘘口(图2D),我们认为在近端注胶需要较长一段返流,可能增加胶返流进入大脑后动脉或基底动脉的风险。最终该病例通过静脉途径栓塞治愈。
1
ADS动脉供血的意义
作者认为避免ADS动脉返流的关键是首先要认识它参与供血的DAVF。ADS动脉的识别可能因竞争血流的影响而存在困难,而Galen静脉型天幕DAVF又常有小脑上动脉或大脑后动脉供血,所以有理由假设大多数镰-幕区DAVF均有潜在的ADS动脉供血。因此应当采用放大高帧数DSA及三维旋转造影MPR重建来仔细评估ADS动脉的血供。即使未发现ADS供血,仍需十分小心地识别任何自Galen静脉向前沿着天幕游离缘方向的线样返流,这可能表示存在向大脑后动脉或基底动脉的返流。
1
结论
ADS动脉参与供血的DAVF少见,外科手术或介入栓塞困难。作者认为ADS动脉作为硬膜动脉网和后循环软膜动脉的直接沟通,形成了潜在的危险吻合,识别ADS动脉供血可以避免液体栓塞材料返流进入软膜血管造成医源性栓塞。
张晓龙教授点评:
即日起“神经介入资讯”更名为“神介资讯”






