随着人口老龄化趋势的进展和医学影像学技术的进步,需要住院治疗的颈动脉狭窄患者的检出率越来越高。颈动脉狭窄是引起缺血性卒中的重要因素之一,对其及时治疗有利于改善患者的症状和生存质量。对于颈动脉狭窄,目前的治疗方法主要有颈动脉内膜切除术(carotid endarterectomy,CEA)和颈动脉支架成形术(carotid artery stenting,CAS)。对于两种方法孰优孰劣目前仍有争议。本研究对分别接受CEA和CAS治疗的两组患者的疗效进行比较,现报道如下。
回顾性分析2017年7月至2018年12月于苏州大学附属第一医院神经外科或介入科因颈内动脉狭窄行手术治疗的136例患者。病例纳入标准:患者在术前均行经颅多普勒(transcranial Doppler,TCD)、头颅CT血管成像(CTA)或数字减影血管造影(DSA)以及头颅CT灌注成像(CTP)确诊为颈内动脉狭窄[1]。如狭窄程度为50%~69%为中度狭窄,狭窄程度≥70%则为重度狭窄。排除标准:(1)同侧或对侧已行CAS或CEA治疗;(2)合并颅内动脉瘤等颅内其他病变,并同期行开颅手术治疗;(3)合并对侧颈动脉狭窄,并同期行CEA治疗;(4)行复合手术治疗颈动脉狭窄。其中78例在神经外科行CEA(CEA组),58例在介入科行CAS(CAS组)。CEA组患者中,男69例,女9例;年龄为(66.7±7.6)岁;颈动脉狭窄位于右侧43例,左侧35例。术前合并高血压57例,合并糖尿病14例,有脑梗死病史19例,心脏病史12例。CAS组患者中,男48例,女10例;年龄为(65.1±95)岁;狭窄位于右侧29例,左侧29例。术前合并高血压41例,合并糖尿病15例,有脑梗死病史14例,心脏病史6例。所有患者或家属均知情同意并签署知情同意书。本研究经苏州大学附属第一医院伦理委员会批准[伦理批号:(2019)伦研批第083号]。
所有患者术前均行头颈部TCD、头颈部CTA+CTP或DSA,明确颈内动脉狭窄的诊断并评估其狭窄程度。对于行CEA的患者,术前1周口服氯吡格雷(75 mg/d)和阿托伐他汀(20 mg/d);术中行TCD检测大脑中动脉的血流情况,如血流量较术前增加2倍以上,术后需严格控制收缩压在140 mmHg(1 mmHg=0.133 kPa)以下,防止术后出现过度灌注。术后常规口服氯吡格雷(75 mg/d)和阿托伐他汀(20 mg/d)3个月。对于行CAS的患者,术前5 d开始口服氯吡格雷(75 mg/d)和阿司匹林(100 mg/d),术后常规使用氯吡格雷(75 mg/d)和阿司匹林(100 mg/d)共3个月,3个月后长期口服阿司匹林(100 mg/d)[2]。
(1)所有行CEA治疗的患者均在全身麻醉下手术。术中予心电监护,动态监测血压。术前评估动脉内膜斑块远端与颈动脉分叉的距离,并据此选择合适的手术切口。切口位于胸锁乳突肌前缘,逐层分离颈前组织,充分显露颈总动脉、颈内动脉、颈外动脉。分离显露过程中需注意保护舌下神经、迷走神经等重要结构。在阻断颈总动脉、颈内动脉、颈外动脉前予静脉给药全身肝素化(1 mg/kg),并调整收缩压大于基础血压约20 mmHg,防止术中出现脑组织低灌注。动脉内膜斑块完整剥离后,以7-0缝合线连续缝合,根据患者的斑块和血管特征分别行标准CEA(57例)、外翻式CEA(13例)或标准CEA+补片成形术之一[3](8例)。切口缝合完毕,将血压调整至基础血压,静脉推注鱼精蛋白中和肝素,解除动脉临时阻断(图1)。术后留置皮下引流管48 h,严格控制血压。(2)行CAS的患者在全身麻醉下手术。术中予心电监护,动态血压监测。穿刺右侧股动脉,置入8 F动脉鞘,全身肝素化后将导引导管(Vatar,美国Cordis公司)置于颈动脉狭窄近端,先放置保护伞(Spider,美国Medtronic公司),再用球囊(Invatec,美国Medtronic公司)进行预扩张,扩张满意后置入自膨式支架(Protege,美国Medtronic公司),准确定位后释放支架,回收保护伞,撤出导丝和导管,缝合股动脉(图2)。术后心电监护至少应用48 h,严格控制血压。
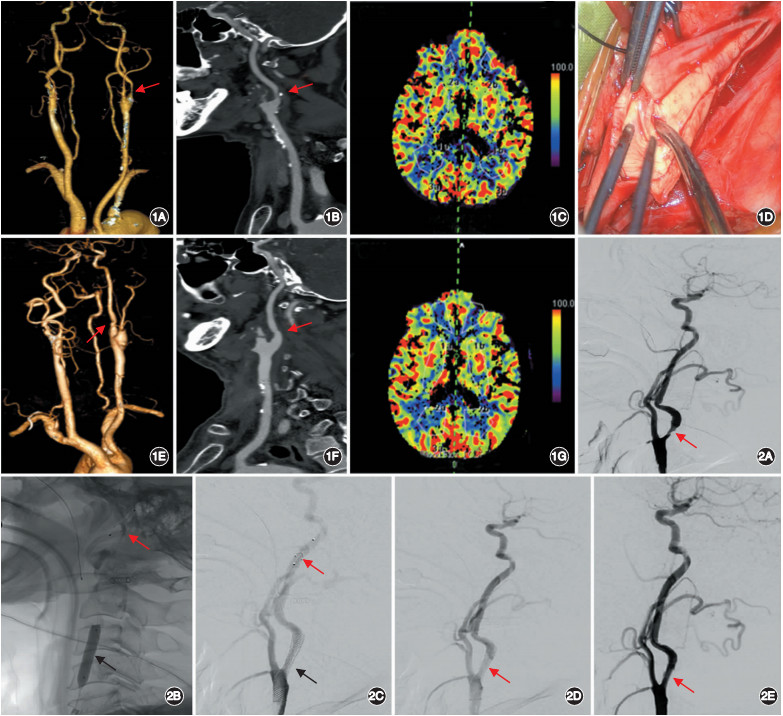
图1. 患者男,65岁,因“头晕3个月余”入院,既往高血压病史10余年A,B.术前CT血管成像(CTA)提示左侧颈内动脉狭窄,狭窄率达80%(箭头所示);C.术前头颅CT灌注成像(CTP)未见明显异常;D.术中显露斑块,可见颈总动脉、颈内动脉及颈外动脉;E,F.术后第3天复査CTA提示颈内动脉狭窄明显减轻(箭头所示);G.术后CTP检査未见明显新发缺血灶 图2.患者男,71岁,因“间断头晕5个月余”入院,既往有高血压病史10余年、糖尿病病史3年A.术前头颅数字减影血管造影(DSA)提示右侧颈内动脉重度狭窄,狭窄率为87%(箭头所示);B.术中DSA显示球囊扩张狭窄部(红色箭头指示保护伞,黑色箭头指示球囊);C.术中DSA显示释放支架(红色箭头指示保护伞,黑色箭头指示支架);D.支架置入后即刻DSA提示血流恢复良好,无明显狭窄(箭头所示);E.术后6个月复査DSA,未发生再狭窄(箭头所示)
患者分别于出院后1、3、6个月常规门诊复查,行头颈部TCD、头颈部CTA+CTP。随访过程出现以下事件则终止随访:短暂性脑缺血发作、重度大面积脑梗死、肢体致残等。对出院超过6个月的患者至少电话随访1次。
采用SPSS 22.0统计软件分析数据。符合正态分布的计量资料以均数±标准差
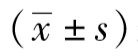
表示,两组比较采用独立样本t检验;计数资料以百分率或构成比表示,两组比较采用卡方检验。以P<0.05为差异有统计学意义。
两组临床资料的比较结果见表1。两组的性别组成、年龄、病变侧别、有无临床症状、术前合并症方面的差异均无统计学意义(均P>0.05),表明两组具有可比性。136例患者的术后随访时间为3~21个月。CEA组与CAS组术前颈内动脉狭窄率、手术时长的差异无统计学意义(均P>0.05,表1)。CEA组患者术后出现伤口感染2例,因切口渗血出现窒息1例,过度灌注2例,急性脑梗死1例。CAS组术后短期发生穿刺部位假性动脉瘤1例,过度灌注2例,心律失常1例。两组术后并发症发生率的差异无统计学意义[分别为7.7%(6/78)和6.9%(4/58),P>0.05]。CEA组的术后住院时长和住院费用均少于CAS组(均P<0.01)。两组术后再狭窄发生率的差异无统计学意义(P>0.05)。
表1. 两组临床患者资料的比较结果
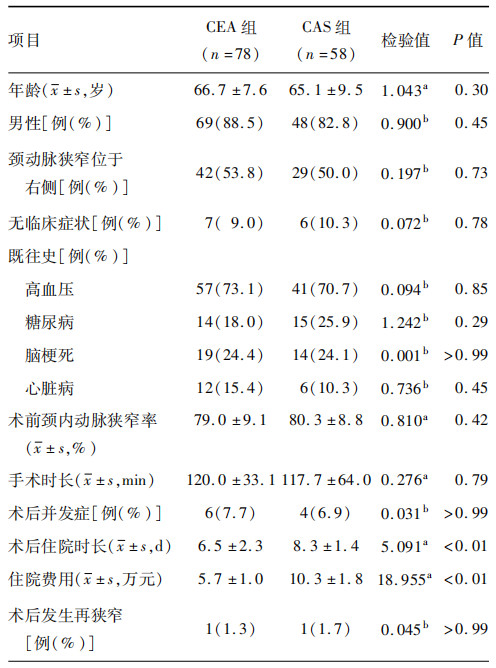
注:a为t值,b为χ2值;CEA为颈动脉内膜切除术,CAS为颈动脉支架成形术
颈动脉狭窄是导致缺血性中风的重要原因,正逐渐成为影响公众健康的焦点问题[4]。对于轻度颈动脉狭窄,目前通常采用药物治疗,而中、重度狭窄(狭窄率≥50%)则往往需要手术干预。既往CEA一直被认为是颈内动脉狭窄治疗的金标准[5]。
近年来,随着介入技术的快速发展,采用CAS治疗颈内动脉狭窄患者的比率从1998年的2.8%增至2008年的12.6%[6],且这一比例仍在快速增长。最近一项韩国的研究显示,16065例接受手术治疗的颈内动脉狭窄患者中,接受CAS手术的患者比率占75.8%[7]。本研究中,采用CAS的患者占比达42.6%(58/136),与Howie等[8]报道的结果相似。本研究从两组患者的手术时长、术后并发症、术后住院天数、住院费用以及术后再狭窄发生率入手,探讨两种术式的优劣。结果显示,与CAS组相比,采用CEA的患者术后住院时间较短,总的住院费用更少;而在其他方面两种手术方法的差异并无统计学意义。
CEA具有较长的临床应用历史,其安全性已被验证[9]。考虑到常规CEA的不足,逐步演化出外翻式CEA和常规CEA+补片技术[10-12]。这几种技术均被证实对颈内动脉狭窄具有良好的适用性,并且在患者的预后方面并无明显差别[10]。CEA技术最主要的问题是术中阻断一侧颈内动脉可能造成术后脑缺血症状,对此,一方面可通过缩短手术时间减少该并发症;另一方面,转流技术的使用大大降低了这一风险。此外,CEA也有导致颈部神经、血管损伤的风险。
CAS是近20年发展起来的血管内治疗技术。根据现有的指南,CAS仍作为CEA的补充,主要用于具有严重心脏、肾脏等疾病的患者[13-14]。CAS最大的弊端是术中或术后短期斑块脱落造成新发脑梗死,原本存在于血管内的斑块被挤压后断裂、松动是主要原因[15]。而一项纳入2001例颈内动脉狭窄患者的研究证实,血管保护装置的运用可极大降低术中脑梗死的发生率[16]。有学者认为,CAS术后再发卒中的风险高于CEA,而CEA术后发生心肌梗死的风险高于CAS[17]。另一部分研究表明,CAS与CEA术后发生卒中及心肌梗死的风险相当[18]。最近一项纳入6094例患者的研究显示,对于有症状的颈内动脉狭窄患者,接受CAS的患者住院期间的病死率高于接受CEA的患者[19]。
行CEA或CAS患者的长期预后结果主要指术后120 d以上发生再卒中或再狭窄的情况[20]。研究表明,虽然CAS围手术期卒中的发生率大于CEA组,但从长期预后来看,两种术式相近。文献报道,CEA术后的再狭窄率为6%~36%,主要发生于术后2年之后[21]。一项针对CAS的荟萃分析显示,CAS的术后再狭窄率约为10%[22]。Peluso等[23]比较了CEA和CAS的术后再狭窄率(中位随访时间为3年),分别为5.5%和3.2%,且两者的差异并无统计学意义。本研究结果与文献报道结果相似,均显示两种术式的预后无明显差异,本组患者的再狭窄率(1.5%,2/136)较文献报道的结果(6%~36%)明显偏低,可能与本研究随访时间较短有关。
本研究尚有几点不足。首先,本研究为小样本回顾性分析,特别是CAS组患者仅58例,不具有完全的代表性;回顾性分析会受到患者的一般特征和术者治疗习惯的影响,虽然本研究中患者的临床特征并无明显的组间差异,仍需前瞻性随机队列研究验证本研究结论的可靠性。其次,随访时间较短。在随访期内仅出现2例再狭窄患者,根据文献报道,再狭窄一般发生于术后2年,故而今后更长时间的随访研究是必要的。第三,分组尚需更加细化,本研究两组患者中均包括有症状和无症状的患者,如能增大样本量,探讨两种术式对于无症状性颈动脉狭窄治疗效果的差异将更有说服力。
总之,本研究结果表明,对于单纯颈内动脉狭窄患者,CEA和CAS均为安全、有效的治疗手段。接受CEA和CAS两种手术方式的患者群体在一般特征上并无明显差异。考虑到住院时间和经济因素,CEA具有一定的优势。
利益冲突 所有作者均声明不存在利益冲突
即日起“神经介入资讯”更名为“神介资讯”
参考文献













