Hippo通路在癌症中的研究是近年来的热点之一。Hippo通路相关蛋白包括LATS1、LATS2、YAP、TAZ等的异常表达与肿瘤患者病理特征及临床预后的相关。已有研究证实,调控异常的Hippo通路在胶质瘤的发生发展中起到了关键性作用,包括细胞增殖、凋亡、侵袭迁移等。日前,山东大学齐鲁医院、脑与类脑科学研究院李新钢、王剑课题组在Nature子刊Oncogene杂志(一区,影响因子6.634)上发表两篇研究性论文,题为“RNA splicing factor USP39 promotes glioma progression by inducing TAZ mRNA maturation”和“PMEPA1 isoform a drives progression of glioblastoma by promoting protein degradation of the Hippo pathway kinase LATS1”。这两篇文章揭示了癌基因USP39和PMEPA1a如何通过影响Hippo通路的关键元件来调控胶质瘤发展,阐明Hippo信号通路在癌症中失调的分子机制,为脑胶质瘤开发靶向治疗方案提供了新的思路。齐鲁医院研究生丁凯凯和季剑雄为两篇文章共同第一作者,通讯作者为李新钢、王剑和王新宇教授,合作者包括齐鲁医院“外专双百计划”特聘专家Frits Thorsen教授及挪威卑尔根大学脑科学团队等。山东大学齐鲁医院为第一作者和通讯作者单位。
恶性胶质瘤是成人最常见的侵袭性和致命性的原发性脑瘤。其中胶质母细胞瘤(GBM)患者的中位生存时间仅有14.6个月。阐明胶质瘤侵袭、复发、放化疗抵抗的分子机制,寻找有效的潜在治疗靶点,成为提高胶质瘤患者生存率的关键,也是世界胶质瘤研究的难题。
USP39是去泛素化蛋白家族中的一员,但USP39并不具备去泛素化活性。USP39作为剪切复合物的分子之一,参与mRNA剪接的调控。在本研究中,研究人员通过转染一系列双荧光素酶报告基因系统检测USP39敲减后对7条经典癌症通路的影响,并证实USP39和Hippo通路转录共激活因子TAZ有相关性。随后,研究人员又通过设计特异性的引物,揭示USP39通过促进TAZ mRNA的成熟促进胶质瘤恶性进展。
PMEPA1,又名TMEPAI,已被证明在前列腺癌发生中发挥重要作用。研究人员首次发现其蛋白亚型PMEPA1a在胶质瘤中高表达,并能促进胶质瘤恶性发展。随后利用免疫共沉淀-质谱分析技术,揭示PMEPA1a通过募集泛素连接酶NEDD4导致了Hippo通路上游激酶LATS1的蛋白酶体降解,从而引起Hippo通路沉默,最终促进胶质瘤的生长侵袭等恶性生物学行为。
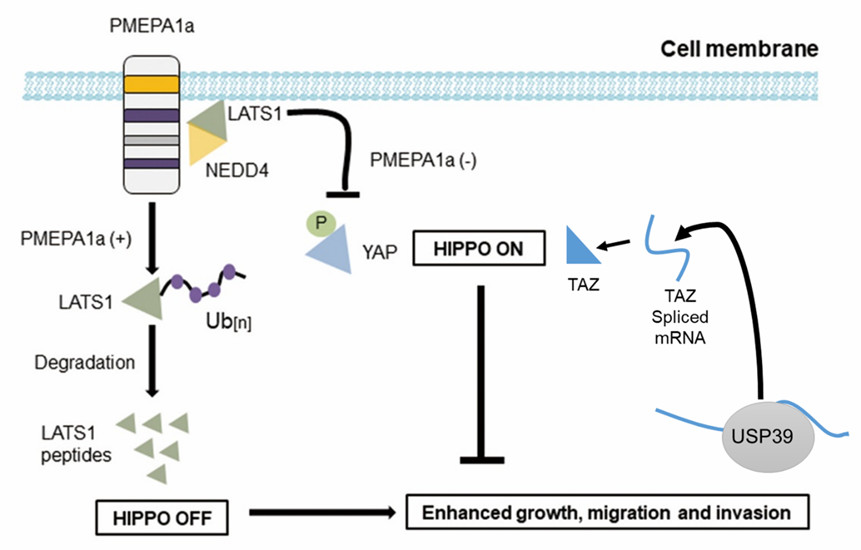
这两篇论文揭示了USP39和PMEPA1a在胶质瘤细胞中发挥作用的具体机制,揭示Hippo通路在胶质瘤发生进展中的关键地位,为寻找有效杀伤胶质瘤细胞的治疗靶点及临床治疗提供了新的理论支持。
Ding K, Ji J, Zhang X, et al. RNA splicing factor USP39 promotes glioma progression by inducing TAZ mRNA maturation. Oncogene. 2019 Sep;38(37):6414-6428. doi: 10.1038/s41388-019-0888-1.
Ji J, Ding K, Luo T, et al. PMEPA1 isoform a drives progression of glioblastoma by promoting protein degradation of the Hippo pathway kinase LATS1. Oncogene. 2019 Oct 11. doi: 10.1038/s41388-019-1050-9.






